真空冷冻干燥机应用过氧化氢蒸气灭菌的效果监测与验证
2013-10-31郑金旺
郑金旺
(上海东富龙科技股份有限公司,上海 201108)
过氧化氢是一种较强的氧化剂,分子具有非对称的链状结构。过氧化氢分子极易穿透微生物的细胞膜,与细胞内的过渡金属离子(或其他物质)作用,产生羟基自由基,从而攻击细菌、霉菌、芽孢及病毒中的酶、核酸等生命大分子物质,致使微生物灭活[1]。2001年,过氧化氢被美国环境保护署(EPA)推荐作为灭菌剂对房屋和建筑进行消毒[2]。随后,过氧化氢蒸气灭菌设备被开发并在欧美各国的制药、生物、医疗和卫生保健等领域得到广泛应用。
随着中国GMP(2010版)的颁布和实施,我国制药行业对无菌生产的要求不断提升,真空冷冻干燥机实现‘在位灭菌’(Sterilization-in-place,SIP)是冻干机通过GMP(2010版)认证的最基本前提。然而,据统计,目前在国内运营的所有冻干生产线中,约60%的冻干机不具备SIP的功能。由于过氧化氢蒸气灭菌工艺具有杀菌作用快速、灭菌能力强、刺激性小、腐蚀性低、环保等优点,越来越多的制药企业考虑用过氧化氢蒸气灭菌系统对缺乏SIP的冻干机进行灭菌。
我公司将自主研发的过氧化氢蒸气灭菌系统(HPVS V-50)应用于Tofflon Lyo-40-CIP冻干机(不具备SIP功能)进行灭菌,其灭菌效果良好。

图1 过氧化氢蒸气灭菌系统(HPVS V-50)
1 材料与方法
1.1 试剂与仪器
生物指示剂(嗜热脂肪芽孢杆菌孢子,孢子量106)、化学指示剂、TSB、30% 500 ml过氧化氢溶液、无菌操作台、记号笔、便携式过氧化氢气体浓度探测器(ATi-PortanSen Ⅱ)及手持式温湿度测量仪(Testo-645)。
1.2 HPVS V-50灭菌器
HPVS V-50灭菌器是由上海Tofflon公司自主研发的针对密闭区域进行灭菌的过氧化氢蒸气发生系统。整个过氧化氢蒸气灭菌过程分为泄露测试、预处理、高速注入、低速注入和通风五个阶段。
(1)泄露测试:通过泄露测试以确认该系统的密闭性良好。
(2)预处理:调节并控制冻干机箱体的相对湿度和温度在设定参数范围内。
(3)高速注入:30%的双氧水被不断汽化成含有高浓度的过氧化氢气体的蒸气。
(4)低速注入:保持过氧化氢足够的作用时间和浓度以确保微生物被完全灭活。
(5)通风:该阶段不再向冻干机内部注入过氧化氢蒸气,冻干机箱体内部残余的过氧化氢气体催化分解成水和氧气。在本案例中,通过真空空气置换以排除箱体内部的残余过氧化氢气体,从而使冻干机箱体内部的过氧化氢气体浓度低于职业允许暴露水平(1 ppm)。
1.3 Lyo-40 CIP冻干机的过氧化氢灭菌
该Lyo-40 CIP冻干机由Tofflon 公司生产,具有14个板层,总板层面积为40 m2,干燥箱内腔体的体积约11.5m3(2.20 m×2.20 m×2.35 m),具备“在位清洗”(Cleaning-in-place,CIP)功能,不具备SIP功能。
在对冻干机进行简单改造后,通过Φ38气体传输管道将HPVS V-50灭菌器与冻干机连接,并形成闭合的气流循环回路,如图1所示。HPVS V-50灭菌器通过充气管道将过氧化氢蒸气注入到冻干机箱体内部,然后再通过回气管道将未充分作用的过氧化氢蒸气回流到灭菌器中,如此不断循环直到灭菌结束。
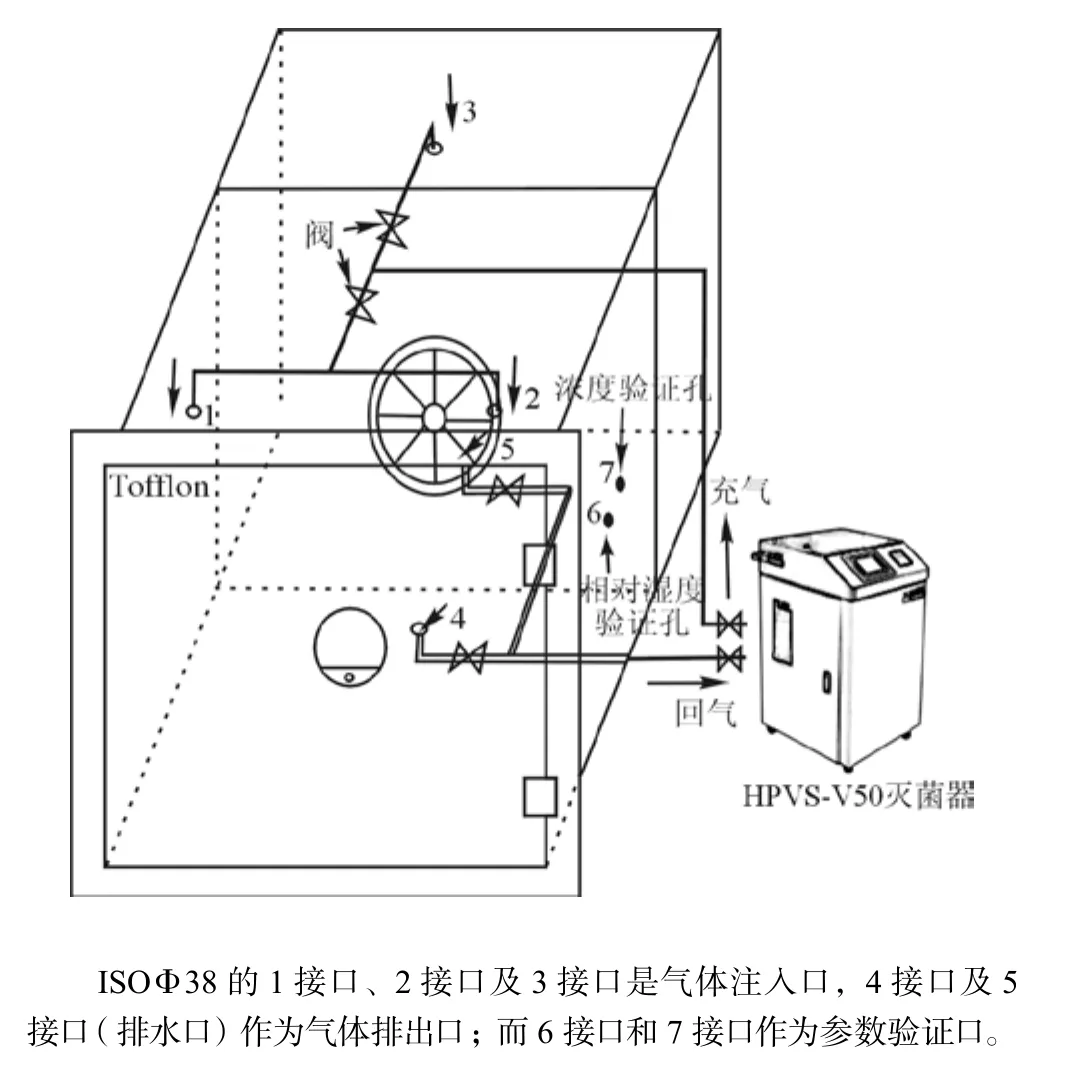
图2 冻干机与HPVS V-50灭菌器连接示意图
Lyo-40冻干机的过氧化氢灭菌循环参数是Tofflon公司根据冻干机的结构、规格和温湿度状况并通过灭菌工艺开发程序确定的灭菌参数,如表1所示。
1.4 灭菌循环的监测与验证
在灭菌过程中,通过HPVS V-50灭菌器的参数测量系统对冻干机箱体的压力、气流传递的管道内相对湿度、过氧化氢溶液注入流量、风机转速、气流传递温度、汽化温度及过氧化氢气体浓度等参数进行监测。此外,通过手持式温湿度测量仪对灭菌初始温湿度进行验证,并通过便携式过氧化氢气体浓度探测器对灭菌循环结束后的冻干机箱体内部过氧化氢气体浓度值进行确认。在灭菌结束后,将该浓度传感器放置于过氧化氢浓度验证孔(如图2的接口7所示)进行测量,以确认该冻干机箱体内部的过氧化氢气体的浓度值低于国家规定的过氧化氢职业允许暴露水平值(1ppm)。

表1 Tofflon Lyo-40 CIP冻干机的过氧化氢灭菌参数
过氧化氢蒸气灭菌效果的监测和验证主要采用化学指示剂和生物指示剂。通过化学指示剂在灭菌循环作用前后的色带颜色变化,以评定该灭菌循环的过氧化氢浓度分布和灭菌作用情况。而生物指示剂用来评估过氧化氢灭菌循环的灭菌效力,并确认该灭菌工艺的灭菌效果达到无菌保证水平(SAL)。该生物指示剂是由载有孢子数约为106的嗜热脂肪芽孢杆菌孢子的不锈钢载片和Tevek包装组成。
灭菌效果的监测和验证过程:在每个灭菌循环运行前,将已编号的化学指示剂和生物指示剂放置于冻干机箱体内部相应的灭菌挑战位点(如图3所示),然后运行灭菌循环,在灭菌循环完成后,将指示剂其逐个取出,记录化学指示剂的监测结果,而将生物指示剂经过无菌操作置于放入对应编号的TSB培养基中,然后将其置于在55℃~60℃条件下培养7天后观察生物指示剂培养结果。培养基保持紫色不变,则视无菌生长;同时阳性对照培养基由紫色澄清液体变为黄色浑浊即表示合格。连续运行三次该灭菌循环以确认该灭菌工艺的可重演性。
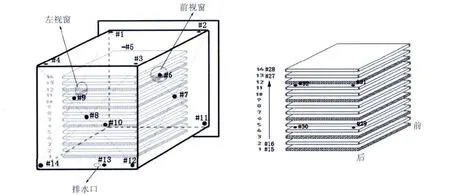
图3 BI/CI测试位点图
2 结果
由于监测位点的不同及灭菌循环的差异,化学指示剂受过氧化氢作用的程度都有所不同,造成化学指示剂监测效果的差异。为了较好地统计和说明化学指示剂对过氧化氢灭菌工艺的监测效果,我们将测试后的化学指示剂的变色的程度进行分类以区分。其中,将经历一个完整的灭菌循环作用后,色卡颜色为紫蓝色的化学指示剂标记为A;而受过氧化氢作用程度较差,有一定变色(深灰色)的化学指示剂标记为B;将受过氧化氢作用程度适中但未完全呈现米黄色的化学指示剂标记为C;最后,将色卡颜色为米黄色的化学指示剂标记为D。如表2所示,3次灭菌循环的每个灭菌循环的32个监测位点的CI均由紫蓝色变成米黄色,说明该灭菌工艺的过氧化氢气体分布较均匀。然而,冻干机箱体底部(除#12位点外,#11~#14)及冻干机箱体侧壁的中心区域(#6~#9)的过氧化氢指示剂变色程度较其他位点要明显一些,说明这些位点或区域较其他位置受过氧化氢作用程度要充分一些。
除臭规模总风量Q为13 000 m3/h,共计2套处理系统,其中,一期设计风量9 000 m3/h,二期设计风量4 000 m3/h,除臭工艺采用生物土壤滤池除臭技术。首先将O池中的恶臭气体密封加盖,防止恶臭气体外溢,采用不锈钢收集风管进行收集,通过引风机将恶臭气体引至生物土壤滤池进行处理,处理后的气体无组织达标排放。
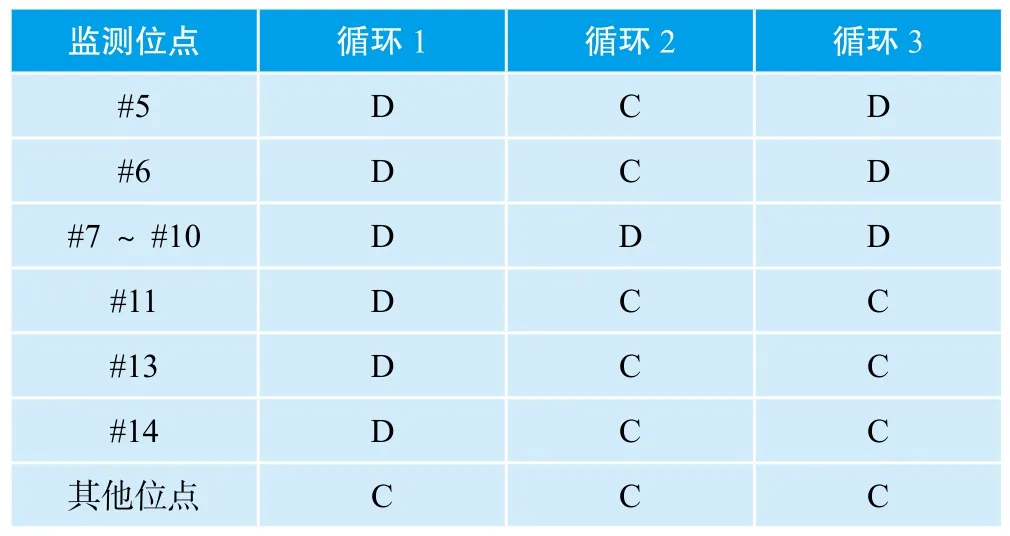
表2 化学评估-CI测试结果

表3 BI培养结果
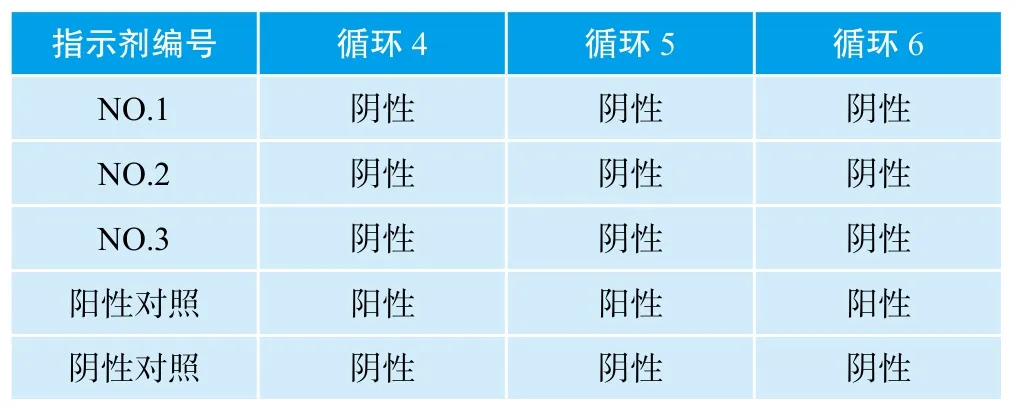
表4 #27位点-微生物挑战测试结果
如表3所示,除第2次灭菌循环的#27位点外,经历三次连续的灭菌循环的所有灭菌监测生物指示剂的培养结果皆为阴性。在第2次灭菌循环的位点#27处(即从上至下的第2个板层中心)的BI培养结果显示为阳性。
第2次灭菌循环的#27位点出现阳性结果,可能是因为在生物指示剂培养操作过程中验证人员操作不慎造成该位点的指示剂培养出现“假阳性”结果;也可能是在第2次灭菌循环#27位点的生物指示剂为Rogue BIs[3],由于Rogue BIs的细菌孢子结块或簇积从而使该生物指示剂呈现更强的灭菌抗性,造成灭菌失败。随后,我公司在#27位点再放置3个生物指示剂并重复运行3次上述灭菌循环,以此对该位点进行确认。#27位点的微生物挑战实验生物指示剂培养结果,如表4所示,该位点的挑战生物指示剂连续经历3次该灭菌循环未出现有菌生长。
此外,在应用安全性方面,我公司用过氧化氢浓度探测仪对HPVS V-50灭菌器设备周围环境及冻干机内部的残留浓度进行测量。结果如表5所示,在灭菌过程中,HPVS灭菌器周围环境中的过氧化氢气体的浓度低于1ppm;在每次灭菌循环结束后,冻干机箱体内部的过氧化氢浓度都低于1ppm。说明该灭菌系统的密闭性良好;并且在灭菌循环结束后,冻干机箱体内部过氧化氢气体已经排尽。
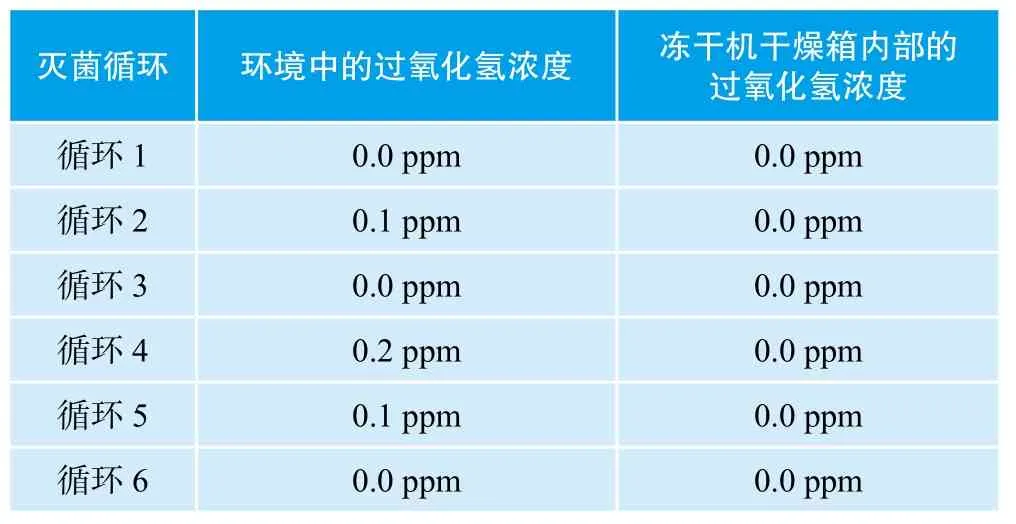
表5 过氧化氢灭菌安全监测结果
总之,对过氧化氢蒸气灭菌工艺的灭菌效果监测和验证可知,冻干机应用过氧化氢蒸气进行灭菌的灭菌效果良好。应用HPVS V-50过氧化氢蒸气灭菌器对Tofflon Lyo-40-CIP冻干机进行灭菌对人和环境没有造成危害。此外,在灭菌循环结束后,冻干机箱体内部没有产生过氧化氢残留,过氧化氢气体浓度低于职业允许暴露水平值(1ppm)。
3 讨论
目前国内制药企业正在使用的真空冷冻干燥机绝大多数不具备在线蒸汽灭菌系统。冻干机改造添加SIP系统需要满足以下条件:
(1)冻干机按D类压力容器进行设计和制造,并备有压力容器设计检测证书和备案证书;
(2)该冻干机的热循环系统使用硅油作为导热油;
然而,国内大多数冻干机不能满足上述条件,通过给不具备SIP功能的冻干机配备过氧化氢蒸气灭菌系统,通过充气管道和回气管道将灭菌器与冻干机连接并形成气流闭合回路,即可使冻干机实现“在位灭菌”。
冻干机内部复杂的结构(CIP清洗管道、搁板、蘑菇阀和冷凝盘管等部件)影响过氧化氢蒸气的分布和扩散,合理的过氧化氢气体传输以及较好的过氧化氢扩散方案较为重要。利于过氧化氢蒸汽的扩散的CIP管道布置、避免在过氧化氢蒸气传输过程中热量过度的损失、冻干机前后箱底面的斜面排水优化设计、在冻干机灭菌过程中实行分段灭菌和真空气流置换等措施都有利于冻干机充分灭菌。
在冻干机的灭菌验证过程中,通过确立冻干机灭菌最不利位点(Worst case location)、使用更多的指示剂及添加更多的监测位点都能较全面地对该灭菌工艺进行验证和评估。
总之,规范的灭菌工艺、科学有效的灭菌监测和验证、严格的无菌控制和保障,成为当前我国无菌制剂生产满足国内外市场日益增高的质量诉求和认可的首要前提。现代中国制药行业高速发展并日渐成熟,冻干机实现在位灭菌已势不可挡,越来越多的真空冷冻干燥机通过简单改造配置过氧化氢蒸气发生系统,从而实现“在位灭菌”。我们相信过氧化氢蒸气灭菌工艺因其低温、快速、易验证、无毒及环保等优点将会在制药行业有更大的发展。
[1] 袁勤生. 超氧化物歧化酶[M].上海:华东理工大学出版社,2009:209-210.
[2] Andrew M. McAnoy. Vaporous Decontamination Methods:Potential Uses and Research Priorities for Chemical and Biological Contamination Control[M].Australia:Australian Government Department of Defence,2006.
[3] James E.Akers. Acceptance Criteria In the Validation of VPHP Decontamination[R].A3P 22nd Congress, October 2010.
