铜和对苯二甲酸金属有机骨架材料绿色合成
2013-10-24那立艳张伟华瑞年宁桂
那立艳,张伟,华瑞年,宁桂 玲
(1.大连理工大学 精细化工国家重点实验室,辽宁 大连 116024;2.大连民族学院 生命科学学院,辽宁 大连 116600)
0 引言
金属有机骨架(MOFs)材料是在微孔晶体材料上发展起来的一种新型功能材料,由于其在气体存储与分离、催化、药物传递和传感器等方面的潜在应用而备受关注[1-5].目前用于合成MOFs材料的方法有溶剂诱导沉淀法[6]、溶剂热合成法[7]、反相微乳液法[8]、微波辅助合成法[9]、超声法[10]等.然而这些合成方法往往存在反应时间长、反应温度高、大量使用有机溶剂或复杂的反应设备等缺点,对其实际应用造成了制约,因而开发快速、简便、节约能源和环境友好的合成路线具有重要意义.
DMF由于具有较高的沸点(140℃)和对羧酸类配体良好的溶解能力,是合成MOFs材料经常使用的溶剂.DMF分子中的氧原子通常以配体或客体分子的形式填充到孔道当中,因而,为了获得金属活性中心和开放的骨架结构,通常要对合成的产物进行热处理,以除去配位及孔道中的DMF分子.如果能在反应中以水代替DMF 溶剂,那么不仅能够节约成本,而且在热处理过程中,只需将水分子除去即可,可以明显缩短热处理过程的时间,降低热处理温度,进而有效地节约能源.
本文的合成策略是先将非水溶性的配体对苯二甲酸与甲胺反应,生成水溶性的甲胺羧酸盐;然后利用水溶性配体与金属盐在水溶液中完成聚合反应.由于CuBDC具有独特的磁性、优良的气体分离性能及催化活性[11],本文分别在水溶液及DMF溶液中进行CuBDC 的合成探索,通过对比两种反应体系的合成条件及产物性能,探索羧酸类配体构筑的MOFs材料的快速、高效、低能耗合成.
1 实验部分
1.1 试剂与仪器
原料:试剂均为市售分析纯.
仪器:日本岛津XRD-6000 衍射仪;Nicolet FT-IR 740红外光谱仪;日本日立S-4800高分辨电子显微镜;Micromeritics ASAP 2020表面分析仪;美国Perkin-Elmer SDTA 851热失重分析仪.
1.2 合 成
1.2.1 水溶性配体前驱体((NH3CH3)2BDC)的合成 取1.667g(10mmol)对苯二甲酸,搅拌下滴加20%~30%的甲胺水溶液至溶液澄清,于真空干燥箱中20℃下减压至溶液黏稠,室温挥发得白色晶体.将上述晶体用水转移至100 mL 容量瓶中,配制成0.1mol/L甲胺盐水溶液,反应方程式如下:
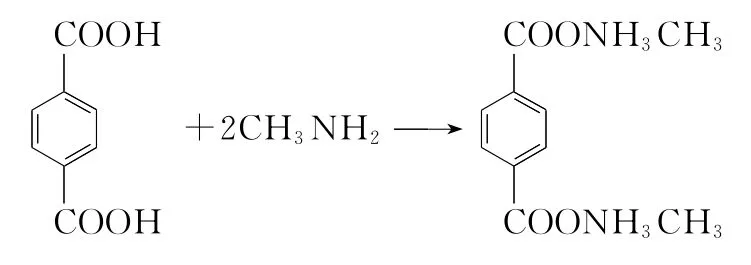
1.2.2 CuBDC-H2O的合成称取0.03 g Cu(OAc)2·H2O溶于7 mL 水中,搅拌下滴入0.1mol/L(NH3CH3)2BDC 溶液3 mL,马上产生浅蓝色沉淀,搅拌2h后离心.然后将产物经乙醇洗涤—超声分散—离心两次,自然干燥.
1.2.3 CuBDC-DMF的合成称取0.03 g Cu(OAc)2·H2O溶于4mL水中,再称取0.04g H2BDC溶于6 mL DMF 中,两种溶液充分溶解后,搅拌下将配体溶液滴入金属盐水溶液中,马上产生蓝色沉淀,搅拌2h后,静置2h,离心.然后将产物经乙醇洗涤—超声分散—离心两次,自然干燥.
2 结果与讨论
2.1 XRD 表 征
两种产物及经140℃真空热处理10h 后CuBDC-DMF的粉末XRD 谱图见图1.由图可知有机溶液中获得的CuBDC-DMF 与水溶液中获得的CuBDC-H2O 峰位明显不同(图1曲线a、c),说明两者结构不同.CuBDC-DMF 是一种已知结构的化合物[11-12](与本文合成方法不同),具有开放的骨架结构,结构中的金属中心铜为五配位,4个氧原子来自于BDC基团,另外一个氧原子来自于DMF分子(图2(a)).当CuBDC-DMF 在140℃真空热处理10h脱除了DMF 基团后,其XRD 谱图(图1曲线b)与CuBDC-H2O(图1 曲线c)相同.这说明CuBDC-DMF高温脱除溶剂分子后,与在水溶液中一步获得的产物CuBDCH2O 具有相同的结构,图2(b)是CuBDC-H2O 的可能结构.
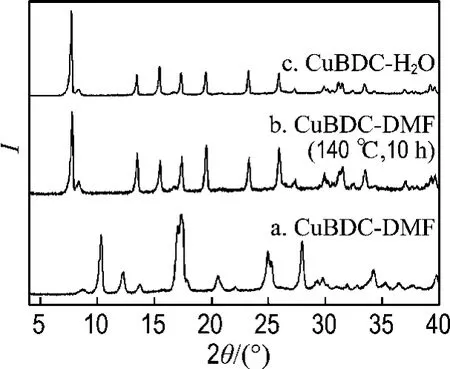
图1 粉末XRD 谱图Fig.1 Powder X-ray diffraction(PXRD)patterns
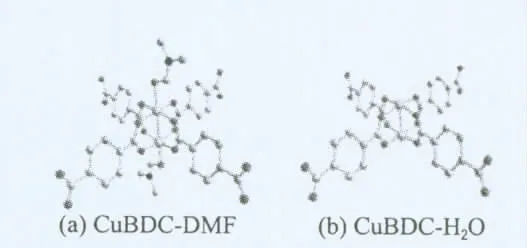
图2 晶体结构Fig.2 Crystal structures
2.2 红外表征
用KBr压片法测定了CuBDC-H2O、CuBDCDMF及经140℃真空热处理10h后的CuBDCDMF红外光谱,见图3.通过对比吸收峰的位置,发现CuBDC-DMF经热处理后的红外谱图(图3曲线b)与CuBDC-H2O(图3曲线c)基本一致,两个谱图中,1 575cm-1与1 398cm-1处的吸收峰归属为BDC配体中羧酸基团的非对称伸缩振动和对称伸缩振动;1 690~1 730cm-1没有出现羰基的吸收峰,说明配体上的羧酸基团已全部去质子化.而在CuBDC-DMF 的红外谱图(图3曲线a)中,1 688cm-1处的吸收峰为客体DMF中羰基的吸收峰,1 628cm-1处的吸收峰可归属为与金属中心配位的DMF 中羰基的吸收峰,氧原子与金属中心配位作用的存在,使得吸收峰向短波数方向移动.1 292cm-1处的吸收峰为酰胺中C—N 键的伸缩振动.以上3个与DMF相关的特征吸收峰在真空热处理后消失,说明通过加热,已成功去除客体DMF 分子及配位的DMF基团,并且其结构与水溶液中一步获得的产物CuBDC-H2O 相同.
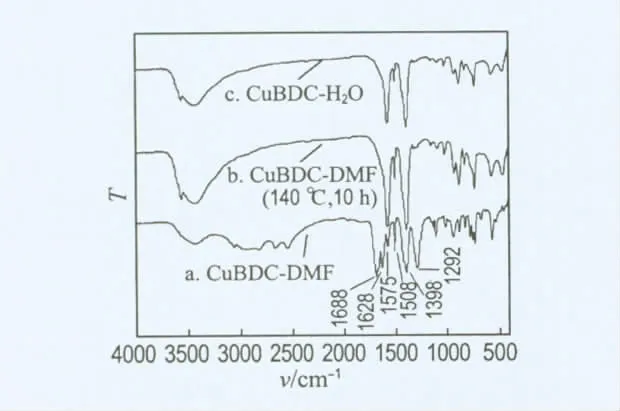
图3 红外谱图Fig.3 IR spectra
2.3 SEM 表征
图4(a)和图4(b)分别是CuBDC-DMF 和CuBDC-H2O 的扫描电镜照片,可以看出,两种合成条件下获得的产物均为方形片状晶体.CuBDCDMF晶体长和宽约为400nm,厚度在50nm 左右,与文献报道该化合物的形貌基本一致[12];CuBDC-H2O 晶体长为10μm,宽为4μm,厚度在1μm 左右.由于在水溶液中进行反应时,配体已经提前完成了去质子化的过程,因而反应速度比较快,所以CuBDC-H2O的尺寸明显大于CuBDC-DMF.

图4 扫描电镜照片Fig.4 SEM images
2.4 吸附测试
采用-196℃下氮气吸附的方法对两种不同条件下获得的化合物进行了氮气吸附等温测试.样品量约为0.2g,测试前均在140℃真空干燥10h,采用BET 方法在p/p0=0.05~0.33获得比表面积.从图5可以看出,两种化合物在相对低的压力范围内(p/p0<0.1),都有一个明显的台阶存在,然后曲线趋于平缓,吸附等温曲线为I型,说明了样品中微孔孔道的存在.CuBDC-DMF和CuBDC-H2O 在低压区(p/p0=0.01)时,氮气的吸附量分别为65cm3/g和68cm3/g,随着压力的升高,吸附量略有增加,在高压区(p/p0=1.0)时,氮气的吸附总量分别为89cm3/g和80cm3/g,BET 比表面积分别为407m2/g和439m2/g.从以上结果可以看出,在CuBDC-DMF脱除客体及配位的DMF基团后,与在水溶液中获得的产物CuBDC-H2O 具有相似的比表面及孔结构信息.
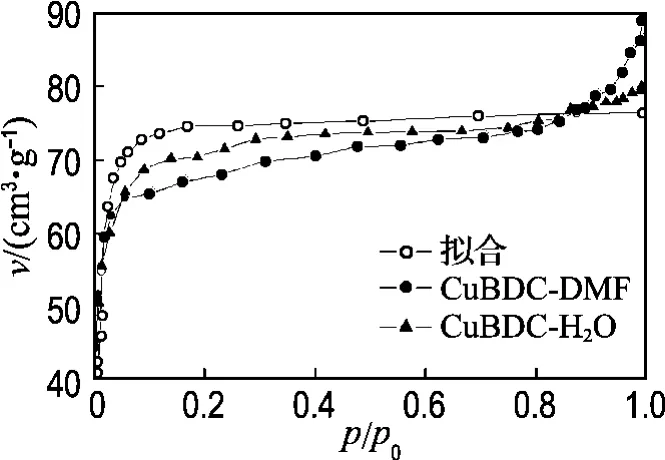
图5 氮气吸附等温曲线Fig.5 N2adsorption isotherms
采用巨正则蒙特卡罗法(grand canonical Monte Carlo)模拟了CuBDC-DMF在77K时的氮气吸附曲线[13],见图5.分子模型是通过CuBDC-DMF的实验XRD 晶体学数据建立的.采用通用力场(UFF)描述MOF骨架原子[14],N2力场参数为σ=0.331nm,ε=36 K.利用Music code软件进行模拟[15],并用BET 方法对模拟吸附等温线的线性段(p/p0=0.001~0.015)进行拟合,进而得到BET 方程参数及比表面积,结果如图6所示.模拟吸附曲线及理论比表面积均与实验结果接近.
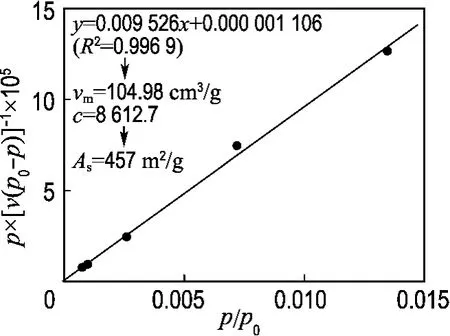
图6 BET 法比表面积计算Fig.6 Specific surface area calculation by the BET method
2.5 热稳定性测试
对CuBDC-DMF、CuBDC-H2O 及经140℃真空热处理10h后CuBDC-DMF进行了热失重分析,温度区间为30~500℃,氮气气氛.CuBDCDMF热失重曲线(图7 曲线a)显示该化合物在90~250℃失重值约为27%,100℃左右的失重可归属为水分子的脱除,在140~250℃的失重可归属为配体DMF的失去,温度超过300℃,化合物的骨架开始塌陷.图7中曲线c是CuBDC-H2O的热失重曲线,可以看出化合物在200℃之前基本没有失重,骨架结构可稳定存在至300℃.图7中曲线b 是CuBDC-DMF 经真空热处理后的热失重情况,热失重曲线与CuBDC-H2O 的基本相同,说明热处理过程除去了配位的DMF 分子后,CuBDC-DMF与CuBDC-H2O 拥有相同的骨架热稳定性能.
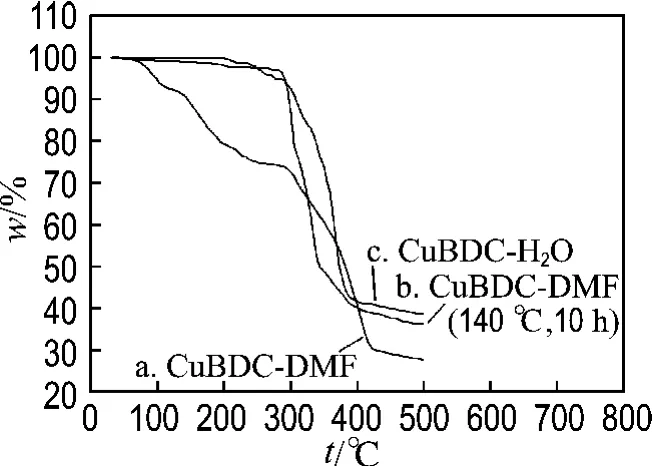
图7 热失重曲线Fig.7 TGA curves
3 结论
(1)通过水溶性羧酸甲胺盐配体的合成,开发出一种一步绿色合成金属有机骨架材料的新方法.
(2)对比有机体系和水体系中CuBDC 合成过程及产物性质,发现有机体系下获得的配合物在真空热处理除去配位的溶剂分子后,与在水溶液中一步获得的产物具有相同的结构和相似的性质.但以水溶液代替有机溶剂使用,不仅降低了合成成本,减少了污染,同时缩短了真空热处理过程的时间,降低了热处理温度.
(3)本文开发的水溶液合成路线具有简便、快速、节能和环保的特点,该绿色合成路线具有可推广性,可用于更多以羧酸类配体构筑的金属有机骨架材料的合成.
[1]Murray L J,Dinca M,Long J R.Hydrogen storage in metal-organic frameworks[J].Chemical Society Reviews,2009,38(5):1294-1314.
[2]Li J R,Kuppler R J,Zhou H C.Selective gas adsorption and separation in metal-organic frameworks[J].Chemical Society Reviews,2009,38(5):1477-1504.
[3]WU Chuan-de,HU Ai-guo,ZHANG Lin,etal.A homochiral porous metal-organic framework for highly enantioselective heterogeneous asymmetric catalysis [J].Journal of the American Chemical Society,2005,127(25):8940-8941.
[4]Horcajada P,Serre C,Vallet-Regi M,etal.Metalorganic frameworks as efficient materials for drug delivery [J].Angewandte Chemie International Edition,2006,45(36):5974-5978.
[5]CHEN Bang-lin,WANG Liang-bo,XIAO Yunqing,etal.A luminescent metal-organic framework with Lewis basic pyridyl sites for the sensing of metal ions [J].Angewandte Chemie International Edition,2009,48(3):500-503.
[6]Oh M,Mirkin C A.Chemically tailorable colloidal particles from infinite coordination polymers [J].Nature,2005,438(7068):651-654.
[7]Jung S,Oh M.Monitoring shape transformation from nanowires to nanocubes and size-controlled formation of coordination polymer particles [J].Angewandte Chemie International Edition,2008,47(11):2049-2051.
[8]Rieter W J,Taylor K M,An H,etal.Nanoscale metal-organic frameworks as potential multimodal contrast enhancing agents [J].Journal of the American Chemical Society,2006,128(28):9024-9025.
[9]Ni Z,Masel R I.Rapid production of metal-organic frameworks via microwave-assisted solvothermal synthesis[J].Journal of the American Chemical Society,2006,128(38):12394-12395.
[10]QIU Ling-guang,LI Zong-qun,WU Yun,etal.Facile synthesis of nanocrystals of a microporous metal-organic framework by an ultrasonic method and selective sensing of organoamines[J].Chemical Communications,2008(31):3642-3644.
[11]Carson C G,Hardcastle K,Schwartz J,etal.Synthesis and structure characterization of copper terephthalate metal-organic frameworks [J].European Journal of Inorganic Chemistry,2009(16):2338-2343.
[12]XIN Zhi-feng,BAI Jun-feng,SHEN Yong-ming,etal.Hierarchically micro- and mesoporous coordination polymer nanostructures with high adsorption performance [J].Crystal Growth &Design,2010,10(6):2451-2454.
[13]Walton K S,Snurr R Q.Applicability of the BET method for determining surface areas of microporous metal-organic frameworks [J].Journal of the American Chemical Society,2007,129(27):8552-8556.
[14]Karra J R,Walton K S.Effect of open metal sites on adsorption of polar and nonpolar molecules in metal-organic framework Cu-BTC [J].Langmuir,2008,24(16):8620-8626.
[15]Gupta A,Chempath S,Sanborn M J,etal.Objectoriented programming paradigms for molecular modeling[J].Molecular Simulation,2003,29(1):29-46.
