注射用头孢哌酮钠舒巴坦钠的无菌检查方法学研究
2013-10-19江苏省泰州市食品药品检验所225300黄勇柏大为
江苏省泰州市食品药品检验所(225300)黄勇 柏大为
根据2010年版《中国药典(二部)》的规定[1],建立药品无菌检查方法时。应进行方法学验证,以证明方法的适用性。注射用头孢哌酮钠舒巴坦钠对大肠埃希菌、克雷伯菌属、变形杆菌属、伤寒沙门菌、志贺菌属、枸橼酸杆菌属等肠杆菌科细菌和铜绿假单孢菌有良好抗菌作用。头孢哌酮主要抑制细菌细胞壁的合成。舒巴坦本身抑菌作用较弱,是一种竞争性、不可逆的β内酰胺酶抑制药,与头孢哌酮联合应用后,可增加头孢哌酮抵抗多种β内酰胺酶降解的能力,对头孢哌酮产生明显的增效作用[2][3][4]。为确保方法科学、结果准确,本文建立了注射用头孢哌酮钠舒巴坦钠无菌检查方法,并验证检查法的可靠性,现总结如下。
1 仪器与材料
1.1 仪器 HTY-2000A集菌仪、脱卸式薄膜过滤器,均由杭州高德医疗器械有限公司生产。隔水式电热恒温培养箱,上海跃进医疗器械厂;PL202-L电子天平,梅特勒-托利多仪器(上海)有限公司。
1.2 菌种 验证用菌种为枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501]第4代;金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]第3代;大肠埃希菌(Escherichia coli)[CMCC(B)44102]第4代;白色念珠菌(Candida albicans)[CMCC(F)98001]第4代;黑曲霉(Aspergillus niger)[CMCC(F)98003]第3代;铜绿假单孢菌(Pseudomonas aeruginosa)[CMCC(F)10104]第3代。
1.3 培养基 培养基为硫乙醇酸盐流体培养基、改良马丁培养基、营养肉汤培养基、改良马丁琼脂培养基、营养琼脂培养基。上述培养基均为符合药典规定的干燥培养基,由中国药品生物制品检定所提供。
1.4 稀释剂 pH7.0氯化钠-蛋白胨缓冲液、0.9%无菌氯化钠溶液均按药典方法配制。
1.5 样品 注射用头孢哌酮钠舒巴坦钠(齐鲁制药有限公司,批号为1070229BR,规格1.0g/瓶)。
2 方法与结果
2.1 菌液制备 接种金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌、铜绿假单孢菌新鲜培养物至营养肉汤培养基中,置30~35℃培养18~24h,分别取上述培养物1ml,加0.9%的无菌氯化钠溶液9ml,10倍递增稀释制成每1ml含菌数为50~100cfu的菌悬液;接种白色念珠菌的新鲜培养物至改良马丁培养基中,置23~28℃培养24~48h,取培养物1ml,加0.9%的无菌氯化钠溶液9ml,10倍递增稀释制成每1ml含菌数为50~100cfu的菌悬液;接种黑曲霉的新鲜培养物至改良马丁琼脂培养基中,置23~28℃培养5~7d,用0.05%ml/ml聚山梨酯80的0.9%的无菌氯化钠溶液5ml将孢子洗脱并过滤孢子悬液至无菌试管内,再取孢子悬液1ml加0.05%ml/ml聚山梨酯80的0.9%的无菌氯化钠溶液5ml,作为原液,备用。取原液1ml,加0.05%ml/ml聚山梨酯80的0.9%的无菌氯化钠溶液9ml,10倍递增稀释制成含50~100cfu的孢子悬液。
2.2 培养基灵敏度检查 取每管装量为12ml的硫乙醇酸盐流体培养基9支,分别接种小于100cfu的金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌、生孢梭菌各2支,另1支不接种作为空白对照,培养3d;取每管装量为9ml的改良马丁培养基5支,分别接种小于100cfu的白色念珠菌、黑曲霉各2支,另1支不接种细菌作为空白对照,培养5d,每日观察结果。结果如下:空白对照管无菌生长,加菌的培养基管细菌均生长良好,结果灵敏度检查符合规定。见附表1。
2.3 方法验证
2.3.1 方法的选择 注射用头孢哌酮钠舒巴坦钠为注射用冻干粉针,抗生素有较强的抑菌作用,所以采用薄膜过滤法进行试验。
2.3.2 方法验证试验1 取注射用头孢哌酮钠舒巴坦钠30支,以无菌操作加0.9%无菌氯化钠溶液溶解后,转移至不少于500ml的0.9%无菌氯化钠溶液中,作为供试品溶液,采用封闭式薄膜过滤器过滤,向过滤器中加入硫乙醇酸盐流体培养基或改良马丁培养基100ml,作为供试品阴性对照组,另取一装有同体积相同培养基的容器,加入等量实验菌,作为供试品阳性菌试验组,按规定温度培养3~5d。阴性对照组:用pH7.0无菌氯化钠-蛋白胨缓冲液冲洗100ml,向过滤器中加入硫乙醇酸盐流体培养基或改良马丁培养基100ml。结果见附表2和3。

附表1 培养及灵敏度检查结果
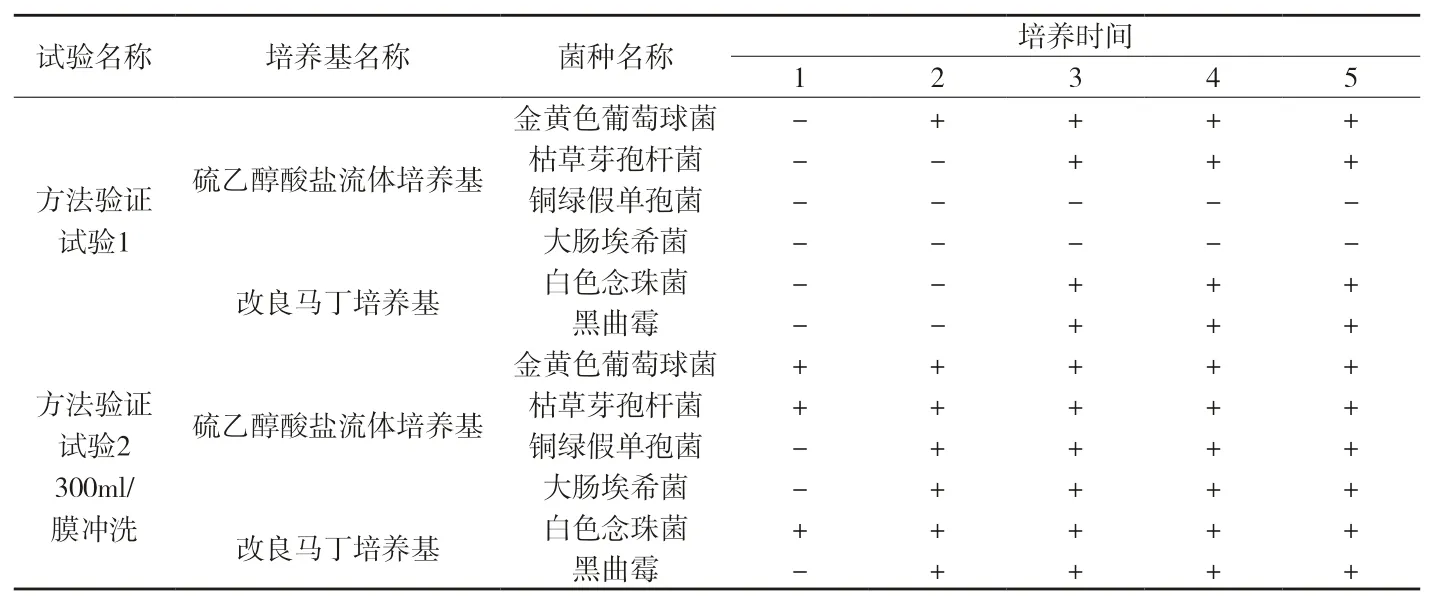
附表2 试品阳性菌试验组实验结果观察表

附表3 供试品阴性与阴性对照组实验结果观察
2.3.3 方法验证试验2 取注射用头孢哌酮钠舒巴坦钠30支,以无菌操作加0.9%无菌氯化钠溶液溶解后,转移至不少于500ml的0.9%无菌氯化钠溶液中,作为供试品溶液,采用封闭式薄膜过滤器过滤,用1000ml的pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,每次100ml,在最后一次冲洗液中加入青霉素酶(1ml/筒)并放置5min后滤干,冲洗完毕后,向过滤器中加入硫乙醇酸盐流体培养基或改良马丁培养基100ml,作为供试品阴性对照组,另取一装有同体积相同培养基的容器,加入等量实验菌,作为供试品阳性菌试验组,按规定温度培养3~5d。阴性对照组:用1000ml的pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,每次100ml,冲洗完毕后向过滤器中加入硫乙醇酸盐流体培养基或改良马丁培养基100ml。结果见附表2和3。
2.3.4 培养条件及结果观察 由附表2和3可见,在验证试验1的条件下,对细菌,特别是铜绿假单孢菌和大肠埃希菌有明显抑制作用,而实验条件2中含供试品各管的实验菌试验组在300ml/膜冲洗并加入加入青霉素酶(1ml/筒)时各滤筒微生物均生长良好,阴性对照及样品澄清无菌生长,试验组有菌生长。说明在该检验条件下已去除注射用头孢哌酮钠舒巴坦钠的抑菌作用。
2.4 样品的无菌检查 取注射用头孢哌酮钠舒巴坦钠30支,以无菌操作加0.9%无菌氯化钠溶液溶解后,转移至不少于500ml的0.9%无菌氯化钠溶液中,采用封闭式薄膜过滤器过滤,用1000ml的pH7.0无菌氯化钠-蛋白胨缓冲液冲洗(400ml/筒),每次100ml,在最后一次冲洗液中加入青霉素酶(1ml/筒)并放置5min后滤干,于两筒中接种硫乙醇酸盐流体培养基(其中一筒加入小于100cfu的金黄色葡萄球菌作为阳性对照管),另一筒加入改良马丁培养基,按规定温度培养14d,逐日观察生长情况。
本实验结果显示,供试品无菌检查阳性对照菌筒均在24h内正常生长,阴性对照均澄清呈无菌生长,无菌试验结果符合规定,证明所建立的无菌检查法科学、可靠,该实验条件能消除头孢匹胺钠对细菌的抑制作用。
3 讨论
3.1 通过方法验证试验表明注射用头孢哌酮钠舒巴坦钠在未冲洗时对细菌有明显的抑制作用,在冲洗量达到1000ml并加入青霉素酶之后抑菌作用消除,可以达到验证试验要求。
3.2 薄膜过滤法操作过程中应注意:在每次加冲洗液前应尽量抽干,每次加冲洗液后要充分振摇,每次冲洗量控制在50ml,其冲洗总量会显著降低。
