双(8-乙氧羰甲氧基-2-亚甲喹啉基)缩连氮的合成及其选择传感性能
2013-10-17刘利平
刘利平 张 强
(1内蒙古农业大学理学院,呼和浩特 010018)
(2内蒙古师范大学化学与环境科学学院,呼和浩特 010022)
由胺和活性羰基缩合而成的希夫碱是一类具有重要应用价值的化合物,其结构中所含的C=N基团具有良好的配位性能和光谱活性,目前已发现有多种希夫碱及其配合物具备特定的功能,如生物药理活性[1-2],抗癌、消炎、杀菌抑毒活性[3-6],催化活性[7-8],光致或电致发光活性[9-11]等。因此,该类化合物在生物化学、临床医学、分析化学、光、电、磁功能材料及酶催化等方面已有了不同程度的应用,并继续吸引着众多学者进行广泛、系统、深入的理论和应用研究[12-15]。
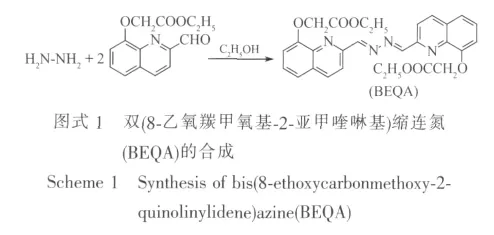
喹啉是一种萘状含氮化合物,其中8-羟基喹啉由于其配位原子N和O在分子中的恰当位置以及自身良好的共轭结构,已表现出了良好的螯合性能和光谱活性;但由于配位的普适性,8-羟基喹啉对金属离子的选择性较差,通常将喹啉环的2位和7位引入辅助配位基团以改善其选择性[16-20],对8位羟基进行结构修饰是近年来的一种新的尝试[21-23]。本文采取对8-羟基喹啉的2位和8位羟基分别进行双重修饰,将2-甲酰基-8-乙氧羰甲氧基喹啉键连到水合肼分子两端,合成了一种新型含喹啉环的希夫碱双(8-乙氧羰甲氧基-2-亚甲喹啉基)缩连氮(BEQA)(图式1),并采用紫外可见光谱法初步研究了在乙醇-水混合溶剂中该化合物对H+及其他10种金属离子的光谱敏感性和选择性传感机理。
1 实验部分
1.1 主要试剂与仪器
2-甲酰基-8-乙氧羰甲氧基喹啉由本实验室合成;水合肼(80%)、无水乙醇、苯、盐酸、邻苯二甲酸氢 钾 等 均 为 市 售 分 析 纯 试 剂 ;CaCl2、MgCl2、SrCl2、MnCl2、CoCl2、NiCl2、CuCl2、ZnCl2、CdCl2及 HgCl2均为国药集团化学试剂有限公司产品,部分金属盐在使用前经EDTA标定。
元素分析数据用德国产Vario MICRO元素分析仪测定;核磁共振氢谱在瑞士Bruker公司产AdvanceⅢ500核磁共振仪上获得;质谱测定在美国Thermo LCQ Advantage-MAX LC-MS质谱仪上完成;熔点用微电脑控温的XT5型显微熔点测定仪测定 (温度计未经校正);紫外可见光谱用U-2900型UV-Vis分光光度计(日本Hitachi公司)测定;pHS-3C数字酸度计(配E-201-C型复合电极)测定体系pH值。
1.2 双(8-乙氧羰甲氧基-2-亚甲喹啉基)缩连氮(BEQA)的合成
在 50 mL 单口烧瓶中加入 0.388 7 g(1.5 mmol)2-甲酰基-8-乙氧羰甲氧基喹啉和8 mL无水乙醇,室温下搅拌 35 min 后加入 46 μL(0.75 mmol)水合肼(80%),继续搅拌约0.5 h即出现黄色固体,在磁力搅拌下加热回流4 h,停止反应,冷却。将反应混合物抽滤得到黄色固体,用苯重结晶,得到黄色晶体,干燥后称量, 得 297.6 mg, 产率为 77%,m.p.158.1~159.2 ℃。
1H NMR(500 MHz,TMS,CDCl3)δ值:1.30(t,J=7.0 Hz,6H,2CH3),4.30(q,J=7.0 Hz,4H,2COOCH2-),5.03(s,4H,2OCH2COO),7.06(dd,J1=2.0 Hz,J2=7.0 Hz,2H,2QL-6-H),7.48~7.52(m,4H,2QL-5-H,2QL-7-H),8.22(d,J=9.0 Hz,2H,2QL-4-H),8.37(d,J=9.0 Hz,2H,2QL-3-H),8.90(s,2H,2N=CH-QL)。
ESI-MS,m/z:515.07[M+H]+,537.07[M+Na]+。
分析计算化合物C28H26N4O6(514.54)的元素含量为:C 65.37%,H 5.06%,N 10.89%;元素分析测定结果为:C 65.47%,H 5.07%,N 10.88%。
1.3 光谱测定
通过条件实验确定全部光谱测定均使用体积比4∶1的乙醇-水混合物为溶剂;BEQA对金属离子的选择性测定采用盐酸-邻苯二甲酸氢钾缓冲体系(0.02 mol·L-1,pH=3.1)以恒定其 pH 值;测定 pH 值对BEQA光谱影响时,采用混合溶剂的KCl溶液(I=0.02)来恒定体系的离子强度,用混合溶剂的盐酸和氢氧化钾稀溶液调节体系的pH值;配制浓度由高到低递变的系列BEQA溶液,试验其在紫外可见光谱上能够被检测的最低极限浓度,由此确定BEQA的适宜光谱测试浓度为6 μmol·L-1;为了保证实验的一致性,配制系列溶液均在相同的环境及时间内平衡后进行紫外可见光谱测定。
2 结果与讨论
2.1 BEQA对H+的传感
由图1可以看出,随着体系pH值的逐渐增大,化合物BEQA的紫外可见光谱发生了显著的变化。当pH值由2.90逐渐增大到约7.50时,光谱变化非常规律:开始在380 nm处的吸收峰逐渐降低,最终消失;而在338 nm处逐渐产生了新的吸收峰,且强度随pH值增大而增大,这可以被认为是380 nm处的吸收峰发生了蓝移;位于305 nm和260 nm两处的吸收峰基本不受酸度的影响,但随着pH值增大引起280 nm及288 nm的邻近双峰迅速产生并升高,淹没了305 nm和260 nm两处的吸收峰;240 nm处的吸收峰随pH值增大在逐渐减小,但没有发生位移。
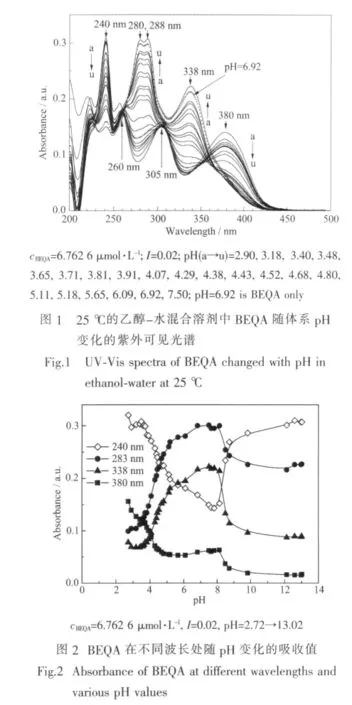
从图2可见,当体系pH值从7.50继续增大时,BEQA的吸收光谱仍然受酸度显著影响,虽然吸收峰位没有发生变化,但三处峰位 (位于240 nm、280 nm和288 nm的双峰及338 nm)的吸收强度与pH值在2.90到7.50的变化趋势相比逐渐发生了逆转,尤其在pH值从8.1增加到9.0之间,光谱吸收强度发生了急剧的变化,使338 nm处的吸收峰迅速降低并趋于消失,280 nm和288 nm处的双峰也有显著降低过程,240 nm处的吸收峰反而急剧地增大。
通过体系酸度对化合物BEQA吸收光谱的影响实验表明,BEQA对H+离子具有特殊的敏感性,当体系的pH值小于7.5时,酸度对BEQA吸收光谱的影响是规律的,说明分子结构中的氮原子键合氢离子而被质子化,改变了分子内电荷的分布,从而引起光谱的变化。在图1中约355 nm、305 nm和260 nm处出现了近似的等吸收点,说明随着pH值的降低过程,BEQA被单质子化以致多质子化,在体系中存在着多种质子化产物的平衡。从结构上看,BEQA分子中喹啉环上含有电子亲和性的氮原子而使其具有拉电子性质,2个喹啉环间有2个C=N自由双键与之共轭,因此BEQA形成了分子内共轭的电荷转移(ICT)化合物,但2个喹啉环间的N-N键和C-C键均有可能会发生旋转,致使喹啉环与C=N以及整个分子不完全在同一平面上,这在一定程度上影响分子的共轭程度。对于BEQA的这种结构特征,当体系中酸度增大时,分子中喹啉环上的氮原子将结合质子而带正电荷,表现出更强的电子亲和性,从而产生强拉电子效应而形成分子内电荷转移(ICT),导致体系338 nm处的吸收峰红移到380 nm。随着pH值增大,质子化程度逐渐降低,ICT效应随之减弱[24-26],380 nm处的吸收峰强度逐渐下降以致消失。当体系pH值从7.50继续增大时,BEQA的多处质子相继被中和,因而导致338 nm和280 nm处的双峰强度降低。
文献实验结果也表明[27-28],质子对该类化合物吸收光谱的影响具有一定的规律:当缩连氮分子两端的芳香环上含有氮原子时 (比如是吡啶环或喹啉环),氢离子浓度增大将导致吸收峰红移;当芳香环上连有酚羟基时,氢离子浓度的极度减小可以导致吸收峰的红移。这说明增大氢离子浓度可以增强含氮芳环中氮原子的拉电子效应,促使ICT的形成;而极度减小氢离子浓度可以使后者的酚羟基氢电离,使其共轭体系增大。
2.2 BEQA对金属离子的选择性传感
为了研究乙醇-水体系中BEQA对金属离子的选择性识别性能,考虑到大多数二价金属离子的水解特性,并参考不同pH值对BEQA紫外可见光谱影响的测定结果(见图2),确定实验中采用酸性的盐酸-邻苯二甲酸氢钾缓冲体系 (pH=3.1)来恒定pH值。图3给出了BEQA及其与80倍浓度的金属离子共存下的紫外可见光谱图。
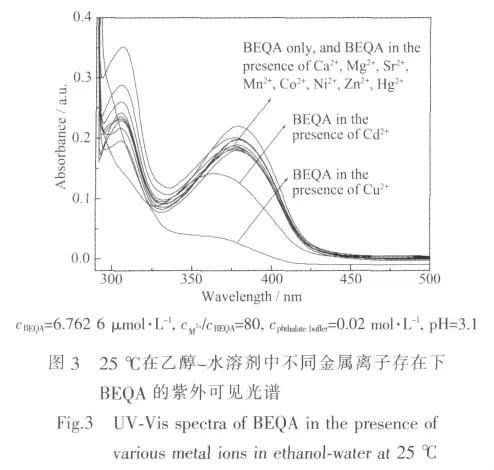
从图3可以看出,在pH值为3.1的乙醇-水缓冲溶液中,双(8-乙氧羰甲氧基-2-亚甲喹啉基)缩连氮 (BEQA)的紫外可见光谱对碱土金属离子Ca2+、Mg2+、Sr2+以及过渡金属离子 Mn2+、Co2+、Ni2+、Zn2+和Hg2+均无明显的敏感响应,而只对Cu2+和Cd2+有特殊的识别能力。在80倍于BEQA的Cu2+和Cd2+存在下,BEQA的紫外可见光谱在380 nm处的吸收峰已基本消失或显著降低,并且伴随有显著的蓝移。由于BEQA在380 nm处的吸收峰是分子中氮原子结合H+后产生的,所以此峰的降低或消失说明Cu2+和Cd2+能够有效地与BEQA分子中的氮原子键合,改变了BEQA分子内电荷转移(ICT)的性质,使化合物的ICT吸收峰发生移动。可能的机理是BEQA分子中两喹啉基团之间的缩连氮原子与金属Cu2+或Cd2+进行了配位,导致了喹啉环的拉电子效应减弱,从而减小了分子内电荷转移的程度,使380 nm处的吸收峰强度降低且发生蓝移。
2.3 Cuギ、Cdギ对BEQA光谱的影响
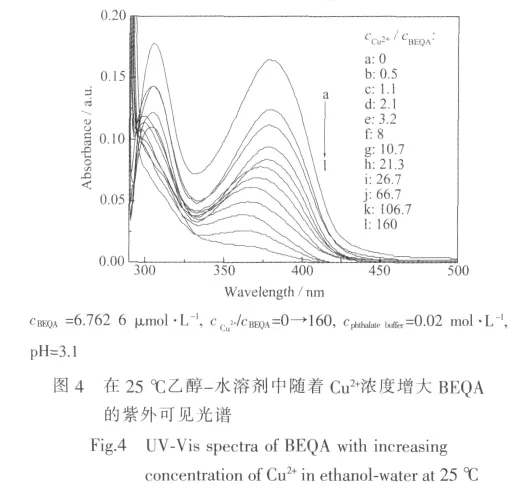
在固定BEQA浓度及体系pH值的情况下,逐渐增大Cu2+或Cd2+离子的浓度,分别进行紫外可见光谱的系列测定,图4、图5给出两种离子分别对BEQA吸收光谱影响的系列光谱。
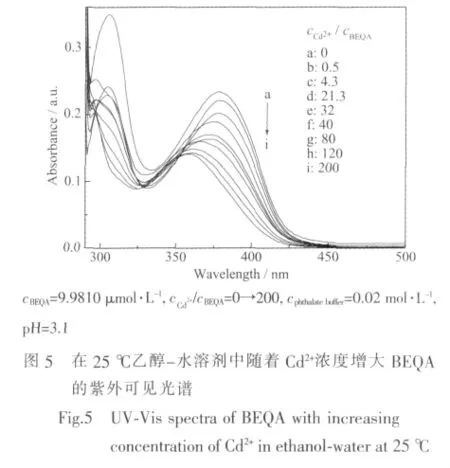
由图4、图5可见,在Cu2+离子或Cd2+离子浓度逐渐增大的过程中,BEQA分子在380 nm处的吸收峰均有规律地以不同程度的降低,当Cu2+离子、Cd2+离子的浓度分别增大到BEQA浓度约8倍和21倍以上时,均伴随出现蓝移现象,这说明BEQA分子中的键合质子有相当份额已被Cu2+或Cd2+离子所取代,使BEQA的质子化结构逐渐解体;由于较小浓度的Cu2+离子即可引起BEQA分子吸收光谱的蓝移,所以,相比之下Cu2+取代质子的能力较强,Cu2+-BEQA配合物的稳定性也相对更高。
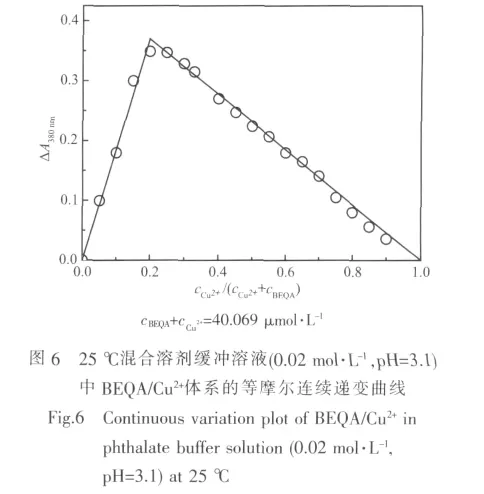
为了考察BEQA分子与Cu2+、Cd2+离子形成配合物的组成情况,本文采用等摩尔连续递变法(Job′s方法)测定了Cu2+、Cd2+与BEQA键合的化学计量比,图6绘制了BEQA/Cu2+体系的Job′s曲线。可以看出,相同实验条件下单一BEQA体系与配合物体系的光吸收差ΔA极大值位于金属离子组分占0.2的摩尔比处,因此Cu2+-BEQA配合物的化学计量比为1:4;同样方法测定的Cd2+-BEQA配合物也具有1∶4的计量比。
3 结 论
紫外可见光谱法测定合成主体BEQA对客体H+及10种金属离子选择传感性能的结果表明,H+离子能显著地影响BEQA主体化合物的光谱特征,随着体系中H+离子浓度的增大,BEQA分子在338 nm处的特征吸收峰强度逐渐降低,并红移到380 nm处。此现象表明,BEQA分子中的氮原子随着酸度的增加质子化程度增大,使分子中喹啉环上的氮原子具有更强的拉电子效应,明显地增强了BEQA的分子内电荷转移。此外,BEQA仅对10种金属中的Cu2+和Cd2+有特殊的传感作用,这2种金属离子可以不同程度地降低并蓝移BEQA在380 nm处的吸收峰,说明Cu2+和Cd2+离子能够竞争性地取代BEQA分子中键合的H+;BEQA与Cu2+离子的键合稳定性大于 Cd2+离子,Job′s法测定其形成 M2+-BEQA配合物的化学计量比为1∶4。
[1]Kumar S,Dhar D N,Saxena P N.Sci.Indust.Res.,2009,68:181-187
[2]Lü J,Liu T T,Cai S L,et al.J.Inorg.Biochem.,2006,100(11):1888-1896
[3]Hodnett M E,Mooney P D.J.Med.Chem.,1970,13(4):786-786
[4]Ren S J,Wang R B,Komatsu K,et al.J.Med.Chem.,2002,45(2):410-419
[5]Chohan Z H,Arif M,Sarfraz M.Appl.Organomet.Chem.,2007,21(4):294-302
[6]Sinha D,Tiwari A K,Singh S,et al.Eur.J.Med.Chem.,2008,43(1):160-165
[7]Wang Q,Zhang B Z,Hu G W,et al.Org.Biomol.Chem.,2007,5:1161-1163
[8]Pier G C.Chem.Soc.Rev.,2004,33:410-421
[9]ZHAO Jian-Zhang(赵建章),ZHAO Bing(赵冰),XU Wei-Qing(徐蔚青),et al.Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),2003,24(2):141-145
[10]CHEN Xiao-Xia(陈晓霞),SHAO Hui-Bo(邵会波).J.Instrum.Anal.(Fenxi Ceshi Xuebao),2006,25(z1):68-70
[11]Sun Z Y,Yuan R,Chai Y Q,et al.Anal.Bioanal.Chem.,2004,378:490-494
[12]Gholivand M B,Rahimi-Nasrabadi M,Ganjali M R,et al.Talanta,2007,73(3):553-560
[13]Fakhari A R,Khorrami A R,Naeimi H.Talanta,2005,66(4):813-817
[14]Lü X Q,Bi W Y,Chai W L,et al.New J.Chem.,2008,32:127-131
[15]CAI Tie-Jun(蔡铁军),PENG Zhen-Shan(彭振山),DENG Qian(邓谦),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2004,20(6):731-733
[16]Prodi L,Bargossi C,Kontalti M,et al.J.Am.Chem.Soc.,2000,122(28):6769-6770
[17]Bronson R T,Bradshaw J S,Savage P B,et al.J.Org.Chem.,2001,66(14):4752-4758
[18]Royzen M,Durandin A,Young V G,et al.J.Am.Chem.Soc.,2006,128(12):3854-3855
[19]Song K C,Kim J S,Park S M,et al.Org.Lett.,2006,8(16):3413-3416
[20]Xue L,Liu Q,Jiang H.Org.Lett.,2009,11(15):3454-3457
[21]Zhang H,Han L F,Zachariasse K A,et al.Org.Lett.,2005,7(19):4217-4220
[22]YANG Dong-Rui(杨东瑞),ZHANG Zhi-Jun(张志君),ZHANG Heng-Yi(张衡益),etal.Chem.J.ChineseUniversities(Gaodeng Xuexiao Huaxue Xuebao),2011,32(9):2169-2174
[23]ZHANG Qiang(张 强),XU Juan(许 娟 ).Acta Chim.Sin.(Huaxue Xuebao),2011,69(19):2287-2292
[24]Yasutake M,Koga T,Sakamoto Y,et al.J.Am.Chem.Soc.,2002,124:10136-10145
[25]Zhu Q Y,Liu Y,Lu W,et al.Inorg.Chem.,2007,46(24):10065-10070
[26]Seo J,Kim S,Park S Y.J.Am.Chem.Soc.,2004,126:11154-11155
[27]De Torre A G,Valcarcel M,Pino F.Talanta,1973,20(9):919-922
[28]Ziółek M,Gil M,Organero J A,et al.Phys.Chem.Chem.Phys.,2010,12:2107-2115
