纳米金/Nafion/石墨烯修饰玻碳电极检测对苯二酚的研究
2013-10-08康天放
孙 雪,康天放
(北京工业大学 环境与能源工程学院,北京 100124)
石墨烯具有优良的导电性、生物相容性、机械强度、化学稳定性等,近些年已被用作制备高选择性和高灵敏性化学修饰电极的纳米材料[1-6]。到目前为止,石墨烯修饰电极的制备方法一般是通过化学方法将氧化石墨烯(GO)还原为石墨烯(Chemically reduced graphene oxide,CRGO),然后再将分散于溶剂中的CRGO滴涂于电极表面而完成制备[7-10]。然而,这种方法制备的石墨烯需要消耗大量的有毒试剂,如肼、NaBH4、碱性试剂等,而且这些试剂具有很强的腐蚀性,甚至有爆炸的危险。此外,这种合成方法的实验条件不易掌控,大量的有毒试剂易对环境造成污染。近年来,科研工作者报道了基于电化学方法合成电化学还原石墨烯(Electrochemical reduced graphene oxide,ERGO)的方法[11-14]。相对于其它方法,该方法由于绿色环保、高效、简便、成本低廉而成为研究热点。该方法制备的ERGO已经成功用于如葡萄糖[1]、DNA[2]、酚类[4-5,15]、多巴胺[16]、H2O2[17-18]等的分析检测。
对苯二酚(HQ)是一种重要的酚类化合物,在日常生产和生活中广泛应用于照相显影剂、合成染料、阻聚剂、抑制剂、橡胶防老剂和食品抗氧化剂等,对人体有较大毒性,对皮肤、眼睛、粘膜有刺激作用。目前测定对苯二酚的方法主要有分光光度法、高效液相色谱法、薄层色谱法、毛细管电泳法等。这些技术虽然应用比较广泛,但使用的仪器昂贵、试剂消耗量大且分析时间较长,不能满足现场快速检测的需求。大多数电分析方法具有省时、成本低、选择性好、灵敏度高、响应快、仪器简单等优点。目前,已有一些关于用纳米材料修饰电极快速检测对苯二酚的文献报道[4,19-21]。
本研究采用一步电化学共还原的方法将纳米金(AuNPs)、Nafion、电化学还原石墨烯(ERGO)修饰到玻碳电极(GCE)表面,制成修饰电极AuNPs/Nafion/ERGO/GCE,并将制备的修饰电极用于对苯二酚的检测,研究结果表明,该方法简便、灵敏,具有较好的选择性。
1 实验部分
1.1 仪器与试剂
电化学实验均在CHI430b电化学工作站(上海辰华仪器有限公司)上进行,采用三电极系统,以AuNPs/Nafion/ERGO/GCE为工作电极,饱和甘汞电极(SCE)为参比电极,铂丝电极为辅助电极。IRPrestige-21傅立叶变换红外光谱仪(日本岛津公司),JEOL_JSM_6500F扫描电子显微镜(SEM)。修饰电极界面的电化学交流阻抗(EIS)实验在含5.0 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1∶1)的0.1 mol/L KCl溶液中进行,测量范围为0.2 Hz~100 kHz。
氧化石墨烯购于南京先锋纳米材料科技有限公司,Nafion(5%,乙醇溶液)购于Sigma公司,氯金酸HAuCl4·4H2O(Au% >47%,北京化学试剂公司)、对苯二酚(天津市福晨化学试剂厂)以及实验所用其它试剂均为分析纯,实验以pH 7.0的0.1 mol/L磷酸缓冲溶液(PBS)为底液,实验用水为二次蒸馏水。
1.2 修饰电极的制备
玻碳电极用0.03 μm Al2O3粉末抛光成镜面,用水冲洗后,依次用无水乙醇和水各超声清洗5 min,氮气吹干备用。取1.0 mg GO在10 mL水中超声分散30 min,制成0.10 g/L的GO悬浊液。用微量进样器吸取10.0 μL GO悬浊液滴涂于清洗干净的裸玻碳电极表面,室温下自然晾干,制成GO/GCE。用微量进样器将0.5%的Nafion溶液6.0 μL滴涂在GO/GCE表面,自然晾干,用水清洗后备用。
将制得的Nafion/GO/GCE在0.5 g/L HAuCl4溶液中(预先通入高纯氮气除氧30 min,氮气氛保护),于-1.3 V恒电位电沉积400 s,使金微粒沉积于电极表面,将该电极用水清洗干净,高纯氮气吹干,即制得修饰电极AuNPs/Nafion/ERGO/GCE。
1.3 电化学测定
在测定之前,修饰电极在0.1 mol/L PBS中于-0.6~0.6 V循环扫描至稳定。在盛有10 mL pH 7.0的PBS中,加入一定量的对苯二酚,通高纯氮气除氧10 min后,进行电化学测定,整个实验均在氮气氛保护下进行。微分脉冲伏安法(DPV)实验参数为:电位扫描范围为-0.3~0.3 V;振幅0.05 V;脉冲宽度0.05 s;脉冲时间0.2 s;静止时间20 s。整个实验过程均在室温下进行。
2 结果与讨论
2.1 电化学还原制备ERGO
图1为氧化石墨烯在PBS中以-1.3 V恒电位还原的I~t曲线,从图中可观察到,在前5 s时电流下降很快,随后电流下降逐渐变缓,在100 s左右电流达到稳定状态。采用傅立叶变换红外光谱(FTIR)对-1.3 V恒电位制备的ERGO薄膜作进一步表征(见图2),图中曲线a为纯GO的红外光谱,在853、1 049、1 171、1 232、1 730cm-1附近的吸收带均由 GO 中含氧官能团产生[14,22-23],在 1 619 cm-1附近的吸收带归结为夹层中水分子O-H的变形振动。GO经过电化学还原后,其含氧基团的FTIR吸收带明显减少甚至消失(曲线b),表明恒电位电化学法已成功地将GO转变成ERGO。在后续实验中均采用-1.3 V对GO进行电化学还原。
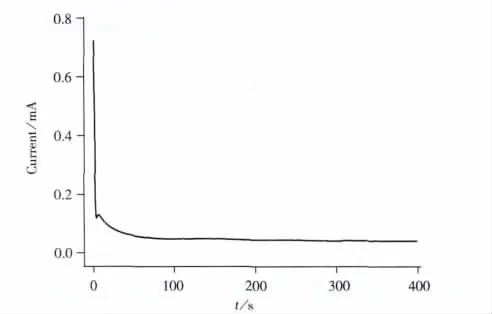
图1 GO/GCE在除氧的PBS(0.1 mol/L,pH 7.0)中以-1.3 V恒电位电化学还原GO的I~t曲线Fig.1 I-t curve of GO/GCE in PBS(0.1 mol/L,pH 7.0)at the potential of-1.3 V

图2GO(a)及ERGO(b)的傅立叶变换红外光谱图Fig.2 FTIR spectra of GO(a)and ERGO(b)
2.2 SEM表征
图3为金纳米粒子沉积在GO/GCE和Nafion/GO/GCE上的扫描电镜图,对比图3A、B可以看出,在未修饰Nafion的GO/GCE上电沉积的纳米金分布比较致密(图3A),而在玻碳电极表面修饰上Nafion和GO之后电沉积纳米金,会使电极的比表面积增大(图3B),Nafion膜具有网状结构,能使金属纳米粒子分布更均匀,从而加快电子的传递速率[24]。如图3所示,金纳米粒子的粒径在40~60 nm之间。

图3 AuNPs/ERGO/GCE(A)及AuNPs/Nafion/ERGO/GCE(B)修饰电极表面放大50 000倍的SEM图Fig.3 SEM images of AuNPs/ERGO/GCE(A)and AuNPs/Nafion/ERGO/GCE(B)with 50 000 times magnification insert images are 100 000 times magnification
图4为不同修饰电极的电化学阻抗图谱,在高频观察到的半圆部分与电荷转移限制过程相对应。电荷转移电阻Rt可以通过直接测量半圆直径获得。从图4插图可看到,当GO被修饰到裸玻碳电极后,半圆直径明显增大。这说明电极表面电阻增大,阻碍了界面电荷转移。此外,GO电极表面的负电荷排斥铁氰化物和亚铁氰化物离子通过电荷传递到达电极表面[13-14]。当电极表面上的 GO膜被电化学还原后,半圆直径明显减小,说明ERGO能够加快[Fe(CN)6]3-/4-与电极间的电荷传递。对于Nafion/ERGO/GCE,半圆直径非常小,而在AuNPs/Nafion/ERGO/GCE修饰电极上,界面阻抗最小,说明Nafion和金纳米粒子均可降低电极表面的界面阻抗并提高电荷的传递性能。因此,本文设计的修饰电极能加快电荷在溶液与电极间的传递过程。
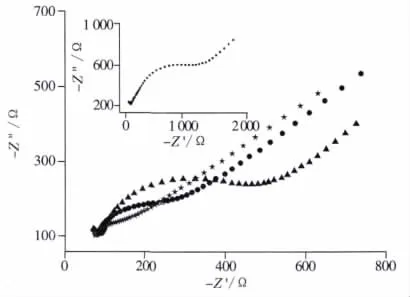
图4 不同修饰电极在含有5.0 mmol/L K3[Fe(CN)6] /K4[Fe(CN)6](1 ∶1)的 0.1 mol/L KCl溶液中的电化学阻抗图谱Fig.4 EIS curves of different electrodes in 5.0 mmol/L K3[Fe(CN)6] /K4[Fe(CN)6](1 ∶1)and 0.1 mol/L KCl▲:ERGO/GCE,●:Nafion/ERGO/GCE,★:AuNPs/Nafion/ERGO/GCE;insert:GO/GCE
2.3 对苯二酚电化学行为的研究
采用循环伏安法考察了不同修饰电极在含有5.0×10-4mol/L HQ的PBS缓冲溶液中的电化学行为(图5)。从图中可以观察到,裸玻碳电极(曲线a)分别在0.0 V和0.124 V附近出现1个还原峰和1个氧化峰,其峰电位差ΔEp=0.124 V。在修饰了GO的GO/GCE电极上(曲线 b),ΔEp=0.217 V,峰电流减小,然而在ERGO/GCE上(曲线c),ΔEp=0.171 V且峰电流明显增大,这是由于GO含有大量的含氧官能团如COOH,导电性能差,阻碍了电子传递。GO通过恒电位电化学还原后,转变为导电性良好的石墨烯,增加了电子传递速率。在AuNPs/ERGO/GCE上(曲线d),ΔEp=0.061 V且峰电流进一步增强。实验结果说明电沉积的纳米金粒子和电化学还原石墨烯对对苯二酚有较强的协同催化活性。在AuNPs/Nafion/ERGO/GCE上(曲线 e),峰电位差几乎不变,但峰电流略有增加,这是由于修饰Nafion后,增大了电极表面沉积纳米金的比表面积。

图5 不同修饰电极在5.0×10-4mol/L HQ中的循环伏安图Fig.5 Cyclic voltammograms of 5.0×10-4mol/L HQ at different electrodes a.GCE,b.GO/GCE,c.ERGO/GCE,d.AuNPs/ERGO/GCE,e.AuNPs/Nafion/ERGO/GCE;pH 7.0 PBS
2.4 电极修饰条件的优化
采用微分脉冲伏安法对GO、Nafion及金微粒负载量、检测溶液的pH值进行优化,溶液中HQ的浓度为5.0×10-5mol/L。在裸玻碳电极表面修饰10 μL GO时,HQ氧化峰电流达到最大。当GO用量超过10 μL后,氧化峰电流随着GO用量的增加而减小。HQ氧化峰电流首先随着Nafion用量的增加而增加,但当Nafion用量超过6 μL后,由于电极表面Nafion膜过厚,增大了修饰电极的界面电阻,阻碍了对苯二酚与玻碳电极的电子交换,之后氧化峰电流随Nafion用量的逐渐增加而降低。故本文以GO用量为10 μL、Nafion用量为6 μL作为制备AuNPs/Nafion/ERGO/GCE的最佳用量。
实验通过控制恒电位沉积的时间对金纳米粒子的负载量进行控制。随着沉积时间的增加,氧化峰电流也相应增大。当沉积时间超过400 s后,峰电流减小,这是由于随着电沉积时间的延长,导致金粒子的粒径过大,从而降低了其电催化活性。因此,本文选择-1.3 V电位下沉积400 s时的金纳米粒子的量作为最佳负载量。
底液的pH值也显著影响HQ在修饰电极上的电流响应。在pH 4.0~7.0间,随着pH值的增大,HQ的氧化峰电流也逐渐增大。当pH值等于7.0时,HQ氧化峰电流达到最大。pH值进一步增大时,则氧化峰电流随之减小。HQ的阳极峰电位(Epa)和阴极峰电位(Epc)则均随着pH值增大而逐渐正移,说明H+参与了HQ在电极表面的电化学氧化还原过程。本文以pH 7.0的0.1 mol/L PBS作为测试底液。
2.5 工作曲线
在-0.3~0.3 V电位范围内用微分脉冲伏安法记录不同浓度的HQ在AuNPs/Nafion/ERGO/GCE电极上的伏安曲线(如图6)。优化条件下,在2.0~800 μmol/L范围内,HQ氧化峰电流随其浓度的增大而增大,且HQ氧化峰电流与其浓度分别在 2.0 ~100 μmol/L 和100~800 μmol/L 范围内呈良好的线性关系,线性方程分别为:Ipa(μA)=1.904+0.162 0c(μmol/L)(r=0.997)和Ipa(μA)=14.36+0.404 4c(μmol/L)(r=0.998),检出限(S/N=3)为 3.0×10-7mol/L。

图6 不同浓度HQ在AuNPs/Nafion/ERGO/GCE上的微分脉冲伏安图Fig.6 DPV curves of HQ at AuNPs/Nafion/ERGO/GCE HQ concentration(a-k):0,5.0,10.0,25.0,50.0,75.0,100,200,400,600,800 μmol/L;0.1 mol/L PBS(pH 7.0);insert:the corresponding calibration curve
表1比较了一些用于HQ检测的不同修饰电极方法,本文所采用的修饰电极展现了较宽的线性范围和较低的检出限。
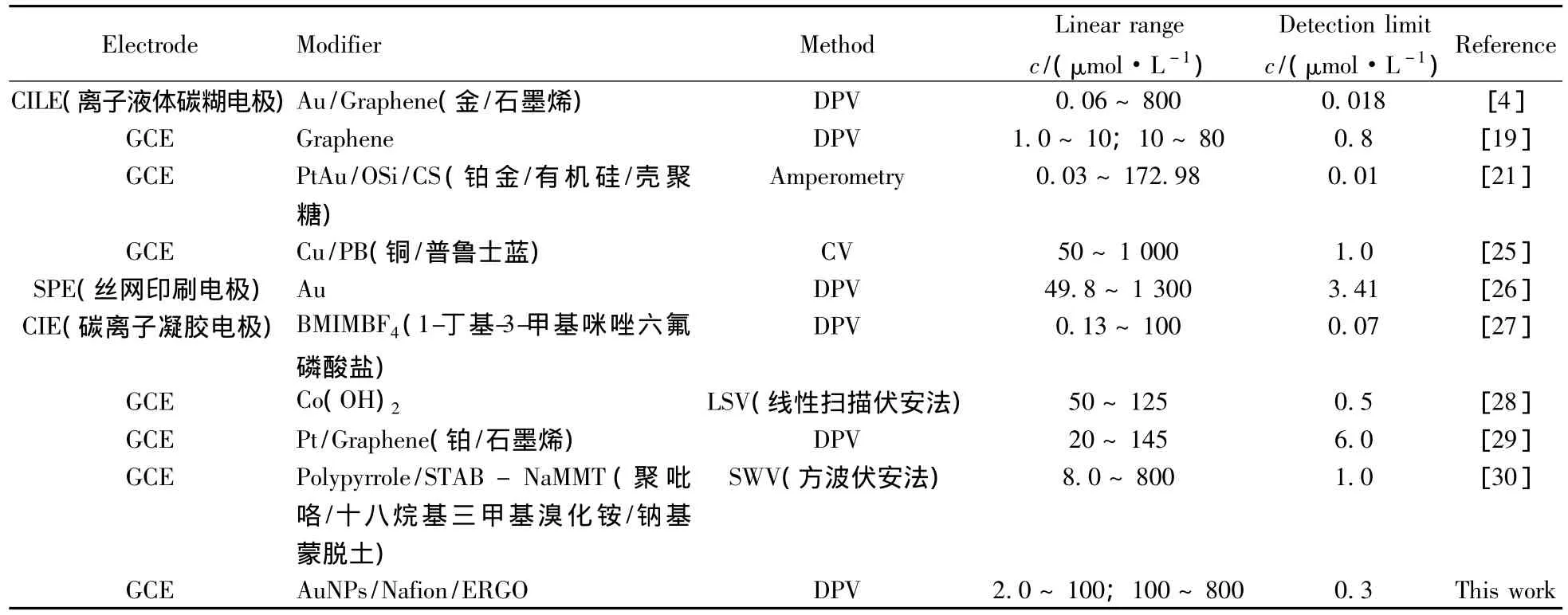
表1 用于检测HQ的不同电极间的比较Table 1 Comparison of the different electrodes for the detection of HQ
2.6 共存组分的干扰
考察了不同浓度的共存组分对HQ测定的干扰,实验结果表明:对于5.0×10-5mol/L的HQ溶液,100 倍的 Na+、K+、Ca2+、Mg2+、Cl-、SO24-、NO3-、CO23-均不干扰HQ的测定;300倍的葡萄糖,100倍的尿素,5倍的苯酚、间苯二酚、氨基乙酸、苯甲酸均不干扰HQ的测定(峰电流改变<5%)。
2.7 重现性与稳定性
用同1支修饰电极平行测定8次,HQ峰电流的相对标准偏差(RSD)为2.1%;以相同条件下制备的5支电极进行测定,HQ峰电流的相对标准偏差(RSD)为3.4%。将使用过的修饰电极清洗干净后,于4℃保存15 d,该电极对HQ的响应电流仍为最初响应电流的95%以上。表明电极具有良好的重现性和稳定性。
2.8 实际水样的测定
实际水样分别取自北京市凉水河、通惠河以及自来水,经0.45 μm滤膜抽滤处理后进行HQ的检测实验。以 AuNPs/Nafion/ERGO/GCE为工作电极测定水样,均未检测出HQ。加入一定量的HQ配成模拟水样,采用标准加入法进行检测,得到样品的回收率在97.8%~104%之间(见表2),说明本方法可用于实际样品中HQ的测定。
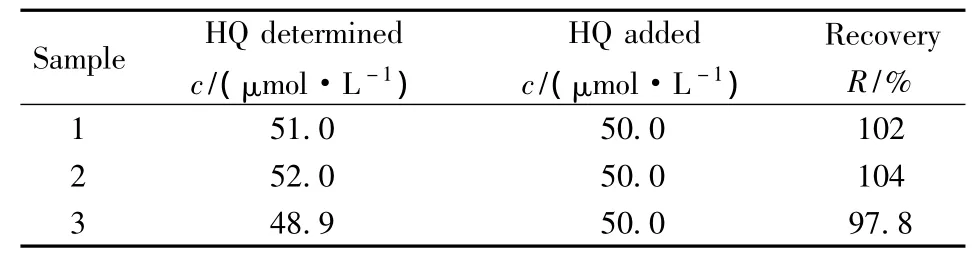
表2 模拟水样中HQ加标回收率的测定(n=4)Table 2 Recoveries of HQ in simulated water samples(n=4)
3 结论
本文利用一步共还原的方法在玻碳电极上修饰AuNPs/Nafion/ERGO/复合膜,研究了HQ在修饰电极上的电化学行为,建立了灵敏测定HQ的新方法。实验结果表明,该修饰电极在中性条件下对HQ的氧化还原过程具有良好的电催化活性。该修饰电极制备简单、响应快、重现性好,可用于实际水样中对苯二酚的测定。
[1] Luo J,Zhang H Y,Jiang S,Jiang S S,Jiang J Q,Liu X Y.Microchim.Acta,2012,177(3/4):485 -490.
[2] Fan Y,Huang K J,Niu D J,Yang C P,Jing Q S.Electrochim.Acta,2011,56(12):4685 -4690.
[3] Zhao J,Chen G F,Zhu L,Li G X.Electrochem.Commun.,2011,13(1):31 -33.
[4] Hu S,Wang Y H,Wang X Z,Xu L,Xiang J,Sun W.Sens.Actuator B,2012,168(20):27-33.
[5] Huang K J,Yu S,Wang L,Gan T,Li M.Acta.Chim.Sin.,2012,70(6):735 -740.
[6] Wang Y,Yu H,Jian X,He X F,Qi G C.J.Instrum.Anal.(王毅,于浩,简选,贺小芳,齐广才.分析测试学报),2012,31(12):1581-1585.
[7] Liu T,Xu M R,Yin H S,Ai A Y,Qu X J,Zong S S.Microchim.Acta,2011,175(1/2):129 -135.
[8] Unnikrishnan B,Palanisamy S,Chen S M.Biosens.Bioelectron.,2013,39(1):70 -75.
[9] Umasankar Y,Unnikrishnan B,Chen S M,Ting T W.Anal.Methods,2012,4(11):3653 -3660.
[10] Bo Y,Wang W Q,Qi J F,Huang S S.Analyst,2011,136(9):1946 -1951.
[11] Chen L Y,Tang Y H,Wang K,Liu C B,Luo S L.Electrochem.Commun.,2011,13(2):133-137.
[12] Ping J F,Wang Y X,Fan K,Wu J,Ying Y B.Biosens.Bioelectron.,2011,28(1):204-209.
[13] Deng K,Zhou J,Li X.Colloid.Surf.B,2013,101:183-188.
[14] Guo H L,Wang X F,Qian Q Y,Wang F B,Xia S H.ACS.Nano,2009,3(9):2653-2659.
[15] Zhang Y,Zhang J L,Wu H X,Guo S W,Zhang J Y.J.Electroanal.Chem.,2012,681:49-55.
[16] Si P,Chen H L,Kannan P,Kim D H.Analyst,2011,136(24):5134 -5138.
[17] Palanisamy S,Unnikrishnan B,Chen S M.Int.J.Electrochem.Sci.,2012,7(9):7935-7947.
[18] Zhang L L,Cheng H H,Zhang H M,Qiu L G.Electrochim.Acta,2012,65:122-126.
[19] Li S J,Xing Y,Wang G F.Microchim.Acta,2012,176(1/2):163 -168.
[20] Li Y Y,Qin C,Chen C,Fu Y C,Ma M,Xie Q J,Sens.Actuators B,2012,168:46-53.
[21] Yuan D H,Chen S H,Hu F X,Wang C Y,Yuan R.Sens.Actuators B,2012,168:193-199.
[22] Li S J,Deng D H,Pang H,Liu L,Xing Y,Liu S R.J.Solid State Electrochem.,2012,16(9):2883 -2889.
[23] Zhou M,Zhai Y M,Dong S J.Anal.Chem.,2009,81(14):5603-5613.
[24] Zhou Z L,Kang T F,Zhang Y,Cheng S Y.Microchim.Acta,2009,164(1/2):133-138.
[25] Liu Z R,Wang Y C,Gong Q J,Ma H X.J.Instrum.Anal.(刘赵荣,王玉春,弓巧娟,马会宣.分析测试学报),2010,29(2):171-175.
[26] Song W,Zhang L,Shi L,Li D W,Long Y T.Environ.Chem.(宋伟,张磊,石磊,李大伟,龙亿涛.环境化学),2010,29(1):132-136.
[27] Sun X Y,Hu S,Li L F,Xiang J,Sun W.J.Electroanal.Chem.,2011,651(1):94-99.
[28] Fan L F,Wu X Q,Guo M D,Gao Y T.Electrochim.Acta,2007,52(11):3654-3659.
[29] Li J,Liu C Y,Cheng C.Electrochim.Acta,2011,56(6):2712 -2716.
[30] Li R,Xiong J,Zhu W Q,Han Y Y,Xu J,He X Y.Electrochemistry(李荣,熊健,朱伟琼,韩园园,徐进,何晓英.电化学),2011,17(4):453-457.
