高效液相色谱法构建黄连上清丸指纹图谱
2013-10-08张少君车燕妮苏秀娟张凌斐张吉芬
张少君 车燕妮 苏秀娟 张凌斐 张吉芬
威海市疾病预防控制中心,山东 威海 264003
应用指纹图谱监控中药材或中成药的质量的稳定性和专一性在国际上已成为一种趋势[1],美国食品药品监督管理局(FDA)[2]、欧共体药审委(EMEA)[3]和世界卫生组织(WHO)均要求提供植物药产品的指纹图谱以保证其质量的一致性。2000年,国家药品监督管理局颁发了《中药注射剂指纹图谱的技术要求(暂行)》,确立了指纹图谱的法定地位。
黄连上清丸是著名的解表药,主要功能是清热通便,散风止痛[4]。中国药典(2010版)采用薄层扫描法控制其中盐酸小檗碱的含量,药方中黄连和黄柏两者都含有小檗碱,但二者功效不同,只测定小檗碱的含量不能真实反映药品的质量。黄连上清丸结构复杂,其指纹图谱尚未见报,本文利用高效液相色谱(HPLC)法研究构建指纹图谱及数字化指纹谱,以便较全面有效地评价控制该制剂的质量,供企业鉴别质量参考。
1 材料和方法
1.1 实验材料
高效液相色谱系统(岛津,日本)。色谱柱(250×4.6mmI.D.,5 m,安捷伦,美国)。紫外分光光度计(UV2401PC,岛津,日本);分析天平(Sartorius,BS210S,德国);超声波清洗器(Cole-Pharmer, USA)。
色谱纯甲醇(Caledon Laboratories, Canada),乙腈(Fisher Scientific, UK),乙酸(科密欧,天津,中国)和三乙胺(Tedia, USA)用于样品的制备和配制流动相。所有样品的制备均使用超纯水。盐酸小檗碱(批号:110713-200208)和黄芩苷(批号:110715-200514)均购自于中国药品生物制品检定所。黄连上清丸随机购于全国各医院或药房(见表1)。

表1 黄连上清丸的生产厂家及批号
1.2 实验方法
1.2.1 样品溶液的制备
将黄连上清丸水丸研成粉末,称取100 mg,用70%甲醇+30% 0.2M盐酸溶液超声提取60 min;再用5,000 r/min离心10 min,0.45μm滤膜过滤,备用。
1.2.2 高效液相色谱的分析条件
实验采用双泵洗脱梯洗脱:流动相A相(甲醇-水-乙酸-三乙胺=10:89.1:0.8:0.1),B相(甲醇-水-乙酸-三乙胺=89.1:10:0.8:0.1)[5];洗脱梯度:0~10 min: 5~20%B, 10~50 min: 20~55% B, 50~70 min: 55~100% B,70~80 min: 100% B。流速0.9 mL/min。检测波长254 nm,柱温40℃。上样量20μl。
2 结果与讨论
2.1 检测方法的评价
根据《中华人民共和国药典》(2005年版),《中药质量标准分析方法验证指导原则》的规定,进行方法学评价。本实验验证的内容包括准确度、精密度、检测限、定量限和线性。
2.1.1 准确度
标准样品中小檗碱和黄芩苷的含量分别为0.058mg/mL和0.308mg/mL,再分别加入0.1mg/mL的标准品,用6个测定结果进行评价,测得平均回收率分别为96.8%,99.5%,RSD分别为0.9%,0.7%。
2.1.2 精密度
取同一样品溶液重复进样6次,计算得小檗碱、黄芩苷保留时间的RSD分别是0.4232%和0.4738%,具有较高的精密度。
2.1.3 检测限和定量限
黄连上清丸在信噪比为3:1的条件下检测,标准品的检测限都低于0.1μg/mL。以信噪比为10:1时相应的浓度进行确定,定量限为1μg/mL。
2.1.4 线性
分别将储备液稀释成0.001mg/mL-1.0mg/mL制成系列标准品溶液,用HPLC法进行线性回归分析。盐酸小檗碱0.001~1mg范围内线性良好,回归方程为y=111702327x-146629(R2=0.9998,n=7);黄芩苷在0.001mg~1.5mg范围内线性良好,回归方程为y=32382153x-18828(R2=0.9999,n=7)。
方法学评价的结果证明此方法的各项指标符合指纹图谱的要求,适合本研究的应用。
2.2 HPLC指纹图谱的构建
为有效控制不同厂家黄连上清丸中有效成分的含量及分布,本文根据《中药注射剂指纹图谱研究的技术要求》建立了HPLC指纹图谱。当采用1.2.3的分析条件时,主要色谱峰基本达到基线分离,指标成分盐酸小檗碱与其相邻色谱峰的分离度很好。12个黄连上清丸图像式指纹图谱见图1,每个记录曲线均有50多个峰,样品间的比较和描述比较困难,因而从这些色谱峰中挑选出在样品中均稳定出现的峰,即共有峰,黄连上清丸共设定了17个共有峰(图2)。一组样品中的共有峰,代表了一类生物样品的共性,体现了该品种的特性,是与其他品种的区别之处。从而构成了该生物体所特有的指纹,也称为特征指纹。特征指纹峰的差异反映了同一品种生物体因不同产地、不同采收期等因素造成的质量差异,可用作原料药材、原料药、中间体及成药的质控参数。为保障特征指纹峰的代表性,共有峰的峰面积至少占总峰面积的60%。从图象式指纹谱上可以看出主要成分的浓度的整体分布、保留时间和共有峰的含量大致差异。但仅通过图像式指纹谱难以对12个样品做出定量的判断,而且图像式指纹谱本身也受操作因素的影响,从而导致较低的稳定性和重现性。

图1 黄连上清丸图象式指纹谱Fig. 1 HPLC fingerprint of 12 coptis bolus for clearing the upper heat samples

图2 黄连上清丸的共有峰Fig. 2 Common peaks of coptis bolus for clearing the upper heat
2.3 黄连上清丸高效液相色谱数字化指纹谱
数字化色谱指纹谱是将复杂难辨的图谱转为直观的数字,建立一系列参数和相应的一整套比较规则和计算公式,有效地改善了原始色谱图的波动性,使色谱图之间的直观比较改变为数据之间的比较,从而增强了样品相互间的可比性。
洪筱昆教授最早创立了数字化指纹谱法,以相对保留时间和相对峰面积为主要参数,计算指纹谱重叠率、相似度和n强峰、特征指纹差异率并绘制特征指纹曲线等。本实验组以此为基础并对数字化指纹图谱的表现形式进行了改进。
2.3.1 特征峰的相对保留时间和相对峰面积
黄连上清丸设定以盐酸小檗碱作为参照峰,因它它是中药的主要有效成分、它位于谱图的中央位置而且与周围峰有良好的分离度,并在12个样品中稳定出现,且与前后两色谱峰分离度较好。其相对保留时间和相对峰面积设为1.00,其他共有峰的保留时间及峰面积分别与之相比,得到了特征指纹峰的相对保留时间和相对峰面积。共有峰的相对保留时间的RSD在0.357~0.959%之间,均在方法误差范围内,认为对应色谱峰均为同一组分。各厂家黄连上清丸样品中各组对应洗脱峰相对峰面积的RSD在66.020%~112.281%之间,远大于10%,超出了方法误差,认为对应组分含量差异显著。
2.3.2 特征指纹峰差异率
共有峰差异率及特征指纹差异率按式(1.1)及式(1.2)计算,假定以1号样品作为标准制剂,因为1号样品的含量适中,其他样品为待鉴制剂,各样品的差异率及总差异率见表2。可以看出2号样品、5~7号、9~12号样品与S1相似程度较高,而3号、4号、8号样品与标准样品间均存在较大差异。

AI鉴—待鉴样品中某个峰的归一化面积值;AI标—标准样品中某个峰的归一化面积值;n—特征指纹谱峰的总数。
2.3.3 特征指纹曲线
黄连上清丸样品的特征指纹曲线(图3)可以直观地反映不同样品之间的近似程度,从整体角度看2号、5~7号、9~12号样品与作为标准样品S1相似程度很高,而3号、4号、8号样品与标准样品间均存在很大差异,这与总差异率的实验结果一致。
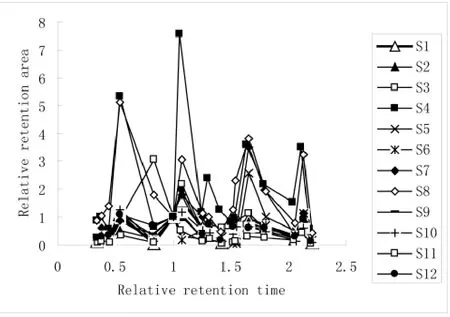
图3 黄连上清丸特征指纹曲线Fig. 3 Characteristic fingerprint curve of coptis bolus for clearing the upper heat samples
2.3.4 数字化指纹谱的改进
本实验组建立的数字化指纹图谱以洪教授的数字化指纹谱法为基础,改进了原有数字化指纹谱的表现形式,不仅包括相对保留时间和相对峰面积,还包括它们的相对标准偏差及差异率,使样品间的量化比较一目了然。所反映的化学成分包括了研究对象的重要指标成分,体现了指纹图谱的系统性;指纹图谱中反映的化学成分信息(如保留时间或迁移值)具有高度选择性,这些成分之间的顺序、比值在一定范围内是固定的,体现了特征性;在样品制备方法、分析条件、结果处理等环节规范操作的前提下,由不同的操作者作出的指纹图谱,其误差在允许范围内,保证了指纹图谱的使用具有通用性和实用性(表2)。
3 结语
本文构建了黄连上清丸的图象式指纹图谱和数字化指纹谱。从图象式指纹谱上可以直观地判断不同样品共有峰的含量差异比较显著,这是由于原料、加工过程等多种因素引起。在数字化指纹谱中,通过对不同参数进行评价,推断出每个厂家都按规定投入了十七味原药材,而药材的品质以及药材的投入量却有显著差异。该方法可借鉴用于其他不同厂家不同批次的制剂鉴定与评价参考。

表2 黄连上清丸改进后的的数字化指纹图谱
[1]Manhua Liu, Pew-Thian Yap, Invariant representation of orientation fields for fingerprint indexing. Pattern Recognition, 2012, 45(7):
2532-2542.
[2]FDA Guidance for Industry-Botanical Drug Products (Draft Guidance).US Food and Drug Administration, Rockville, 2000, pp.18 22.
[3]Note for Guidance on Quality of Herbal Medicinal Products.European Medicines Agency, London, 2001.
[4]国家药典委员会. 中华人民共和国药典, 2010年版,一部[S]. 北京:人民卫生出版社,2005.
[5]Shaojun Zhang, Fan Ouyang, Changhai Wang, and Ming Gu,Fingerprint of Tablet of Corydalis tuber for Alleviating Pain by HPLC.Journal of Liquid Chromatography & Related Technologies, 31: 452-464, 2008。
[6]洪筱坤,王智华. 中药数字化色谱指纹谱[M]. 上海:上海科学技术出版社,2003.
