夏天无鲜药材的产地初加工工艺研究△
2013-09-26张双李瑶钟晓红曾建国
张双,李瑶,钟晓红,曾建国,*
(1.湖南农业大学,湖南 长沙 410128; 2.湖南农业大学,国家中药材生产(湖南)技术中心,湖南 长沙 410128; 3.湖南省中药提取工程研究中心,湖南 长沙 410331)
夏天无鲜药材的产地初加工工艺研究△
张双1,李瑶2,3,钟晓红1,曾建国1,2,3*
(1.湖南农业大学,湖南 长沙 410128; 2.湖南农业大学,国家中药材生产(湖南)技术中心,湖南 长沙 410128; 3.湖南省中药提取工程研究中心,湖南 长沙 410331)
目的:本文以夏天无药材为研究对象,通过比较不同产地初加工方法对夏天无鲜药材中原阿片碱、盐酸巴马汀及延胡索乙素3种生物碱的影响,确定夏天无最佳产地初加工工艺。方法:采用HPLC法测定夏天无中三种生物碱的含量,对采收期内的夏天无鲜药材进行晒干、阴干、不同温度烘干等干燥处理,比较不同干燥方式对3种生物碱的影响,确定夏天无的最佳产地初加工工艺。结果:不同干燥处理方式的对夏天无中3种生物碱指标成分的含量有较大的影响,在30 ℃晒干条件下3种指标成分含量最高。结论:夏天无的最佳产地初加工工艺流程:春季或初夏出苗后采挖→除去茎、叶及须根→清洗或擦净→30 ℃晒干。
夏天无;原阿片碱;盐酸巴马汀;延胡索乙素;产地初加工
夏天无为罂粟科Papaveraceae植物伏生紫堇Corydalisdecumbens(Thunb.)Pers.的干燥块茎。主产于江西,在湖南、浙江、江苏等地有分布[1],为民间常用药材,具有活血祛瘀,通络,行气止痛的功效,能降压镇痉。用于中风偏瘫,半身不遂,跌打损伤,风湿性关节炎,坐骨神经痛,小儿麻痹后遗症。夏天无的主要有效成分为生物碱类,含有原阿片碱、延胡索乙素等20余种生物碱[2-3]。2010年版《中国药典》规定,夏天无以原阿片碱和盐酸巴马汀为指标成分[4]。研究报道原阿片碱具有镇痛、改善微血管循环等作用[5-6]。盐酸巴马汀具有抗炎、抗肿瘤和抗菌等药理药效作用[7]。而延胡索乙素镇痛作用强,对持续性、慢性钝痛有极佳镇痛效果[8]。因此对夏天无中原阿片碱、盐酸巴马汀及延胡索乙素3种成分含量的控制可以作为夏天无产地初加工的重要指标。
2010年版《中国药典》规定夏天无春季或初夏出苗后采挖,产地初加工方式为除去茎、叶及须根,洗净,干燥[4],但干燥方式不明确。大量现代研究表明,鲜药材和干药材以及经加工炮制过的中药饮片的化学成分在种类和含量上存在着较大的差异,药效作用上也有显著不同[9]。本研究以夏天无为目标药材,通过比较不同初加工方式对夏天无3种指标成分含量的影响,确定最佳的产地初加工工艺,最大程度地保留夏天无鲜药材中的活性成分,将最佳使用状态的鲜药材转变为高品质、可稳定储存的干药材,为中药的有效利用提供坚实的基础。
1 仪器与材料
Agilent 1260 Series 高效液相色谱仪(G1311C二元高压梯度水泵G1329B在线脱气机,G1315D二极管阵列检测器,ChemStation化学工作站);XCharge C18色谱柱(华谱新创科技有限公司);AE240型电子天平(梅特勒-托利多仪器有限公司);KQ5200DE型超声波清洗器(昆山超声仪器有限公司);DHG-9246A型电热恒温干燥箱(上海精宏实验设备有限公司);冷冻离心机(HERMLE 2323K,德国);FW100型高速万能粉碎机(天津市太斯特仪器有限公司);微波炉(格兰仕);Milli-Q纯水处理系统(美国MILLIPORE公司)
原阿片碱(86.2%)对照品购自中国药品生物制品鉴定所,盐酸巴马汀(98%)、延胡索乙素(98%)对照品购自中国食品药品检定研究院;乙腈(色谱纯,美国默克),甲醇(色谱纯,美国默克),三乙胺(国药集团化学试剂有限公司),乙酸胺(国药集团化学试剂有限公司),水为Milli-Q超纯水。
2.1 检测方法
参照2010版《中国药典》夏天无项下方法进行检测,色谱图如图1所示,为夏天无样品以及对照品盐酸巴马汀、原阿片碱和延胡索乙素的高效液相检测图谱。图A、图B分别为混标在345 nm波长下盐酸巴马汀对照品检测图谱及混标在289 nm波长下原阿片碱和延胡索乙素对照品检测图谱。图C、图D分别为夏天无样品在345 nm波长下盐酸巴马汀对照品检测图谱及夏天无样品在282 nm波长下原阿片碱和延胡索乙素对照品检测图谱。
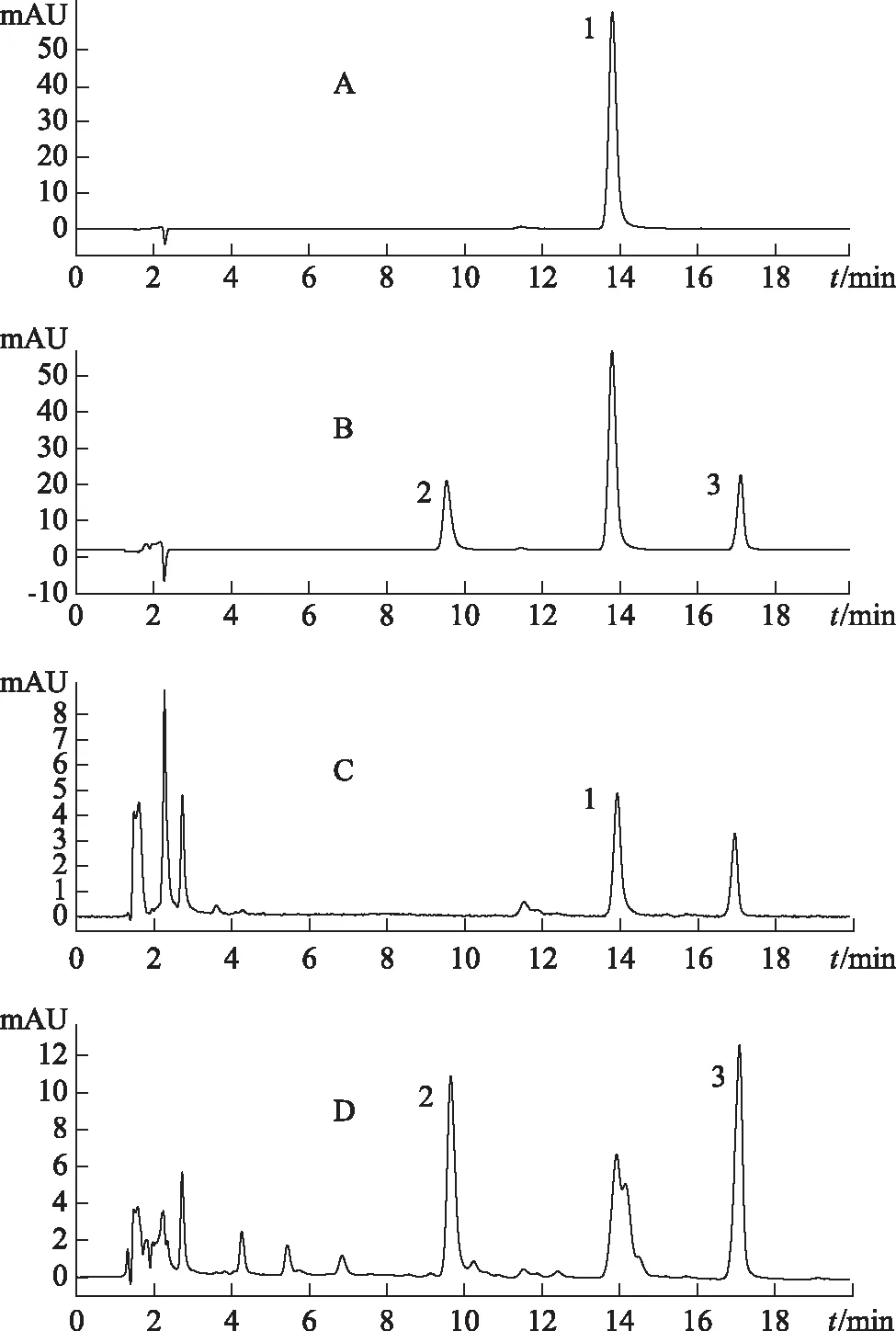
1.盐酸巴马汀 2.原阿片碱 3.延胡索乙素图1 标准品盐酸巴马汀(A),原阿片碱和 延胡索乙素(B)及夏天无样品中盐酸巴马汀(C), 原阿片碱和延胡索乙素(D)的高效液相色谱图
2.2 混合对照品溶液
单标溶液配制:精密称取盐酸巴马汀29.5 mg,加入甲醇50 mL,配成含盐酸巴马汀0.506 mg·mL-1的溶液;精密称取原阿片碱15.1 mg,加入甲醇10 mL,配成含原阿片碱1.47 mg·mL-1的溶液;精密称取延胡索乙素15.1 mg,加入甲醇10 mL配成含延胡索乙素1.47 mg·mL-1的溶液,作为对照品贮备液,于4 ℃冰箱避光保存。
混标溶液配制:分别取上述盐酸巴马汀溶液10 mL、延胡索乙素与原阿片碱各5 mL至25 mL容量瓶中,用甲醇定容(含盐酸巴马汀0.203 mg·mL-1,延胡索乙素0.294 mg·mL-1,原阿片碱0.294 mg·mL-1)至25 mL。
2.3 供试品溶液
采摘:初夏从国家中药材生产(湖南)技术中心核心基地采采摘,经湖南农业大学园艺园林学院谢红旗副教授鉴定为罂粟科植物伏生紫堇Corydalisdecumbens(Thunb.)Pers.。
洗净沥干:将所采集的夏天无,除去茎、叶及须根,挑选新鲜、无腐败的鲜药材,去除表面杂物洗净,沥干表面水分,待用。
干燥:夏天无鲜药材采摘后4 h内作如下处理:
烘干:将夏天无的根平铺于不锈钢方盘中,厚度不超过2 cm,分别于45 ℃、60 ℃、85 ℃、105 ℃烘箱中快速烘干;
晒干:将夏天无的根平摊在太阳下直晒至干,温度为30 ℃左右;
阴干:将夏天无的根平铺于室内干燥通风处晾干;
微波干燥:将夏天无的根平铺于不锈钢方盘中,厚度不超过2 cm,放入微波炉中干燥。
鲜药材供试品溶液的制备:取鲜药材适量于粉碎机中快速粉碎,快速称取粉碎样0.5 g于锥形瓶中,其它步骤同前,即得供试液(此过程均在采样4 h之内完成)。
干药材供试品溶液的制备:取不同加工方式得到的干药材粉碎,称取0.5 g左右药材粗粉,加入甲醇50 mL,密封,称定重量,超声提取(250 W,频率100 kHz)30 min,再称定重量,用甲醇补足减失的重量,离心(转速:8 000 r·min-1,5 min),取上清液,过0.45 μm微孔滤膜,即得供试液。
2.4 线性范围考察
分别精密吸取混标溶液8.00、6.00、3.00、1.00、0.50、0.10 mL于10.00 mL容量瓶中,加甲醇定容至10 mL,稀释成不同质量浓度的对照品溶液。按照2.1项下的色谱条件测定,以峰面积Y对进样浓度X进行线性回归。三种指标成分回归方程、线性范围和相关系数见表1。从表1可以看出,三种指标成分在该色谱条件下具有较好的线性关系。

表1 线性范围、相关系数r
2.5 稳定性考察
取适宜浓度的原阿片碱、延胡索乙素、盐酸巴马汀对照品的溶液,室温避光保存,分别于2 h、4 h、8 h、12 h、24 h取5 μL注入高效液相色谱仪,记录峰面积。结果如表2所示,原阿片碱、延胡索乙素、盐酸巴马汀对照品溶液峰面积的RSD分别为1.11%、1.06%、0.69%。表明夏天无标准品溶液在24 h内较为稳定。
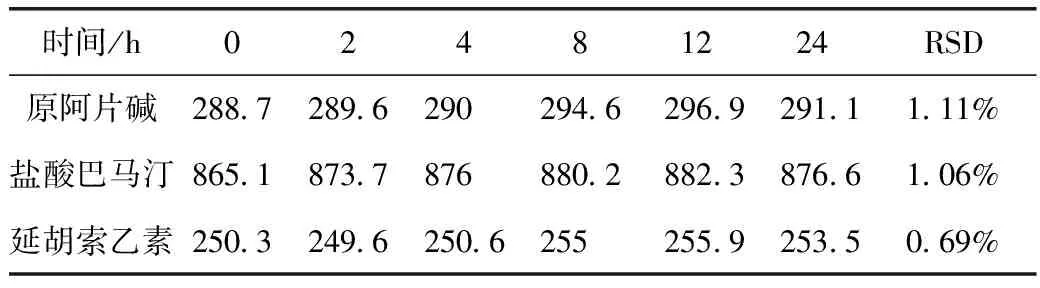
表2 稳定性考察数据
2.6 精密度试验
取适宜浓度的原阿片碱、延胡索乙素、盐酸巴马汀对照品溶液,分别取5 μL,注入HPLC仪,记录待测生物碱各自的峰面积。连续进样6次,计算精密度和RSD值,结果见表3。数据显示,6次进样后原阿片碱、延胡索乙素和盐酸巴马汀峰面积RSD值分别为1.11%、1.06%、0.69%,均远小于2%。说明本分析方法精密度很好。
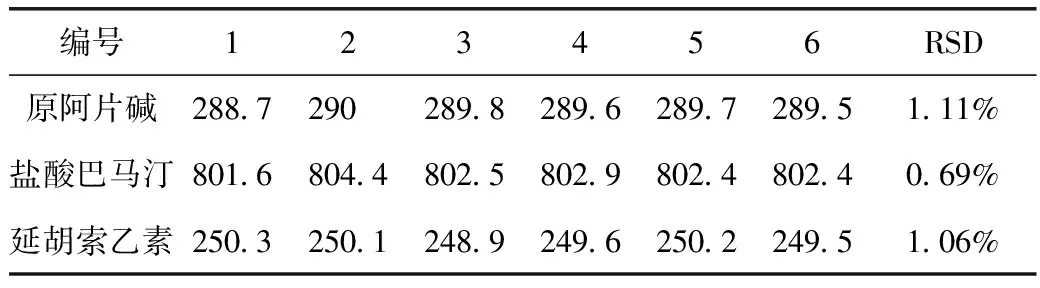
表3 精密度考察数据
2.7 重复性试验
取同一产地的夏天无药材五份,按照2.3项下制备样品溶液,在2.1项,色谱条件下测定3种生物碱的含量。检测结果见表4,该方法下原阿片碱、延胡索乙素和盐酸巴马汀的峰面积RSD值分别为2.60%、2.19%、2.33%,其值小于5%。表明该前处理方法和检测方法重复性良好。

表4 重复性考察数据
2.8 加样回收试验
精密称定已知浓度的夏天无粉末六份(含原阿片碱0.50%、延胡索乙素0.15%、盐酸巴马汀0.79%),每份约0.1 g,按照样品中各自含量的80%、100%、120%,分别精密加入三种待测生物碱对照品,每个含量各三份。按照2.2.2项方法制备供试液,按2.1项下色谱条件检测指标成分的含量,计算加样回收率。实验结果显示三种生物碱的加样回收率分别为97.32%、98.01%和99.70%;RSD分别为0.23%、0.12%、0.38%。
2.9 样品测定
2.9.1 药材中水分的测定 参照2010年版《中国药典》一部附录IX H 项下第一法(烘干法)测定供试品中含水量。取供试品2~5 g,均匀铺在干燥的铝盒(在105 ℃下干燥4小时)中,精密称定,置105 ℃下干燥4 h,盖好盖子,移至干燥器中冷却30 min,精密称定,再在上述温度中干燥1 h,冷却,称重,连续两次称重的差异不超过5 mg为止,根据减失的重量计算供试品中的含水量[9]。
2.9.2 药材中指标成分的测定 将不同干燥方式的夏天无制备成供试品溶液,进样10 μL测定,按外标法计算药材中原阿片碱、延胡索乙素和盐酸巴马汀的折干含量。
2.10 不同干燥方式下指标成分的变化情况
采收夏天无进行产地初加工工艺研究,所得干燥样品按照2.3项下制备供试品溶液,按2.1项下色谱条件测定原阿片碱、延胡索乙素和盐酸巴马汀的含量,结果如图2。新鲜夏天无样品中三种生物碱总量含量最高,晒干对三种生物碱总量影响最小,较鲜样降低20.00%左右;微波干燥下三种生物碱总量较鲜样下降22.50%左右;在阴干和45 ℃烘干两种不同干燥方式下,三种生物碱总量均下降25.00%左右;在105 ℃烘干条件下,三种生物碱总量变化较大,降低66.88%左右。新鲜夏天无中原阿片碱含量最高;阴干对原阿片碱含量影响最小,较鲜样含量降低22%左右;晒干对原阿片碱含量影响也比较小,较鲜样降低27%左右;45 ℃烘干后含量最低,较鲜样降低52%左右。晒干对盐酸巴马汀含量几乎没有影响,含量较鲜样没有明显差异。以上几种干燥方式下延胡索乙素含量均无明显差异。
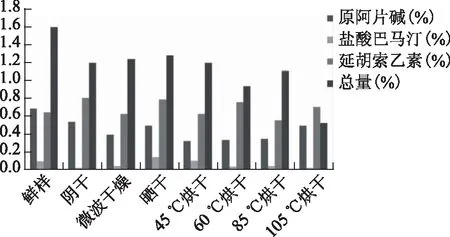
图2 不同初加工方式下夏天无指标成分含量比较
3 讨论
2010年版《中国药典》中夏天无中指标成分的提取方法为加热回流。本试验比较加热回流提取与超声提取两种不同提取工艺下有效成分提取率的变化(见表5),结果表明:加热回流与超声两种提取工艺下有效成分提取率无明显差异,而超声提取较加热回流提取方法操作简便快速,因此本文优先选用了夏天无超声提取工艺。

表5 提取方法考察数据
2010年版《中国药典》规定夏天无药材:春季或初夏出苗后采挖,除去茎、叶及须根,洗净,干燥。其干燥方式不明确,然而不同的干燥过程将会大大的影响其指标成分含量,从而影响产地药材真实质量的表达。本实验以夏天无为研究对象,在适宜采收时期获得原材料,以最大限度的保留其活性为目的,减少药材在采集、前处理过程中有效成分的流失。本实验研究数据显示:不同干燥方式对夏天无中各指标成分含量有较大的影响,阴干后原阿片碱损失最小,其次为晒干。晒干对盐酸巴马汀几乎
没有影响;然而阴干对盐酸巴马汀的影响最大。对于延胡索乙素,任何干燥方式对其含量都无明显差异。不同干燥方式对夏天无中三种指标成分总量变化有显著地影响:晒干>微波干燥>阴干>45 ℃烘干>85 ℃烘干>60 ℃烘干>105 ℃烘干。考虑到原阿片碱与盐酸巴马汀的功效不同,在实际生产应用中,我们可根据所需的功效辩正地采用不同的干燥方式。在实际生产过程中考虑到经济效益及生产条件,建议夏天无的最佳初加工方式为晒干。基于鲜药材的研究可充分表征药材质量,从药材初加工源头降低活性成分的损失,同时研究不同干燥方式对中药材有效成分的影响,对现实产地中药材品质的真实性,保持中药资源的高效利用都具有重要的参考价值。
此外,本研究还可为进一步探索不同鲜药材中有效成分在不同干燥过程中生物酶、微生物等因素的影响机理提供参考依据。
[1] 马宏达,郭涛,颜呜.HPLC法测定夏天无中原阿片碱、延胡索乙素和巴马亭[J].解放军药学学报,2009,25(3):208-211.
[2] Liao J,Liang WZ,Tu GS.Isolation and Identification of Eleven Tertiary Alkaloids in Coydalis decumbens[J].Journalof Chinese Pharmceutica Sciences,1995,4(2):57-61.
[3] 朱大元,宋纯清,高耀良,等.夏天无及其他十一种化学成分的分离和结构鉴定[J].中草药,1980,11(8):341-343.
[4] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社.2010,262.
[5] 李良国.原阿片碱对抗血小板聚集作用[J].国外医药·植物药分册,1992,2:417.
[6] 余丽梅,黄燮南,孙安盛,等.原阿片碱对兔胸主动脉的松弛作用[J].遵义医学院学报,1999,22(3):5.
[7] 杨勇,叶小利,李学刚.李时珍国医国药[J].2007,18(12):3013-3014.
[8] 吕清文,丛雅勤.延胡索药理作用及临床应用浅议[J].内蒙古中医药,2005,26(1):26.
[9] 曾建国.基于鲜药材的中药现代炮制技术[J].中草药,2009,40(1):1-5.
PreliminaryProcessingTechnologyStudyofCorydalisdecumbentisRhizoma
ZHANG Shuang1,LI Yao2,3,ZHPNG Xiao-hong1,ZENG Jian-guo1,2,3*
(1.HunanAgricuturalUnivesity,Changsha410128,China;2.NationalChineseMedicinalHerbs(Hunan)TechnologyCenter,HunanAgriculturalUniversity,Changsha410128,China; 3.HunanEngneeringResearchCenterofBotanicalExtracts,Changsha410331,China)
Objective:To determine the best preliminary processing method of Corydalis decumbentis Rhizoma by comparing the impact of the different preliminary processing methods on protopine,palmatine chloride and tetrahydropalmatine in this traditional chinese medicine.Methods:HPLC method was adapted to quantify the contents of three alkaloids inRhizomaCorydalisDecumbentis.Contents of the three alkaloids originated from different drying methods,ie.,dried in the sun,dried in the shade and dried at diferent temparatrue were compared to determine the best preliminary processing method.Results:The contents of index components in Corydalis decumbentis Rhizoma dried by the above methods had obvious difference.The one dried in the sun at 30 ℃ has the highest content of three index components.Conclusion:This study indicated that the best preliminary processing procedures of Corydalis decumbentis Rhizoma is excavating after emergence in spring or early summer→removing stems,leaves and fibrous roots→washing or wiping→drying in the sun at 30 ℃.
Corydalis decumbentis Rhizoma;Protopine;Palmatine chloride;Tetrahydropalmatine;Preliminary processing method
2013-07-17)
国家科技支撑计划(No.2012BA129B04,No.SQ2010BAJY1411)
*
曾建国,博士,教授,研究方向:中药资源及其综合利用,Tel:(0731)84673824,E-mail:ginkgo@world-way.net
