以常用药物布洛芬为起始原料的两个大学化学有机合成实验*
2013-09-25孙礼林
孙礼林
(安徽师范大学化学与材料科学学院 安徽芜湖 241000)
1 实验一 布洛芬高分子载体药物的合成
现在用来治病的药物,不论是人工合成的还是天然的,大多是相对分子质量不大的小分子化合物,也叫低分子药物。许多传统的低分子药物存在很多不足之处,如在体内新陈代谢快、半衰期短、体内浓度很快降低从而影响疗效等;为此需要加大剂量,增加进药次数,但过高的药剂浓度又会增加药物的副作用。与低分子药物相比,许多高分子药物具有长效、增效、缓释、低毒副作用及药理活性高等优点。因此,通过低分子药物高分子化克服其缺点已成为当前广泛研究的课题。
高分子药物一般可分为以下几种:① 高分子化的低分子药物;② 本身具有药理活性的高分子;③ 药物的微胶囊化,即将小分子药物通过范德华力与高分子基质结合并为其包裹。通常高分子药物主要指高分子化的低分子药物,即高分子载体药物,也就是将低分子药物连接到高分子上制成高分子药物以获得缓释或靶向功能[1]。
布洛芬(brufen)又名依布洛芬或异丁苯丙酸,化学名称为2-(4-异丁基苯基) 丙酸,具有抗炎、镇痛、解热等作用。该药口服吸收虽快,但排泄也很快,1h后血液浓度即达最高峰,且半衰期较短。为维持一定的血药浓度,需频繁给药,导致明显的峰谷效应[2]。
本实验将低分子药物布洛芬以酯键连接到甲基丙烯酸-2-羟乙酯(HEMA)上制成可聚合的含布洛芬的单体,然后单体在引发剂偶氮二异丁腈(AIBN)的存在下,经过自由基聚合反应[3-6]合成出布洛芬高分子载体药物[7]。布洛芬药物的有效成分通过羧酸酯键连接在高分子主链上,通过酯键的逐步水解或酶解可望达到布洛芬药物的缓释和长效的结果。虽然合成的布洛芬高分子前体药物的药理性能有待进一步研究,但开展此实验显然有助于学生了解高分子载体药物的概念、原理、合成方法以及烯类单体自由基聚合的原理和操作技术。实验具有趣味性和探究性,涉及多种合成操作技能,有利于培养学生的学习兴趣,增强其实验动手能力,同时也能促进基础化学实验教学方法的改革。
1.1 实验目的
(1) 了解高分子载体药物的概念及其应用的基本原理。
(2) 初步了解高分子载体药物的合成方法。
(3) 掌握烯类单体在引发剂存在下自由基聚合的基本原理和操作。
1.2 合成路线设计
布洛芬高分子载体药物的合成路线见图1。
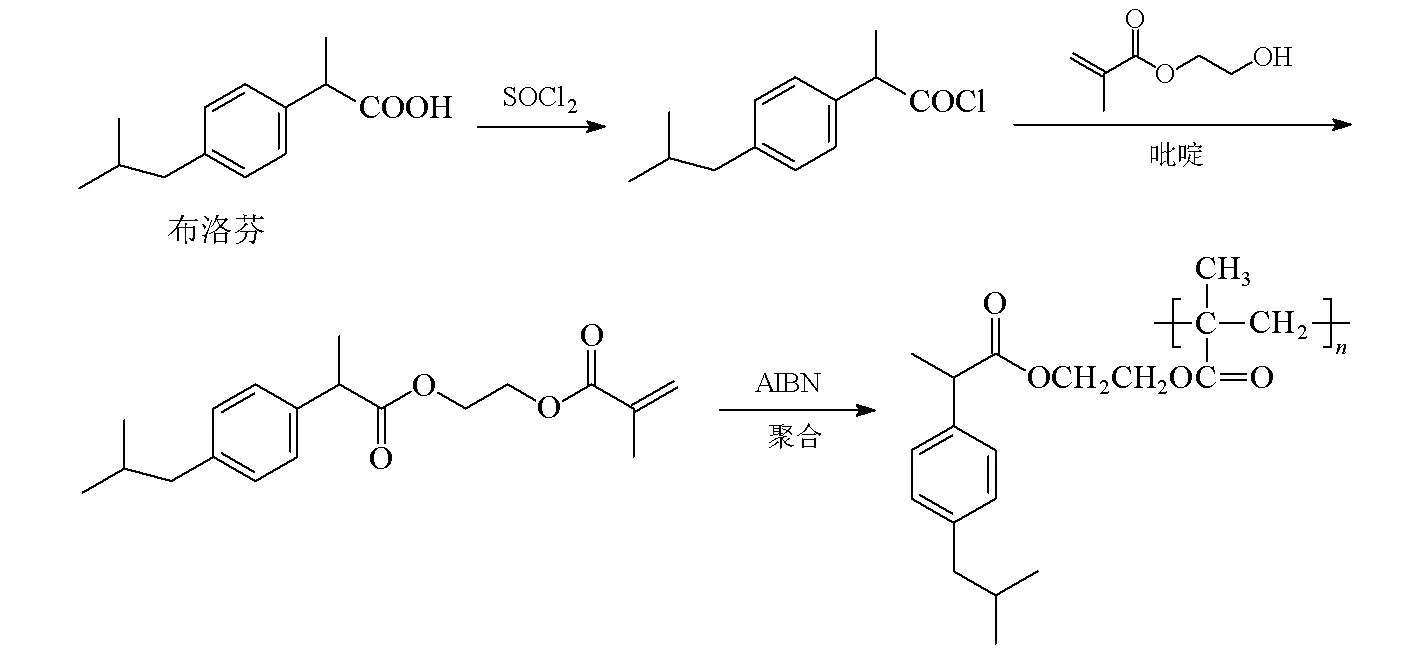
图1 布洛芬高分子载体药物的合成路线
1.3 主要仪器和试剂
仪器:Bruker AV300核磁共振谱仪,Nicolet FTIR 5DX红外光谱仪,NMR样品管,三颈烧瓶,二颈烧瓶,回流冷凝管,干燥管,玻璃漏斗,旋转蒸发仪等。
试剂:布洛芬(市售布洛芬药片),甲基丙烯酸-2-羟基乙酯(HEMA)(AR),N,N-二甲基甲酰胺(DMF)(AR),氯化亚砜(AR),吡啶(AR),氯仿(AR),偶氮二异丁腈(AIBN)(CP,经乙醇重结晶纯化),无水乙醇(AR),四氢呋喃(THF)(AR,使用前经钠丝回流后蒸出),5%碳酸氢钠溶液,饱和食盐水,无水硫酸镁(AR),氘代氯仿(内标TMS)。
1.4 实验步骤
(1) 布洛芬的提取:将市售布洛芬药片研碎,加无水乙醇搅拌后静置过夜,过滤后减压抽干乙醇溶剂得布洛芬。
(2) 单体的合成:在干燥无水条件下,将6mL SOCl2加入到装有回流冷凝管、干燥装置及气体吸收装置的100mL三口烧瓶中,用冰水浴冷却并搅拌,加入10.3g布洛芬,滴入7~8滴无水DMF,搅拌后转入油浴缓慢升温到80℃左右,回流5h,减压抽去过量的SOCl2,得黄色油状的布洛芬酰氯。在冰盐浴下向上述反应瓶中加入10mL无水THF,强烈搅拌,先加入4.3mL无水吡啶,再加入5.8mL HEMA和20mL THF的混合溶液,反应6h。反应结束后过滤,将沉淀溶于水中,用氯仿萃取,将萃取液与滤液合并,相继用水、5%碳酸氢钠水溶液、饱和食盐水洗涤,无水硫酸镁干燥。过滤后滤液减压浓缩得淡黄色油状产物(单体)12.1g,产率约为80%。
(3) 含药单体的聚合:在装有冷凝管和氩气导入管的双颈瓶中加入15mL THF,1g单体及40mg 引发剂AIBN,通入氩气10min除氧。加热到75℃,氩气氛下反应5h,反应结束后用冰水浴急速冷却。产物用甲醇沉淀,离心沉降后弃去上层甲醇,沉淀经THF溶解,再用甲醇沉淀。如此重复3次并抽干得纯化的米白色聚合物粉末0.4g左右。
(4) 单体和布洛芬高分子载体药物的表征:单体和聚合物的1H NMR谱用Bruker AV300 核磁共振仪测试,以CDCl3(内标TMS)为溶剂;单体及聚合物的IR用Nicolet FTIR 5DX红外光谱仪测试,液膜法或KBr压片制样(聚合物的相对分子质量和相对分子质量分布可由Water-150C凝胶色谱仪测定,THF为流动相,柱温30℃,以聚苯乙烯为标准样品进行普适校正)。
1.5 实验结果
1.5.1 产物状态及产率
产物的状态、相对分子质量及产率见表1。

表1 产物状态、相对分子质量及产率
注:单体相对分子质量根据分子式计算,聚合物相对分子质量和相对分子质量分布用凝胶色谱法(GPC)测定。Mn:数均相对分子质量,Mw:重均相对分子质量。
1.5.2 谱图数据
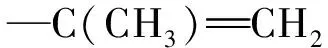
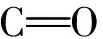
1.6 实验要点及注意事项
(1) 布洛芬与SOCl2作用制备酰氯时,由于SOCl2和酰氯都易水解而导致实验失败,故实验装置和试剂都应干燥无水,回流冷凝管上应加干燥管以防止湿气进入。此外,应使用气体吸收装置吸收反应中放出的有害气体氯化氢。
(2) 空气中的氧气对自由基聚合有一定的阻聚作用,所以,在单体聚合时应向反应装置中通氮气或氩气等惰性气体以充分除氧,并使反应在惰性气氛下进行。
(3) 测定产物红外光谱、核磁共振谱的有关操作要点参见实验教材有关内容。
1.7 问题讨论
(1) 高分子药物有哪几种类型?与传统的低分子药物相比有什么特点?
(2) 酰氯与醇作用生成酯时加吡啶的作用是什么?商品中的烯类单体在存放时为什么要加入阻聚剂(如对苯二酚等)?
(3) 常见的自由基聚合引发剂有哪几种类型?偶氮二异丁腈(AIBN)的结构式和其作为引发剂的机理是什么?精制引发剂为什么要在较低的温度下进行?
(4) 如何通过单体和聚合物的1H NMR谱图的对比及红外光谱图的吸收情况的变化来说明单体是否已聚合?
2 实验二 含芳基肽类表面活性剂的合成
随着人类资源与环境压力的增加,研究并开发环境友好的表面活性剂成为表面活性剂工业的主要方向。以生物质资源为原料,通过生物技术或化学方法得到环境友好的表面活性剂是国内外研究的热点。氨基酸类表面活性剂就是以生物质为基础的表面活性剂,由于其良好的生物降解性以及环境相容性而受到广泛的关注,成为食品、医药和化妆品行业的首选,在药物制造和生物化学领域中也取得了重要成果。氨基酸类表面活性剂是利用氨基酸或者肽等基团作为亲水基、以分子结构中的高碳链为亲油基的具有良好表面活性的一类分子。肽类产品含有与人体蛋白质结构相近的肽键,适当利用对人体的安全性相对较高,对皮肤刺激性小,可降解性能强,对环境友好[8-10]。本实验通过羧基保护法合成了布洛芬酰甘氨酸及其钠盐,利用布洛芬分子结构中的烷基苯环作为亲油基,肽键和羧基作为亲水基,设计合成了一种含芳基的肽类表面活性剂,所合成的产物用1H NMR进行了表征,并对其表面活性进行了初步研究。
2.1 实验目的
(1) 了解氨基酸肽类表面活性剂的有关概念及其结构特征。
(2) 初步了解肽类表面活性剂的合成方法及表面活性的研究方法。
(3) 掌握有关实验操作的基本原理和技能以及柱层析纯化方法。
2.2 合成路线设计
布洛芬酰甘氨酸钠的合成路线见图2。
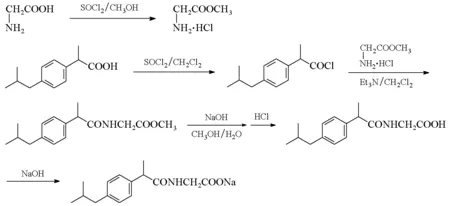
图2 布洛芬酰甘氨酸钠的合成路线
2.3 主要仪器和试剂
仪器:Bruker AV300核磁共振谱仪,NMR样品管,三颈烧瓶,单颈烧瓶,回流冷凝管,干燥管,玻璃漏斗,层析柱,滴液漏斗,10mL具塞刻度试管,旋转蒸发仪等。
药品:布洛芬,甘氨酸(AR),甲醇(AR),氯化亚砜(AR),无水氯化钙(AR),二氯甲烷(AR),乙醚(AR),三乙胺(CP,加氢氧化钾浸泡过夜,使用前蒸馏 ),硫酸(AR),苯(AR),无水乙醇(AR),氢氧化钠(AR),浓盐酸(AR),氘代氯仿(内标TMS)。
2.4 实验步骤
(1) 甘氨酸甲酯盐酸盐的合成:取一个100mL三口烧瓶,加入0.75g甘氨酸,50mL甲醇,装上滴液漏斗、无水氯化钙干燥管和回流冷凝管,于冰盐水浴中冷却至0℃。在搅拌下缓慢滴加1mL(1.31g)氯化亚砜,维持温度0℃,继续反应1h,加热升温至40~45℃,搅拌1h,使固体全溶。减压蒸馏出过量的氯化亚砜和盐酸,剩余物用热甲醇溶解,冷却滤去不溶物。加入60mL乙醚,有大量白色沉淀出现,静置,倾取上层清液,再在清液中加入10mL乙醚,静置,倾取上层清液,重复上述操作3次,直到生成的沉淀很少为止。白色沉淀即为甘氨酸甲酯盐酸盐。对白色沉淀进行抽滤,所得固体用真空泵减压干燥,得1.09g白色固体,产率为87%。
(2) 布洛芬酰氯的合成:在装有无水氯化钙干燥管的三口烧瓶中加入0.93g(4.5mmol)布洛芬和23mL二氯甲烷,稍加热使固体全溶。充分搅拌下缓慢滴加0.59g(4.95mmol)氯化亚砜,滴加完毕后再继续搅拌反应1h,减压蒸馏除去二氯甲烷、过量的氯化亚砜和生成的氯化氢,得到1.04g油状的布洛芬酰氯。

(4) 布洛芬酰甘氨酸的合成:在单口烧瓶中加入0.95g布洛芬酰甘氨酸甲酯,再加入10mL水和10mL甲醇的混合溶剂溶解,搅拌下加过量(约0.15g)氢氧化钠固体。加热至95℃,反应过夜,再用盐酸调节pH为1~2,析出沉淀。沉淀水洗后用无水乙醇重结晶,得到0.70g产品,产率为78%。
(5) 布洛芬酰甘氨酸钠盐的制备:在圆底烧瓶内将合成的布洛芬酰甘氨酸溶于乙醇中,再加入等物质的量的氢氧化钠,水浴加热至固体全部溶解,然后蒸出乙醇和水,干燥制得0.69g布洛芬酰甘氨酸钠盐,产率为91%。
2.5 实验结果
2.5.1 谱图数据
布洛芬酰甘氨酸甲酯:1H NMR(300MHz,CDCl3):δ0.88(d,6H,(CH3)2CHCH2—Ph—),δ1.49(d,3H,—Ph—CH(CH3)—),δ1.82(m,1H,(CH3)2CHCH2—Ph—),δ2.42(d,2H,(CH3)2CHCH2—Ph—),δ3.61(q,1H,—Ph—CH(CH3)—),δ3.68(s,3H,—COOCH3),δ3.98(m,2H,—NH—CH2—),δ6.02(s,1H,—NH—),δ7.18(m,4H,Ph—H)。
布洛芬酰甘氨酸:1H NMR(300MHz,CDCl3):δ0.88(d,6H,(CH3)2CHCH2—Ph—),δ1.49(d,3H,—Ph—CH(CH3)—),δ1.82(m,1H,(CH3)2CHCH2—Ph—),δ2.42(d,2H,(CH3)2CHCH2—Ph—),δ3.66(q,1H,—Ph—CH(CH3)—),δ3.95(m,2H,—NH—CH2—),δ6.35(s,1H,—NH—),δ7.17(m,4H,Ph—H),δ10.21(s,1H,—COOH)。
2.5.2 布洛芬酰甘氨酸钠的表面活性性能
配制质量分数为5%的布洛芬酰甘氨酸钠盐水溶液,用pH试纸测得该钠盐水溶液的pH约为6.5。取3mL该钠盐5%水溶液于10mL的具塞刻度试管内,水浴加热至50℃,然后上下振荡50次,记录泡沫高度为60mm,5分钟后泡沫高度45mm,说明该钠盐溶液具有良好的发泡能力和泡沫稳定性。取5%的该钠盐水溶液3mL和3mL苯,倒入10mL具塞刻度试管内,上下振荡5次,静置1min,再振荡5次,依次重复5次,然后记录分水时间。分水0.5mL所需时间为20min,分水1mL所需时间为45min,说明该钠盐溶液具有良好的乳化能力。
2.6 实验要点及注意事项
SOCl2和酰氯都极易水解而导致实验失败,故实验装置和试剂都应干燥无水,回流冷凝管上应加干燥管以防止湿气进入。同时,应使用气体吸收装置吸收反应中放出的有害氯化氢气体。柱层析分离提纯的操作方法和要点可参见有关实验教材。
2.7 问题讨论
(1) 分析1H NMR 谱图中各个峰的归属。如何通过谱图中吸收峰的变化来说明布洛芬酰甘氨酸甲酯已水解?
(2) 查阅有关文献和资料,分析和讨论环境友好表面活性剂的发展现状和趋势。
3 结语
安徽师范大学的基础化学实验课程体系和教学方法的深化改革教学研究项目自2008年立项以来,在基础化学实验课程体系和教学方法的深化改革等方面做了许多有益的尝试。对基础化学实验内容进行了大幅度的调整和改变,增加了综合性实验和设计性实验的比例,添加了能反映学科最新进展的实验内容,使学生能及时把握学科的最新动态。本文介绍的两个大学化学有机合成实验的内容在教改过程中作为综合实验被编入新的实验讲义或作为本科生毕业论文的研究课题,在教学中均取得了良好的效果,调动了学生学习的热情和积极性。布洛芬是一种价格较低廉的常用药物,将其作为较大规模的学生合成实验的起始原料,在价格和成本上都比较合适。
参 考 文 献
[1] 王国建,王公善.功能高分子.上海:同济大学出版社,1996
[2] 王汝龙,原正平.化工产品手册(药物).北京:化学工业出版社,1999
[3] Popa M,Dumitriu M.JBioactCompatPolym,1989,4:151
[4] Gallardo A,Roman J S.Polymer,1993,34:394
[5] Davaran S,Entezami A A.JControlRel,1997,47:41
[6] Davaran S,Entezami A A.JBioactCompatPolym,1997,6:47
[7] 孙礼林,孙玉,汪凌云,等.功能高分子学报,2004,17(1):97
[8] Infante M R,Pinazo A,Seguer J.ColloidsSurfA,1997,123-124:49
[9] 陈丽,周美华.精细与专用化学品,2004,19:7
[10] 饶小平,宋湛谦,高宏.林产化学与工业,2006,26(4):97
