纳米多孔金薄膜的表面等离子体共振传感特性
2013-09-21逯丹凤祁志美
张 喆 逯丹凤 祁志美
(中国科学院电子学研究所,传感技术国家重点实验室,北京100190)
1 引言
纳米多孔金(NPG)材料是近年来的一个研究热点,它具有比表面积大,化学稳定性好、导电能力强等优点,在表面增强拉曼光谱(SERS)、生化传感、光学成像、气体存储、燃料电池、隐形材料、催化反应及电化学反应等方面拥有巨大的应用前景.1-14此外,金与巯基(-SH)还可以结合形成稳固的Au-S配位键,15-17使其对含巯基的生化小分子的探测表现出卓越的性能.
目前,纳米多孔金的制备方法主要是脱合金法,1-13利用硝酸作为腐蚀液,经过一定时间的浸泡,合金中的银成分与硝酸反应溶解,保留的金成分经过原子重构形成具有三维无序孔结构的纳米多孔金薄膜.利用该方法制备的纳米多孔金薄膜已经应用于表面等离子体共振(SPR)传感研究,18-23然而这些研究大多采用市售的金银合金薄片,经脱合金后形成纳米多孔金薄膜,之后再转移到表面预处理过的玻璃基片上制成SPR传感芯片.此方法存在一些缺点,首先厚度小于100 nm的金银合金薄片受限于制作工艺而较难获得;其次将制备好的纳米多孔金薄膜转移至玻璃基片表面时容易损坏、成品率低;再次为了更好的使纳米多孔金薄膜与玻璃基片结合,需要预先对玻璃基片进行表面处理,增加了制备的复杂度.
本文提出了一种新的纳米多孔金薄膜制备方法.该方法首先利用射频溅射技术在玻璃基片上淀积数十纳米厚的金银合金薄膜,然后将玻璃基片置于浓度给定的硝酸溶液中腐蚀一定时间,清洗干燥后获得纳米多孔金薄膜.该方法不仅能够在纳米量级精确控制纳米多孔金薄膜厚度,而且通过调节腐蚀液浓度和腐蚀时间可以对孔结构进行调控.该方法制备的纳米多孔金薄膜SPR传感器可以同时产生传播等离子体共振效应和局域等离子体共振效应.18-23但是,本文制备的纳米多孔金薄膜厚度较薄,所以局域等离子体共振效应不是十分明显,因此本文着重研究了其传播等离子体共振效应及基于该效应的传感特性.实验分析了腐蚀时间对纳米多孔金薄膜SPR传感性能的影响,确定了纳米多孔金薄膜的最优制备条件.研究了L-谷胱甘肽、L-半胱氨酸、2-氨基乙硫醇三种含巯基的生化小分子的吸附行为,并与传统的SPR传感器灵敏度进行了比对.此外,还原位实时监测了乙醇蒸气在纳米多孔金薄膜内的吸附过程.
2 实验部分
2.1 试剂与仪器
L-谷胱甘肽(纯度≥99%)、L-半胱氨酸(纯度≥98%)、2-氨基乙硫醇(纯度~95%)购自美国Sigma公司;硝酸(纯度~68%)购自国药集团化学试剂有限公司;实验中使用的去离子水经过Milli-Q纯净水机二次净化.
厚度为1 mm的玻璃片购自日本Matsunami株式会社,在633 nm波长下折射率为1.522;角度为45°/45°/90°的玻璃棱镜购自北京北东光电自动化开发公司,在633 nm波长下折射率为1.799;LS-1型卤钨灯、HR4000型电荷耦合器件(CCD)光谱分析仪购自美国Ocean Optics公司;多模石英光纤购自浙江雷畴科技有限公司;透镜、线性偏振片购自北京大恒光电技术公司;硅橡胶测试槽购自南京永润橡塑有限公司;蠕动泵购自保定兰格恒流泵有限公司.
2.2 芯片制备及仪器搭建
采用真空溅射与脱合金相结合的两步法制备纳米多孔金薄膜SPR芯片.首先在清洗好的玻璃基片上采用射频镀膜技术依次溅射铬膜(厚度~3 nm)和金银合金膜(厚度~60 nm),金银合金靶材中金银质量百分比为55:45,设定溅射仪的参数为:溅射功率150 W,自偏压60 V,工作压0.5 Pa,氩气流量27 cm3·min-1,该条件下金银合金靶材的溅射速率约为1 nm·s-1,在此速率下溅射60 s得到厚度约为60 nm的金银合金薄膜,铬膜的作用是为了增加玻璃基片与金银合金膜间的结合力;其次将镀有铬膜和金银合金膜的玻璃基片浸入硝酸溶液中按照预定的时间腐蚀,金银合金膜中的银原子被硝酸溶解而脱去,留下的金原子经过重构形成纳米多孔结构,之后将腐蚀好的玻璃基片快速取出,在去离子水中反复冲洗掉残留的硝酸并用干燥空气吹干,即制备出本文所使用的纳米多孔金SPR芯片.图1(a)给出了纳米多孔金薄膜的扫描电子显微镜(SEM)照片,薄膜呈现三维无序结构,孔隙率高,孔径大.在纳米多孔金SPR芯片的制备过程中伴随着有趣的颜色变化,腐蚀前芯片呈银白色,腐蚀后呈棕黄色,相关研究表明这种棕黄色来自于纳米多孔金的局域等离子体共振效应.采用本方法制备的纳米多孔金SPR传感芯片可以同时产生致密金膜所表现的传播等离子体共振效应和纳米结构金膜所表现的局域等离子体共振效应,本文着重研究其传播等离子体共振效应.
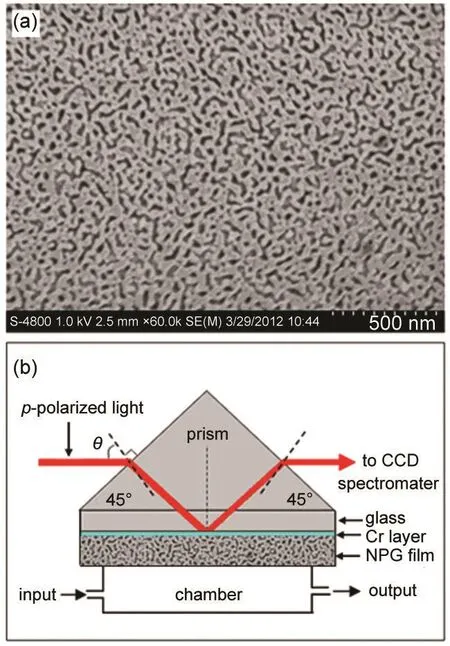
图1 (a)纳米多孔金薄膜的扫描电子显微镜(SEM)照片,(b)用于表征纳米多孔金薄膜的波长检测型表面等离子体共振(SPR)传感器测试平台示意图Fig.1 (a)Scanning electron microscope(SEM)image of the nanoporous gold film,(b)schematic diagram of the wavelength-interrogated surface plasmon resonance(SPR)sensor platform used for characterization of nanoporous gold films
图1(b)是本文搭建的基于Kretschmann结构的波长检测型SPR传感检测装置示意图.纳米多孔金SPR芯片的玻璃基底紧贴于棱镜底面,并在玻璃基底与棱镜底面缝隙处滴加高折射率匹配液,样品槽固定在纳米多孔金SPR芯片的表面.卤钨灯发出的宽波段光经光纤、聚焦透镜及线性偏振片后变为p偏振的准平行光束(发散角小于0.2°)照射到玻璃棱镜上.进入棱镜的光束在SPR芯片的玻璃基片/纳米多孔金膜界面发生全反射并在纳米多孔金膜/待测样品界面激发表面等离子体共振,使得全反射光谱在激发波段呈现出波谷.棱镜另一端输出的全反射光束经透镜聚焦到另一石英光纤的一端被CCD光谱仪记录.
3 结果与讨论
3.1 腐蚀时间及入射角度对芯片特性的影响
实验时首先测试了金银合金SPR传感芯片腐蚀前的共振反射光谱,如图2(a)中黑色曲线所示,在该条件下没有观察到共振峰.然后按照前文所述的制备方法,对同一片SPR芯片进行腐蚀,每隔15 s从腐蚀液中取出芯片洗净并吹干后记录一次共振反射光谱,之后再将芯片放回腐蚀液中继续腐蚀,实验依次记录了腐蚀时间为15、30、45、60、75及90 s的共振反射光谱如图2(a)所示.光谱中波谷的位置代表共振峰的位置,对应的波长即共振波长(λR).由图2(a)可知随着腐蚀时间的逐渐增加,共振吸收增强.图2(b)是腐蚀时间与共振波长的关系曲线,共振波长随腐蚀时间按照指数规律向长波长方向移动.前期研究结果24-26表明,共振波长对传感器的敏感特性有影响,在相同的测试条件下共振波长越大,传感器的灵敏度越高,而半高峰宽也越宽,不利于共振波长的精确确定,综合考虑灵敏度和精确度的因素,腐蚀时间为60 s制备得到的纳米多孔金SPR传感芯片性能最好.需要指出的是,每次腐蚀后均记录传感器在入射角范围内的多个共振反射光谱(角度范围为-6°--15°),通过旋转测角转盘实现对入射角的改变,图2是入射角θ=-12°条件下的测量结果,在其它角度下的测量结果具有相同的结论.

图2 (a)入射角θ=-12°时不同腐蚀时间得到的纳米多孔金薄膜在空气中的传播等离子体共振谱,(b)共振波长(λR)随腐蚀时间的变化规律Fig.2 (a)Propagating plasmon resonance spectra at the incident angle of θ=-12°for the nanoporous gold films prepared at different immersion time durations,(b)resonance wavelengths(λR)as a function of the immersion time
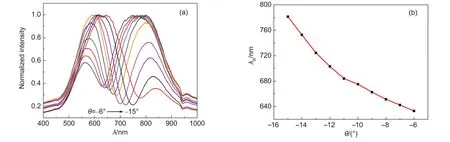
图3 (a)不同入射角θ下测得的纳米多孔金薄膜的SPR共振谱,(b)共振波长随入射角的变化规律Fig.3 (a)SPR spectra of the nanoporous gold film measured at different incident angles(spectra were normalized to their intensity maxima),(b)Resonance wavelengths as a function of the incident angles
图3 (a)所示为经过硝酸60 s腐蚀后得到的纳米多孔金SPR传感器在不同入射角度下测量得到的归一化共振反射光谱,图3(b)显示随着入射角度θ从-15°增加到-6°,共振吸收峰的位置从781 nm蓝移至633 nm.比较归一化共振反射光谱的吸收强度,θ为-12°和-13°时反射率均在0.22附近,共振吸收效果相近,而θ=-12°时,共振波长λR=704 nm,半高峰宽(FWHM)为145 nm,θ=-13°时,共振波长λR=724 nm,FWHM为157 nm.综合考虑上述参数,确定本实验的最佳入射角度为-12°.本文后续实验均是采用经过60 s硝酸腐蚀制得的纳米多孔金SPR芯片在入射角为-12°的条件下进行的.
3.2 巯基小分子的吸附敏感特性研究
L-谷胱甘肽、L-半胱氨酸以及2-氨基乙硫醇均含有巯基,巯基与金原子之间可以形成稳定的Au-S键,因此这些含巯基的小分子可以在纳米多孔金薄膜内大量富集.实验中针对这三种样品分别配制了一系列浓度的水溶液用于纳米多孔金薄膜吸附特性研究.
由于共振吸收峰仅在气相环境中出现,因此吸附实验采用离位测试的方法.首先记录背景信号的反射光强度(IB)谱和参比物(水)的反射光强度(IR)谱,之后将待测溶液注入到样品槽中,每个样品在样品槽中停留10 min,确保样品分子在纳米多孔金薄膜内的吸附达到稳定,然后将待测溶液泵出,用去离子水反复清洗样品槽5次将残留以及结合不稳固的样品分子清洗干净,最后用干燥空气将样品槽吹干,并记录纳米多孔金薄膜吸附样品分子后的反射光强度(IS)谱.由公式(1)可计算得到传感器的共振吸收光谱,吸光度(A)最大值处对应的波长为λR,该方法确定的λR与通过直接测得的共振反射光谱所确定的λR相同,但该方法更容易实现对较小的λR变化的精确区分.

L-谷胱甘肽是一种由L-半胱氨酸、谷氨酸和甘氨酸组成的三肽,分子量为307.32 Da.L-半胱氨酸上的巯基分子为其活性基团,易与某些药物和毒素(如重金属金、铅、汞、砷等)结合,具有整合解毒作用.实验中配制了0,1,5,10 μmol·L-1四种浓度的L-谷胱甘肽水溶液用于吸附测试,测试时按照浓度由低到高的顺序进行.图4(a)所示为纳米多孔金SPR传感器在不同浓度下测得的共振吸收光谱,图中显示随着L-谷胱甘肽水溶液浓度的增加,共振光谱相应红移,表明在纳米多孔金薄膜中吸附的L-谷胱甘肽分子数量在增加.当L-谷胱甘肽水溶液的浓度为1 μmol·L-1时,共振峰从λR=704 nm 红移至λR=710 nm,变化量为 6 nm,当浓度增加至 10 μmol·L-1时,共振峰移至725 nm的位置,波长变化总量为21 nm.采用传统致密金膜SPR传感器在相近的起始共振波长λR=718 nm(此时θ=11°,共振峰出现于液相环境)条件下对10 μmol·L-1的L-谷胱甘肽水溶液进行了原位对比测试,结果如图4(b)所示,吸附平衡时其波长变化量仅为3 nm.实验结果显示了纳米多孔金SPR传感器在小分子L-谷胱甘肽的吸附测试中具有更高的灵敏度,约为传统致密金膜SPR传感器的7倍.这一高吸附灵敏度一方面来源于纳米多孔金薄膜的大比表面积提供了更多的分子结合位点,使得L-谷胱甘肽分子可以在其多孔层内大量富集,另一方面SPR传感器的消逝场与样品分子的作用深度从传统的单分子层厚度(~1 nm)增加到了多孔薄膜的厚度(~60 nm),因此传感器的灵敏度得到了显著提高.
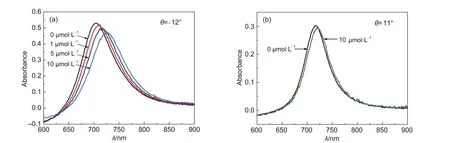
图4 (a)在不同浓度L-谷胱甘肽水溶液中浸泡后的纳米多孔金薄膜暴露到空气中产生的SPR吸收峰,(b)传统的致密金膜在纯水中和在10 μmol·L-1的L-谷胱甘肽水溶液中的SPR吸收峰Fig.4 (a)SPR absorption peaks of the nanoporous gold film exposed to air after immersion in different concentrations of aqueous L-glutathione solutions,(b)SPR absorption peaks measured with a conventional dense gold film in pure water and in an aqueous solution of 10 μmol·L-1L-glutathione
L-半胱氨酸的分子量为121.16 Da.实验中配制了浓度从1 nmol·L-1至1000 nmol·L-1的水溶液.图5(a)为纳米多孔金SPR传感器对不同浓度的L-半胱氨酸测量得到的共振吸收光谱,随着浓度的增加,共振波长红移,图5(b)显示了共振波长改变量与L-半胱氨酸水溶液浓度的依赖关系,吸附规律遵循Langmuir等温吸附理论,当达到吸附平衡时共振波长变化量(ΔλR)为28 nm.
采用相同的方法对分子量更小的2-氨基乙硫醇(77.15 Da)在纳米多孔金薄膜中的吸附特性进行测试,图6给出了共振波长改变量与2-氨基乙硫醇水溶液浓度的依赖关系,当吸附达到平衡时ΔλR达到47 nm.实验结果表明样品分子的分子量越小,SPR传感器的响应越大,这可能是由于更多的小分子可以吸附进入纳米多孔金薄膜中,从而导致有效折射率的变化增大.
3.3 乙醇蒸气的敏感测试
虽然本文制备的纳米多孔金SPR传感器在液相环境中没有产生共振吸收峰,只能进行离位测试,但在气相环境中却可以观察到共振峰,因此可以对气相分子进行原位测试.图7是对纯乙醇蒸气在纳米多孔金薄膜中的吸附特性原位实时测得的传感器的共振反射光谱,图中显示随着吸附时间的增加,共振反射光谱呈现规律性的红移,插图显示当吸附时间达到160 min时,共振反射光谱不再变化,表明乙醇分子在纳米多孔金薄膜中的吸附达到饱和,此时共振波长的总改变量ΔλR为27.5 nm.

图5 (a)在不同浓度L-半胱氨酸水溶液中浸泡后的纳米多孔金薄膜暴露到空气中产生的SPR吸收峰,(b)共振波长改变量随L-半胱氨酸水溶液浓度的变化规律Fig.5 (a)SPR absorption peaks of the nanoporous gold film exposed to air after immersion in different concentrations of aqueous L-cysteine solutions,(b)the resonance-wavelength shifts(ΔλR)as a function of L-cysteine concentration
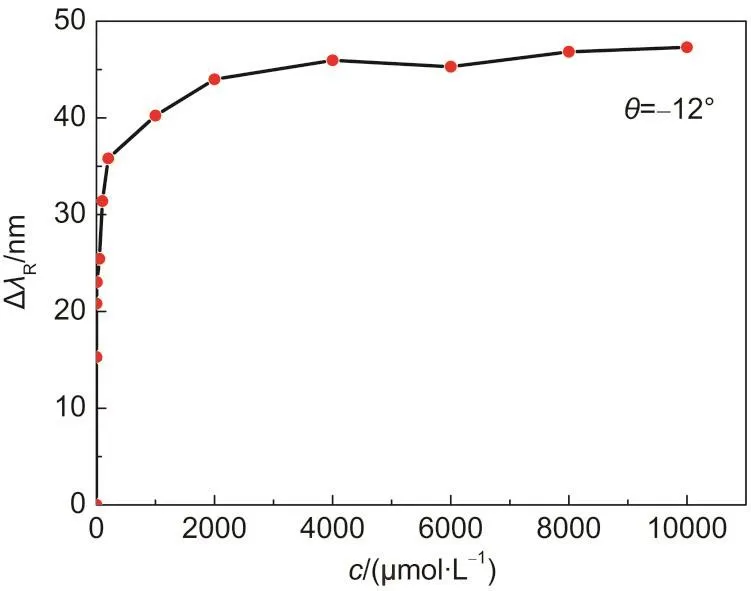
图6 置于空气中的纳米多孔金薄膜的共振波长改变量随2-氨基乙硫醇水溶液浓度的变化规律Fig.6 Resonance-wavelength shifts of the nanoporous gold film exposed to air as a function of concentration of aqueous cysteamine solutions
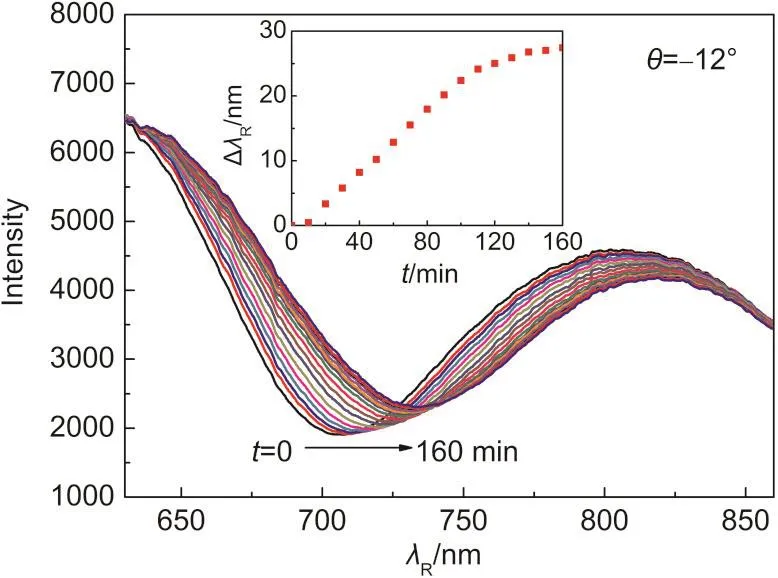
图7 乙醇蒸气在纳米多孔金薄膜内的吸附导致的薄膜SPR共振谱的红移Fig.7 Ethanol vapor adsorption induced redshift of the SPR band of the nanoporous gold film
4 结论
本文采用射频溅射和硝酸腐蚀两步法制备了厚度约60 nm的纳米多孔金薄膜,利用自建的波长检测型SPR传感装置研究了腐蚀时间对纳米多孔金薄膜SPR敏感特性的影响,结果表明经过60 s硝酸腐蚀制备的纳米多孔金薄膜的SPR传感特性较好,并在入射角度为-12°条件下研究了纳米多孔金薄膜的传感特性.离位测试了三种含巯基的生化小分子(L-谷胱甘肽、L-半胱氨酸和2-氨基乙硫醇)的吸附特性:对L-谷胱甘肽的测试结果表明,纳米多孔金薄膜SPR传感器的灵敏度是传统致密金膜SPR传感器灵敏度的7倍;实现了对浓度为1 nmol·L-1的L-半胱氨酸和2-氨基乙硫醇的高灵敏度检测,这两种小分子的吸附规律均遵循Langmuir等温吸附理论.本文还对纯乙醇蒸气进行了原位实时监测,吸附达到平衡时所需时间为160 min,共振波长的总变化量为27.5 nm.
(1) Fujita,T.;Guan,P.;Mckenna,K.;Lang,X.;Hirata,A.;Zhang,L.;Tokunaga,T.;Arai,S.;Yamamoto,Y.;Tanaka,N.;Ishikawa,Y.;Asao,N.;Yamamoto,Y.;Erlebacher,J.;Chen,M.Nat.Mater.2012,11,775.doi:10.1038/nmat3391
(2) Detsi,E.;Punzhin,S.;Rao,J.;Onck,P.R.;De Hosson,J.T.M.ACS Nano 2012,6,3734.doi:10.1021/nn300179n
(3) Feng,J.;Wu,J.Small 2012,8,3786.doi:10.1002/small.201201591
(4) Fang,C.;Bandaru,N.M.;Ellis,A.V.;Voelcker,N.H.J.Mater.Chem.2012,22,2952.doi:10.1039/c2jm14889g
(5)Cherevko,S.;Chung,C.H.Electrochem.Commun.2011,13,16.doi:10.1016/j.elecom.2010.11.001
(6)Wittstock,A.;Wichmann,A.;Biener,J.;Bäumer,M.Faraday Discuss 2011,152,87.doi:10.1039/c1fd00022e
(7) Jiao,Y.;Ryckman,J.D.;Ciesielski,P.N.;Escobar,C.A.;Jennings,G.K.;Weiss,S.M.Nanotechnology 2011,22,295302.doi:10.1088/0957-4484/22/29/295302
(8)Wittstock,A.;Zielasek,V.;Biener,J.;Friend,C.M.;Bumer,M.Science 2010,327,319.doi:10.1126/science.1183591
(9)Musat,R.;Moreau,S.;Poidevin,F.;Mathon,M.H.;Pommeret,S.;Renault,J.P.Phys.Chem.Chem.Phys.2010,12,12868.doi:10.1039/c0cp00967a
(10)Qian,L.;Shen,W.;Qin,G.W.;Das,B.Nanotechnology 2010,21,305705.doi:10.1088/0957-4484/21/30/305705
(11) Seker,E.;Reed,M.L.;Begley,M.R.Materials 2009,2,2188.doi:10.3390/ma2042188
(12) Qiu,H.J.;Xu,C.X.;Ji,G.L.;Huang,X.R.;Han,S.H.;Ding,Y.;Qu,Y.B.Acta Chim.Sin.2008,66,2075.[邱华军,徐彩霞,姬广磊,黄锡荣,韩书华,丁 轶,曲音波.化学学报,2008,66,2075.]
(13) Wang,J.L.;Li,S.;Xia,R.;Zhang,X.;Chen,Y.F.Nanotechnology and Precision Engineering 2012,10,30.[王建立,李 晟,夏 热,张 兴,陈云飞.纳米技术与精密工程,2012,10,30.]
(14) Wang,D.;Schaaf,P.J.Mater.Chem.2012,22,5344.doi:10.1039/c2jm15727f
(15)Abraham,A.;Mihaliuk,E.;Kumar,B.;Legleiter,J.;Gullion,T.J.Phys.Chem.C 2010,114,18109.doi:10.1021/jp107112b
(16) Gutiérrez,A.;Osegueda,S.;Gutiérrez-Granados,S.;Alatorre,A.;García,M.G.;Godínez,L.A.Electroanalysis 2008,20,2294.doi:10.1002/elan.200804324
(17)Sudeep,P.K.;Joseph,S.T.S.;Thomas,K.G.J.Am.Chem.Soc.2005,127,6516.doi:10.1021/ja051145e
(18) Ruffato,G.;Romanato,F.;Garoli,D.;Cattarin,S.Opt.Express 2011,19,13164.doi:10.1364/OE.19.013164
(19) Lang,X.;Qian,L.;Guan,P.;Zi,J.;Chen,M.Appl.Phys.Lett.2011,98,093701.doi:10.1063/1.3560482
(20)Yang,Y.;Wu,Y.H.;Hao,P.;Zhang,Z.Q.Spectroscopy and Spectral Analysis 2010,30,1898. [杨 胤,吴一辉,郝 鹏,张志强.光谱学与光谱分析,2010,30,1898.]
(21) Ahi,S.;Caneron,P.J.;Liu,J.;Knoll,W.;Erlebacher,J.;Yu,F.Plamonics 2008,3,13.doi:10.1007/s11468-007-9048-5
(22) Maaroof,A.I.;Gentle,A.;Smith,G.B.;Cortie,M.B.J.Phys.D:Appl.Phys.2007,40,5675.doi:10.1088/0022-3727/40/18/024
(23)Yu,F.;Ahi,S.;Caminade,A.M.;Majoral,J.P.;Knoll,W.;Erlebacher,J.Anal.Chem.2006,78,7346.doi:10.1021/ac060829h
(24) Qi,Z.M.;Honma,I.;Zhou,H.S.Appl.Phys.Lett.2007,90,011102.doi:10.1063/1.2424643
(25) Zhang,Z.;Lu,D.F.;Qi,Z.M.J.Phys.Chem.C 2012,116,3342.doi:10.1021/jp2102429
(26) Zhang,Z.;Lu,D.F.;Liu,Q.;Qi,Z.M.;Yang,L.B.;Liu,J.H.Analyst 2012,137,4822.doi:10.1039/c2an16057a
