瞬时受体电位2通道介导动物氧化应激的机理及其营养调控
2013-09-20马思聪李海燕敖远扬唐志如
马思聪 李 磊 李海燕 敖远扬 唐志如*
(1.西南大学动物科技学院,生物饲料与动物营养重点实验室,重庆 400716;2.西南大学动物科技学院,重庆市草食动物生产与利用工程中心,重庆 400716)
氧化应激是指机体在遭受各种有害刺激时,体内活性氧自由基(reactive oxygen species,ROS)和活性氮自由基(reactive nitrogen species,RNS)产生过多,氧化程度超出氧化物的清除,氧化系统和抗氧化系统失衡,从而导致组织损伤。机体氧化应激产生的过氧化物和自由基会损害细胞内物质(如蛋白质、脂类和DNA)。瞬时受体电位2(transient receptor potential 2,TRPM2)是一种具有离子通道和二磷酸腺苷核糖(adenosine diphosphate ribose,ADPR)水解酶双重功能的蛋白质[1]。在介导氧化应激ROS诱导Ca2+内流和随后产生依赖性的细胞反应中,TRPM2通道是一种内源性氧化还原传感器,因此在氧化应激诱导的细胞死亡过程,TRPM2通道是一个重要组成成分[2]。TRPM2通道具有调控内皮屏障功能,并在氧化已经中断内皮屏障中起重要作用,抑制TRPM2通道是消除氧化应激方法[3]。在溶酶体室内,TRPM2可作为胞质ADPR激活Ca2+释放通道。TRPM2通道对活性氧的反应能力使得其成为氧化应激相关疾病的潜在靶点。TRPM2通道的研究将为探索抗氧化营养物质作用机理提供重要的科学依据。
1 TRPM2通道的基本特征
1.1 TRPM 2通道的基因定位与组织分布
在基因组DNA序列中,最初TRPM2基因被定义为瞬时受体潜在相关通道7(transient receptor potential-related channel 7,TRPC7)。该基因位于人类21q22.3染色体上,标记在 D21S400和D21S171之间,由32个外显子组成,其跨度约90 kb,21q22.3与双向情感障碍有密切联系,靠近超氧化物歧化酶1(SOD1)轨迹(21q22.1~22.2)(图1)[4],TRPM2的位置表明其与氧化应激具有密切联系。
TRPM2基因主要在动物大脑中表达,其中在海马体、大脑皮质、丘脑和中脑中表达量最高,在小胶质细胞和神经细胞中表达量次之。TRPM2基因在动物胃肠道、骨髓、脾脏、心脏、肝脏、胰腺、胎盘、卵巢、肺、血管平滑肌、造血细胞、单核细胞内分泌细胞和内皮细胞中也有表达。
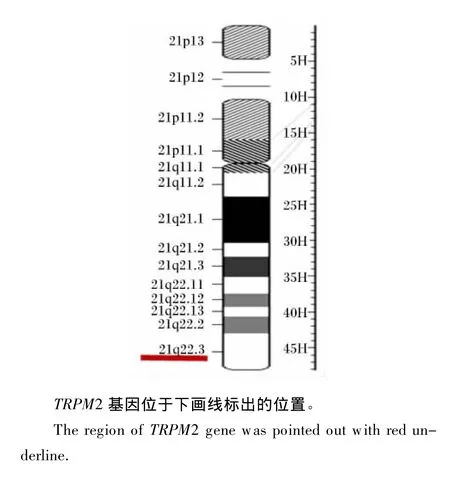
图1 人染色体21基本图谱Fig.1 The master map of Homo sapiens(human)chromosome 21[4]
1.2 TRPM2通道结构
人TRPM2通道是一种含有1 503个氨基酸,分子质量为70 ku的蛋白质。鼠TRPM2通道是一种含有1 507个氨基酸的蛋白质。TRPM2通道结构见图2-A,TRPM2通道N-端具有4个未知功能的同源区域(four homologous regions,MHR)和一个与IQ-like motif结合的钙调节蛋白(calmodulin,CaM),紧接着是6个跨膜片段(transmembrane segments,TM,S1 ~ S6)[5]。TRPM2 通道的门孔环域位于S5和S6。TRPM2通道C-端含有1个TRP盒、1个 CC域(coil-coil domain,CC)和 1个C-端 ADPR域(NUDT9 homology domain,NUDT9-H)[6]。如图2-B 所示,TRPM2 通道 C-端和N-端面向胞质溶胶。细胞溶质的ADPR能与NUDT9-H结合,开启TRPM2通道,允许Ca2+和Na+内流,ADPR被TRPM2的 NUDT9-H酶活水解成 5-磷酸核糖和 AMP[7]。H2O2、环 ADPR(cyclic ADPR,cADPR)和Ca2+能促进受控于ADPR的TRPM2通道开启[8]。而AMP抑制受控于ADPR的TRPM2通道开启,cADPR的拮抗剂8-Br-cADPR能抑制cADPR和H2O2介导的反应[9]。
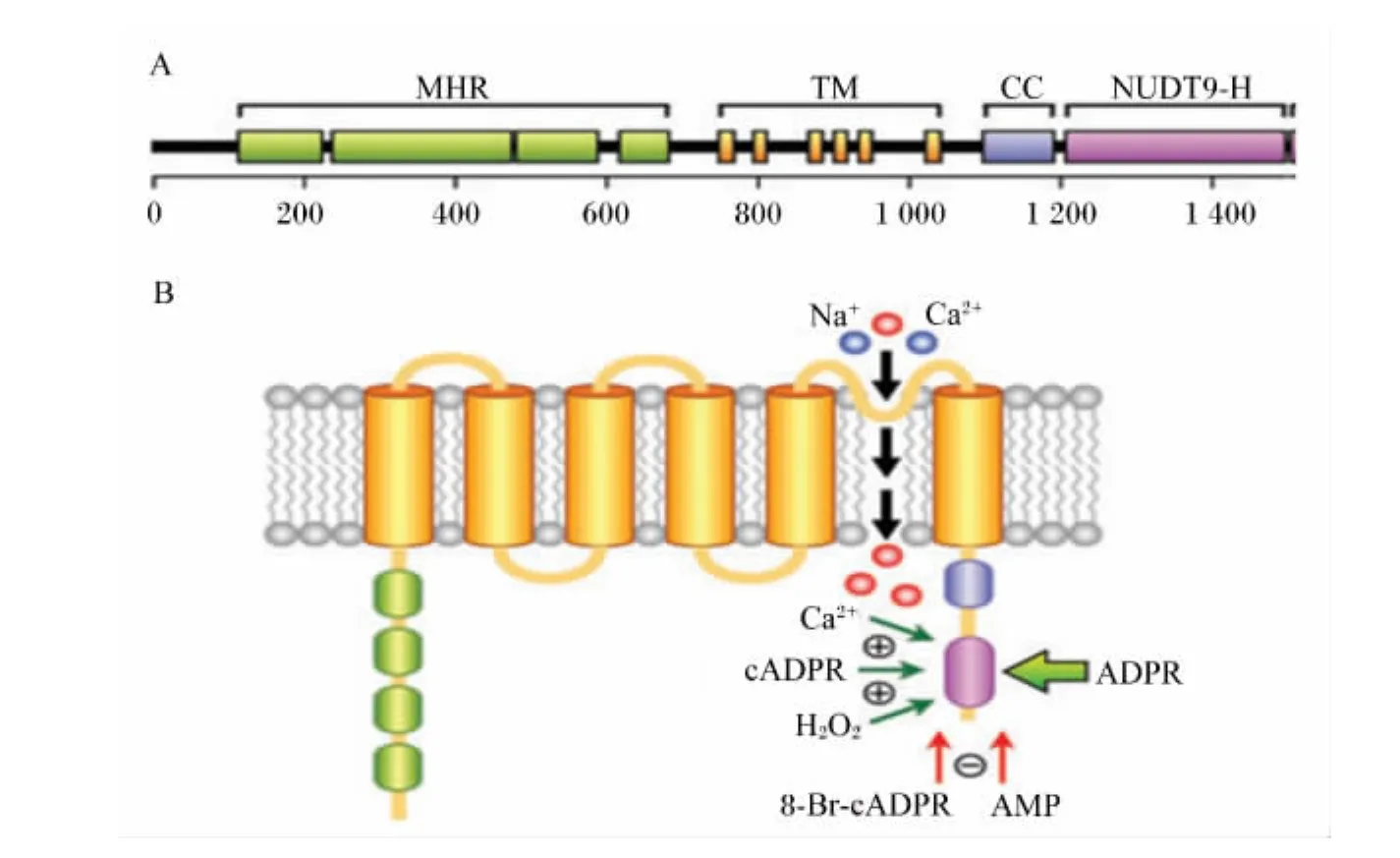
图2 TRPM2结构图(A)和跨膜图(B)Fig.2 Diagrams of structure(A)and transmembrane topology of TRPM2(B)[6]
2 氧化应激激活TRPM2通道的机理
2.1 H2O2激活TRPM2通道的机理
H2O2能引起动物氧化应激,H2O2和ADPR能结合NUDT9-H结构域而激活TRPM2通道。H2O2激活TRPM2是通过线粒体或胞外酶CD38释放ADPR而实现的,cADPR可以刺激TRPM2通道[10]。ADPR在TRPM2门控和Ca2+促进调钙素激活中十分重要(图 3)[5]。Hara 等[11]报道,H2O2激活TRPM2是由烟酰胺腺嘌呤二核苷酸(NAD+)水平的提高以及NAD+结合NUDT9-H结构域而介导的,cADPR的拮抗剂8-Br-cADPR能完全阻断cADPR和烟酸腺嘌呤二核苷酸磷酸(NAADP)介导的TRPM2门控。沉默TRPM2蛋白乙酰化反应的独特代谢产物(ADPR、cADPR、NAADP),已被列为衍生NAD+第二信使,这些信使具有调节Ca2+信号释放,介导细胞生长的功能。TRPM2基因在β细胞中表达,并且NAADP能激活大鼠胰岛瘤细胞系的TRPM2,从而维持胰岛素分泌的控制和整体葡萄糖稳态[12]。ADPR使TRPM2能有效调节胞质内的 Ca2+[13]。细胞内Ca2+是一个重要的TRPM2调制器和辅因子,细胞内Ca2+升高可显著提高TRPM2对ADPR的灵敏度[14]。
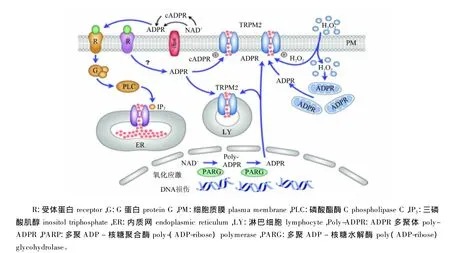
图3 H2O2和氧化应激自由基激活TRPM2通道的机理Fig.3 Signalling mechanisms for TRPM2 activated by H2O2and oxidative stress free radical[5]
2.2 自由基激活TRPM2通道的机理
研究发现,TRPM2通道参与氧化应激第二信使的产生过程[15]。细胞溶质在氧化应激的条件下产生的氧化剂,能刺激ADPR在核和线粒体中形成[16]。自由基中间体在机体受到氧化应激的时候在胞液产生,包括超氧阴离子(·)、H2O2、一氧化氮,还有更具破坏性的化合物羟基自由基(·OH)。这些自由基导致DNA氧化和损伤,发起PARP介导ADPR。PARP作为电位源为TRPM2在氧化应激中提供电能。聚腺苷二磷酸能结合的单链和双链。DNA断裂和催化分解成的烟酰胺和聚NAD(ADPR)启动DNA修复机制(图 4)[17]。
2.3 热应激激活TRPM2通道的机理
TRPM2也是温度敏感TRP通道之一,可以通过暴露在较高温度环境(>35℃)中被激活。在胰岛细胞内,TRPM2与胰岛素在轻微加热这些细胞的条件下,可以使Ca2+和胰岛素的释量增加。在体温的温度下,配体激活后TRPM2将参与胰岛素的合成,TRPM2调节Ca2+进入胰腺β细胞取决于生产循环ADPR分子的数量,从而调节胰岛素分泌[18]。
2.4 抑制TRPM 2通道能缓解动物氧化应激
根据氧化应激激活TRPM2通道的机理,抑制TRPM2通道能缓解动物氧化应激。TRPM2抑制剂可分为2大类:灭酸酯类(如氟芬那酸)和抗真菌类(如咪康唑和克霉唑咪)(图5)。氟芬那酸是一类TRPM2通道的pH依赖拮抗剂,因此降低细胞外的pH可加速氟芬那酸抑制TRPM2。但氟芬那酸不易溶于水,很难制备高浓度的氟芬那酸来抑制TRPM2[19]。作为磷脂酶A2抑制剂,ACA也是一种TRPM2的抑制剂,采用一种不同于8-Br-ADPR的机制来干扰通道的激活,在细胞内可诱导一个完整的TRPM2电流。由于ACA对TRPM2的高效力和有效性,ACA常作为一个药理工具来研究H2O2诱导Ca2+信号和TRPM2通道在原生细胞生物功能。但是,ACA、咪康唑和克霉唑以一种不可逆的方式抑制 TRPM2[20]。2-APB被证明是另一个研究TRPM2功能的有效工具,采取可逆地的方式抑制 TRPM2[21]。

图4 热应激激活TRPM2通道的机理Fig.4 Signalling mechanisms for TRPM2 activated by thermal stress[17]

图5 TRPM2通道抑制剂分子结构Fig.5 Molecular structures of TRPM2 channel inhibiter
3 抗氧化营养物质与TRPM2通道之间的关系
营养与氧化应激间存在着双重关系。一方面,营养素在体内代谢过程中可以产生活性氧及中间产物自由基,如铁离子、铜离子可促进活性氧生成。另一方面,营养平衡饲粮可增强机体的抗氧化防御功能。氧化剂、抗氧化剂平衡的破坏是细胞损伤的主要原因。抗氧化剂可以减缓氧化应激带来的危害。平衡膳食、合理营养也可增强机体的抗氧化防御功能,某些营养素和食物成分(牛磺酸、硒、维生素E和维生素C等)能直接或间接地发挥抗氧化作用。不同抗氧化营养物质的抗氧化作用机理是不同。目前抗氧化营养物质与TRPM2通道之间的关系研究报道甚少。
3.1 牛磺酸
牛磺酸可调控线粒体对Ca2+的摄入与释放。牛磺酸能抑制离体大鼠肝脏线粒体对Ca2+的摄入,并且抑制作用随牛磺酸浓度增加而增强,牛磺酸同时促进线粒体对Ca2+的释放,促进作用也呈剂量-效应关系。牛磺酸抑制线粒体Ca2+摄入、促进线粒体Ca2+释放以调节线粒体钙稳态的作用可能是其对细胞进行保护的重要机制之一[22]。TRPM2的激活依赖细胞内Ca2+水平。氧化应激通过产生氧代谢产物,如H2O2,增加血管内皮渗透压,H2O2能促进ADP-核糖体的形成,从而开启TRPM2通道[23](图4)。因此,推测牛磺酸可能通过抑制线粒体Ca2+摄入,进而抑制TRPM2的激活,最终达到抑制细胞膜脂质过氧化和保护细胞的目的。
3.2 维生素和硒
维生素C和硒作为自由基清除剂,能清除活性氧自由基,抑制TRPM2通道,发挥抗氧化功能,从而增强机体对外界环境的应激能力,提高机体对疾病的抵抗能力[24]。维生素E是一种具有抗氧化功能的维生素,对幼畜来说,维生素E在维持机体的免疫功能、预防疾病方面发挥发重要作用[25]。虾青素的清除自由基能力和抗氧化活性是维生素E的1 000倍,又称为超级维生素E。维生素E与TRPM2通道之间的关系未见报道。
3.3 植物提取物
植物多酚又称单宁,是多羟基化合物的总称,主要存在于植物体的叶、根、皮、壳和果肉中,为植物体内的复杂酚类次生代谢物。其含量仅次于纤维素、半纤维素和木质素。在许多针叶树皮中含量高达20% ~40%。葡萄、蔬菜、茶叶、豆制品中也含有较多的多酚。多酚类物质具有清除活性氧自由基和提高抗氧化酶的活性的功能[26],但多酚类物质的抗氧化功能与TRPM2通道之间的关系有待于进一步研究。
4 小结
由于氧化应激在生理病理状况中扮演着重要的角色,而在介导氧化应激/ROS诱导的Ca2+内流以及随后的特定的Ca2+依赖的细胞反应中,TRPM2通道是一种内源性氧化还原传感器,是氧化应激产生的重要靶点。许多营养素具有抗氧化的作用,但这些营养素是如何通过TRPM2通道发挥作用的目前还不清楚,因此,TRPM2通道与营养物质之间的内在联系在动物营养研究中具有重要意义。
[1]PERRAUD A L,SHEN B,DUNN C A,et al.NUDT9,a member of the Nudix hydrolase family,is an evolutionarily conserved mitochondrial ADP-ribose pyrophosphatase[J].The Journal Biological Chemistry,2003,278(3):1794-1801.
[2]ZENG X,SIKKA S C,HUANG L,et al.Novel role for the transient receptor potential channel TRPM2 in prostate cancer cell proliferation[J].Prostate Cancer Prostatic Disease,2010,13(2):195-201.
[3]HECQUET C M,AHMMED G U,MALIK A B.TRPM2 channel regulates endothelial barrier function[J].Advance in Experimental Medicine and Biology,2010,661:155-167.
[4]LIU JJ,JUO S H,TERWILLIGER J D,et al.A follow-up linkage study supports evidence for a bipolar affective disorder locus on chromosome 21q22[J].A-merican Journal of Medical Genetics,2001,105(2):189-194.
[5]SUMOZA-TOLEDO A,PENNER R.TRPM2:a multifunctional ion channel for calcium signaling[J].The Journal of Physiology,2011,589(7):1515-1525.
[6]XIA R,MEI Z Z,MAO H J,et al.Identification of pore residues engaged in determining divalent cationic permeation in transient receptor potential melastatin subtype channel 2[J].The Journal of Biological Chemistry,2008,283(41):27426-27432.
[7]KÜHN F J,KÜHN C,NAZIROGLU M,et al.Role of an N-terminal splice segment in the activation of the cation channel TRPM2 by ADP-ribose and hydrogen peroxide[J].Neurochemical Research,2009,34(2):227-233.
[8]MEI Z Z,MAO H J,JIANG L H.Conserved cysteine residues in the pore region are obligatory for human TRPM2 channel function[J].American Journal of Physiology Cell Physiology,2006,291(5):C1022-C1028.
[9]MARUYAMA Y,OGURA T,MIO K,et al.Three-dimensional reconstruction using transmission electron microscopy reveals a swollen,bell-shaped structure of transient receptor potential melastatin type 2 cation channel[J].The Journal of Biology Chemistry,2007,282:36961-36970.
[10]BECK A,KOLISEK M,BAGLEY L A,et al.Nicotinic acid adenine dinucleotide phosphate and cyclic ADP-ribose regulate TRPM2 channels in T lympho-cytes[J].FASEB Journal,2006,20(7):962-964.
[11]HARA Y,WAKAMORI M,ISHII M,et al.LTRPC2 Ca2+-permeable channel activated by changes in redox status confers susceptibility to cell death[J].Molecular Cell,2002,9(1):163-173.
[12]MOYNIHAN K A,GRIMM A A,PLUEGER M M,et al.Increased dosage of mammalian Sir2 in pancreatic beta cells enhances glucose-stimulated insulin secretion in mice[J].Cell Metabolism,2005,2(2):105-117.
[13]HEINER I,EISFELD J,WARNSTEDT M,et al.Endogenous ADP-ribose enables calcium-regulated cation currents through TRPM2 channels in neutrophil granulocytes[J].Biochemistry Journal,2006,398(2):225-232.
[14]KOLISEK M,BECK A,FLEIG A,et al.Cyclic ADP-ribose and hydrogen peroxide synergize with ADP-ribose in the activation of TRPM2 channels[J].Molecular Cell,2005,18(1):61-69.
[16]PERRAUD A L,TAKANISHIC L,SHEN B,et al.Accumulation of free ADP-ribose from mitochondria mediates oxidative stress-induced gating of TRPM2 cation channels[J].The Journal of Biology Chemistry,2005,280:6138-6148.
[17]MARTIN E,ROSENTHAL R E,FISKUM G.Pyruvate dehydrogenase complex:metabolic link to ischemic brain injury and target of oxidative stress[J].Journal of Neuroscience Research,2005,79(1/2):240-247.
[18]TOGASHI K,HARA Y,TOMINAGA T,et al.TRPM2 activation by cyclic ADP-ribose at body temperature is involved in insulin secretion[J].The EMBO Journal,2006,25(9):1804-1815.
[19]HILL K,BENHAM C D,MCNULTY S,et al.Flufenamic acid is a pH-dependent antagonist of TRPM2 channels[J].Neuropharmacology,2004,47(3):450-460.
[20]HILL K,MCNULTY S,RANDALL A D.Inhibition of TRPM2 channels by the antifungal agents clotrimazole and econazole[J].Naunyn-Schmiedeberg’s Archives Pharmacology,2004,370(4):227-237.
[21]TOGASHI K,INADA H,TOMINAGA M.Inhibition of the transient receptor potential cation channel TRPM2 by 2-aminoethoxydiphenyl borate(2-APB)[J].British Journal Pharmacology,2008,153(6):1324-1330.
[22]GEORGIA B,SCHULLER L,EUNKYUE P.Taurine:new implications for an old amino acid[J].FEMS Microbiology Letters,2003,226(2):195-202.
[23]HECQUET C M,AHMMED G U,VOGEL S M,et al.Role of TRPM2 channel in mediating H2O2-induced Ca2+entry and endothelial hyperpermeability[J].Circulating Research,2008,102(3):347-355.
[24]SELMAN C,MCLAREN J S,MEYER C,et al.Lifelong vitamin C supplementation in combination with cold exposure does not affect oxidative damage or lifespan in mice,but decreases expression of antioxidant protection genes[J].Mechanisms of Ageing and Development,2006,127(12):897-904.
[25]HUANG R F,HUANG SM,LIN B S,et al.N-acetylcysteine,vitamin C and vitamin E diminish homocysteine thiolactone-induced apoptosis in human promyeloid HL-60 cells[J].The Journal of Nutrition,2002,132(8):2151-2156.
[26]马力,陈永忠.植物多酚的生物活性研究进展[J].农业机械,2012(21):119-121.
