模板分子诱导的微孔镧系-2-羧基肉桂酸超分子配合物的合成与结构
2013-09-15孙长艳李文军
孙长艳 李 杨 李文军 车 平
(功能分子与晶态材料科学与应用北京市重点实验室,北京科技大学化学与生物工程学院,北京 100083)
0 引 言
近年来,具有微孔结构的配合物成为配位化学和材料化学的研究热点,这是因为该类配合物不仅具有丰富多彩的结构,而且在催化、吸附、分离等方面都具有潜在的应用前景[1-4]。深入研究微孔结构形成过程的影响因素以及其影响机理,能够为微孔结构配合物的定向设计和可控合成提供指导。影响配合物结构的最主要的因素是金属离子和有机配体的性质,除此以外,反应物比例[5-6]、反应温度[7-8]、反应 pH[9-10]、反应溶剂[11-12]、模板分子[13-14]等也会对配合物的结构产生重要的影响。其中,模板分子的引入往往会占据孔道,避免结构穿插,有利于微孔结构的形成。但是,关于引入模板分子构筑微孔结构的配合物方面的报道仍然较少。
镧系金属离子因为配位数较高,配位几何构型多变,不容易形成微孔结构的配合物。但是镧系金属离子具有特殊的光学和磁学性质,将它们引入配合物中,有可能获得同时具有微孔结构和光学或磁学性质的复合多功能材料。因此,用镧系金属离子构筑微孔配合物也受到了人们的关注。考虑到镧系金属离子属于硬酸,容易和含氧原子的配体配位,用来构筑镧系配合物的配体常选用二元羧酸或多羧酸配体,如对苯二甲酸[15-16]、2,6-吡啶二甲酸[17-18]、吡嗪四甲酸[19-20]。2-羧基肉桂酸含有2个不对称的羧基,其中长臂的羧基可以在一定的角度范围内旋转,容易得到螺旋结构,已经被成功的用于构筑各种过渡金属配合物[21-26]。但是到目前为止,还没有关于2-羧基肉桂酸镧系配合物的报道。因此,本论文选取2-羧基肉桂酸为配体,并引入1,10-菲啰啉作为辅助配体,与镧系金属离子反应,成功合成了两个镧系超分子配合物[Ln(CCA)(OH)(phen)(H2O)]n·n(phen)·n H2O(Ln=Yb,1;Er,2)。晶体结构测定表明该配合物具有微孔结构。1,10-菲啰啉在其中起到了模板作用。
1 实验部分
1.1 仪器和试剂
所用试剂均为市售分析纯试剂。红外光谱使用Nicolet Avatar 360 FT-IR红外光谱仪(KBr压片,cm-1为单位);晶体结构测定使用Bruker SMART 1000 CCD单晶衍射仪在常温下收集衍射数据;元素分析采用Elementar Vario EL元素分析仪;热稳定性采用TGA-SDTA 851e热重分析仪(空气气氛,升温速率 10 ℃·min-1)。
1.2 配合物的合成
将 YbCl3·6H2O(0.039 g,0.1 mmol),H2CCA(0.020 g,0.1 mmol),phen·H2O(0.042 g,0.2 mmol),NaOH 水溶液(0.15 mL,0.65 mol·L-1)和 5 mL 去离子水混合,置于25 mL聚四氟乙烯内胆的密封不锈钢反应釜中,在100℃下加热3 d后缓慢降至室温。过滤得到无色块状晶体,分别用去离子水和乙醇洗涤,自然干燥,得配合物 1:产量 0.021 g(27.0%)。 元素分析计算值 C34H27N4O7Yb(%):C,52.53;H,3.48;N,7.21;测定值(%):C,52.66;H,3.52;N,7.23。 主要的红外吸收峰 (KBr压片,cm-1):3 449(m),1 644(w),1 581(s),1 544(m),1 518(m),1 482(w),1 426(s),1 413(s),1 348(m),1 284(w),1 135(w),1 080(w),972(m),842(m),764(m),729(s)。
配合物2的合成过程与配合物1相似,只是用ErCl3·6H2O 代替 YbCl3·6H2O,得粉色块状晶体,产量 0.020 g(25.9%)。 元素分析计算值 C34H27N4O7Er(%):C,52.95;H,3.50;N,7.27;测定值(%):C,52.87;H,3.64;N,7.32。主要的红外吸收峰 (KBr压片,cm-1):3 549(m),3 449(m),1 647(w),1 579(s),1 544(m),1 512(m),1 485(w),1 425(s),1 391(s),1 350(m),1 286(w), 1 138(w),1 083(w),975(m),841(m),769(m),727(s)。
1.3 配合物晶体结构的测定
将挑选出的单晶置于Bruker SMART 1000 CCD单晶衍射仪上,用经石墨单色器单色化的Mo Kα 射线(λ=0.071 073 nm),以 φ-ω 扫描方式收集衍射点。晶体结构用直接法解出[27],结构解析及修正程序为SHELX-97[28],所有非氢原子均从差值傅里叶图中确定并对其原子坐标和各向异性热参数进行全矩阵最小二乘法修正;所有氢原子均为理论加氢。配合物1和2的晶体学数据列于表1中,主要的键长和键角数据列于表2中。
CCDC:917027,1;917028,2。

表1 配合物1和2的晶体学数据Table 1 Crystallographic data of complexes 1 and 2
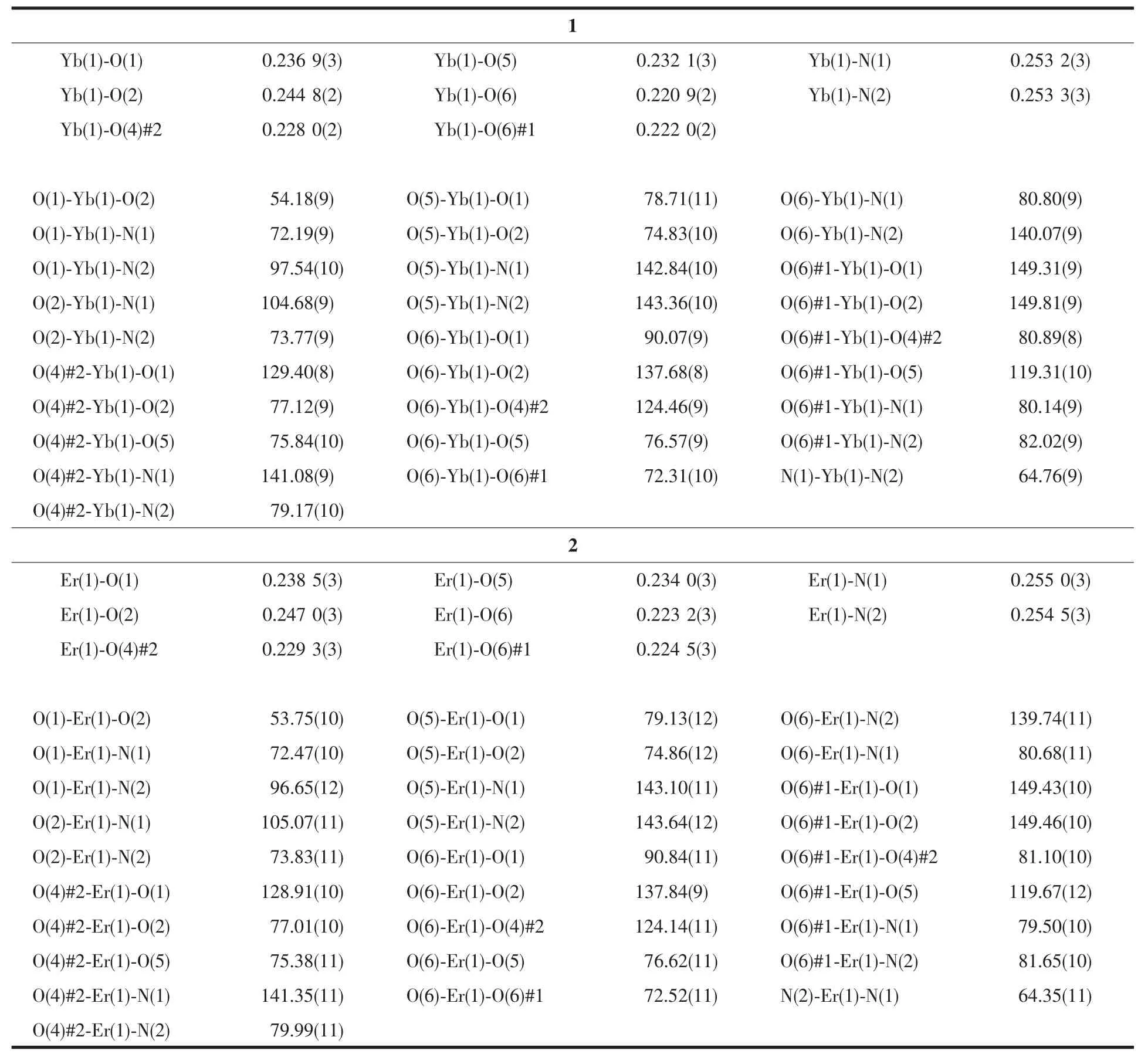
表2 配合物1和2的主要键长和键角Table 2 Selected bond distances(nm)and bond angles(°)of complexes 1 and 2
2 结果与讨论
2.1 配合物的晶体结构
单晶结构分析表明,配合物1和2是同构的,下面仅以配合物1为例讨论其结构。在配合物1中只有一种配位环境的Ybバ离子,如图1所示,Ybバ离子位于八配位的四方反棱柱中心。每个Ybバ离子与6个氧原子以及2个氮原子配位。其中,3个氧原子来自于 2个 CCA2-配体的羧基 (O1,O2和O4#2),3个氧原子来自于2个羟基(O6和O6#1)和1个配位水分子(O5),而2个氮原子来自于1个螯合的 1,10-菲啰啉分子(N1 和 N2)。O1、O2、N1 和 N2 构成的平面与O4#2、O5、O6和O6#1构成的平面夹角仅为3.9°。Yb-N平均键长0.253 3 nm,大于Yb-O平均键长(0.230 8 nm)。
在配合物1中,羟基以桥连双齿配位,由两个羟基桥联的双核单元[Yb2(OH)2]可以看作是其最小构筑单元 (见图1),其中Yb…Yb距离为0.357 6 nm。CCA2-配体采取三齿配位模式,长臂羧基以螯合双齿配位,短臂羧基以单齿配位。CCA2-配体将这些最小构筑单元连接起来,形成沿c轴方向的一维双链结构,如图2所示。1,10-菲啰啉分子位于链的上下两侧。链间1,10-菲啰啉分子所在的平面相互平行,且面间距为0.370 nm,显示了π-π堆积作用的存在。CCA2-配体的羧基氧原子与配位水分子之间形成氢键,O5…O3#2距离为0.271 2 nm。正是这些氢键和π-π堆积作用将一维链连成了三维微孔超分子网络结构 (见图3)。配合物1中有两种类型的1,10-菲啰啉分子,一种以螯合双齿参与配位,另一种不参与配位,与晶格水分子一起位于孔道中。游离的1,10-菲啰啉分子所在的平面相互平行,且面间距为0.351 nm,说明也存在π-π堆积作用,它们对于微孔超分子结构的形成起到了模板作用。配合物中的羧基氧原子和1,10-菲啰啉的氮原子都是潜在的氢键受体,配位水和晶格水分子都是潜在的氢键给体,实际上它们都参与形成了氢键。O7…O2#2距离为0.291 7 nm,O7…O3#2距离为0.295 4 nm,O5…N4#1距离为0.275 9 nm。这些氢键的形成使得超分子结构更加稳定。详细的氢键数据列于表3。2.2 配合物的热稳定性
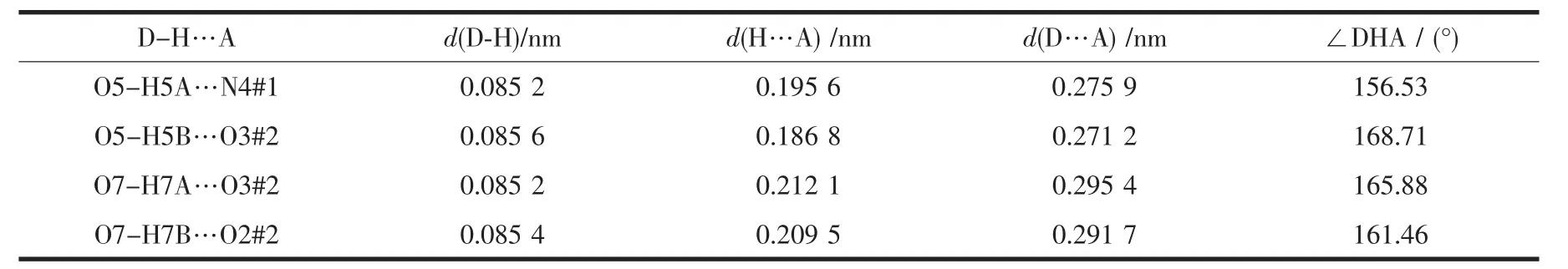
表3 配合物1和2中的氢键数据Table 3 Hydrogen bond geometry in complexes 1 and 2
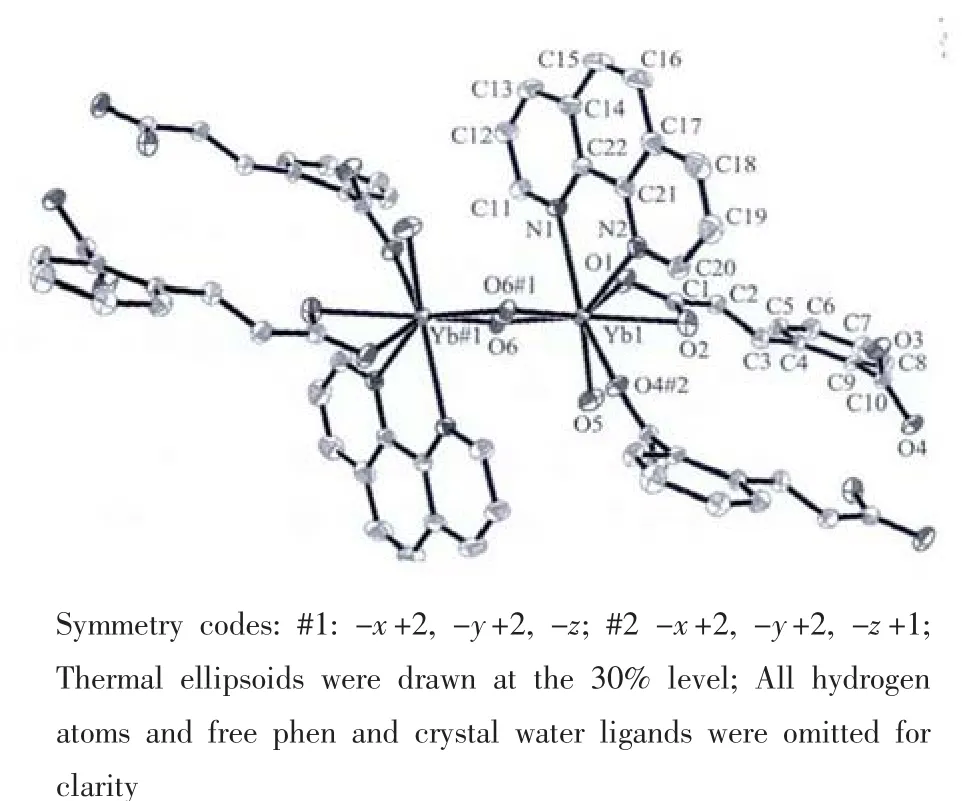
图1 配合物1中Ybバ离子的配位环境Fig.1 Coordination environment of Ybバion in complex 1
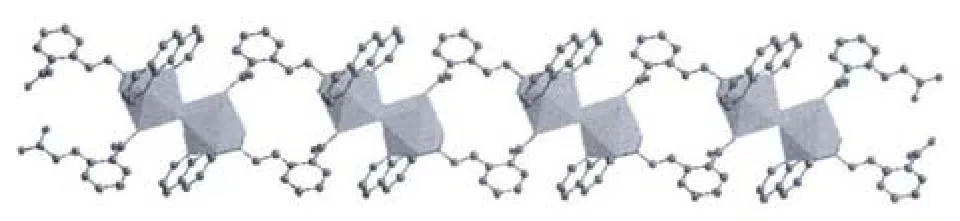
图2 配合物1中沿c轴方向的一维双链结构Fig.2 1D double-stranded chains in complex 1

图3 配合物1的三维微孔超分子网络结构Fig.3 3D microporous network of complex 1
标题配合物在空气中稳定,不溶于通常的溶剂如水、乙醇和丙酮。为了研究标题配合物的热稳定性,测定了两个配合物的热重分析曲线。结果显示两个配合物具有相似的热分解过程,都只经历一次失重过程。加热到156和125℃时,两个配合物分别开始分解。在失去晶格中的1,10-菲啰啉和水的同时,骨架结构就发生崩塌。这也进一步说明了游离的1,10-菲啰啉在微孔结构的形成中起到了模板作用。
[1]Fernandez C A,Liu J,Thallapally P K,et al.J.Am.Chem.Soc.,2012,134:9046-9049
[2]Wee L H,Wiktor C,Turner S,et al.J.Am.Chem.Soc.,2012,134:10911-10919
[3]Soubeyrand-Lenoir E,Vagner C,Yoon J W,et al.J.Am.Chem.Soc.,2012,134:10174-10181
[4]Jiang L,Meng X R,Xiang H,et al.Inorg.Chem.,2012,51:1874-1880
[5]Gao Q,Xie Y B,Li JR,et al.Cryst.Growth Des.,2012,12:281-288
[6]Hutchinson D J,Hanton L R,Stephen S C.Inorg.Chem.,2011,50:7637-7649
[7]Zuo Y,Fang M,Xiong G,et al.Cryst.Growth Des.,2012,12:3917-3926
[8]Hu TL,Tao Y,Chang Z,et al.Inorg.Chem.,2011,50:10994-11003
[9]Wu H,Yang J,Liu Y Y,et al.Cryst.Growth Des.,2012,12:2272-2276
[10]Sun D,Wei Z H,Yang CF,et al.CrystEngComm,2011,13:1591-1601
[11]Li L N,Wang S Y,Chen T L,et al.Cryst.Growth Des.,2012,12:4109-4115
[12]Lan Y Q,Jiang H L,Li S L,et al.Inorg.Chem.,2012,51:7484-7491
[13]Su C Y,Cai Y P,Chen C L,et al.Angew.Chem.,Int.Ed.,2002,41:3371-3375
[14]Liu F J,Sun D,Hao H J,et al.Cryst.Growth Des.,2012,12:354-361
[15]Chen K,Dong D P,Sun Z G,et al.Dalton Trans.,2012,41(36):10948-10956
[16]Chen L,Huang L,Zhang D,et al.Inorg.Chem.Commun.,2012,21:182-185
[17]Carr R,Evans N H,Parker D.Chem.Soc.Rev.,2012,41(23):7673-7686
[18]Bo QB,Sun GX,Geng DL,Inorg.Chem.,2010,49:561-571
[19]Quan Y P,Zhao L H,Yang A H,et al.CrystEngComm.,2009,11:1679-1685
[20]ZHAI Bin(翟滨),YI Yong-Ling(伊勇玲),HAN Nan-Nan(韩楠楠),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2012,28(12):2535-2539
[21]Lei Z H,Cha Y E,Li X,et al.J.Coord.Chem.,2012,65(9):1592-1599
[22]Li X Y,Wang S S,Liu C B,et al.Chin.J.Struct.Chem.,2011,30(12):1803-1809
[23]Huang Y,Yan B,Shao M.J.Mol.Struct.,2009,919(1-3):185-188
[24]Sun CY,Zhou J,Jin L P.J.Mol.Struct.,2007,843(1-3):95-101
[25]Sun CY,Li L C,Jin L P.Polyhedron,2006,25:3017-3024
[26]Li F,Ma Z,Wang Y L,et al.CrystEngComm,2005,7:569-574
[27]Sheldrick G M.SHELXS 97,Program for Crystal Structure Solution,University of Göttingen,Göttingen,Germanny,1997.
[28]Sheldrick G M.SHELXL 97,Program for Crystal Structure Refinement,University of Göttingen,Göttingen,Germanny,1997.
