吉西他滨联合奥沙利铂经肝动脉化疗栓塞治疗原发性肝癌
2013-09-15张永裕张晓霞刘永华张泽富
张永裕 张晓霞 刘永华 张泽富
吉西他滨联合奥沙利铂经肝动脉化疗栓塞治疗原发性肝癌
张永裕 张晓霞 刘永华 张泽富
目的 探讨吉西他滨联合奥沙利铂经肝动脉化疗栓塞(TACE)治疗原发性肝癌的临床疗效及安全性。方法 原发性肝癌患者40例, 随机分为两组, 观察组采用吉西他滨联合奥沙利铂进行TACE治疗, 对照组采用注射用盐酸吡柔比星为主进行TACE治疗, 进行疗效及不良反应评价。结果 观察组的近期有效率(50.0%)高于对照组(45.0%), 疾病控制率(85.0%)高于对照组(75.0%), 差异无统计学意义(P>0.05); 在远期疗效上, 观察组在1年内的生存率高于对照组, 差异无统计学意义( P>0.05)。观察组骨髓抑制发生率低于对照组, 神经系统毒性高于对照组。结论 吉西他滨联合奥沙利铂方案TACE治疗原发性肝癌的近期疗效较好, 不良反应可耐受, 在不增加不良反应基础上, 为中晚期肝癌行TACE治疗提供了新的药物组合方案, 但其远期疗效尚待进一步观察。
原发性肝癌;吉西他滨;奥沙利铂;经肝动脉化疗栓塞;疗效
原发性肝癌为常见的恶性肿瘤, 多数患者发现时已属中晚期, 失去了手术切除的机会。经导管肝动脉化疗栓塞术(TACE)在原发性肝癌的综合治疗中发挥着越来越重要的作用, 已成为中晚期肝癌的首选治疗方法[1-3]。中山大学附属第五医院放射科于2010年7月~2012年7月应用吉西他滨+奥沙利铂联合方案(GEMOX方案)行经肝动脉化疗栓塞(TACE)治疗原发性肝癌, 探讨其临床疗效及安全性, 现报告如下。
1 资料与方法
1.1 一般资料 2010年7月~2012年7月收治的原发性肝癌40例, 其中男26例, 女14例;年龄25~80岁, 平均年龄54.8岁;巨块型23例, 结节型17例, 肿瘤大小23~138 mm(共48个肿瘤, 平均68 mm)。将患者随机分为观察组、对照组, 各20例。
1.2 入选标准 所有患者根据原发性肝癌规范化诊治的专家共识及原发性肝癌诊疗规范诊断为原发性肝癌, 肝功能为Child-Pugh A或B级, KPS评分≥70, 临床病灶可测量, 有介入治疗适应证, 无介入治疗绝对禁忌证, 预计生存期在2个月以上, 无其他恶性肿瘤病史, 患者知情同意。
1.3 方法 所有患者均采用Seldinger技术, 经皮股动脉穿刺,用5F RH导管插入腹腔动脉造影, 并延迟门静脉显示, 了解肝动脉及肿瘤血管形态及走行后, 将导管B超选至肿瘤供血动脉(35%患者使用微导管), 行药物灌注加栓塞。观察组先给予吉西他滨1000 mg/m2缓慢灌注, 再用奥沙利铂85 mg/m2和超液化碘油 5~20 ml充分混合成乳剂缓慢注入供血动脉。对照组用吡柔比星40 mg/m2和超液化碘油 5~20 ml充分混合成乳剂缓慢注入供血动脉。所有患者分别接受2~5次TACE治疗。
1.4 疗效评定及安全性评价 所有患者均在首程TACE治疗后3个月进行CT平扫+增强复查, 根据 mRECIST1.1标准[4]分析评估患者疗效, 统计肿瘤客观有效率(ORR)/疾病控制率(DCR), ORR=CR+PR; DCR=CR+PR+SD。随访时间为1~2年,统计两组治疗6个月、1年生存率。根据 WHO 抗癌药物毒性反应分度标准及NCI-CTCAEv3.0标准、Levi 专用感觉神经毒性分级标准评定不良反应[4]。
1.5 统计学方法 所有数据统计均采用SPSS13.0软件包进行, 采用χ2检验, P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效比较 对两组患者首次TACE治疗3个月后,进行疗效评价, 结果如表1所示, 观察组的近期有效率(50.0%)高于对照组(45.0%), 疾病控制率(85.0%)高于对照组(75.0%),但差异均无统计学意义 ( P>0.05)。
2.2 两组患者生存情况比较 结果如表2 所示, 观察组患者治疗1年后生存率(75.0%)高于对照组(55%), 两组间差异有统计学意义。
2.3 两组患者之间不良反应的比较 结果如表3 所示, 两组患者其不良反应均以恶心、呕吐、肝、肾功能受损、血小板减少、中性粒细胞减少为主, 观察组骨髓抑制发生率低于对照组(P<0.05), 观察组神经毒性高于对照组, 差异无统计学意义(P>0.05)。

表1 两组患者近期临床疗效结果比较

表2 两组患者远期临床疗效结果比较
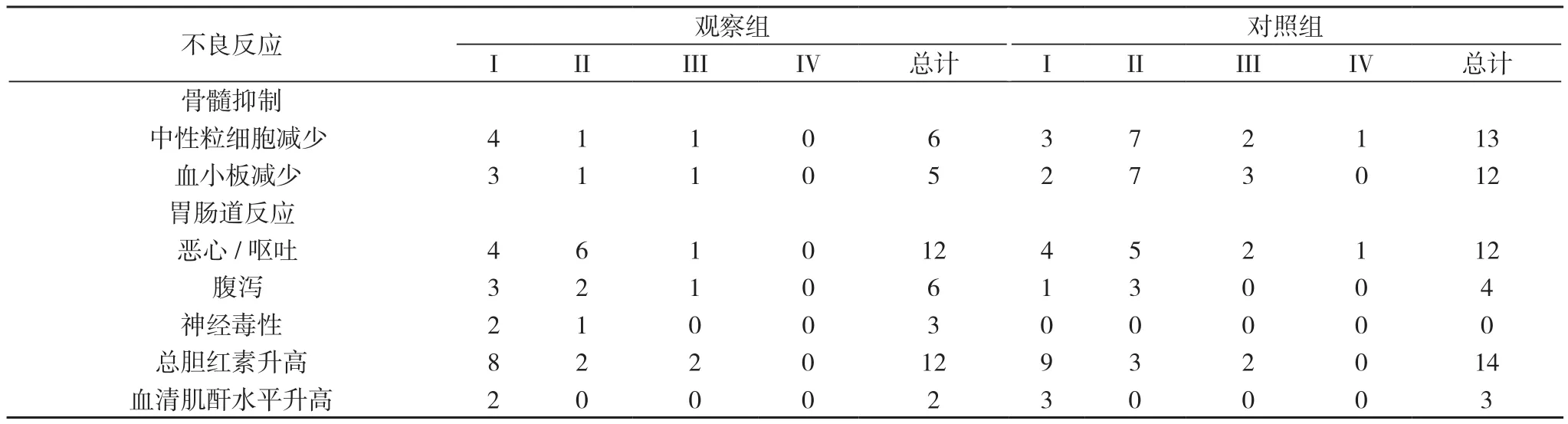
表3 两组不良反应的比较
3 讨论
肝癌患者早期常无症状, 多数患者确诊为肝癌时已为中晚期, 丧失了手术机会。TACE是中晚期肝癌的首选治疗方法[1-3]。吉西他滨是新一代抗代谢类核苷类抗肿瘤药, 奥沙利铂是第3代铂类代谢药物, 吉西他滨与奥沙利铂具有协同作用, GEMOX方案已应用于多种肿瘤的治疗, 并取得良好的疗效, 较低的不良反应[5]。肝癌是一种对化疗相对不敏感的肿瘤, 近年来已有多个GEMOX 方案治疗肝癌的临床研究,取得良好效果[6-8]。
本临床研究中, 作者采用GEMOX方案行TACE术治疗原发性肝癌, 对两组患者临床疗效比较, 发现观察组患者的近期有效率(50.0%)稍高于对照组(45.0%), 疾病控制率(85.0%)高于对照组(75.0%), 但差异均无统计学意义 ( P>0.05), 与胡其艳、吴海丽等[9,10]报道GEMOX 方案优于阿霉素为主的方案有所不同。在远期疗效上, 观察组在1年内的生存率高于对照组, 但差异无统计学意义( P>0.05), 亦与胡其艳、吴海丽等[9,10]报道有差异, 可能为样本量较小所致。在对两组患者不良反应比较中, 发现观察组骨髓抑制发生率低于对照组(P<0.05), 与胡其艳、吴海丽等[9,10]报道相似。观察组神经毒性高于对照组, 差异无统计学意义(P>0.05)。两组患者其余主要不良反应发生率差异无统计学意义。本研究部分结果与已有报道不一致, 可能为样本量较小所致, 同时未对影响近期疗效及生存率的可能因素进行分层分析, 有待扩大样本量, 进一步评价。
综上, 吉西他滨联合奥沙利铂治疗原发性肝癌患者, 疗效较好, 不良反应较轻, 患者耐受性好。在不增加不良反应的情况下, 为肝癌行 TACE 术提供了新的药物组合方案, 但其远期疗效尚待进一步观察。
[1] 刘波, 刘乾贵, 越太迁, 等. 原发性肝癌介入化疗灌注与化疗栓塞疗效评价. 现代医药卫生, 2010,26(16):2469-2470.
[2] Shin SW. The current practice of transarterial chemoembolization for the treatment of hepatocellular carcinoma. Korean J Radiol, 2009, 10:425-434.
[3] Bruix J, Llovet JM. Major achievements in hepatocellular carcinoma. Lancet, 2009,373:614-616.
[4] Lencioni R, Llovet JR. Modified RECIST(Mresist)assessment for hepatocellular carcinoma. Semin Liver Dis, 2010,30:52-60.
[5] Meriggi F, Zaniboni A. Gemox: a widely useful therapy against solid tumors-review and personal experience. J Chemother. 2010, 22(5): 298-303.
[6] Dhooge M, Coriat R, Mir O, et al. Feasibility of gemcitabine plus oxaliplatin in advanced hepatocellular carcinoma patients with Child-Pugh B cirrhosis. Oncology, 2013,84(1):32-38.
[7] Zaanan A, Williet N, Hebbar M, et al. Gemcitabine plus oxaliplatin in advanced hepatocellular carcinoma: a large multicenter AGEO study. J Hepatol, 2013,58(1):81-88.
[8] 田思源, 徐爱兵, 沈茜, 等. 吉西他滨联合奥沙利铂治疗晚期原发性肝癌的临床观察. 肿瘤基础与临床, 2012,25(1):52-53.
[9] 胡其艳, 王 蕾, 孙秋实, 等. 吉西他滨联合奥沙利铂经肝动脉化疗栓塞对肝癌术后复发的预防作用探究. 现代生物医学进展, 2013,13(3):530-535.
[10] 吴海丽. 含奥沙利铂方案经导管肝动脉化疗栓塞术治疗原发性肝癌的临床观察. 临床和实验医学杂志, 2013,12(11):856-857.
519000 中山大学附属第五医院放射科(张永裕 刘永华 张泽富), 内分泌皮肤介入科(张晓霞)
张泽富
