低分子肝素皮下注射治疗轻-中度活动性溃疡性结肠炎的疗效评价
2013-09-11宋军民
宋军民,李 卉,李 岩
中国医科大学附属盛京医院消化内科,辽宁 沈阳 110004
溃疡性结肠炎(ulcerative colitis,UC)是临床上常见的疾病之一,多数患者症状反复发作,常规治疗效果较差,探索对UC治疗有效的药物具有重要的临床意义。近年来国内外的研究表明,UC患者存在高凝状态,部分患者合并多处深静脉或动脉血栓,而且血栓形成在疾病发生发展过程中具有重要作用,因此,抗凝治疗可能对UC患者具有良好的疗效,许多临床医生已经开始对UC患者进行常规抗凝治疗,但目前国内外系统的临床研究很少,且其疗效一直存在争议。中国医科大学附属盛京医院消化内科近年来对部分轻-中度活动性UC患者应用低分子肝素(low-molecularweight-heparin,LMWH)治疗,现报告如下。
1 资料与方法
1.1 一般资料 选取2008年8月-2012年8月于中国医科大学附属盛京医院消化内科首次诊断为轻-中度活动性UC的住院患者48例,所有患者诊断前均进行结肠镜检查,诊断标准见参考文献[1]。男29例,女19例,年龄25~65岁,平均(42.7 ±8.4)岁,病程3~17 个月,平均(8.3 ±3.7)个月。
1.2 治疗方案和疗效评价 48例入选患者随机分成2组,每组24例,2组患者的年龄、性别、病程、病变累及范围和病情严重程度构成差异均无统计学意义(见表1)。常规治疗组的方案为:5-氨基水杨酸1.0 g,3次/d口服,黄连素和锡类散保留灌肠,肠道微生态制剂和复方谷氨酰胺胶囊口服;LMWH治疗组在常规治疗组的基础上加用低分子肝素钙注射液4100 IU抗Xa因子(WHO单位),每12 h 1次皮下注射,疗程为15 d。需要使用糖皮质激素或免疫抑制剂的患者不进入该研究。
所有研究对象治疗前均进行临床活动指数(CAI)、内镜指数(EI)评分[2],炎症指标:CRP(C-反应蛋白,正常值:0~8 mg/L)、ESR(红细胞沉降率,正常值:0~15 mm/h)、FIB(纤维蛋白原含量,正常值:2~4 g/L)和凝血指标:PT(凝血酶原时间,正常值:10.5~13.5 s)、APTT(活化部分凝血活酶时间,正常值:21~37 s)、TT(凝血酶凝结时间,正常值:13.5 ~19.5 s)、D-dimer(D-二聚体,正常值:0 ~252 μg/L)、血小板计数(正常值:135~350×109/L)检测。治疗期间每天观察患者的症状和体征,每3 d复查上述指标,15 d疗程结束后复查结肠镜,评价两组患者的CAI、EI和上述指标,并进行组间疗效比较。同时随机选取同时期的结肠息肉内镜下切除患者12例,作为对照组检测上述指标。
疗效标准判定[1]:完全缓解(临床症状消失,结肠镜复查见黏膜大致正常);有效(临床症状基本消失,结肠镜复查见黏膜轻度炎症或假息肉形成);无效(经治疗后临床症状、内镜和病理检查结果均无改善)。
1.3 统计学分析 采用SPSS 13.0软件,计量资料用表示,两组间比较采用Mann-Whitney U检验,计数资料组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 治疗前常规治疗组、LMWH治疗组、结肠息肉组患者炎症和凝血指标的比较 48例轻-中度UC患者和12例结肠息肉患者均进行 CRP、ESR、FIB、PT、APTT、TT、D-二聚体和血小板计数检测,UC患者CRP、ESR、FIB、D-二聚体和血小板计数均较结肠息肉患者显著升高(P <0.001;P <0.001;P <0.001;P <0.01;P <0.05),而 PT、APTT、TT 与结肠息肉组无显著差异(P 均>0.05);治疗前LMWH治疗组和常规治疗组上述指标的比较,差异无统计学意义(P均>0.05,见表2)。
2.2 治疗后常规治疗组、LMWH治疗组患者炎症和凝血指标的比较 15 d治疗结束后,2组患者的CRP、ESR、FIB、D-二聚体和血小板计数均较治疗前显著下降(P均<0.01);LMWH治疗组 CRP、D-二聚体均较常规治疗组显著下降(P均<0.05),观察2组患者的CRP、D-二聚体变化趋势发现,第10~13天开始出现显著差异(P<0.05)(见图1A、图1B),而LMWH治疗组与常规治疗组ESR、FIB和血小板计数差异无统计学意义(P 均 >0.05,见表2)。
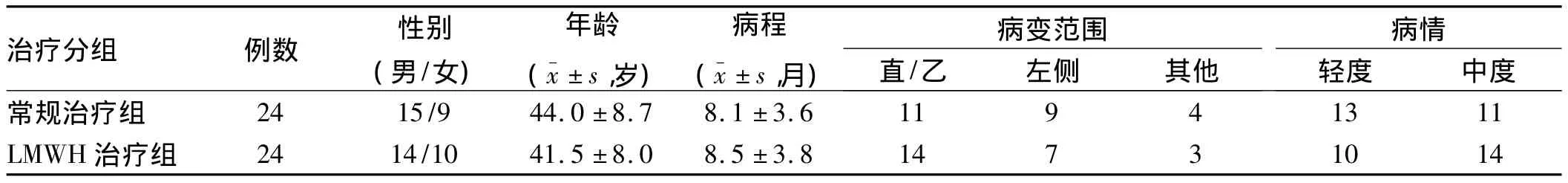
表1 常规治疗组和LMWH治疗组患者治疗前各特征的比较Tab 1 Comparison of features between conventional group and LMWH group before treatment
表2 结肠息肉组、常规治疗组和LMWH治疗组患者的炎症和凝血指标比较()Tab 2 Comparison of markers of inflammation and coagulation among colonic polyp group,conventional group and LMWH group()
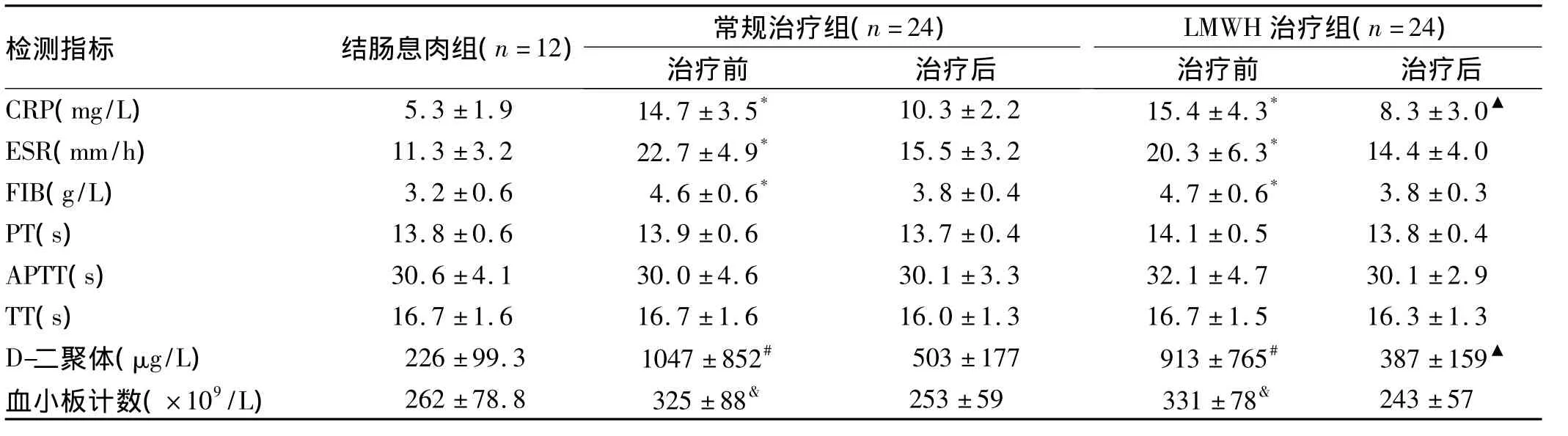
表2 结肠息肉组、常规治疗组和LMWH治疗组患者的炎症和凝血指标比较()Tab 2 Comparison of markers of inflammation and coagulation among colonic polyp group,conventional group and LMWH group()
注:与结肠息肉组比较,*P <0.001,#P <0.01,& P <0.05;与常规治疗组治疗后比较,▲P <0.05。
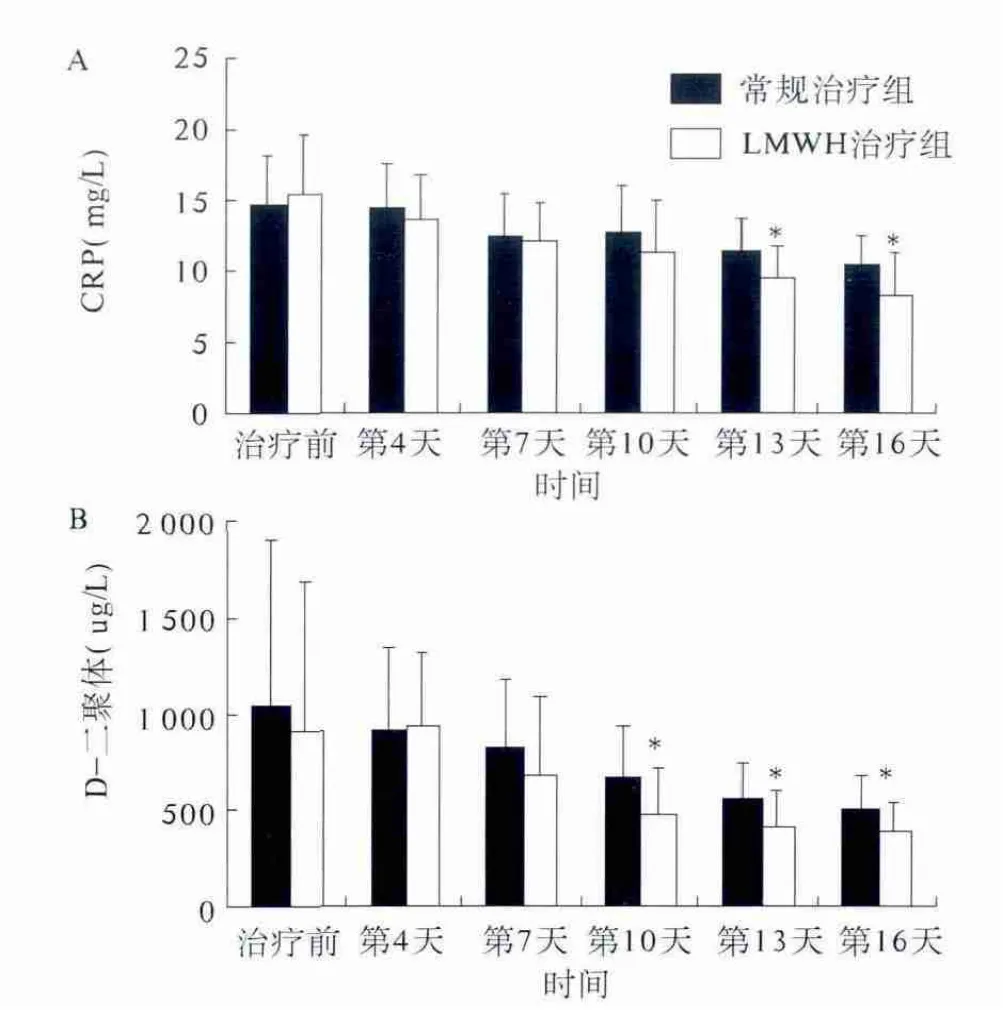
图1 治疗过程中常规治疗组和LMWH治疗组患者指标的比较 A:CRP;B:D-二聚体 *P<0.05Fig 1 Comparison of markers between conventional group and LMWH group during the treatmentA:CRP;B:D-dimer*P <0.05
2.3 治疗前后常规治疗组、LMWH治疗组患者CAI评分的比较 治疗前2组患者的CAI评分无显著差异(P>0.05),15 d治疗结束后,2组患者CAI评分均较治疗前显著下降(P均<0.01),但治疗后2组患者的CAI评分无显著差异(P>0.05,见图2A)。

图2 治疗前后常规治疗组和LMWH治疗组患者CAI和EI评分的比较 A:CAI评分;B:EI评分Fig 2 Comparison of CAI scores and EI scores between conventional group and LMWH group before as well as after the treatmentA:CAI scores;B:EI scores
2.4 治疗前后常规治疗组、LMWH治疗组患者EI评分的比较 治疗前2组患者的EI评分无显著差异(P>0.05),15 d治疗结束后,2组患者EI评分均较治疗前显著下降(P均<0.01),但治疗后2组患者的EI评分无显著差异(P>0.05,见图2B)。
2.5 治疗后常规治疗组、LMWH治疗组患者临床疗效的比较 15 d治疗结束后,2组均未发现达到完全缓解的患者;LMWH治疗组24例UC患者中,16例有效,8例无效;常规治疗组24例UC患者中,19例有效,5例无效,两组患者的有效率差异无统计学意义(P>0.05)。
2.6 不良反应 LMWH治疗组无1例发生出血、过敏等不良反应。
3 讨论
UC的发病过程涉及遗传易感性、免疫应答、肠道菌群和生活环境等多方面的因素,目前尚不十分清楚。研究表明,上述因素作用于机体,激活体内的凝血系统,易引起微静脉、微动脉,甚至是大静脉和大动脉等血管的血栓形成,导致上述血管舒张功能下降,组织低灌注状态和肠道黏膜愈合不良,症状反复发作,因此,UC是血栓形成的一个独立的风险因素[3]。在UC等炎症性肠病的患者中,血栓栓塞是其他疾病患者的3~4 倍[4],UC 患者并发布 - 加综合征[5]、颅静脉窦血栓[6]、门静脉血栓[7]、肾静脉血栓[8]、左心室血栓[9]等血栓性疾病已有广泛报道。研究发现,UC患者凝血因子表达增加,Kume等[10]研究发现,与缓解期UC相比,活动期UC患者体内凝血因子vWF、纤维蛋白原(FIB)、凝血因子Ⅺ、Ⅸ、Ⅷ、凝血酶原片段F1+2等因子的浓度均显著升高,这种表现与缺血性结肠炎类似。此外,血小板活化也是UC发生过程中作用的一个病理机制。Shen等[11]研究发现,与健康人相比,UC患者血小板、血小板分布宽度等指标也显著升高。上述研究提示UC患者血液促凝物质增多,是血栓形成的重要机制。在我们的研究中,48例轻-中度UC患者的CRP、ESR、FIB、D-二聚体和血小板计数均较结肠息肉组显著升高,提示UC患者处于血液高凝状态。但PT、APTT、TT与结肠息肉组差异无统计学意义,可能与本研究的样本过小或患者的病情较轻(本研究未纳入重度UC患者)有关。
由于血液高凝状态是UC患者症状反复发作的重要因素,国内外开展了许多应用肝素治疗UC的研究。曾有研究表明,传统肝素(unfractionated heparin,UH)治疗UC取得了良好的疗效[12]。与传统肝素UH相比,LMWH具有安全性高、疗效良好等优点,在临床上逐渐取代传统肝素。但至今为止,多数研究未能证实LMWH 皮下注射显著优于传统治疗[13-15]。Zezos等[16]的研究提示UC患者应用LMWH的安全性和耐受性良好,但未发现其疗效明显优于常规治疗;在Zezos的研究中,LMWH与糖皮质激素联合应用,糖皮质激素对炎症、免疫反应和凝血具有显著的影响,可能干扰LMWH的疗效。因此,在本研究中我们选择未应用糖皮质激素的轻-中度UC患者,从而独立的观察LMWH的疗效。CRP是反映UC炎症活动的敏感指标之一[17],D-二聚体与 UC 的病情活动密切相关[18],在研究中我们发现LMWH能改善UC患者的CRP和D-二聚体,提示LMWH可能对UC治疗有效。但本研究中两组患者的CAI和EI评分无显著的差异,提示LMWH对UC患者的临床症状和内镜下表现无显著改善作用。近年来的研究表明,LMWH对UC的疗效可能与其用法有关,常规皮下注射剂量较低,因而疗效有限,若增加剂量将增加出血等并发症的风险。目前正在研究的新型口服型LMWH在结肠内释放,局部药物浓度较高,治疗 UC 取得一定的疗效[19]。Luo等[20-21]研究发现,LMWH直肠内给药对实验性UC大鼠能显著降低血清TNF-a、IL-6和FXa,修复大鼠的肠黏膜屏障,因而口服型LMWH可能使UC患者受益。Pastorelli等[22]应用口服型 LMWH治疗轻 -中度左侧UC,临床缓解率达70%,其中1例取得内镜下愈合,无1例发生出血等不良反应。这些研究使口服型LMWH有望成为治疗UC的重要用药。
总之,本研究表明,血液高凝状态在轻-中度UC患者中普遍存在,LMWH皮下注射能改善部分炎症和凝血指标,但对临床症状和内镜下表现无显著改善作用,这种情况可能与它的用法(皮下注射)有关,今后应加强对口服型或局部作用的LMWH疗效的研究。
[1]Cooperative Group of inflammtory bowel disease,Chinese Society of Gastroenterology.Chinese consensus on standard diagnosis and treatment of inflammtory bowel disease[J].Chin J Gastroenterol,2007,12(8):488-495.中华医学会消化病学分会炎症性肠病协作组.对我国炎症性肠病诊断治疗规范的共识意见[J].胃肠病学,2007,12(8):488-495.
[2]Rachmilewitz D.Coated mesalazine(5-aminosalicylic acid)versus sulphasalazine in the treatment of active ulcerative colitis:a randomised trial[J].BMJ,1989,298(6666):82-86.
[3]Papa A,Scaldaferri F,Danese S,et al.Vascular involvement in inflammatory bowel disease:pathogenesis and clinical aspects[J].Dig Dis,2008,26(2):149-155.
[4]Stadnicki A.Involvement of coagulation and hemostasis in inflammatory bowel diseases[J].Curr Vasc Pharmacol,2012,10(5):659-669.
[5]Dacha S,Devidi M,Osmundson E.Budd-Chiari syndrome in a patient with ulcerative colitis and no inherited coagulopathy[J].World J Hepatol,2011,3(6):164-169.
[6]Kawanishi M,Yoshida Y,Sakaguchi I,et al.Cerebral venous sinusthrombosis in a patient with ulcerative colitis[J].J Stroke Cerebrovasc Dis,2003,12(6):271-275.
[7]Rauh P,Mönkemüller K,Rickes S.Portal vein thrombosis in a patient with ulcerative colitis[J].Acta Gastroenterol Latinoam,2009,39(2):98,167.
[8]Yang DJ,Park YS,Yu YH,et al.A case of renal vein thrombosis in a patient with ulcerative colitis[J].Korean J Gastroenterol,2009,54(4):248-251.
[9]Saleh T.Left ventricular thrombosis in ulcerative colitis[J].Case Rep Gastroenterol,2010,4(2):220-223.
[10]Kume K,Yamasaki M,Tashiro M,et al.Activations of coagulation and fibrinolysis secondary to bowel inflammation in patients with ulcerative colitis[J].Intern Med,2007,46(17):1323-1329.
[11]Shen J,Ran ZH,Zhang Y,et al.Biomarkers of altered coagulation and fibrinolysis as measures of disease activity in active inflammatory bowel disease:a gender-stratified,cohort analysis[J].Thromb Res,2009,123(4):604-611.
[12]Folwaczny C,Wiebecke B,Loeschke K.Unfractioned heparin in the therapy of patients with highly active inflammatory bowel disease[J].Am J Gastroenterol,1999,94(6):1551-1555.
[13]Shen J,Ran ZH,Tong JL,et al.Meta-analysis:the utility and safety of heparin in the treatment of active ulcerative colitis[J].Aliment Pharmacol Ther,2007,26(5):653-663.
[14]de Bièvre MA,Vrij AA,Schoon EJ,et al.Randomized,placebocontrolled trial of low molecular weight heparin in active ulcerative colitis[J].Inflamm Bowel Dis,2007,13(6):753-758.
[15]Chande N,MacDonald JK,Wang JJ,et al.Unfractionated or low molecular weight heparin for induction of remission in ulcerative colitis:a Cochrane inflammatory bowel disease and functional bowel disorders systematic review of randomized trials[J].Inflamm Bowel Dis,2011,17(9):1979-1986.
[16]Zezos P,Papaioannou G,Nikolaidis N,et al.Low-molecular-weight heparin(enoxaparin)as adjuvant therapy in the treatment of active ulcerative colitis:a randomized,controlled,comparative study[J].Aliment Pharmacol Ther,2006,23(10):1443-1453.
[17]Henriksen M,Jahnsen J,Lygren I,et al.C-reactive protein:a predictive factor and marker of inflammation in inflammatory bowel disease.Results from a prospective population-based study [J].Gut,2008,57(11):1518-1523.
[18]Drzewoski J,Gasiorowska A,Małecka-Panas E,et al.Plasma total homocysteine in the active stage of ulcerative colitis[J].J Gastroenterol Hepatol,2006,21(4):739-743.
[19]Baumgart DC.CB-01-05-MMX,a novel oral controlled-release low molecular weight heparin for the potential treatment of ulcerative colitis[J].Curr Opin Investig Drugs,2010,11(5):571-576.
[20]Luo J,Cao J,Jiang X,et al.Effect of low molecular weight heparin rectal suppository on experimental ulcerative colitis in mice[J].Biomed Pharmacother,2010,64(7):441-445.
[21]Luo JY,Zhong Y,Cao JC,et al.Efficacy of oral colon-specific delivery capsule of low-molecular-weight heparin on ulcerative colitis[J].Biomed Pharmacother,2011,65(2):111-117.
[22]Pastorelli L,Saibeni S,Spina L,et al.Oral,colonic-release low-molecular-weight heparin:an initial open study of Parnaparin-MMX for the treatment of mild-to-moderate left-sided ulcerative colitis[J].Aliment Pharmacol Ther,2008,28(5):581-588.
