地佐辛注射液细菌内毒素检查法研究
2013-09-07时荣同谢冬梅郭道华王群
时荣同 谢冬梅 郭道华 王群
地佐辛注射液细菌内毒素检查法研究
时荣同 谢冬梅 郭道华 王群
目的 建立地佐辛注射液细菌内毒素检查方法。方法 参照《中国药典》2010版(二)部附录细菌内毒素检查法及其原则进行实验。结果 当地佐辛注射液稀释至100倍时可消除对鲎试剂与细菌内毒素凝聚反应的干扰。 结论 可以用细菌内毒素检查法对地佐辛注射液进行热原检查。
地佐辛注射液; 细菌内毒素检查; 鲎试剂; 干扰试验
地佐辛是一种强效阿片类镇痛药, 能有效缓解术后疼痛,其镇痛强度、起效时间和作用持续时间与吗啡相当。当稳态血药浓度超过5~9 ng/ml时, 能较好的缓解术后疼痛, 但是对阿片类镇痛药过敏的患者禁用。笔者通过研究, 发现地佐辛注射液目前没有细菌内毒素检查法这方面的研究。为了控制地佐辛注射液的质量和减少临床热原反应的发生, 笔者参照有关文献[1,2],对地佐辛注射液细菌内毒素检测方法进行了可行性试验,现总结如下。
1 试验材料
1.1 样品 地佐辛注射液3批, 规格1 ml(0.5 mg), 批号13042721,13051621 13062921, 生产厂家:扬子江药业集团有限公司。
1.2 试剂 鲎试剂:批号121206, 规格0.1 ml:λ=0.5 EU/ml, 湛江安度斯生物有限公司;批号130120, 规格0.1 ml:λ=0.25EU/ ml, 湛江博康海洋生物有限公司。
细菌内毒素工作标准品:批号2012-3, 效价120EU 规格1ml, 中国药品生物制品检定所。细菌内毒素检查用水, 以下简称(BET), 批号1207150, 规格5 ml/支 湛江安度斯生物有限公司。
1.3 仪器 XW_80A旋涡混旋器, 上海医科大学仪器厂;HH.214电热恒温水浴锅,江苏医疗器械厂。
2 试验方法与结果
2.1 鲎试剂灵敏度复核[3]按照《中国药典》2010版(二部)进行鲎试剂的标示灵敏度复核, 结果见表1所示。
2.2 样品内毒素理论限值(L)的确定及最大有效稀释浓度倍数MVD的计算[3]。
2.2.1 样品内毒素理论限值(L)的确定 本品临床使用每次最大剂量是20 mg,成人体重按60 kg计,人体致热阀(k)为5.0 EU/(kg·h)则L=K/M=5.0 EU·(kg·h)-1÷(20 mg÷60 kg)=15 EU·mg-1。
2.2.2 最大有效稀释浓度倍数的计算MVD 根据公式计算MVD=CL/λ计算。
MVD(λ=0.5)=5.0 mg·ml-1×15 EU·ml-1÷0.5 EU·ml-1=150倍。
MVD(λ=0.25)=5.0 mg·ml-1×15 EU·ml-1÷0.25 EU·ml-1=300倍。
2.3 样品干扰试验
2.3.1 干扰预试验 为排除样品自身对TAL与细菌内毒素凝胶反应可能存在干扰,取样品批号为13042721的原液, 分别按表2所列的稀释倍数稀释, 制成样品溶液浓度系列, 并制备含2λ 细菌内毒素的样品稀释液(PPC)进行干扰预试验,同时作阳性和阴性对照。结果见表2。
由干扰预试验可见, 两个厂家鲎试剂对地佐辛注射液用细菌内毒素检查在100倍稀释时无干扰。
2.3.2 干扰确证试验 为了最终确定是否存在干扰, 现进行以下正式干扰试验。取地佐辛注射液用细菌内毒素检查用水进行稀释100倍, 按《中国药典》2010版(二部)附录细菌内毒素检查供试品干扰试验项进行试验, 结果见表3。
干扰试验表明, 最大浓度2.0λ管均为阳性, 最低浓度0.25λ管均为阴性, 阴性对照管均为阴性, 用BET水和样品溶液制成的内毒素溶液的反应终点浓度几何平均值Es在0.5~ 2.0λ, Et在0.5~2.0Es范围内, 说明样品在该浓度下对两批鲎试剂均无干扰, 可进行细菌内毒素检查。
2.4 样品细菌内毒素检查 取地佐辛注射液3批, 将原液1:100倍稀释后用以上两批鲎试剂分别按《中国药典》2010版(二部)附录细菌内毒素检查法进行细菌内毒素检查, 结果3个批号供试品的内毒素检查均符合规定, 与家兔法检查一致。结果见表4。

表1 鲎试剂灵敏度复核结果

表2 干扰预试验结果鲎试剂批号121206 λ=0.5 EU/ml, 批号130120 λ=0.25 EU/ml
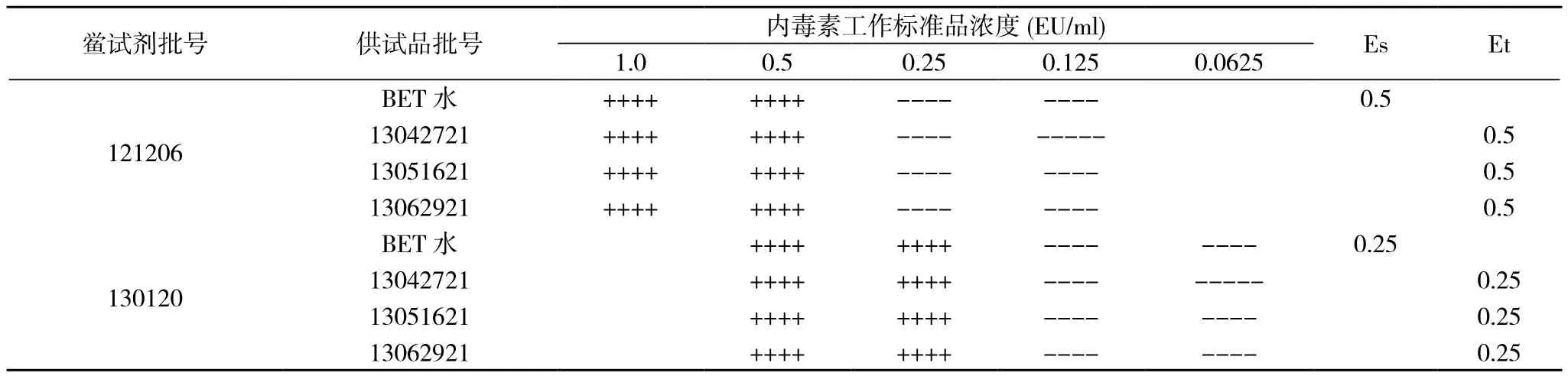
表3 干扰试验结果(1:100稀释液)
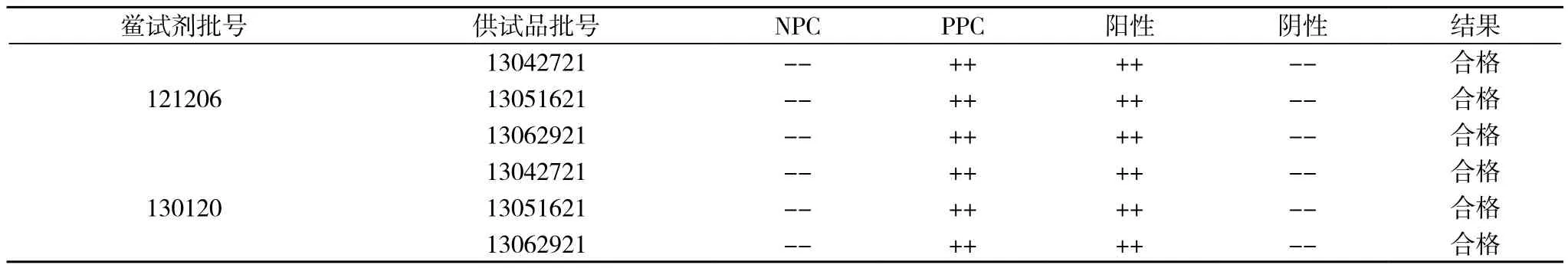
表4 地佐辛注射液细菌内毒素检查结果
3 讨论
地佐辛注射液的原液对TAL凝聚反应存在干扰, 通过预试验确证样品在1:100倍稀释时, 对细菌内毒素检查无干扰作用。本法操作简单, 精确度高, 重现性好, 因此本试验细菌内毒素法代替热原检查法是可行的[4]。通过本试验证明了地佐辛注射液的细菌内毒素检查法的可行性。本文通过干扰预试验确定样品的有效稀释倍数, 再由干扰试验进一步验证,从而减少干扰试验的盲目性。用不同厂家的鲎试剂进行试验且结果相同, 由此说明鲎试剂可以用于本品的细菌内毒素检查。
[1] 蔡彤,张国来,李波,等.84种注射液药品细菌内毒素检查法的方法学研究.中国药学杂志, 2010,45(2):150-155.
[2] 朱勤.复合磷酸氢钾注射液的细菌内毒素检查法.安徽医药, 2012,16(8):1190-1192.
[3] 国家药典委员会.中国药典(二部).北京:中国医院科技出版社, 2010:附录99-102.
[4] 王群,谢冬梅.阿扎司琼注射液的细菌内毒素检查法的探讨.安徽医药, 2011,15(5):564-565.
Study of bacterial endotoxin test for dezocine injection
SHI Rong-tong, XIE Dong-mei, GUO Dao-hua, WANG Qun.
Pharmacy Department,General Hospital of Wanbei Coal Mine Bureau, Suzhou Anhui 234011, China.
Objective To establish the bacterial endotoxin test in Dezocine Injection.Methods According to the CHP(2010 Edt.), inhibition or enhancement test forbacterial endotoxin test was carried out of sodium bicarbonate injection.Results The interference could be eliminated when Dezocine injection was diluted by 100 times .Conclusion bacterial endotoxin inspection method can be used for testing the pyrogen of Dezocine injection.
Dezocine injection; Bacterial endotoxin test(BET); Tachypleus amebocyte lysate(TAL); Interference test
234011 宿州市皖北煤电集团总医院药剂科(时荣同);蚌埠医学院第一附属医院药剂科(谢冬梅 郭道华 王群)
谢冬梅 E-imal:xiedongmei410@163.com
