XELOX方案与FOLFOXs方案治疗中国晚期胃癌患者的Meta分析
2013-09-05张瑞雪金启成杨薏帆曹邦伟
张瑞雪 闫 涵 王 民 金启成 杨薏帆 曹邦伟*
(1.首都医科大学附属北京友谊医院肿瘤科,北京100050;2.首都医科大学附属北京友谊医院消化科,北京100050)
胃癌是世界上发病率最高的恶性肿瘤之一,位于全球恶性肿瘤病死率第2位,据统计[1-2]世界上每年大约有7 000 000名患者死于胃癌。近几十年来,虽然胃癌的发病率已经大大减低,但在东欧、南美和亚洲地区,胃癌仍然保持着较高的发病率[3-4]。在胃癌患者的临床诊断与治疗中,大部分患者在就诊时已属于胃癌的晚期,即美国癌症联合委员会(American Joint Committee on Cancer,AJCC)的TNM分期中为Ⅲ(部分)或Ⅳ期的阶段,失去了进行根治性手术的机会,因此全身化疗成为这些患者主要的临床治疗手段。目前胃癌的化疗,尤其对于局部晚期或转移性胃癌患者,尚未有一个统一抑或标准的优化推荐方案。临床较常用的化疗方案是以5-氟尿嘧啶(5 fluorouracil,5-Fu)类药物为基础联合铂类的方案,而其中优化的铂类药物选择为奥沙利铂。最近的临床试验及药物分子机制研究[5]表明,5-Fu的前体药物卡培他滨在胃癌患者中具有较好的疗效,目前已广泛应用于临床。因此本研究拟通过Meta分析,比较卡培他滨联合奥沙利铂(XELOX)与5-Fu联合奥沙利铂(FOLFOXs)2种化疗方案对于胃癌治疗的疗效和安全性,从而为胃癌临床化疗方案的优化选择提供循证医学的证据。
1 材料与方法
1.1 检索策略
在CNKI(http://www.cnki.net/)、万方数据库(http://www.wanfangdata.com.cn/)、维普(http://lib.cqvip.com/)、Pubmed数据库(http://www.ncbi.nlm.nih.gov/pubmed/)中检索2组化疗方案(XELOX与FOLFOXs)治疗中国人群局部晚期或转移性胃癌患者的随机对照试验;语种为中文或英文。中文检索词为氟尿嘧啶、卡培他滨、希罗达、奥沙利铂、胃癌,英文检索 词 为 XELOX、FOLFOXs、5-Fu、5-fluorouracil、capecitabine、xeloda、oxaliplatin、gastric cancer。
1.2 文献检索结果及纳入研究的方法学评价
按照Jadad质量计分法[6]对所纳入的每篇文献逐篇进行方法学质量评估,评价内容包括:各研究中心伦理委员会的批准、受试者知情同意书的签署、方案的设计、盲法水平、随机化方法、对比基线的一致性等方面。对以上每项指标均进行各自评分,0~2分为低质量研究,3~5分为高质量研究。每篇文献均有2名研究员(闫涵、王民)按照上述标准独立提取及评价,所有分歧通过讨论解决,必要时可由第3方裁决。
1.3 纳入、排除标准及干预、评价方法
1.3.1 纳入标准
纳入的文献研究类型均为随机对照试验(randomized controlled trial,RCT),研究对象为经组织病理学检查,并由其他影像学资料证实为局部晚期或转移性中国胃癌患者,组织病理类型均为腺癌。患者年龄18~70岁,预期生存时间≥3个月,ECOG评分≤2或Karnofsky评分≥70,且无其他化疗禁忌证。
1.3.2 排除标准
对于论文报告质量差、重复报告、报道信息少、基本数据不全等无法利用的文献予以剔除;重复发表剔除资料不完整的文献;相似或相同的重复报道文献,只选用最新报道者;同一研究单位重复研究剔除年限久远的文献;样本量较少的文献(N<20)予以剔除。
1.3.1 干预与评价方法
化疗方案应为XELOX与FOLFOXs方案的比较(FOLFOXs可以为FOLFOX4,6,7等)。评价指标为,有效性即总缓解率=完全缓解率(complete remission,CR)+部分缓解率(particial remission,PR)以及中位肿瘤进展时间(time to progression,TTP);毒性反应按照世界卫生组织(World Health Organization,WHO)毒性反应分级标准,取1~4级毒性反应为测量对象。
1.4 统计学方法
采用Review Manager 5.0(http://www.cochrane.org/)和 Stata 10.0软件(Stata Corporation,College Station,Texas)进行统计学分析,首先进行研究的齐性检验,结果若显示各研究的同质性较好,则采用固定效应模型分析(fixed effects model,FEM);若各研究的同质性较差时,则采用随机效应模型分析(random effects model,REM);评价指标采用率的差值(rate difference,RD)及其95%可信区间(confidence interval,CI),绘出荟萃分析森林图,并进行敏感度分析。最后,利用Egger法[7]回归分析评价发表偏倚,并绘制出Egger发表偏倚图,从而更客观地进行发表偏倚评估。
2 结果
2.1 文献筛选及数据资料提取
从最初检索的65篇文献中,通过浏览全文共筛选出18篇RCT文章,按照Jadad质量计分法对18篇文献逐篇进行方法学质量评估,经过进一步的评价后剔除5篇,最终获得符合标准研究13篇。共计783例患者,均为Ⅲ或Ⅳ期中国胃癌患者,其中应用XELOX方案化疗患者398例,应用FOLFOXs方案患者385例。在纳入的13篇文献中,其中6篇未提供中位肿瘤进展时间(time to progression,TTP),为保证本文的严谨性,我们仅选取总缓解率进行安全性评价的标准。每项研究的具体数据详见表1。
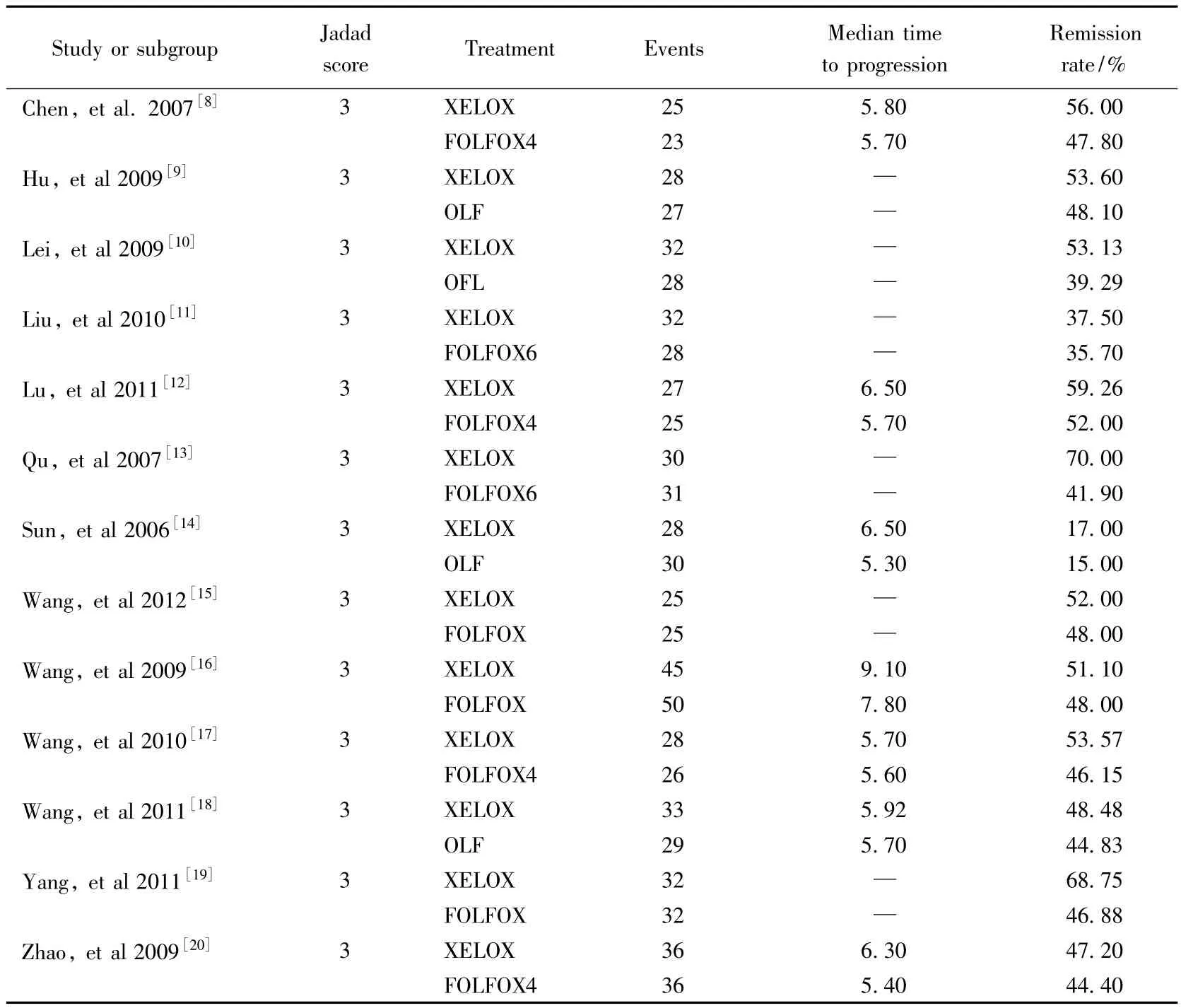
表1 纳入Meta分析总计13项临床研究的RCT数据资料Tab.1 Characteristics of the 13 RCTs included in the Meta-analysis
2.2 2种化疗方案的有效性即缓解率评价
本研究纳入的13篇文献均报道了局部晚期或转移性中国胃癌患者,经过化疗后的完全缓解率、部分缓解率以及有效率等研究数据。首先提取数据资料进行异质性检验(P=0.97),提示这些研究间无异质性,因此采用固定效应模型分析。Review Manager 5.0软件进行统计学分析XELOX组缓解率为53.52%,FOLFOXs组缓解率为45.71%(OR=1.18,95%CI:1.02~1.35)。XELOX方案与FOLFOXs方案化疗的缓解率评价的森林图详见图1。采用Egger's test方法[7],在本文所纳入的13项研究中以各研究的精确度(标准误的倒数)为自变量,标准效应指标[OR/SE(OR)]为应变量进行直线回归,得出Egger偏倚系数为0.015,图2中截距线段横跨0点,且95%的可信区间包含 0(t=0.01,95%CI:-3.772~3.803,P=0.993),故认为无显著性发表偏倚,对最终2种化疗方案缓解率的综合OR值结论无实质性影响,因此结论较可靠。
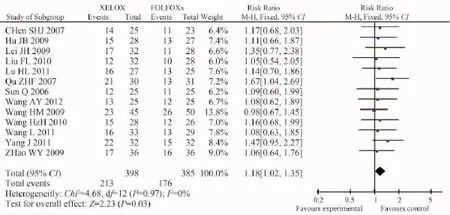
图1 2种化疗方案的缓解率评价Fig.1 Forest plot of the remission between XELOX and FOLFOXs
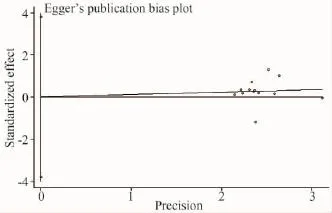
图2 13项病例-对照研究发表偏倚的Egger检验Fig.2 Egger's test of the publication bias between 13 case-control studies
2.3 安全性评价
在本研究纳入的13篇文献报道中,XELOX方案与FOLFOXs方案引起的常见毒性反应包括白细胞减少、贫血、血小板减少、恶心、呕吐、腹泻、手足综合征、周围神经损伤和口腔炎等。对于每种毒性反应,本研究以1~4级不良反应为研究对象,进行荟萃分析,并绘制森林图。结果显示,对于恶心、呕吐以及腹泻这两方面的不良反应,经异质性检验未发现明显偏倚(P=0.45,P=0.23),因此采用固定效应模型分析。使用Review Manager 5.0软件进行统计学分析,结果显示:XELOX方案较之FOLFOXs方案恶心、呕吐及腹泻的发生率明显减低,差异有统计学意义(P=0.010,P=0.006)。而经异质性检验发现2种治疗方案在引起手足综合征方面存在明显偏倚(P=0.003),因此采用随机效应模型分析,结果显示:XELOX组较FOLFOXs组手足综合征发生率明显增高(P=0.006)。最后,对于白细胞减少、贫血、血小板减少、周围神经损伤、口腔炎等不良反应的发生率,差异无统计学意义(P>0.05);详细的不良反应Meta分析数据具体见表2。
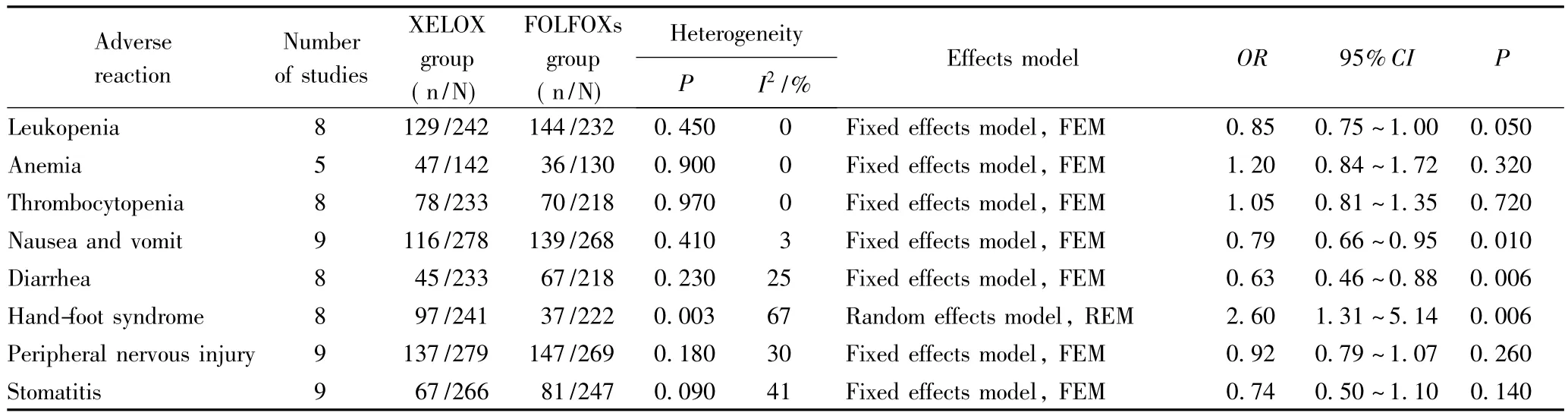
表2 XELOX方案与FOLFOXs方案化疗的不良反应评价Tab.2 Adverse reactions assessment:XELOX and FOLFOXs
3 讨论
5-氟尿嘧啶(5-Fu)一直被认为是治疗消化道肿瘤最有效的化疗药物,也被认为是消化系肿瘤化疗领域的基石,而奥沙利铂是隶属于铂类药物中的第3代铂类化疗药物。因此,奥沙利铂与5-Fu联合使用被认为可以显著提高局部晚期或转移性胃癌患者化疗的有效率。奥沙利铂与其他铂类作用原理相似,均以DNA为作用靶点,铂原子与DNA形成链内和链间交联,最终阻断DNA的合成和修复。与其他铂类相比,奥沙利铂与DNA结合更加紧密,因此相对于其他铂类在消化系肿瘤的化疗中更为有效。有国外学者[21]报道奥沙利铂与顺铂相比,在进展期、且不能手术切除的胃癌化疗中能够明显提高患者的无进展生存期(progression-free survival,PFS)及总生存期(overall survival,OS),并且患者不良反应的发生率较之顺铂组明显减低。
卡培他滨(capecitabine)是一种口服氟尿嘧啶类的前体药物,在胃肠道吸收后经过3个酶催化反应的步骤才能激活,发挥其细胞毒性。卡培他滨转化为氟尿嘧啶的最后步骤需要胸腺嘧啶酸化酶(thymidine phosphorylation enzyme,TP)的催化,而这种酶在肿瘤组织中的含量明显高于正常组织,因此具有针对于肿瘤细胞的靶向选择性。Schuller等[22]报道在大肠癌患者中,口服卡培他滨后癌组织中5-Fu浓度比邻近组织高3.2倍,是血浆中的5-Fu浓度的21.4倍;相比之下,静脉注射5-Fu后,组织或细胞中未发现任何选择性分布[22]。Kang等[23]学者比较了卡培他滨与5-Fu分别联合顺铂两种方案治疗晚期胃癌患者的疗效及安全性;结果显示:含有卡培他滨的方案明显优于氟尿嘧啶方案,两组患者PFS分别为5.6和5.0个月,OS分别为10.5及9.3个月,结果差异均有统计学意义。而本研究Meta分析的结论与之相似,在中国局部晚期或转移性胃癌患者的治疗中,XELOX方案的有效率明显优于FOLFOXs方案,有效率分别为53.52%和45.71%。
另外,严重的毒性反应也是我们在选择联合化疗方案时需要慎重考虑的问题,尤其是对于那些年龄大、PFS评分低的患者。本研究显示XELOX方案较FOLFOXs方案在恶心、呕吐以及腹泻的发生率方面显著减低,而手足综合征的发生率略有增加。Cassidy等[24]报道卡培他滨导致的手足综合征发生率为31%,多于5-Fu组的11%。卡培他滨引起手足综合征的原因目前还不是很清楚,可能和组织中某些基因的变异有关[25]。虽然手足综合征的发生率较高,但大部分患者都是可以通过药物减量、增加辅助用药、以及间断停药等措施后好转[26]。而作为5-Fu替代物的卡培他滨,不需要行中心静脉插管术,避免了由此导致的感染、血栓和其他导管相关风险,因此对于老年和有基础疾病患者,选择卡培他滨获益会更大[27-29]。
总之,本研究结果证实在中国人群中,对于局部晚期或转移性胃癌患者XELOX方案较之FOLFOXs方案的疗效确切,并且不良反应的发生率更低,尤其对于老年患者是一种更为优化的选择。需要指出的是,本研究也存在一定局限性,对于PFS和OS,由于文献报道的均采用中位时间,因此无法进行Meta分析;其次,因为每个研究中的化疗方案药物剂量和应用时间差异有统计学意义,可能会给本文的分析结论带来一定的偏倚。因此提示我们在以后的临床试验研究中,应对于可能会出现的研究偏倚做出缜密的调整。
[1]Krejs G J.Gastric cancer:epidemiology and risk factors[J].Dig Dis,2010,28(4-5):600-603.
[2]Yang D,Hendifar A,Lenz C,et al.Survival of metastatic gastric cancer:Significance of age,sex and race/ethnicity[J].J Gastrointest Oncol,2011,2(2):77-84.
[3]Bretthauer M,Kalager M.Principles,effectiveness and caveats in screening for cancer[J].Br J Surg,2013,100(1):55-65.
[4]朱圣韬,曹邦伟,徐昌青,等.TIM-3基因启动子区多态性与胃癌易感的相关性研究[J].首都医科大学学报,2010,31(3):299-303.
[5]CervantesA,Roda D,Tarazona N,et al.Current questions for the treatment of advanced gastric cancer[J].Cancer Treat Rev,2013,39(1):60-67.
[6]曹邦伟,于晶琳,荷欢,等.中国人群中HPV感染与食管癌发生关联的Meta分析[J].首都医科大学学报,2010,31(2):258-263.
[7]Egger M,Davey Smith G,Schneider M,et al.Bias in meta-analysis detected by a simple,graphical test[J].BMJ,1997,315(7109):629-634.
[8]陈绍俊,黄海欣,李桂生.卡培他滨与氟尿嘧啶/亚叶酸钙联合奥沙利铂治疗晚期胃癌的随机对照临床研究[J]. 中国癌症杂志,2007,17(6):483-486.
[9]胡建兵,文芳,翁洁.XELOX和OLF方案治疗晚期胃癌的随机对照临床研究[J].中国实用医药,2009,4(15):25-26.
[10]雷俊华,洪涛,曾江正,等.XELOX方案治疗进展期胃癌临床观察[J].华北国防医药,2009,21(4):10-12.
[11]刘风玲,郑毅琳.奥沙利铂联合卡培他滨或氟脲嘧啶/叶酸方案治疗晚期胃癌的临床疗效比较[J].实用临床医药杂志,2010,14(23):50-51.
[12]陆海林,李燕,宁志强,等.XELOX与FOLFOX4方案治疗晚期胃癌疗效观察[J].实用临床医药杂志,2011,15(19):112-113.
[13]曲智锋,冯笑山,高社干,等.奥沙利铂联合卡培他滨治疗晚期胃癌临床疗效观察[J].福建医药杂志,2007,29(4):41-43.
[14]孙清,毛永杰,赵伟,等.卡培他滨联合奥沙利铂治疗晚期胃癌的随机对照临床研究[J].肿瘤防治研究,2005,32(11):729-730.
[15]王爱英,张毛讲.卡培他滨联合奥沙利铂治疗晚期胃癌的临床观察[J].中国医药导报,2012,9(6):58-59.
[16]王红民,程先鸣,张明莉.奥沙利铂加卡培他滨治疗晚期胃癌的疗效观察[J].中国医院用药评价与分析,2009,9(11):856-857.
[17]王海忠,王湘辉,吕志诚.XELOX与FOLFOX4方案治疗进展期胃癌的随机对照临床研究[J].现代肿瘤医学,2010,18(15):947-950.
[18]王磊,胡冰,季楚舒,等.XELOX与FLO方案治疗晚期胃癌的近期疗效及毒副反应比较[J].安徽医药,2011,15(3):329-330.
[19]杨晶.卡培他滨联合奥沙利铂在晚期胃癌中的临床效果研究[J].实用心脑肺血管病杂志,2011,19(3):369-370.
[20]赵文英,吉兆宁.XELOX或FOLFOX4方案治疗晚期胃癌的随机对照分析[J].中国肿瘤临床,2009,36(18):1044-1046.
[21]Francesco M,Gina T,Claudio M,et al.Effectiveness and safety of oxaliplatin compared to cisplatin for advanced,unresectable gastric cancer:a systematic review and meta-analysis[J].Gastric Cancer,2011,14(1):50-55.
[22]Hirsch B R,Zafar S Y.Capecitabine in the management of colorectal cancer[J].Cancer Manag Res,2011,3:79-89.
[23]Kang Y K,Kang W K,Shin D B,et al.Capecitabine/cisplatin versus 5-fluorouracil/cisplatin as first-line therapy in patients with advanced gastric cancer:a randomised phase Ⅲ noninferiority trial[J].Ann Oncol,2009,20(4):666-673.
[24]Cassidy J,Clarke S,Díaz-Rubio E,et al.XELOX vs FOLFOX-4 as first-line therapy for metastatic colorectal cancer:NO16966 updated results[J].Br J Cancer,2011,105(1):58-64.
[25]Caronia D,Martin M,Sastre J,et al.A polymorphism in the cytidine deaminase promoter predicts severe capecitabine-induced hand-foot syndrome[J].Clin Cancer Res,2011,17(7):2006-2013.
[26]Azuma Y,Hata K,Sai K,et al.Significant association between hand-foot syndrome and efficacy of capecitabine in patients with metastatic breast cancer[J].Biol Pharm Bull,2012,35(5):717-724.
[27]肖作珍,肖瑞,姜继臣.奥沙利铂联合表柔比星和5-Fu治疗多发转移性胃癌的临床观察[J].中华肿瘤防治杂志,2010,17(12):946-947.
[28]严冬,戴红.恩度联合XELOX方案一线治疗老年晚期结直肠癌的临床观察[J].中华肿瘤防治杂志,2011,18(12):961-964.
[29]柴慈婧,王骏飞,李罡,等.卡培他滨治疗老年晚期消化道肿瘤的临床观察[J].中华肿瘤防治杂志,2010,17(19):1571-1572,1575.
