核桃油微乳液的制备及抗氧化活性研究
2013-08-29刘峰催莉耿岩玲王晓刘建华
刘峰,催莉,耿岩玲,王晓,刘建华
(山东省分析测试中心,山东 济南 250014)
核桃油为黄色或淡黄色油脂,不饱和脂肪酸含量高达90%以上[1],其中以油酸、亚油酸、亚麻酸为主,是一种高级营养保健油。研究发现核桃油具有降血脂、降低心血管疾病发病风险[2],改善记忆力[3],延缓衰老、清除自由基[4],抗肿瘤[5]等生理活性。由于核桃油中不饱和脂肪酸含量较高,产品极易被氧化,同时,核桃油不溶于水,限制了其在食品工业中的应用。为克服上述不足,制备核桃油微胶囊是目前的主要手段[6-7],但这些方法存在操作复杂,水溶液不稳定等缺点,因此,开发工艺简单、水介质中稳定的核桃油包封制剂,对于扩展核桃油应用领域有重要意义。
微乳液是透明或半透明的热力学稳定体系,能增溶脂溶性或水溶性物质[8]。该体系在食品、日用化工、化妆品以及石油工业等[9-12]方面有着广泛的应用。以表面活性剂为稳定剂,制备核桃油微乳液还未见报道。
本文在原有亚麻酸微乳液研究的基础上,以乙酸异戊酯为核桃油油相溶剂,选择Tween 80 和EL-35 为表面活性剂,采用拟三元相图法制备了稳定的核桃油微乳液体系,研究了体系的相行为、热稳定性、微乳液粒径和流变特性,并通过化学发光法测定了微乳液体系的抗氧化活性。
1 材料与方法
1.1 药品与仪器
核桃油,购自济南市历城区三川果品苗木专业合作社;聚氧乙烯山梨醇酐单油酸酯(Tween80)、蓖麻油聚氧乙烯(35)醚(EL-35),化学纯(BASF Co.);鲁米诺,邻苯三酚,Na2CO3,NaHCO3,浓盐酸,分析纯(中国医药集团上海化学试剂公司);水为二次蒸馏水。
ALV5000 动态光散射仪(Malvern Co.,德国);AR2000EX 流变仪(TA Co.,美国);MPI-B 型多参数化学发光分析测试系统(西安瑞迈分析仪器有限公司);DDS-II C 型数显电导率仪(上海天达仪器有限公司)。
1.2 拟三元相图的绘制
将核桃油与乙酸异戊酯按照质量比1:1 配制成混合油相。清洁干燥的试管中,按照一定比例称取定量的Tween 80,EL-35 为表面活性剂,混合油相,表面活性剂与油相的质量比由10:0 逐渐变化到0:10,室温下搅拌30 min,使其混合均匀。然后在搅拌下逐滴加水,观察并记录相态变化。记录出现相变时的水含量,在相图中标出相应的点,连接成曲线即得到相图。
1.3 电导率测量
先配制一定比例的表面活性剂相和油相的混合物(7:3,8:2,9:1),在25 ±1℃恒温条件下搅拌均匀,逐滴加水,每次滴加后,充分搅拌约5 min 再读数,作出电导率随加水量变化曲线。
1.4 粒径及分散度测量
微乳液粒径及多分散度是考察体系稳定性及均一性的重要参数。通过测定不同浓度核桃油微乳液的粒径,考察核桃油含量对体系的影响。
1.5 流变性质测量
在相图中选择样品点,配置样品后,密封恒温放置一周。在应力控制流变仪上进行流变性能测试。锥板直径为40 mm,锥角为2°,板间距0.05 mm,测量温度为25.0 (±0.1)℃。刮去椎板周围挤出样品(避免边缘效应)后,开始测量。稳态剪切实验采用CR 模式。
1.6 O2- 清除率的测定
本实验采用鲁米诺-邻苯三酚化学发光体系,以未添加核桃油的微乳液为空白,测定不同浓度的核桃油微乳液对O2-的清除率。以0.1 mol/L,pH 值10.2 的Na2CO3-NaHCO3缓冲溶液配制0.2 mmol/L 鲁米诺溶液;采用10 mmol/L 的HCl 溶液配制10 mmol/L 邻苯三酚溶液。在样品池中依次加入鲁米诺溶液4 mL、样品(或空白)溶液0.2 mL、邻苯三酚溶液0.4 mL,记录其在400 s 内的发光强度,以曲线积分面积表示相对发光强度,清除率计算公式如下:
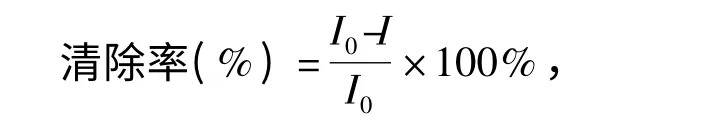
其中,I0、I 分别为空白和核桃油微乳液样品的相对发光强度。计算清除率在50%时的核桃油浓度IC50。
2 结果与讨论
2.1 核桃油微乳液相图
图1 是核桃油微乳液体系的拟三元相图,其中,EL-35 与Tween 80 质量比为8:2,核桃油与乙酸异戊酯质量比为1:1。相图内可得到5 个相区:其中2Φ 相为乳状液;L2相为W/O 微乳液;LC 为液晶相;B.C.为双连续相;O/W 相为O/W 微乳液,油相最大增溶量为9%。各相区的区分由电导率法和偏光显微镜法测得。
2.2 电导率法区分微乳液类型
电导率法是划分微乳液类型的一个常用方法[13]。图2 为油相与表面活性剂相质量比2:8 时,体系电导率随水的质量分数增加的变化曲线。由于水在质量分数58% (b 点)之前体系为液晶相(由偏光显微镜观察判断),因此,电导率测量由水的质量分数为58%时开始。随着体系中水的质量分数的增加,电导率开始是非线性较缓慢的增加,这说明体系处于双连续微乳结构(B.C.),当水质量分数达到73%(c 点)时,溶液的电导率达到最大值。随着含水量的继续增大,电导率下降,此时双连续微乳结构已全部转变为小的油滴分散至水介质中,形成O/W 型微乳液。含水量的增大使得微乳液滴的浓度降低,致使电导率下降。
同样方法,测得其余油相与表面活性剂相质量比的电导率变化,判断体系B.C.与O/W 相,相区划分如图1 所示。
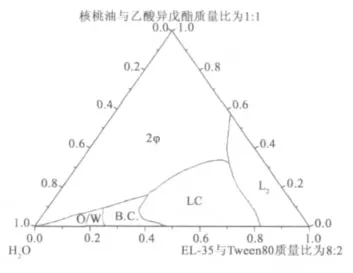
图1 核桃油微乳液体系的拟三元相图Fig.1 Pseudo-ternary phase diagram of a walnut oli microemulsion system
2.3 温度对微乳液的影响
随着温度的变化,微乳液可能会发生相转变,因此测量体系在不同温度下的稳定性,对微乳液体系的应用、储藏有重要意义。微乳液样品(B、C、D 各组分含量见表1)电导率随温度的变化,如图3 所示。微乳液中导电粒子为O/W 型微乳液,温度升高,微乳球之间的碰撞变频繁,电导率上升。在实验温度范围内,微乳液体系澄清透明,无混浊生成,电导率基本呈线形上升,说明在此温度范围内,微乳液类型保持不变。一般货品应用、储藏温度不会高于60℃,因此,该微乳液样品在储藏温度范围内不会发生相转变。

2.4 O/W 微乳液的粒径及稳定性
固定表面活性剂相(Saa)与水相的质量比,考察体系O/W 微乳液的粒径(Rh)及多分散度(PDI)随油相加入的变化,通过动态光散射的方法进行了表征,结果见表1。


表1 不同油相含量的微乳液粒径及多分散度Table 1 Mean hydrodynamic diameter(Rh)and polydispersity index (PDI)of O/W microemulsions of different oil contents
如表1 所示,微乳液的粒径随油相的增加而明显增大。这是因为样品A 中无油相,仅仅是表面活性剂的胶束溶液,随着油相的加入,表面活性剂单分子层变松,曲率变小,油相进入胶束内核或栅栏层,形成O/W 型微乳液,从而使粒径增大。同时,微乳液体系多分散度也随着油相的加入而增大,说明体系混乱度增加,在自发体系中,有的微乳液包封了较多油相,而有的则包封较少,致使粒径分布不均。
2.5 微乳液流变特性
流变学的研究有助于了解溶液、溶胶等流体类型,对微乳液的应用有重要意义。图4(a)是微乳液样品B、C、D 表观粘度(η)在不同剪切速率(˙γ)下的变化曲线,样品粘度表现为剪切变稀行为。中等剪切速率下,微乳液的流动曲线可用Ostwald de Waele 模型[14](幂律模型):
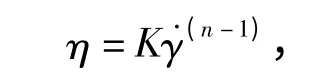
式中K 为稠度系数,n 为流体特性指标,表示与牛顿流体偏离的程度,n=1 时为牛顿流体,n <1 时为拟塑性流体。
对上述公式两边取对数,可得:

图4 微乳液粘度随剪切速率的变化Fig.4 Variation of microemulsion viscosity with the shear rate

表2 微乳液幂律模型中的n,K 值Table 2 n and K values for microemulsion samples
图4(b)为微乳液lg η 随lg ˙γ 的变化曲线,将数据进行线性拟合,可求得K,n 值,结果见表2。样品中n都小于1,说明体系属于拟塑性流体,剪切过程,可使流体组织排列更加有序,有利于延长或改善功能因子或药物的缓释时间。
2.6 核桃油微乳液对O2- 的清除作用
如图5(a)所示,核桃油在微乳液体系内对O-2有明显的清除作用,清除率随核桃油浓度的增加而增大,当核桃油浓度为0.506 mg/mL时,清除率达到82.54%。同时,在微乳液体系中O-2清除率与核桃油的浓度在一定范围内(0.010~0.169 mg/mL)成线性关系,如图5(b)。在此浓度范围内对清除率进行线性拟合,得回归方程y=19.360 +339.273x (R2=0.989),IC50值为0.090 3 mg/mL。
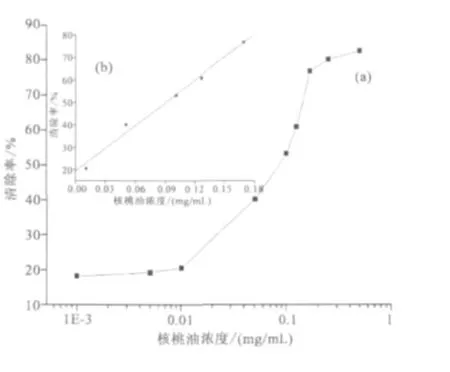
图5 核桃油微乳液对O2-的清除作用Fig.5 Scavenging activity of walnut oil microemulsion on superoxide anion
3 结论
通过拟三元相图法,在无助表面活性剂的条件下,制备了核桃油O/W型微乳液。结果显示,该微乳液具有良好的热稳定性;微乳液粒径随核桃油含量的增加而增大;稳态剪切扫描显示,微乳液剪切变稀,为拟塑性流体;核桃油在微乳液内对O-2有较强的清除作用。本研究为核桃油功能性制剂的进一步研究和开发打下了良好的基础。
[1]刘大群,郜海燕,房祥军,等.核桃油的超临界CO2流体萃取及其脂肪酸成分分析[J].中国粮油学报,2012,27(9):49-52.
[3]王鸿飞,徐超,周明亮,等.山核桃油改善小鼠记忆功能的研究[J].中国粮油学报,2012,27(7):63 -66.
[4]陈默然,沈楠,雷钧涛,等.野生山核桃油对去卵巢大鼠抗氧化能力与海马细胞凋亡的影响[J].食品科学,2011,32(9):272 -275.
[5]ROSE D P,CONNOLLY J M.Omega-3 fatty acids as cancer chemopreventive agents[J].Pharmacology & therapeutics,1999,83(3):217 -244.
[6]王顺民,薛正莲,余建斌.山核桃油微胶囊技术研究[J].食品工业科技,2012,33(1):268 -274.
[7]王文琼,包怡红,王芳,等.复凝聚法制备山核桃油微胶囊的研究[J].食品工业科技,2013,34(3):209 -214.
[8]PAPADIMITRIOU V,SOTIROUDIS T G,XENAKIS A.Olive oil microemulsions:enzymatic activities and structural characteristics[J].Langmuir,2007,23(4):2071 -2077.
[9]BUHLER E,APPELL J,PORTE G.Loose complexation of weakly charged microemulsion droplets and a polyelectrolyte[J].The Journal of Physical Chemistry B,2006,110(12):6415 -6422.
[10]CAMPBELL C J,NJUE C K,NUTHAKKI B,et al.Influence of thickness on catalytic efficiency of cobalt corrin-polyion scaffolds on electrodes in microemulsions[J].Langmuir,2001,17(11):3447 -3453.
[11]ZHANG H,FENG F Q,FU X W,et al.Antimicrobial effect of food-grade GML microemulsions against Staphylococcus aureus[J].European Food Research and Technology,2007,226(1/2):281 -286.
[12]GARTI N.Microemulsions as microreactors for food applications[J].Current opinion in colloid & interface science,2003,8(2):197 -211.
[13]WANG J L,WANG Z W,LIU F,et al.Preparation and in vitro release test of insulin loaded W/O microemulsion[J].Journal of Dispersion Science and Technology,2008,29(5):756 -762.
[14]MENG W,WU L,CHEN D,et al.Ambient self-crosslinkable acrylic microemulsion in the presence of reactive surfactants[J].Iranian Polymer Journal,2008,17(7):555 -564.
