河南省周口地区瓜类白粉病的分子鉴定与分析
2013-08-29徐克东陈佩佩段素娟乔月娥李成伟
张 怡,徐克东,陈佩佩,段素娟,孟 娉,乔月娥,李成伟
(周口师范学院 植物遗传与分子育种重点实验室,河南 周口 466000)
瓜类白粉病是一种世界性病害,在中国每年都因此病害造成大量减产[1].单囊壳白粉菌(Sphaerothecafuliginea)和二孢白粉菌(Erysiphecichoracearum)是瓜类蔬菜白粉病的主要病原菌[2],前者比后者更为常见[3-4].瓜类白粉病在我国各地的保护地和露地各种瓜类上普遍发生.黄瓜、葫芦、甜瓜、南瓜受害较重,冬瓜和西瓜次之,丝瓜抗病性较强.此病一旦发生,扩展蔓延很快,给生产造成巨大损失,一般年份减产10%左右,流行年份减产高达20%~40%.
传统方法通常利用病菌的显微形态对真菌进行小种鉴定和分析.随着分子技术的发展,rDNA序列非转录区的核糖体DNA 转录间隔区序列(internal transcribed spacer,ITS)被广泛应用于真菌小种及进化程度的研究.真菌核糖体基因是由18S、ITS1、5.8S、ITS2 和28S 头尾串联构成的重复序列.18S、5.8S和28SrDNA 属于转录区,与它们相比较,ITS1和ITS2作为非编码区承受的进化选择压力小,相对变化较大,在种间表现出较高的差异,具有广泛的保守性和特异性,设计特异性引物克隆该序列用于植物病原菌的鉴定、检测、病害诊断及防御等,已成为国际上广泛使用的分子生物学方法[5-7].
鉴此针对在河南周口市发现大面积的瓜类白粉病菌,对其进行显微形态学观察、ITS序列鉴定、进化树分析,为瓜类白粉病菌的鉴定分类、系统进化和防治奠定理论基础.
1 材料与试剂
1.1 试验材料
黄瓜、甜瓜、葫芦、南瓜白粉病病菌植株均取自周口师范学院校园.
1.2 主要试剂及仪器
2xTaq Master Mix 购自北京康为世纪生物科技有限公司,琼脂糖凝胶回收试剂盒购自北京索莱宝生物科技有限公司,标准的分子量Marker购自东盛生物科技有限公司,其它试剂均为国产试剂.
2%CTAB抽提液:100 mmol Tris-HCl(pH 8.0),20 mmol EDTA(pH 8.0),1.5 mol NaCl,2%CTAB(W/V),4%PVP40(W/V),高压灭菌,使用前加入2%β-巯基乙醇(V/V);10%CTAB抽提液:100 mmol Tris-HCl(pH 8.0),20 mmol EDTA(pH 8.0),1.5 mol NaCl,10%CTAB(W/V),4%PVP40(W/V),高压灭菌,使用前加入2%β-巯基乙醇(V/V);二氨基联苯胺(Diaminobenzidine,DAB)染色液(1 mg/mL ):溶解100mgDAB于100mL水中(pH3.8);固定液(无水乙醇:冰乙酸=3∶1);台盼兰染液:用0.85%的生理盐水配制成0.3%的台盼兰染液;水合三氯乙醛(2.5g/mL):溶解250g 三氯乙醛于100mL水中.
扫描电子显微镜为FEI公司的Quanta 200型产品,PCR 仪为Biometra公司T1型产品.
2 试验方法
2.1 白粉病菌的形态观察
2.1.1 显微形态观察 对染病叶片的菌落颜色、大小、形状进行普通观察,以及使用DAB 和台盼兰染色的方法进行显微镜观察[8].
2.1.2 纤维状体的观察 取白粉病菌无性世代分生孢子于载玻片上,加1滴3%的KOH 溶液,盖上盖玻片,在10×40倍显微镜下观察分生孢子上是否有纤维状体[9].
2.1.3 扫描电镜观察 剪取1.0×1.0cm2大小的叶片,经真空镀金后,在Quanta 200 型扫描电子显微镜的高真空环境下进行观察,参数设置如下:预设驻留时间为10μs,灯丝电压为20.00KV.
2.2 病原菌的致病性检测
从感染叶片上采集新鲜孢子,采用分生孢子悬浮液分别对黄瓜、甜瓜、葫芦和南瓜叶片进行接种,并以清水接种作为对照,培养约5d后,观察记录发病症状与自然发病症状进行比较,并从叶片上再次分离病原菌,比较它们与自然发病分离出的病原菌的异同.
2.3 白粉病菌总DNA的提取、ITSrDNA序列的PCR扩增
2.3.1 黄瓜、甜瓜、葫芦和南瓜白粉病菌总DNA 的提取 采用改良的真菌DNA 提取方法提取白粉病菌的DNA[8].
2.3.2 PCR 扩增及测序 本实验的PCR 体系(20 μL体系):ITS序列采用真菌核糖体区段通用引物ITS1(5’-TCCGTAGGTGAACCTGCGG-3’)和ITS4(5’-TCCTCCGCTTATTGATATGC-3’).4种白粉病菌ITS扩增体系均为:DNA 模板2μL,ITS1 2μL,ITS4 2μL,Mix 10μL,ddH2O 4μl.PCR 反应条件:预变性94℃,5 min;变性94℃,30s,退火48℃,45s,延伸72℃,45s,35个循环;再延伸72℃,5min.
取6μL PCR 产物电泳,进行1.2%琼脂糖凝胶电泳,溴化乙锭染色,在凝胶成像系统下检测结果.将所得到的目的条带经PCR 产物纯化试剂盒纯化后,送至南京金斯瑞生物科技有限公司进行测序.
2.4 ITS序列比对和系统发育分析
在NCBI的GenBank中对本研究的ITS序列和其他同源序列进行比对分析其同源性,采用Clustal X 1.83)软件中的Alignment程序对获得的所有序列进行划分、多重对位排列(Multiple alignments).采用MEGA 5.02软件做近邻归群法分析,用自展法(Bootstrap)对所构建的系统发育树进行检测,自展重复次数设定为1 000次>40%的支持强度,对其进行系统发育分析和进化树的构建.
3 试验结果
3.1 白粉病菌的显微形态观察
经DAB和台盼兰染色在显微镜下观察,发现4种瓜类白粉病的分生孢子均呈椭圆形,大小为25.64×15.64~29.36×19.23(μm)(图1,A),串生在分生孢子梗上(图1,B),但分生孢子梗上的分生孢子数目有所差异,大约有4~12 个分生孢子(表1).在40倍显微镜下用3%的KOH 观察到4种瓜类白粉病的分生孢子内均有发达的纤维状体(图1,C).初级芽管均从分生孢子侧端萌发(图1,D),但发现黄瓜白粉病菌也有从顶端萌发的现象(图1,E).4种瓜类白粉病子囊数均为1,且有8个子囊孢子.

表1 4种瓜类白粉病菌显微形态比较Tab.1 Comparative analysis of morphology of four cucurbits powdery mildew pathogen

图1 瓜类白粉病菌的显微形态Fig.1 Morphology of cucurbits powdery mildew pathogen
3.2 病原菌的致病性检测
采用分生孢子悬浮液对黄瓜、甜瓜、葫芦和南瓜叶片进行再接种,观察发现,发病初期叶片产生白色近圆形的小粉斑,后逐渐扩大成连片白粉斑,形似撒上一层白粉状物,即病原菌的菌丝体、分生孢子梗和分生孢子.严重时,白粉布满整个叶片,随后白色粉状物渐变为灰白色或灰褐色(图2).病状的发展与自然发病病斑形态相同,而对照组未产生任何症状.取接种后产生的病斑进行显微观察,结果表明与接种病菌相同,证实原接种菌为白粉病菌.

图2 瓜类白粉病菌的症状特征Fig.2 The symptom characteristics of cucurbits powdery mildew pathogen
3.3 白粉病菌DNA 的提取
利用改良的真菌DNA 提取方法提取瓜类白粉病菌的DNA,经分光光度计检测总DNA 的质量,A260/280比值均在1.8左右,0.8%琼脂糖凝胶电泳检测结果显示有两条带,且条带中间有拖尾现象,表明所提取的真菌DNA 有部分降解,理论上可作为模板用于PCR 扩增(图3).
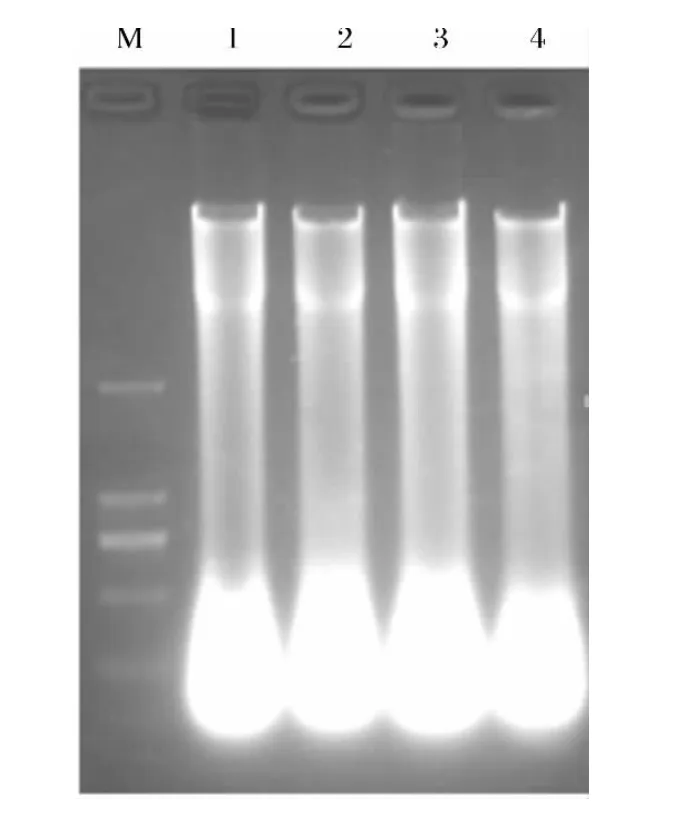
图3 瓜类白粉病菌总基因组DNA 的电泳图Fig.3 Electrophoretic gel image of genomic DNA from cucurbits powdery mildew pathogen
3.4 ITS序列的扩增及分析
本研究采用真菌核糖体ITS区通用引物ITS1和ITS4为引物,分别以黄瓜、甜瓜、葫芦、南瓜白粉病菌DNA 为模板,PCR 扩增瓜类白粉病菌核糖体基因的ITS区,经35个循环后得到500bp左右的目的片段(图4).

图4 瓜类白粉病菌的ITS扩增电泳图Fig.4 Electrophoretic gel image of amplified ITS products in cucurbits powdery mildew pathogen
经过PCR 产物测序得到黄瓜、葫芦、甜瓜、南瓜白粉病菌ITS序列,大小分别为558bp、561bp、563bp、514bp(图5),并做出4种瓜类白粉病菌的系统发育树(图6).将序列上传至NCBI中的Genbank数据库,得到了4种瓜类白粉病菌ITS序列的登录号,与其他同源序列比对后对其进行分析(表2).

图5 4种瓜类白粉病菌的ITS核苷酸序列同源性比较Fig.5 Sequence alignment of the four cucurbits powdery mildew ITS regions

图6 4种瓜类白粉病菌系统发育树Fig.6 The phylogenetic tree of cucurbits powdery mildew
3.5 系统发育树的构建

图7 根据ITS序列构建的瓜类白粉病菌系统进化树Fig.7 Neighbor-joining consensus tree of cucurbits powdery mildew pathogen based on ITS sequence data
将4 种瓜类白粉病菌ITS 序列在NCBI的Blast数据库上比对,搜索同源性较高的序列,聚类分析后发现这些序列明显分为两个亚支,周口地区的黄瓜、甜瓜、葫芦、南瓜白粉病聚在一个进化亚支上,说明4种白粉病菌具有很高的亲缘关系,并且它们与日本美女樱白粉病菌(登录号为AB046985)、英国水母柱树白粉病菌(登录号为GQ390796)同源性均高达100%,同时又与中国商丘豆角白粉病菌(登录号为GQ927253)、中国哈尔滨甜瓜白粉病菌(登录号为EU294368)、美洲南瓜白粉病菌(登录号为AF011321)、澳大利亚豇豆白粉病菌(登录号为AY450961)、日本橹豆白粉病菌(登录号为AB040305)亲缘关系较近,序列保守性较强,聚在同一亚支上.
4 讨论与分析
据文献报道,近几年来白粉病在国内外发病范围不断扩大,不仅在瓜类上发现白粉病菌,在其他蔬菜类(番茄[10])、粮食作物(小麦[11])和景观植物(大叶黄杨[12]、月季[13])上也有白粉病的发生.
本研究首先对周口地区黄瓜、甜瓜、葫芦和南瓜白粉病菌进行显微形态学观察分析,通过对其分生孢子形状及着生方式,纤维状体的有无,初级芽管萌发方式的观察,初步认定4种瓜类白粉病菌属于单囊壳白粉病菌S.fuliginea.
在观察白粉病菌时,笔者发现一些与文献描述有所差异的现象,第一,有文献[14]描述纤维状体的形状为盘状和新月形,而本研究发现还有棒状的纤维状体(图1,C),推测可能是由于显微镜镜深的不同引起这种差异.第二,观察发现分生孢子梗上的分生孢子数目一般为4~12个,而一些文献[11]所提到的分生孢子梗上仅有1~3个分生孢子,可能是由地域差异造成的.第三,S.fuliginea分生孢子的初级芽管从分生孢子侧面萌发长出,而笔者却观察到黄瓜白粉病菌有从侧面和顶端萌发的现象(图1,E),具体原因还有待进一步研究.第四,黄瓜、甜瓜、南瓜白粉病菌的子囊果形态为常见的扁球形,而葫芦白粉病菌子囊果为罕见的长梭形(图1,F),推断可能与其小种间进化有关.
目前国内外对主要利用28SrDNA 和ITS rDNA序列对瓜类白粉病菌进行分子鉴定[15],本研究通过对河南周口市的4种瓜类白粉病菌的ITS序列及进化树分析发现,其一,哈尔滨甜瓜白粉病菌、美洲南瓜白粉病菌、商丘豆角白粉病菌、澳大利亚豇豆白粉病菌、日本黑豆白粉病菌与周口地区4种瓜类白粉病菌均聚在一支.另外,本实验室也对豆类白粉病菌进行了研究,比对发现:周口地区的瓜类白粉病菌和豆类白粉病菌同源性超过97%(未发表),由此推测瓜类白粉病与豆类白粉病在进化上差异极小,保守性很强.其二,周口甜瓜白粉病菌与哈尔滨甜瓜白粉病菌同源性为93%,说明瓜类白粉病菌的进化跟地域的远近有一定的关系,地域的差异导致了小种进化出现一定的变异.其三,4种瓜类白粉病菌与日本美女樱白粉病菌和英国水母柱树白粉病菌同源性均高达100%,而美女樱是一年生的草本花卉,水母柱树是一种常绿小乔木,3种宿主之间的亲缘关系较远,但是白粉病菌同源性却极高,说明该白粉病菌的进化较慢,不同宿主间的白粉病菌差异较小.
由于传统的瓜类白粉病的防治主要依靠农药等杀菌剂,对环境造成了严重的污染,因此,学者开始对生防菌和植物源农药进行研究,发现在黄瓜叶片喷施一定浓度的硅酸盐、碳酸盐、磷酸盐或橄榄油能均有效抑制黄瓜白粉病菌的发生,减少了传统农药防治对环境的污染,并减少由此带来的经济上的花费[16-17];另外,有学者[18]发现用低聚壳聚糖处理感染白粉病菌的黄瓜叶片也可显著减少白粉病菌的发展.除此之外,着重加强分子生物技术和细胞生物技术在瓜类白粉病抗性育种工作中的应用,以及抗白粉病分子机制的研究,可加快瓜类白粉病抗病育种工作的进程.国外对瓜类白粉病菌的鉴定工作起步较早,在对甜瓜白粉病菌生理小种鉴定方面的研究,日本一直处于领先水平,他们对小种的种类、致病性以及分布都做了全面细致的研究[19-20],而且已经选育出了许多抗白粉病菌小种的品种.
本研究通过对无性孢子纤维状、芽管萌发方式及子囊果和子囊孢子的观察,明确了河南省周口地区瓜类白粉病的病原菌为S.fuliginea,为河南省瓜类白粉病菌生理小种、抗性遗传的研究奠定了基础.
[1]刘秀波,崔 琦,崔崇士.瓜类白粉病抗性育种研究进展[J].东北农业大学学报,2005,36(6):794-798.
[2]Davis A R,Thomas C E,Levi A,et al.Watermelon resistance to powdery mildew race 1[C]∥Cucurbitaceae,Alexandria Virginia:ASHS Press,2002:192-198.
[3]董金皋.农业植物病理学[M].北京:中国农业出版社,2001:411-413.
[4]Thomas C E.Physiological specialization in downy and powdery mildews cucurbits[C]∥Cucurbitaceae 88:Proceedings of the EUC-ARPIA meeting on cucurbits genetics and breeding Avignon,France,1988.
[5]刘春来,文景芝,杨明秀,等.rDNA-ITS在植物病原真菌分子鉴定中的应用[J].东北农业大学学报,2007,38(1):101-106.
[6]White T J,Bruns T,Lee S.Analysis of phylogenetic relationships by amplification and direct sequencing of ribosomal RNA genes[C]∥Innis M A.PCR Protocols:A Guide toMethodsand Applications.New York:Academic,1990:15-22.
[7]陈剑山,郑服丛.ITS序列分析在真菌分类鉴定中的应用[J].安徽农业科学,2007,35(13):3785-3786.
[8]张 怡,张佩佩,马晓萌,等.河南两地市小麦白粉病菌的分子鉴定和进化分析[J].华北农学报,2012,27(1):189-192.
[9]马鸿艳,魏尊苗,祖元刚,等.2009-2010年黑龙江省主要瓜类作物白粉病菌生理小种鉴定[J].植物保护学报,2011,38(3):287-288.
[10]Li C W,Pei D L,Wang W J,et a1.First report of powdery mildew caused by Oidium neolycopersici on tomato in China[J].Plant Disease,2008,92(9):1370-1370.
[11]涂 坦.四川省小麦白粉病抗药性测定及其机理的初探[D].雅安:四川农业大学,2010.
[12]Li C W,Zhang Y,Liu Y,et al.First report of powdery mildew caused by erysiphe euonymi-japonici on euonymus japonicus in central China[J].Plant Disease,2011,95(5):611-611.
[13]张喜萍,郭玉莲,许修宏.月季白粉病发生规律及初侵染来源初探[J].东北农业大学学报,2003,34(2):231-233.
[14]张艳菊,左洪波,曲 丽,等.黑龙江省黄瓜白粉病病原鉴定[J].东北农业大学学报,2010,41(4):20-23.
[15]Hyang Burm Lee.Molecular phylogenetic status of korean strain of Podosphaera xanthii,a causal pathogen of powdery mildew on Japanese thistle(Cirsium japonicum)in Korea[J].Journal of Microbiology,2012,50(6):1075-1080.
[16]Deliopoulos T,Kettlewell P S,Hare M C.Inorganic salts for suppressing powdery mildew in cucurbits--a worldwide survey[J].Commun Agric Appl Biol Sci,2008,73(2):51-56.
[17]Raymundo P Á,Raymundo Saúl García-Estrada,JoséArmando Carrillo-Fasio,et al.Powdery mildew(Sphaerotheca fuliginea schlechtend:Fr,Pollaci)control with vegetable oils and mineral salts on cucumber growing in greenhouse in Sinaloa,México[J].Revista Mexicana de Fitopatologia,2010,28(1):17-24.
[18]Qing Ma,Xiao-Ming Zhao,Hui Sun,et al.Ultrastructural study on induced resistance of cucumber plants against sphaerotheca fuliginea by Oligochitosan[J].Plant Pathol J,2011,27(1):8-13.
[19]Hosoya K,Narisawa K,Pitrat M,et al.Race identification in powdery mildew(Sphaerotheca fuliginea)on melon(Cucumis melo)in Japan[J].Plant Breeding,1999,118(3):259-262.
[20]Kuzuya M,Hosoya K,Yashiro K,et al.Powdery mildew(Sphaerotheca fuliginea)resistance in melon is selectable at the haploid level[J].J of Exp Bot,2003,54(384):1069-1074.
