高效液相色谱法单波长切换测定复方氯霉素醇溶液中水杨酸、氯霉素的含量
2013-08-28张瑞麟王逢春
王 敏,张瑞麟,王逢春,李 胜
复方氯霉素醇溶液是一种外用复方制剂,收载于2002年版的《中国人民解放军医疗机构制剂规范,》(以下简称《规范》)[1],由水杨酸、氯霉素和75%乙醇配制而成,用于治疗脂溢性皮炎、皮疹、瘙痒等。《规范》中采用中和滴定法和高效液相色谱法分别测定溶液中水杨酸和氯霉素的含量,但在实际工作中发现测定所需时间较长,造成生产效率较低。目前,陆续有研究者报道采用高效液相色谱法测定氯霉素醇中水杨酸和氯霉素的含量,但方法有一定的局限性,无法用于配备单波长的紫外检测器的高效液相色谱仪[2-8]。本文采用单波长切换的高效液相色谱法测定复方氯霉素醇溶液中水杨酸和氯霉素的含量,较已报道的方法更加简便、快捷,准确度高,能更有效地控制复方氯霉素醇溶液的质量。
1 仪器与试药
1.1 仪器 Agilent 1200 型高效液相色谱仪(包括四元泵、VWD 检测器、自动进样器、ChemStation 化学工作站);Mettler AE240 电子天平(梅特勒公司)。
1.2 试药 水杨酸对照品(中国食品药品检定研究院,批号:100106-200303);氯霉素对照品(中国食品药品检定研究院,批号:130555-200602);复方氯霉素醇溶液(北京军区总医院263 临床部提供,批号:20120326、20120617、20121029)。甲醇为色谱纯,冰醋酸为分析纯,水为重蒸馏水。
2 方法与结果
2.1 色谱条件 色谱柱:Agilent Eclipse XDB-C18(4.6 mm×150 mm,5 μm);流动相:甲醇-水(55∶45);流速:1.0 ml/min;检测波长:303 nm(0~4 min),278 nm(4~7 min);柱温:30℃,进样量:10 μl;检测时间:7 min。
2.2 混合对照品溶液制备 精密称取氯霉素和水杨酸对照品各100 mg,置于100 ml 量瓶中,用水溶解并稀释至刻度,作为混合对照品储备液。
2.3 供试品溶液制备 精密量取复方氯霉素醇溶液供试品1 ml,置于200 ml 量瓶中,加水稀释至刻度,摇匀,0.22 μm 滤膜滤过,取续滤液,即得。精密吸取10 μl 注入液相色谱仪,测定,即得液相色谱图(图1)。

图1 复方氯霉素醇溶液高效液相色谱图
2.4 线性关系考察 精密量取混合对照品储备液0.1、0.2、0.5、1.0、1.5、2.0 ml,置于10 ml 量瓶中,加水稀释至刻度,摇匀,即得不同浓度的系列对照品溶液。按“2.1”项下色谱条件分别进样,测定峰面积。分别以水杨酸及氯霉素的浓度(g/ml)为横坐标(X),以其各自的峰面积积分值为纵坐标(Y),绘制标准曲线。得回归方程为水杨酸:Y=20.22X +0.1769(r=0.9999,n=6);氯霉素:Y=24.97X +0.2418(r=0.9999,n=6)。结果表明,水杨酸和氯霉素在10.00~200.0 g/ml 范围内与其各自的峰面积线性关系良好。
2.5 精密度试验 精密吸取100.0 g/ml 混合对照品溶液,按“2.1”项下色谱条件,连续进样6 次,测定峰面积。结果水杨酸峰面积RSD 为0.74%(n=6),氯霉素峰面积RSD 为0.54%(n=6),表明仪器的精密度良好。
2.6 稳定性试验 取供试品溶液(批号:20120326),按“2.1”项下色谱条件,分别在0、2、4、8、12、24 h 各进样1 次,测定峰面积。结果水杨酸峰面积的RSD 为0.53% (n=6),氯霉素峰面积的RSD 为0.82%(n=6),表明供试品溶液在24 h 内稳定性良好。
2.7 重复性试验 取批号为20120326 的样品6份,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件,分别进样测定。结果水杨酸的平均含量为2.02%,RSD 为0.78%(n=6),氯霉素的平均含量为1.97%,RSD 为0.98%(n=6),表明方法的重复性良好。
2.8 回收率试验 精密量取水杨酸和氯霉素对照品,按复方氯霉素醇溶液处方配成80、100、120 g/ml 3 个浓度水平的样品溶液,每个浓度各分别制备3份供试品溶液,分别进样测定,记录峰面积,计算氯霉素和水杨酸的含量回收率,结果见表1。
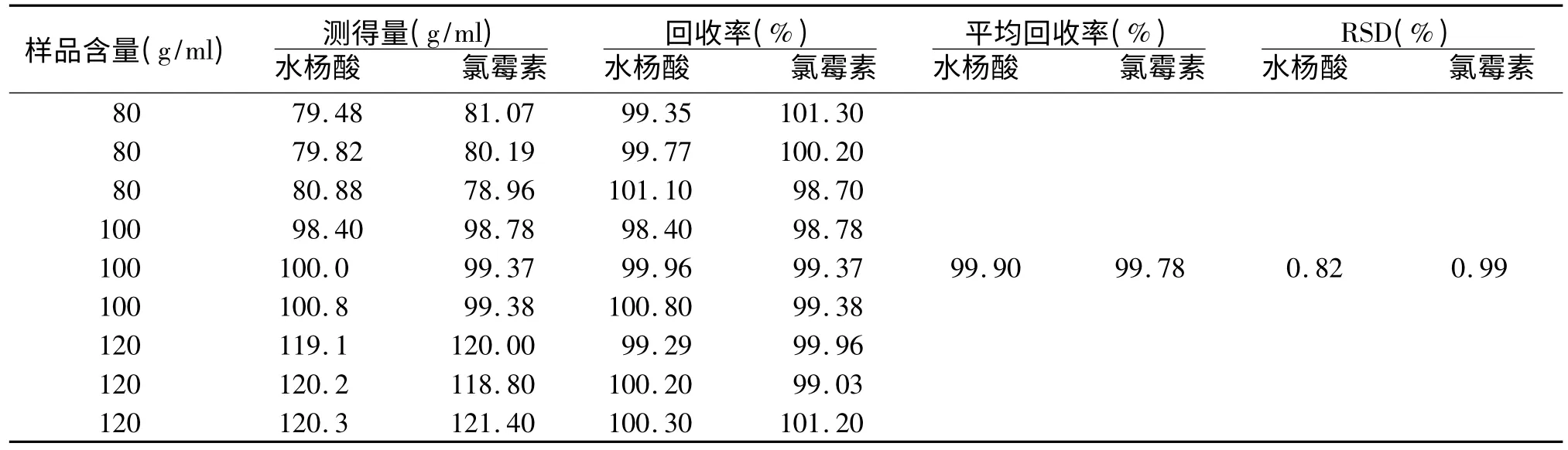
表1 复方氯霉素醇溶液加样回收率试验结果(n=6)
2.9 样品含量测定 取批号为20120326、20120617、20121029 的3份样品,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件,分别进样测定,结果样品中水杨酸的含量分别为2.02%、2.04%、2.07%,氯霉素的含量分别为1.97%、2.01%、2.06%。
3 讨论
目前,高效液相色谱法已广泛应用于各种制剂的含量检测,保证了制剂在临床使用中的安全性和有效性[9-13]。本文采用高效液相色谱法单波长切换测定复方氯霉素醇溶液中水杨酸和氯霉素的含量,方法简单快捷、准确度高。
《规范》中原有的复方氯霉素醇溶液中水杨酸的含量测定采用了滴定法,氯霉素的含量测定采用了高效液相色谱法,测定氯霉素的含量通常需要约30 min,而本实验条件的检测时间仅为7 min,缩短了样品检测时间,可以同时完成水杨酸和氯霉素的含量测定。而且,色谱峰型和理论塔板数均较理想,能够达到复方氯霉素醇溶液质量控制的要求。
水杨酸和氯霉素的最大吸收波长分别为303 nm 和278 nm[14],通常无法在配备紫外检测器的高效液相色谱仪上同时进行含量测定。紫外检测器一般只能在某一固定波长下测定单一组分的含量,对于多成分的同时测定往往无法实现[15]。如果使用多波长检测器,对仪器的要求较高,且方法准确度相对较低。本试验通过采用单波长切换的方法,使用紫外检测器分别在水杨酸和氯霉素的最大吸收波长处测定其含量,具有较高的灵敏度,对仪器的要求较低,具有较高的应用推广价值。
[1]中国人民解放军总后勤部卫生部.中国人民解放军医疗机构制剂规范(2002年版)[M].北京:人民军医出版社,2003:100-101.
[2]郭胜才,谷娜,李华.高效液相色谱法测定复方氯霉素醇溶液中水杨酸与氯霉素含量[J].医药导报,2010,29(6):783-785.
[3]谷娜,邢旺兴,郭胜才.高效液相色谱法同时测定复方氯霉素醇溶液中氯霉素和水杨酸的含量[J].健康研究,2009,29(3):177-178.
[4]黄力,杨宁,刘海英,等.HPLC 法测定复方氯霉素醇溶液中氯霉素的含量[J].中国药事,2009,23(4):373-375.
[5]刘晋华,李玉萍,尤光甫.复方氯霉素醇溶液含量测定方法的改进[J].解放军药学学报,2007,23(3):228-230.
[6]魏立平.HPLC 法同时测定复方氯霉素醇溶液中氯霉素和水杨酸含量[J].解放军药学学报,2007,23(5):378-380.
[7]张燕,孙岚.高效液相色谱法测定氯霉素醇溶液含量[J].医药导报,2008,27(8):986-987.
[8]刘海英,杨宁,黄力,等.高效液相色谱法测定氯霉素醇溶液中氯霉素的含量[J].药学实践杂志,2008,26(4):289-290,293.
[9]杨莹,郭琪,郭丽红,等.高效液相色谱法测定开光复明丸中栀子苷的含量[J].解放军医药杂志,2011,23(4):23-24.
[10]郝影霞,王逢春,王焱.高效液相色谱法测定活血清脑丸中阿魏酸的含量[J].解放军医药杂志,2012,24(7):29-31.
[11]苗爱东,李晓翠,何秀言,等.高效液相色谱法测定替硝唑片中替硝唑含量的不确定度分析[J].解放军医药杂志,2012,24(1):33-35.
[12]罗飞,贺美波,罗巧林.高效液相色谱法测定甲硝唑氯霉素栓中两种成分的含量[J].中国医药导报,2012,9(16):124-125.
[13]周劲康,吴跃丽.高效液相色谱法同时测定复方参芷痤疮酊中甲硝唑和氯霉素含量[J].中国药业,2010,19(16):30-31.
[14]陈晓宝,陶建亮.复方氯霉素醇溶液中氯霉素和水杨酸的含量测定[J].中国现代应用药学,2005,22(3):871-872.
[15]缪春辉,冷爱国,涂飞龙.复方氯霉素醇溶液中3 种成分的含量测定[J].东南国防医药,2003,5(2):102-103.
