ATP-生物荧光体外抗肿瘤药物敏感性检测方法的应用探讨
2013-08-25王钰莹张霓霓余丽梅
王钰莹 罗 清 胡 康 刘 颂 张霓霓 余丽梅*
1.遵义医学院附属医院贵州省细胞工程重点实验室,贵州 遵义 563003;2.遵义医学院附属医院肿瘤医院,贵州 遵义 563003;3.遵义医学院附属医院甲状腺乳腺外科,贵州 遵义 563003;4.遵义医学院附属医院妇科,贵州 遵义 563003;5.遵义医学院附属口腔医院,贵州 遵义 563003
化学治疗是治疗恶性肿瘤的三大治疗手段之一,由于肿瘤患者存在个体差异及肿瘤的异质性,肿瘤对各种化疗药物存在着明显的个体差异[1,2],特别是肿瘤复发和经过多次化疗的患者。因化疗前缺乏患者对化疗药物敏感性和耐药性的直接检测证据,在制定化疗方案时不可避免地存在着一定的盲目性,选择药物不准确。多数化疗药物本身的不良反应可造成对机体的损害,更重要的是可诱导肿瘤细胞产生多药耐药性,贻误治疗时机,增加医疗成本和患者的经济负担。因而在治疗前筛选敏感药物,选择高效、有效药物,进行有的放矢的治疗早已成为研究者和临床医生关注的重要问题。
体外抗肿瘤药物敏感试验的方法及结果准确与否是影响病人治疗方案制订的关键因素。本室对121例开展了ATP-生物荧光体外抗肿瘤药物敏感性的检测,现将检测情况总结如下。
1 材料与方法
1.1 肿瘤标本 收集2011年9月至2012年12月我院121例肿瘤患者的标本进行ATP-生物荧光体外抗肿瘤药物敏感性检测。其中乳腺癌89例,卵巢癌16例,子宫内膜癌4例,宫颈癌4例,口底鳞癌4例,肺癌3例,非霍奇金淋巴瘤1例。121例患者,年龄在29~76岁。
1.2 化疗药物化疗药物为100%药物血浆峰值浓度(100%PPC)(见表1)。联合用药的每个药物的浓度与单药浓度相同。

表1 化疗药物及剂量

*因CTX和IFO在体外无活性,实验中所采用的是CTX的体内活化物苯丁酸氮芥CLB替代。
1.3 仪器和试剂 BHP9504型微孔板发光分析仪(北京滨松光子技术股份有限公司)。ATP生物荧光肿瘤药物敏感性检测试剂盒,含混合消化酶、培养基、红细胞裂解液、细胞培养板(96孔)、ATP提取液和荧光酶-荧光素工作液(北京金紫晶生物医药技术有限公司)。
1.4 体外药敏检测实验
1.4.1 实体瘤标本制备 无菌取得实体瘤手术标本,在含抗生素的培养基中浸泡25min后,剪成0.5~1mm3碎块,置于50 ml离心管中,加用培养基稀释1倍的混合消化酶10ml,于37℃消化2~4h,用培养基洗涤2次,获得单细胞悬液。台盼蓝染色,计数活的肿瘤细胞。
1.4.2 浆膜腔积液标本的制备 将肝素抗凝的浆膜腔积液标本,400g离心10min,去上清,如有大量红细胞(>25%),加入预冷的10ml红细胞裂解液,冰浴5~10min红细胞去除红细胞,再加入20ml RPMI 1640培养液,400g离心10分钟,去上清,加入3~5ml培养基混匀制备得细胞悬液。台盼蓝染色,计数活的肿瘤细胞,调整细胞密度于2~4×106个/ml备用。
1.4.3 加待测药物于96孔培养板,每个药物设100%、50%、25%、12.5%和6.25%PPC 5个浓度,每个浓度2个平行孔,并设无药对照组(M0),和最大抑制对照组(MI)。接种所得肿瘤细胞,细胞数为2×104个/孔。在37℃,5%CO2条件下培养5d后,开始测定。最大抑制对照孔加50μl最大抑制剂,其余各孔加50μlATP提取液,在震荡器上震荡30s,室温静置5min。再次震荡混匀。每孔取50μl液体,按相应的位置加到荧光测试板内,每孔加入50μl荧光素-荧光酶混合液。再次震荡混匀5s,立刻在微孔板发光分析仪上测定荧光强度。
1.5 药敏检测判定标准 计算药物IC90和IC50。IC90<90%且IC50<25%判定为高度敏感;IC90<90%或IC50<25%判定为中度敏感;IC90>90%且IC50>25%判定为不敏感。
1.6 吉姆萨染色检测浆膜腔积液中脱落细胞 收集的浆膜腔积液标本离心后制备的细胞悬液,取0.4ml,按常规方法进行制片及染色。
2 结果
2.1 标本的可评价率 收集的121例标本中,原发灶手术标本61例,组织穿刺标本47例,浆膜腔积液标本10例,淋巴结组织标本3例,有117例进行了成功的体外药敏检测,可评价率为96.69%。4例不成功的标本中均来自乳腺癌患者的穿刺组织,标本由空心针进行组织穿刺所得,体积较小,获得的细胞数太少而放弃检测。
2.2 检测方法可行性 实体瘤手术后瘤组织标本及穿刺活组织标本经过消化分离出肿瘤细胞,将细胞悬液接种培养5~7天后对细胞形态进行观察,可见药物组比M0对照组细胞数量明显减少(见图1)。收集的浆膜腔积液标本经离心,收集0.5ml细胞悬液,按脱落细胞学方法进行常规吉姆萨染色,可观察到转移癌细胞(见图2),说明不论实体瘤组织标本还是浆膜腔积液标本,用ATP-生物荧光法均能分离得到肿瘤细胞,且药物组与M0对照组比较存活的细胞明显减少,由此证明该方法用于体外抗肿瘤药物敏感试验是可行的。
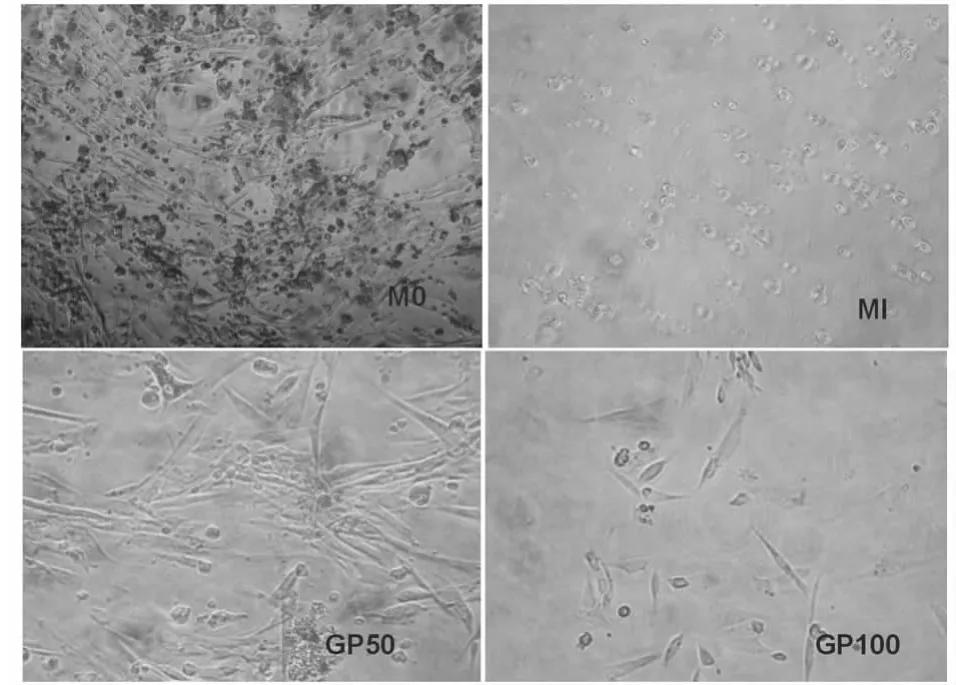
图1 体外抗肿瘤药敏检测细胞形态(×200)
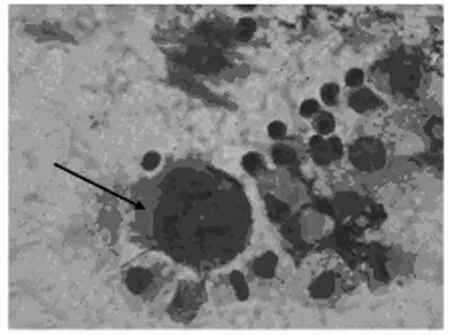
图2 腹水脱落细胞学检测
2.3 药物敏感性个体差异性 有效的117例患者选用的均是4~8个方案,其中有单药和联合用药,针对不同的癌标本类型,其敏感药物不同;同一肿瘤类型的患者的标本,其敏感药物也不同。部分患者按常规方案无效,但按检测结果选择敏感方案后症状得以明显缓解(见图3),可见肿瘤患者标本的药物敏感性存在个体差异。
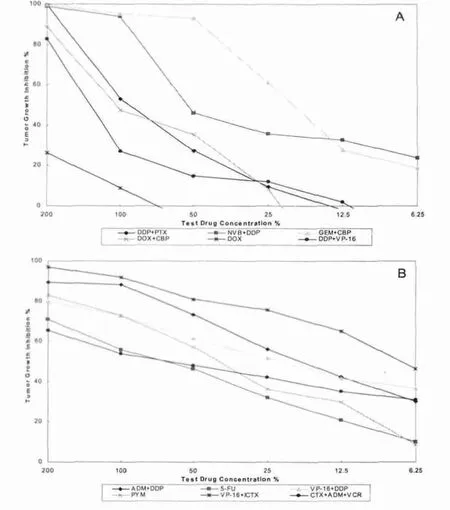
图3 ATP-生物荧光体外抗肿瘤药物敏感性检测结果图示
2.4 与临床治疗效果的吻合度调查 对检测的117例样本的病人资料进行查阅、追踪和统计,因部分病人死亡或仅作一次化疗患者资料不能进入统计外,可统计患者数量为66例。在该检测项目指导下用药后:乳腺癌,17.5%的患者新辅助化疗后肿块明显缩小,77.2%的患者状况平稳,5.3%的患者病情出现进行性恶化;卵巢癌,50%的患者CA125明显降低,37.5%的患者状况平稳,12.5%的患者病情出现进行性恶化。由以上数据可见,该项目在临床中的阳性有效率较高,达87.5%以上,与临床医生反馈信息吻合度较高。
3 讨论
化学治疗是治疗恶性肿瘤的常规有效手段之一。然而,由于肿瘤对化疗药物的敏感性存在个体差异,以及肿瘤细胞具有多重抗药性,导致相同药对同一类型患者的治疗效果不同。如果在用药前缺乏该癌症患者对化疗药物敏感性和耐药性的直接实验依据,在化疗方案的制定上就会存在一定的盲目性,而不敏感药物的治疗及化疗药物对机体的损伤及其降低机体免疫功能等可导致化疗失败,甚至危及生命。
ATP-生物荧光肿瘤体外药敏检测技术(ATP-tumor chemosensitivity assay,ATP-TCA)是目前较为先进的体外药敏检测技术,其原理是在有氧和ATP的条件下,荧光酶催化荧光素发出荧光,反应中所释放的荧光强度与ATP含量呈正相关。ATP是细胞内能量的基本来源,细胞死亡后,胞内的ATP被迅速水解而活细胞中ATP含量基本恒定,因此所测得的荧光强度可以反映活细胞数。从而可根据其判断抗肿瘤药物的药敏结果。肿瘤细胞存活率越低,说明肿瘤细胞对该化疗药物敏感性越高,杀伤力也越强,反之则敏感性越低。
由本室的检测结果可见,该方法能有效地从组织、胸腹水、淋巴结中分离出肿瘤细胞并进行接种培养,培养一定的时间后,药物组较M0无药对照组细胞数明显减少,与药敏检测结果一致。说明用该方法进行体外培养肿瘤细胞的药敏检测是可行的。细胞形态和数量的变化与药物敏感检测结果一致,可见该检测方法的准确性较高。近年来,国内外多家研究机构也已应用该方法,检测了多种恶性肿瘤对化疗药物的敏感性,并且已在世界多个国家对该方法进行了多中心的临床研究,证实其有较高的临床符合率,抗肿瘤药物敏感性试验的检测及药物敏感方案的制定在多种肿瘤治疗中取得了明显的效果。德国科隆大学医学中心Kurbacher等[1,2],于 1998 年和 2003 年分别报道了 ATP -TCA指导化疗与传统化疗比较和ATP-TCA辅助化疗对卵巢癌和乳腺癌治疗临床Ⅱ期试验,结果表明ATP-TCA指导化疗能够显著提高临床疗效,延长病人生存期,与传统化疗模式比较差异极为显著。日本进行的临床研究也表明ATP-TCA指导化疗显著提高了胃肠道肿瘤的治疗效果,延长了病人的生存期[3]。国外在乳腺癌、肺癌等肿瘤上进行的应用ATP-TCA法体外药敏结果和体内有效率的对比研究表明,体内外的结果比较一致[4-6]。本室所做的检测结果经查阅病案后也证实,其与临床治疗方案的符合率较高,所得到的各种单药和联合用药的体外药物敏感性与临床上观察的有效率基本一致,部分患者经常规治疗失败后按药敏方案进行治疗能有效控制病情。这些结果均提示,ATP-TCA法可以用于肿瘤的体外药敏检测。
[1]Kurbacher CM,Cree IA,Bruckner HW,et al.Use of an ex vivOATP luminescence assay to direct chemotherapy for recurrent ovarian cancer[J].Anticancer Drugs,1998,38(9):51 -57.
[2]Kurbacher CM,Grecu OM,Stier U,et al.ATP chemosensitivity testing in ovarian and breast cancer:early clinical trials[J].Recent Results Cancer Res,2003,161(1):221-30.
[3]Kawano K.The experiment and clinical evaluation of chemosensitivity test for esophageaLAnd gastric cancer by ATP assay using endoscopic biopsy[J].Nippon Geka Gakkai Zasshi,1992,93(2):232-240.
[4]Fehm T,Zwirner M,Wallwiener D,et al.Antitumor activity of zoledronic acid in primary breast cancer cells determined by the ATP tumor chemosensitivity assay[J].BMC Cancer,2012,23(12):308.
[5]Ian A Cree,Christian M,Kurbacher,et al.Correlation of the clinical response to chemotherapy in breast cancer with ex vivo chemosensitivity[J].Anticancer Drug,1996,34(7):630 -635.
[6]Knight LA,Kurbacher CM,Glaysher S,et al.Activity of mevalonate pathway inhibitors against breast and ovarian cancers in the ATP-based tumour chemosensitivity assay[J].BMC Cancer,2009,28(9):38.
