2008~2009年南宁市季节性H1N1亚型流感病毒血凝素HA1基因变异分析*
2013-08-24范云燕刘海燕林新勤秦剑秋覃巍巍
范云燕,刘海燕,林新勤,秦剑秋,黄 莉 ,覃巍巍
(广西壮族自治区南宁市疾病预防控制中心 530023)
流行性感冒是由流感病毒引起的急性呼吸道传染病,流感病毒分为 A、B、C 3种型别[1]。血凝素(HA)和神经氨酸酶(NA)是流感病毒主要表面抗原,尤其是HA基因具有高度易变性,是流感病毒发生抗原性漂移的主要原因[2]。流感病毒的HA基因在病毒受体识别和复制中起重要作用,它不仅与机体免疫密切相关,而且还是流感病毒发生抗原性变异的分子基础。研究表明中和抗体针对的抗原位点和受体结合位点(RBS)都位于 HA蛋白分子的头部重链区(HA1)[3]。本研究通过分析2008~2009年度南宁市季节性H1N1流感病毒的流行和HA1基因的变异情况,有助于掌握流感病毒进化方向和流行动态,为及时掌握本地区流感病毒活动动态,及早预测预警流感疫情提供实验信息和依据。
1 资料与方法
1.1 一般资料 2008~2009年南宁市流感病毒监测哨点医院采集到的流感样病例咽拭子,流感疫情采集到的流感样病例鼻咽拭子。
1.2 方法
1.2.1 病毒分离培养 将鼻咽拭子标本接种于狗肾传代细胞(MDCK)进行流感病毒分离培养。根据采样时间,2008年和2009年各选取10株季节性H1N1亚型流感毒株进行序列测定分析。
1.2.2 病毒RNA的提取和HA基因全长扩增 用QIAGEN Rneasy Mini kit RNA提取试剂盒提取20份毒株RNA,方法按试剂盒说明书。取5μL RNA模板,用引物 H1N1-HA-F:5′-AGC AGG GGA AAA TAA AAM CAA CC-3′进行反转录,条件为:25℃10min,42℃1h,98℃5min,冰上冷却。取5 μL cDNA为模板,分别用 H1N1-HA-F和 H1N1-HA-991R:5′-CAC TCT CCT ATT GTG ACT GGG TG-3′,以及 H1HAF768:5′-ACT ACT GGA CTC TGC TGG AAC-3′和 H1N1-HA-R:5′-TTC TGA AAT TCT GGT CTC AGA TGC-3′引物分别进行PCR,PCR条件为:95℃3min,(94℃40s,52℃40s72℃1min)35个循环,72℃10min,50μL体系,以上反转和PCR试剂均购自Fermentas。
1.2.3 HA基因测序和分析 PCR产物送北京诺赛基因组研究中心有限公司进行纯化和测序,测序结果采用VectorNTI 9.0软件进行分析。将获得的HA1氨基酸序列与WHO推荐的北半球 A亚型疫苗株 A/Solomon/3/2006(2007年11月至2008年4月,ABU50586)和 A/Brisbane/59/2007(2008年11月至2010年4月,ACA28844)进行比对,并用 Mega4.1软件构建系统进化树。
2 结 果
2.1 2008、2009年南宁市 H1N1亚型流感病毒流行情况2008、2009年南宁检测标本分别为849份和863份,流感病毒分离培养阳性率为8.00%和26.65%,2008年以季节性H1N1(47.6%)和 H3N2(32.35%)为主,2009年以 H3N2(62.61%)为主,B型流感病毒(20.87%)其次。南宁市流感流行主要集中在夏秋季节,2008年和2009年分别在7月和9月达到病毒分离高峰。见图1。
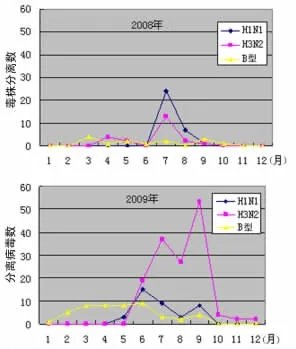
图1 2008、2009年南宁市季节性流感毒株分离分布
2.2 核苷酸序列测定结果及氨基酸进化树分析 2008~2009年20株H1N1亚型流感病毒HA全长1 698bp翻译成566个氨基酸,HA1长为325个残基。将20株H1N1流感病毒HA1蛋白与北半球疫苗推荐进行比对。20株H1N1聚成2个大的类群,其中A/Solomon/3/2006与2008年的毒株形成类群Ⅰ,而A/Brisbane/59/2007与2009年的毒株形成类群Ⅱ,两疫苗株分别在类群中形成独立的亚分支。
2.3 H1N1亚型流感病毒HA1氨基酸序列变异及蛋白质分子结构变化分析
2.3.1 HA1蛋白分子二硫键的变异和糖基化位点的变异情况 H1N1血凝素的基因翻译后经过剪切,52与284、65与77、100与145、289与313的半胱氨酸C间形成二硫键[4]。南宁市2008~2009年20株H1N1二硫键形成位点未发生氨基酸水平的插入、替换或缺失。HA蛋白潜在的糖基化位点序列为N-X-T/S[5]。对糖基化位点分析发现,两疫苗株在 HA1区有8个糖基化位点,20份本地毒株除A/nanning/621/2008氨基酸发生突变(N54K),减少一个糖基化位点。其他毒株糖基化位点相对保守,未发现氨基酸替换。
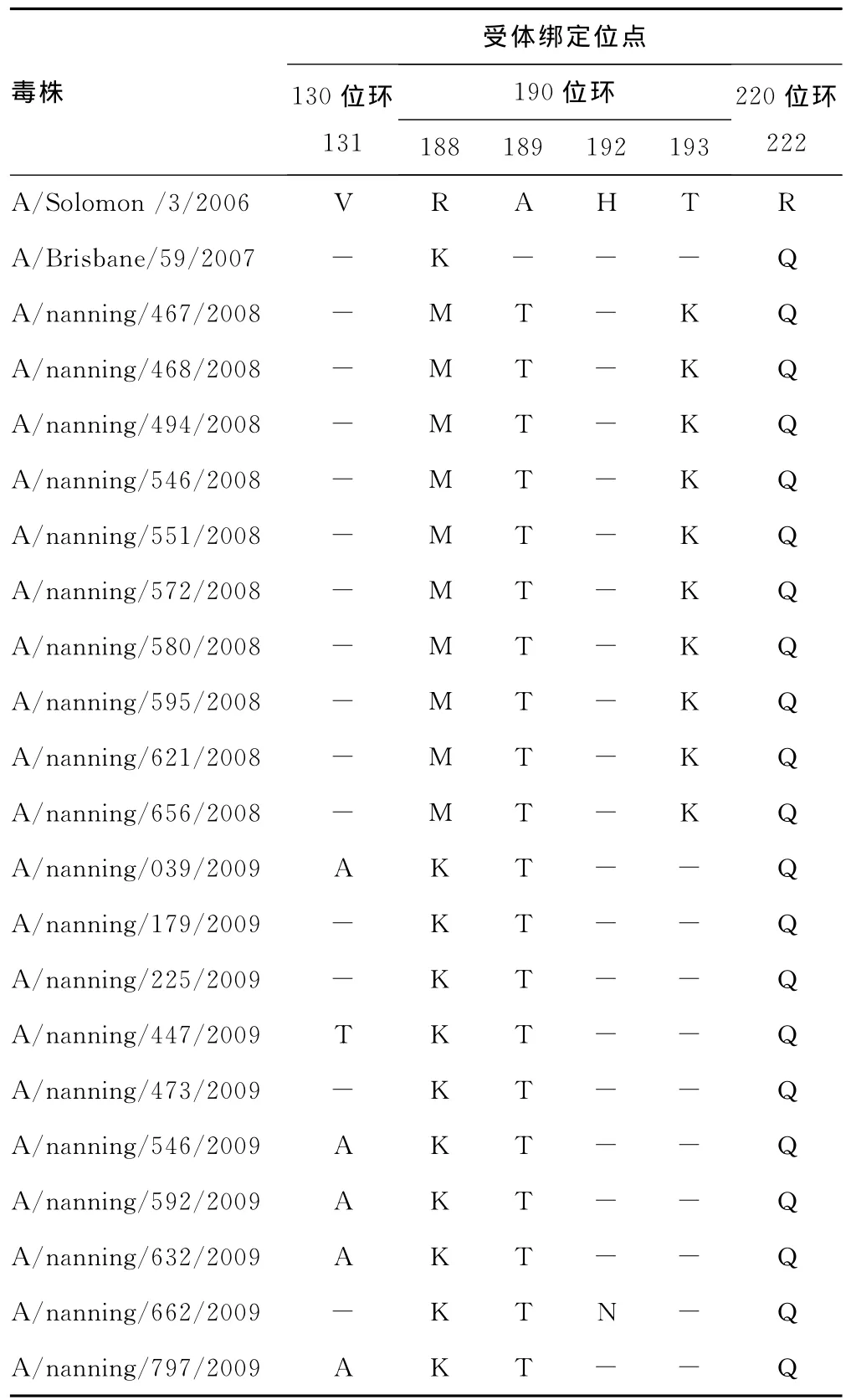
表1 2008~2009人类季节性H1N1流感病毒HA1受体结合位点变异情况位点比对
2.3.2 HA1蛋白分子上受体结合位点(RBS)的变异情况HA上的受体结合位点位于头部末端(HA1部分),每个HA单体上有3个二级结构分别是190螺旋,130环,220环[6]。HA1编码序列受体结合位点变异情况见表1,在3个二级结构中190的R188M(R188K)、A189T、H193N、T193K氨基酸位点均发生了整体的替换;220位环222位点在2008~2009年的毒株以及A/Brisbane/59/2007中均为氨基酸Q;另外,2009年的毒株中已有多个毒株130位环的131位点发生V131A(V131T)的替换。
2.3.3 HA1蛋白分子上抗原决定簇位点的变异情况 H1N1流感病毒HA1蛋白有4个抗原决定簇分别为Cb、Sa、Sb和Ca区[7-10]。通过对抗原位点的统计和分析,47个抗原位点有多个发生了变化,其中Sb、Ca、Cb位点相对活跃,而Sa位点相对保守。在发生氨基酸变异的抗原位点中,相对于A/Solomon/3/2006或A/Brisbane/59/2007毒株,20份毒株的 HA1发生替换的是Sb位点:185、188、189、192;Ca位点:141、167;Cb位点:73;Sa位点未发生氨基酸变异。2008年的10份毒株在188、189、193位点与两疫苗株均不同;2009年毒株除个别毒株外,在185、189、141位点与 A/Brisbane/59/2007相比发生了整体 的 变 异,另 外 A/nanning/473/2009 和 A/nanning/662/2009分别在发生H192N、N167K点变异。
3 讨 论
通过对本地检测标本统计分析,2008~2009年南宁流感流行主要集中在夏秋季节,H1N1和H3N2交替成为2008年和2009年的优势毒株。以上年度的H1N1血凝素基因重链区进化树显示,A/Solomon/3/2006与2008年毒株属于分支Ⅰ,而A/Brisbane/59/2007与2009年毒株属于分支Ⅱ。A/Brisbane/59/2007作为2008年11月至2010年4月疫苗推荐毒株,与2008年毒株相距较远。本地毒株HA1氨基酸序列二硫键和糖基化位点比较保守;而HA1蛋白上的受体结合位点则相对活跃,其中190位环氨基酸位点变异最大,尤其是在188位和189位为高突变位点,但188位和189位氨基酸位点并不直接与宿主受体唾液酸发生结合,因此这些变化可能不影响RBS与受体结合的亲和力[11]。Vines等[12]通过氨基酸定点替换实验证明了流感病毒RBS第222位和224位氨基酸的变化决定了病毒感染宿主的特异性。当H3病毒的HA同时发生L222Q、S224G突变时,可使感染人的H3流感病毒能够感染禽类。本实验当中H1N1病毒的RBS的222和224位点分别为Q和G,这种替换是否影响病毒感染宿主的特异性,尚有待考证。流感病毒HA1蛋白上的抗原决定簇的变异情况是评价该毒株是否有流行病学意义的关键因素,新变种必须具备在其HA区抗原位点有4个以上氨基酸突变,而且必须分布在2抗原决定簇区[13]。分析表明,2009年毒株除 A/nanning/473/2009外,与对应的疫苗株相比抗原决定簇区氨基酸变异未达到4个;2008年毒株与A/Solomon/3/2006相比则存在4个氨基酸的替换并且分布在两个抗原决定簇区域。因此,可以推测,2008年根据WHO疫苗推荐株生产的疫苗对该年南宁市H1N1亚型流感预防效果可能并不理想,这将导致2008年南宁市 H1N1亚型的流行的强度明显增加。而经历了2008年的流行后,人群中有了保护抗体,同时H1N1疫苗及时更新,使得H1N1在2009年流行强度有了明显下降。
[1] Palese P,Young JF.Variation of influenza A,B and C viruses[J].Science,1982,215(4539):1468-1474.
[2] Pontoriero AV,Baumeister EG,Campos AM,et al.Antigenic and genomic relation between human influenza A(H3N2)viruses circulating in Argentina during 1998and the H3N2vaccine component[J].Rev Panam Salud Publica,2001,9(4):246-253.
[3] Weis W,Brown JH,Cusack S,et al.Structure of the influenza virus hemagglutinin complexed with its receptor,sialic acid[J].Nature,1988,333(6172):426-431.
[4] Austin FJ,Kawaoka Y,Webster RG.Molecular analysis of the haemagglutinin gene of an avian H1N1influenza virus[J].J Virol,1990,71(Pt 10):2471-2474.
[5] Sun S,Wang Q,Zhao F,et al.Glycosylation site alteration in the evolution of influenza A(H1N1)viruses[J].PLoS One,2011,6(7):e22844.
[6] Gamblin SJ,Haire LF,Russell RJ,et al.The structure and receptor binding properties of the 1 918influenza hemagglutinin[J].Science,2004,303(5665):1838-1842.
[7] Raymond FL,Caton AJ,Cox NJ,et al.The antigenicity and evolution of influenza H1haemagglutinin,from 1950-1957and 1977-1983:two pathways from one gene[J].Virology,1986,148(2):275-287.
[8] Caton AJ,Brownlee GG,Yewdell JW,et al.The antigenic structure of the influenza virus A/PR/8/34hemagglutinin(H1Subtype)[J].Cell,1982,31(2Pt 1):417-427.
[9]Igarashi M,Ito K,Yoshida R,et al.Predicting the antigenic structure of the pandemic 2009influenza virus hemagglutinin[J].PLoS One,2010,5(1):e8553.
[10]Al-Majhdi,Fahad N.Structure of the sialic acid binding site in influenza a virus:hemagglutinin[J].J Biol Sci,2008,7(1):113-122.
[11]傅天韵,娄维义,石铁流.不同宿主H1N1病毒血凝素蛋白(HA)受体结合位点的变异特征[J].遗传,2010,32(7):701-711.
[12]Vines A,Wells K,Matrosovich M,et al.The role of influenza A virus hemagglutinin residues 226and 228in receptor specificity and host range restriction[J].J Virol,1998(72):7626-7631.
[13]张烨,温乐英,赵翔,等.2004~2005年中国B型流感病毒抗原性及基因特性研究[J].中华实验和临床病毒学杂志,2006,20(2):11-13.
