西部马脑脊髓炎病毒实时荧光RT-PCR检测方法建立及标准质控品制备
2013-08-24吴亚琼高志强乔彩霞张鹤晓吴清民
谷 强,吴亚琼,高志强,刘 环,张 伟,蒲 静,乔彩霞,张鹤晓,吴清民
(1. 中国农业大学 动物医学院,北京 100094;2. 北京出入 境检验检疫局,北京 100026)
西部马脑脊髓炎病毒(western equine encephalitis virus, WEEV)为披膜病毒科甲病毒属成员,可引起人和的发病,病马常呈亚临床感染,病症相对温和,感染马的致死率低于30%。该病潜伏期5~14d,临床症状包括发热、厌食和精神高度沉郁。严重时,病马表现为狂躁不安、失明、共济失调、精神极度沉郁、卧地不起、痉挛,最后可导致死亡。人感染本病毒后,患者表现为高热,头痛,痉挛,呕吐和嗜睡,有的迅速发展为昏迷状态而死亡。WEEV对人的致死率为明显低于东部马脑脊髓炎病毒[1-2]。我国于1990年分别从新疆乌苏县的一组赫坎按蚊和博乐县的全沟硬蜱中分离出WEEV[3]。西部马脑脊髓炎为我国出入境检验检疫中规定的一类检疫对象。 随着马匹国际贸易和国际赛事的日益频繁,来自不同的国家和地区、健康状况不同的马匹可能将该病带进我国,对此除实施严格的隔离检疫制度之外,开展西方马脑炎的快速检测技术也非常重要。
WEEV为单股正链RNA病毒,全长为11.5kb左右。基因组编码4种非结构蛋白(NSP1~4)和5种结构蛋白(衣壳蛋白C,包膜糖蛋白E1、E2、E3,6K,基因排列顺序为 5’-C-E3-E2-6K-E1-3’)。E2蛋白是该病的主要保护性抗原,具有7个部分重叠的抗原表位,分别与血凝抑制、中和病毒和抗病毒感染活性有关,而E2-1区中的C区是甲病毒属特异性抗原表位,含病毒与细胞作用的受体[4]。
目前西部马脑脊髓炎主要检测方法包括病毒分离和鉴定,血清学检测方法(血凝抑制和ELISA)以及基于RT-PCR的检测方法[1]。本研究采用MGB修饰短探针建立的针对WEEV的TaqMan荧光RT-PCR方法具有快速、灵敏,特异和操作简单等优点, 适用于本病流行地区的疫情监测,同时也可应用于马匹等动物的出入境检测。
1 材料和方法
1.1 试剂
1.1.1 病毒核酸
西部马脑脊髓炎病毒McMillan核酸、东部马脑脊髓炎病毒(ssp. North American variant)核酸,由军事医学科学院提供;马动脉炎病毒核酸、马疱疹病毒1型核酸、马流感病毒H3N8核酸,均由本实验室保存。
1.1.2 主要试剂
Trizol购自GIBCO/BRL公司;M-MLV反转录酶、Taq DNA聚合酶、dNTP、RNA酶抑制剂等购自Promega公司;DNA快速纯化回收试剂盒、 质粒快速提取纯化试剂盒、pMD20-T载体购自Takara公司; Ribo MAXTMLarge Scale RNA Production System-SP6 购自 Promega 公司。
1.1.3 实时荧光定量PCR仪
LightCycler 2.0,Roche公司产品;ABI7900,ABI公司产品。
1.2 荧光定量RT-PCR反应引物和探针的设计与合成
对已经发表的WEEV分离株全序列用Vector NTI进行序列比对分析,选择序列中高度保守区域,设计合成引物和探针。引物和探针由上海基康生物技术公司合成,序列见表1。
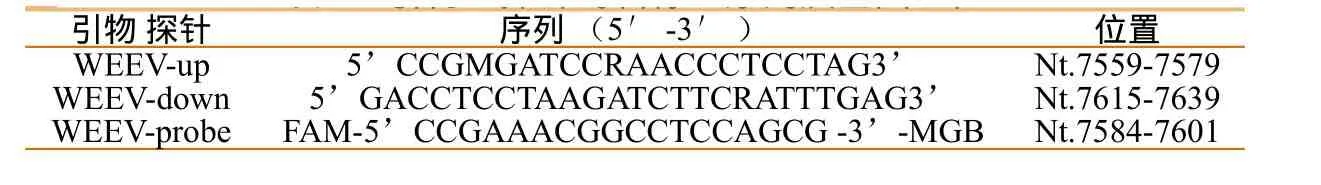
表1 引物、探针的名称、序列及基因组位
1.3 实时荧光RT-PCR反应条件的优化
以西部马脑脊髓炎病毒McMillan核酸作为扩增模板,对各种反应条件进行优化。对引物浓度、探针浓度、Mg2+浓度、Taq DNA聚合酶、逆转录酶用量、循环参数等条件进行了优化,来确定最佳反应条件。
1.4 体外转录合成病毒cRNA
设计合成特异性引物扩增包含WEEV主要结构蛋白片段(约2.5kb核苷酸片段,引物序列和位置见表2,包含有荧光定量RT-PCR扩增区域),将扩增片段纯化回收后分别克隆于pMD20-T载体中。将质粒线性化之后,用RiboM -AXTMLarge Scale RNA Production Systems- SP6试剂盒进行体外转录。转录产物经无RNase的DNase消化除去其中的DNA模板后,75℃ 10min将DNase灭活,再次抽提纯化制备出所需cRNA,按照20 μL/管分装,置-80℃保存备用。

表2 引物名称、序列及基因组位置
1.5 标准质控品制备与初步定值
取制备的cRNA作1:100稀释,测定其260nm和280nm的吸光度值(A260和A280)并计算拷贝数,用75% Trizol水溶液(Trizol:水=3:1)稀释至1.0×108拷贝数/mL。然后进行分装,1.0 mL/管。
1.6 标准质控品均匀性检验
随机抽取10管制备的标准质控品,按照GB/T 19438.1-2004所述方法提取RNA。应用建立的WEEV荧光RT-PCR方法在一次试验中测试提取的10份RNA样品,每个样品重复2孔检测,手动设置基线,获取Ct值。结果数据用单因素方差分析统计处理。
1.7 标准质控品稳定性检验
随机抽取制备的标准质控品,在以下每种条件下放置10支[5]:(1)室温20℃~25℃,相对湿度20% ~ 50%,14d取出进行测试;(2)冰箱冷藏温度2℃~8℃,6个月取出进行测试;(3)-20℃,1年后取出进行测试;(4)对照,-80℃,长期放置。将纯化的含有WEEV 目的基因的质粒通过测定其260nm的吸光度值,计算出其拷贝数,系列稀释制成一系列外标品。应用建立的荧光RT-PCR方法来间接测定上述RNA的拷贝数。采用两样本均数显著性检验-t检验进行统计分析。
1.8 检测极限的确定(灵敏度试验)
把制备的cRNA标准质控品作系列稀释,用去离子水作阴性标准,按优化的条件进行荧光RTPCR测定,由此确定方法的检测极限。
1.9 特异性试验
用建立的方法对西部马脑脊髓炎病毒核酸、东部马脑脊髓炎病毒核酸、马动脉炎病毒核酸、马疱疹病毒1型核酸、马流感病毒H3N8核酸进行检测,以验证方法的特异性。
1.10 重复性试验
各选取3个不同浓度的cRNA标准模板,用所建立的荧光定量RT-PCR检测方法进行3次重复性试验,以验证方法的可重复性和稳定性。
1.11 对临床样品的检测
用上述两种方法对所采集的197份进口马血样品进行检测,验证方法的临床实用性。
2 结果
2.1 引物和探针的设计与合成
对设计的引物和探针进行BLAST分析,证实引物与探针高度特异,并可覆盖所有西部马脑脊髓炎病毒株。
2.2 实时荧光RT-PCR反应条件的优化
以西部马脑脊髓炎病毒McMillan株核酸作为扩增模板,经多次重复性试验发现,西部马脑炎病毒检测方法最适反应总体积25 μL,其中模板10 μL,最适引物浓度为0.4 μmol/L,探针浓度为0.2 μmol/L,Mg2+浓度为4 mmol/L;最适循环参数为42℃/30 min,94℃/3 min;之后94℃/10s,56℃ /5s,60℃ /30s,40 个循环。
2.3 体外转录合成cRNA标准模板
经RT-PCR扩增,获得西部马脑脊髓炎病毒McMillan株7442nt ~10011nt片段(约2.5kb核苷酸片段,包含有荧光定量RT-PCR扩增区域),扩增产物见图1。将扩增片段纯化回收后克隆于pMD20-T载体中,质粒命名为pMD20-T-Weev(7442nt ~10011nt)。经体外转录获得cRNA纯品。

图1 目的片段RT-PCR扩增结果
2.4 标准质控品的制备
获得的cRNA纯品的A260和A280比值为2.043,表明RNA纯度较高。将置于75% Trizol水溶液中含量为108拷贝数/mL的标准质控品按照1.0 mL/管进行分装,置-80℃保存。
2.5 均匀性检验结果
均匀性检验结果数据用SPSS软件进行单因素方差分析统计处理。F值<F0.05临界值,结果见表3,表明标准质控品中的核酸片段是均匀分布的。且分装的标准质控品瓶间变异系数小于5%。

表3 西部马脑脊髓炎标准质控品均匀性检验结果
2.6 稳定性检验结果
不同条件下放置制备的标准质控品的检测结果见表4。将检测组与对照组( - 80℃)数据分别作两样本均数显著性检验-t检验进行统计分析,结果表明检测组与对照组差异均无统计学意义( P>0.05)。
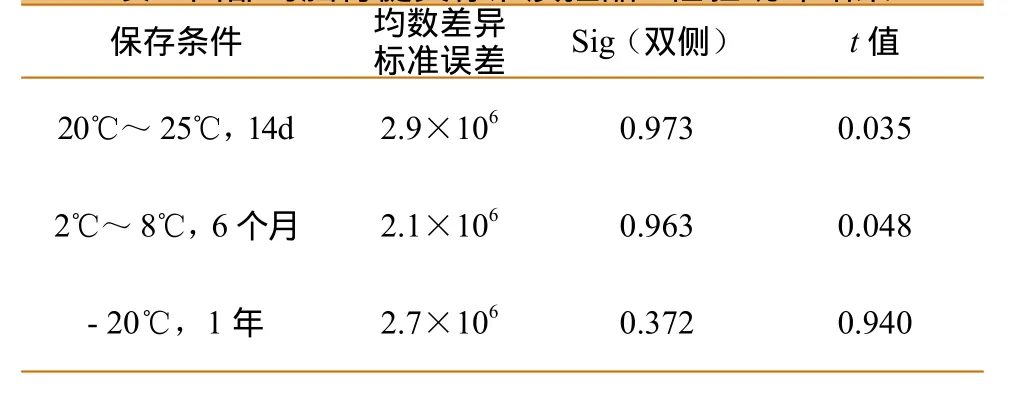
表4 西部马脑脊髓炎标准质控品t检验统计结果
2.7 检测极限的测定(灵敏度试验)结果
结果显示,本方法的检测灵敏度可达10拷贝/反应(图2)。

图2 WEEV荧光RT-PCR 检测方法的检测极限测定
2.8 特异性检测结果
对1.1.1中的病毒核酸进行检测,结果显示,建立的方法只能检出西部马脑脊髓炎病毒,但不能检出其他病原(图3),表明所建立的检测方法特异性好。

图3 WEEV荧光RT-PCR 检测方法的特异性试验结果
2.9 重复性检测结果
对105~107拷贝数cRNA 模板进行连续3 次检测,变异系数均<5%(表5)。
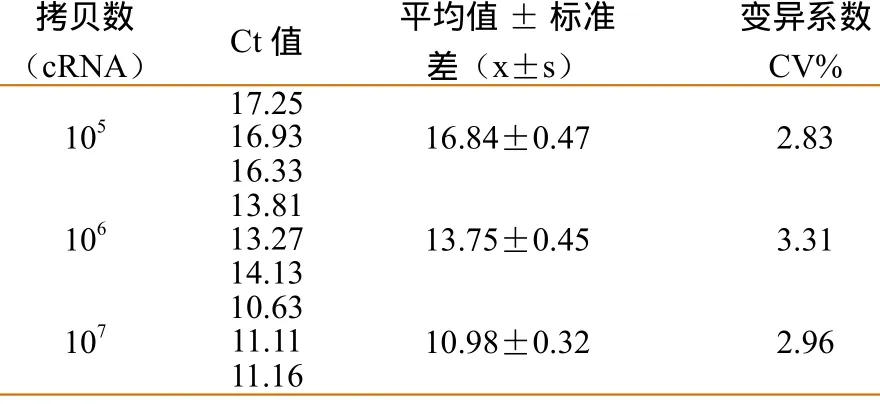
表5 重复性试验结果
2.10 临床样品检测结果
应用建立的方法对197份进口马血样品进行检测,结果显示进口马血均为WEEV阴性,并与文献报道的RT-PCR进行比较[6],两者符合率为100%(表6)。

表6 临床样品检测结果
3 讨论
西部马脑脊髓炎是重要的虫媒传染病,可引起人和马的脑脊髓炎,导致神经组织受损严重。据报道,本病在美国西部、加拿大、墨西哥以及中美洲和南美洲均有发生。也有报道说我国曾从新疆分离到WEEV[1,3]。本病主要呈蚊-鸟传播方式。蚊是病毒的传播媒介,鸟是病毒的贮存宿主,病毒可在蚊体内增值并可达较高滴度,并持续终生存在。尽管本病的确诊必须依靠病毒分离、鉴定,病毒抗原检测等传统方法,但现在国外越来越多实验室采用核酸快速检测方法来快速诊断本病[6]。
由于普通RT-PCR存在灵敏度较低、特异性稍差等缺点,难以满足潜伏期感染和传播媒介体内病毒的检测需求。TaqMan探针实时荧光RT-PCR方法灵敏特异,特别是结合MGB探针检测技术,灵敏度更为提高。本研究通过比对WEEV 不同代表株序列,设计合成引物和MGB修饰探针,对其以及反应条件进行优化。并用含有扩增区域的大片段核酸经体外转录制备标准质控品cRNA,建立了WEEV通用型荧光定量RT-PCR检测技术,实现了对WEEV的快速检测。此外,通过体外转录制备标准品cRNA,测定了方法的分析灵敏度,使该方法更加完善成熟。特异性、重复性试验证明了该方法特异、可重复性好,利用建立的荧光定量RTPCR方法检测临床样品197份,结果均为阴性,与文献报道的普通RT-PCR方法检测结果一致,表明本方法检测结果可信程度高,为WEEV检验检疫以及防治奠定了重要基础。
[1]Office International des Epizooties. Manual of Diagnostic Tests and Vaccines for Terrestrial Animals[M]. Paris: Office International des Epizooties, 2008: 858-865.
[2]Monath T P. Arthropod-borne encephalitis in the Americas[J]. Bull WHO, 1979, 57:513–533.
[3]何海怀,吕新军,杨益良. 我国分离的两株病毒为重组甲病毒[J].中华实验和临床病毒学杂志, 2001, 15(2):120-124.
[4]Strauss J H, Strauss E G. The Alphaviruses: gene expression, replication and evolution [J]. Microbiol Rev,1994, 58 (3): 491.
[5]GB/T15000.3-2008. 标准样品工作导则(3)标准样品定值的一般原则和统计方法[M]. 北京:中国标准出版社,2008:1-47.
[6]Lambert A J, Martin D A, Lanciotti R S. Detection of North American Eastern and western equine encephalitis viruses by nucleic acid ampli fi cation assays [J]. J Clin Microbiol, 2003,41( 1 ):379–385.
