羟磷灰石类纳米与仿生材料盖髓的研究
2013-08-23杨清岭李宝花荣光影王志群
杨清岭,李宝花,荣光影,王志群,赵
(1.佳木斯大学附属第二医院,黑龙江 佳木斯 154002;2.佳木斯大学附属第一医院,黑龙江 佳木斯 154003;3.佳木斯大学医院管理处,黑龙江佳木斯 154007)
羟基磷灰石(Hydroxylapatite,HAP)其化学成份与生物组织如牙齿的无机成份相似,具有好的生物相容性已被广泛用于植骨和盖髓研究[1~4]。但是在细菌感染存在时,使用此材料盖髓是无效的。甲硝唑 Metronidazole于1978年被 W HO确定为抗厌氧感染的首选药。本实验以纳米羟基磷灰石复合甲硝唑糊剂(nHM),纳米羟基磷灰石 /聚酰胺66甲硝唑糊(nHPM)作为盖髓剂,氢氧化钙(CH)作为对照材料,对比两种羟基磷灰石促牙本质桥形成方面的差异,为临床筛选理想的盖髓剂提供实验依据。
1 材料与方法
1.1 主要材料
纳米羟磷灰石 (nHA)和纳米羟磷灰石 /聚酰胺66(nHA/PA66)购自四川国纳科技有限公司 。甲硝唑注射液(上海华源长富药业有限公司),氢氧化钙和玻璃离子(上海齿科材料厂 )。nHA和 nHA/PA66均为粉未型 ,盖髓时分别用甲硝唑注射液调湿呈糊状 nHM和 nHPM。
1.2 实验动物和分组
杂种雄性犬 4只,随机分两组,体重15~ 18kg,牙齿完好无缺损,每组内依次编号选取 75颗牙齿用作实验牙。将75颗实验牙随机分为三组,分别用 nHAM,nHAPM和 CH盖髓,各组25颗牙。
1.3 实验步骤
实验狗用速眠新 0.1mL/kg肌注麻醉后,在实验牙的唇面或颊面备 V类洞,穿髓孔直径约 0.5~1mm。无菌生理盐水冲洗止血,分别用 nHM,nHPM、CH盖髓。玻璃离子充填。术后7d和70d时处死动物,取出上下颌骨,拔出实验牙。固定,脱钙,常规包埋切片,HE染色,光镜下观察各组盖髓后穿髓处修复性牙本质的形成[5]。
1.4 参照标准
分级参照 Josimeri Hebling[6]标准:0:无硬组织形成;1:少量的硬组织沉积在露髓面;2:中等量的硬组织沉积在露髓面;3:大量的硬沉积或形成完整的牙本质桥。
2 结果
术后7d,各组均未见修复性牙本质桥的形成。术后70d nHM组25例其中无硬组织形成的有 9例,16例有少量或中等量的硬组织沉积在露髓面,术中无1例出现大量的硬沉积在露髓面或形成完整的牙本质桥。穿髓处牙髓组织内有或多或少的修复性牙本质团块。盖髓70d时,nHPM组25例其中无硬组织形成的有5例,11例有少量或中等量的硬组织沉积在露髓面,9例出现大量的硬沉积在露髓面或形成完整的牙本质桥,有一小部分牙有完整的牙本质桥形成,其余实验牙能见到牙本质桥从缺损侧形成。
盖髓后 70d时,CH组25例中无硬组织形成的有3例,9例有少量或中等量的硬组织沉积在露髓面,13例出现大量的硬沉积在露髓面或形成完整的牙本质桥,术后70d大部分牙齿有完整的牙本质桥形成,但距牙本质桥较远处的根部牙髓组织中可见少量的较小的修复性牙本质团块。
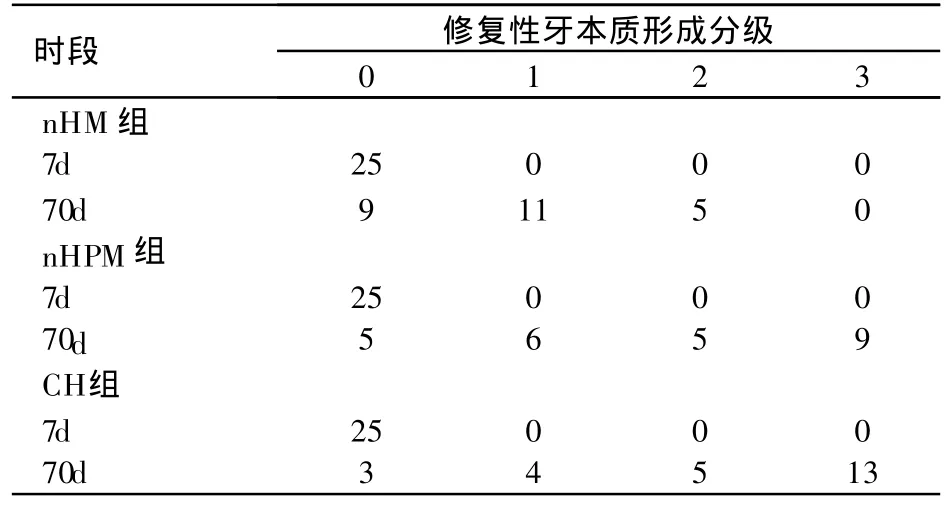
表1 3种材料盖髓后修复性牙本质形成分级(n=25)
3 讨论
Tziafas等[7]提出形成修复性牙本质需要有适宜于牙髓细胞附着的平面。光镜下观察盖髓7d时,三组盖髓材料均无明显的矿化基质出现。盖髓70d时,对照材料由于本身的强碱性和较强的细胞毒性在与牙髓组织接触时出现钙化,产生持续性炎症,甚至牙髓坏死进而导致术中盖髓失败。经统计学分析比较 nHM组与 CH组,nHM诱导修复性牙本质形成的能力较 CH差 (P<0.05),这可能与纳米羟基磷灰石材料脆性大,耐冲击强度低的缺点有关。在直接盖髓术中用做盖髓材料时临床操作不便、无抗压能力、松散易移位等各种因素导致与下方的牙髓组织脱离接触或者是材料本身流失。
而经统计学分析 nHPM与 CH比较,nHPM诱导修复性牙本质形成的能力与 CH无显著差异 (P> 0.05),苏勤等[8]报道的纳米羟基磷灰石 /聚酰胺66虽然具备了盖髓材料较好的生物相容性要求,但是促进修复性牙本质形成的能力不如氢氧化钙有效。分析其与本实验的区别可能在于实验中加入了抗菌药物甲硝唑,细菌感染被认为是影响疗效的主要因素,细菌感染性炎症存在时明显影响牙髓修复能力,所以本实验在羟基磷灰石中加人甲硝唑成份以增强疗效。即使在细菌感染存在时并不影响纳米羟基磷灰石 /聚酰胺66促修复性牙本质形成的能力,且盖髓剂中加入抗菌消炎药物并不影响露髓处的创伤修复。纳米羟基磷灰石 /聚酰胺66是由纳米级羟基磷灰石微晶体与聚酰胺66复合而成,PA66与 nHA之间的氢键作用主要发生在 PA的仲氨基和 nHA的羟基之间,具有较好的机械力和稳定的界面,该平面有利于牙髓细胞的分化附着。另一方面,其有机物和无机物的组成比例及力学性能与牙本质相似,较好的机械力学性能使纳米羟基磷灰石/聚酰胺具有一定的抗压强度。而 CH抗压强度不足,盖髓材料与牙本质间的裂隙成为细菌感染牙髓的通道,最终导致盖髓的失败。苏勤等[9]证实 nHA/PA 66作为盖髓剂较 Dycal与牙髓界面的微渗漏更小。充填物的边缘微渗漏有可能是远期失败的原因之一。使得随着时间的延长 nHPM诱导修复性牙本质形成的能力与 CH无显著差异。nHM与 nHPM,两者之间差异有统计学意义 (P<0.05),而实验组促修复性牙本质形成的能力主要来自羟磷灰石,所以纳米羟基磷灰石/聚酰胺66诱导修复性牙本质形成的能力强于纳米羟基磷灰石。
[1]Wemer J,Lirmcr-Krcmar B,Friess W,et al.Mechanical properties and invitro cellcompatibility of hydrox yapatite ceramics with graded pore structure[J].Biomaterials,2002,23(21):4285-4294
[2]Jaber L,Mascres C,Donohue WB,et al.Reaction of the dental pulp to Hydroxyapatite[J].Oral Surg Oral Med Oral Pathol,1992,73:92
[3]孙庆治,李金良,李忻轩.纳米羟基磷灰石种植体的实验研究[J].黑龙江医药科学,2012,35(1):52-53
[4]赵熙儒,赵刚,莫宏兵,等.壳聚糖修饰后的纳米羟基磷灰石作为BM P-2输送载体转染细胞的研究 [J].黑龙江医药科学,2012,35(1):3-5
[5]杨清岭,李宝花,尹蒙熔.纳米羟基磷灰石和纳米羟基磷灰石 /聚酰胺66直接盖髓术的组织学对比观察 [J].黑龙江医药科学,2010,33(3):27-28
[6]Josimeri Hebling,Elisa Maris,Aparecida Giro& Carlos Alberto de Souza Costa.Biocompatibility of an adhesive system applied to exposed human dental pulp[J].Journal of Endodontics,1999,25(10):676-682
[7]Torabinejad M,Hong CU,McDonald F,et al.Physical and chem ical properties of a new root end filling materials[J].J Endod,1995,21(7):349-353
[8]苏勤,叶玲,周学东.纳米羟磷灰石 /聚酰胺66盖髓的动物实验研究[J].四川大学学报,2005,36(1):43-45
[9]苏勤,叶玲,周学东,等.聚酰胺 /纳米羟磷灰石复合生物材料盖髓封闭性能的体外实验研究[J].华西医大学报,2002,33(4):561-562
