钙掺杂对La2-xCaxCe2O7-δ 性能影响研究
2013-08-20张文静
王 岭 宋 洁 戴 磊 张文静 朱 靖 王 硕
(河北联合大学化学工程学院,唐山 063009)
自从Iwahara 等[1]于1981 年首先发现掺杂三价金属阳离子的钙钛矿型固体电解质SrCeO3在高温(500~1 000 ℃) 含氢气氛下具有良好的质子导电性以 来,其 后,陆 续 发 现 掺 杂 的BaCeO3,SrZrO3,CaZrO3,BaZrO3等钙钛矿也表现出良好的质子导电性[2]。使其在固体氧化物燃料电池、氢的分离提纯和氢传感器等方面得到了广泛应用。但由于这种钙钛矿型质子导体含有碱性较强的离子,容易与水、二氧化碳发生反应,化学稳定性不好,限制了其应用。在不断地改善钙钛矿型质子导体稳定性的同时,研究者也在积极发掘电导率高、稳定性好的新型质子导体。
氧化物A2B2O7(其中A、B 分别是+3 价和+4 价阳离子,属立方晶系),由于其非占据性结构,并且在高温含氢气氛下表现出很好的质子导电性和化学稳定性[3-4]。因而,在燃料电池和氢传感器中具有广泛的应用前景,是近年来备受关注的一类新型质子导体[5-8]。萤石型结构的La2Ce2O7(空间群Fm3m[9])即是此类新型质子导体的一种。国外已有用掺杂Ca2+来提高La2Ce2O7电导率的研究报道[10-11]。
国内也已经开展这种材料的制备和应用研究。王吉德等[12]用溶胶-凝胶法制备了La1.95Ca0.05M2O7-δ(M=Ce,Zr),样品在1 500 ℃烧结10 h 后均形成了立方萤石型结构,相对密度均大于90%。样品在湿润氢气气氛中的电导率比干燥空气中大。800 ℃时,La1.95Ca0.05Ce2O7-δ在湿润氢气和干燥空气气氛下的电导率分别为3.35×10-2S·cm-1和1.48×10-2S·cm-1。并把材料用到合成氨工艺中,得到了较高的氨的产率。陶泽天等[13]用Pechini 法成功地合成了La1.95Ca0.05Ce2O7-δ电解质。XRD 分析可知,该样品在700 ℃下,CO2气氛和含3% H2O 的H2气氛中表现出良好的稳定性,并将此材料用于固体燃料电池的研 究。Fang 和Yan 等 将La0.5Ce0.5O2-δ与Ni 混 合 制成了氢气分离膜,获得了好的氢分离效果[14-15]。Tao等[16]以La0.4875Ca0.0125Ce0.5O2-δ为 电 解 质 制 备 了 燃 料 电池并测定了在不同温度下的开路电压。
虽然Ca2+掺杂的La2Ce2O7已有研究,但并没有系统地研究掺杂量不同的Ca2+对La2Ce2O7性能的影响。本文采用高温固相法制备了La2-xCaxCe2O7-δ(x=0,0.05,0.1,0.15,0.2)系列新型质子导体,研究了Ca部分取代La 位对La2Ce2O7的相结构、烧结性能、化学稳定性、电导率的影响。
1 实验部分
1.1 试剂及仪器
氧化镧、氧化铈(分析纯)、碳酸钙(99.0%,天津市东丽区天大化学试剂厂)、Pt 浆料(西安宏星电子浆料厂)。
IM6e 型电化学工作站(德国Zahner 公司)、SX16型硅钼棒电阻炉(包头灵捷炉业工程有限公司)、球磨机、FW-4 型压片机(天津天光光学仪器有限公司)。
1.2 样品的制备
按所需物质的量比称量La2O3、CeO2、CaCO3,将原料、氧化锆球、无水乙醇按质量比1∶2∶0.5 的比例混匀后放入聚四氟乙烯球磨罐中,球磨10 h,磨好的浆料自然晾干后放入电阻炉中,空气气氛900 ℃预烧5 h,降至常温后,加入1%的粘结剂PVB(聚乙烯醇缩丁醛),再次湿法球磨10 h 后晾干。在玛瑙研钵中研磨成粉体,于15 MPa 的单轴压力下压成圆片,将其在1 500 ℃空气气氛中烧结10 h 后即得所需的试样,升/降温速度均为3 ℃·min-1。
1.3 样品晶型及微观结构表征
采用D/MAX2500PC 型X 射线衍射仪测定烧结试样的XRD 图,X 射线源为Cu Kα (λ=0.154 056 nm),管电压40 kV,管电流为100 mA,扫描速度2°·min-1,扫描范围2θ=10°~90°。
运用S-4800 型扫描电镜对1 500 ℃烧结10 h的试样进行微观结构表征。由于试样本身不导电,对其表面进行喷金处理,喷金设备为日本日立公司生产的E-1010 试样表面处理机。
1.4 化学稳定性试验
CO2中的稳定性试验是将试样置于100%流动CO2气氛中,800 ℃处理10 h,测试试样的物相变化。为了研究试样在水蒸气中的稳定性,将试样在800 ℃经85 ℃水蒸气饱和的氩气处理10 h 后测试试样的物相变化。
1.5 电导率的测定
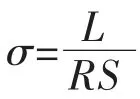
2 结果与讨论
2.1 物相结构和化学稳定性分析
图1 为质子导体La2-xCaxCe2O7-δ在1 500 ℃烧结10 h 后的XRD 图。将所得烧结样品粉体的XRD衍射峰位置和强度与检索到的CeO2(PDF 03-065-2975) 标准图进行比较,结果对应很好,La 填入了CeO2晶格中,只是整体向左偏移,说明已形成立方萤石型结构。从图1 可知1 500 ℃烧结后的样品,峰形清晰,晶格完整,衍射峰型尖锐,未见到CaCO3或其他杂质的衍射峰,表明Ca2+已经进入La2Ce2O7基质中La3+晶格位。
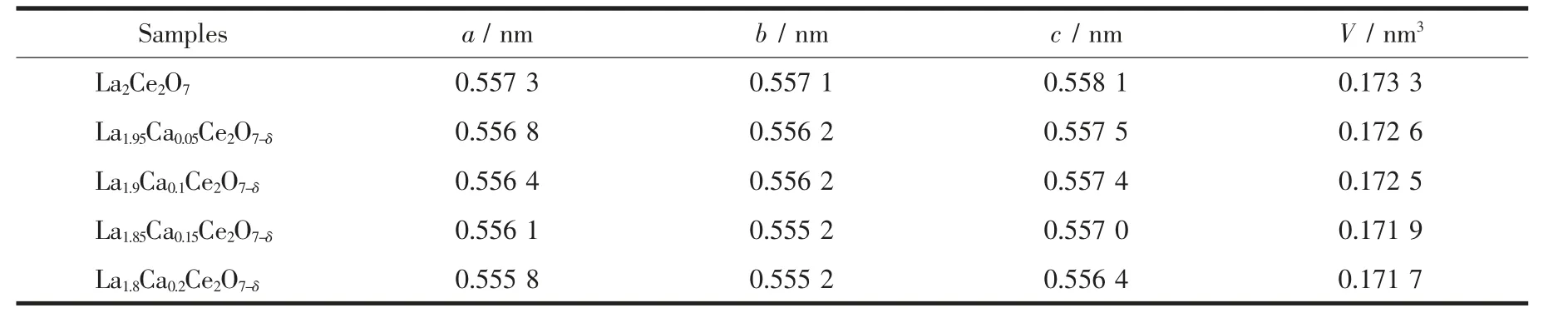
表1 La2-xCaxCe2O7-δ 的晶格参数和晶胞体积Table 1 Lattice parameters and unit volume of La2-xCaxCe2O7-δ
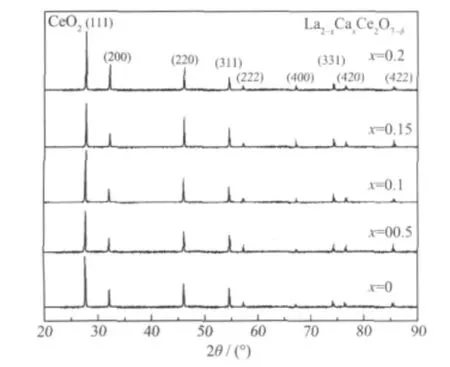
图1 质子导体La2-xCaxCe2O7-δ(0≤x≤0.2) 1 500 ℃处理10 h 后的XRD 图Fig.1 XRD patterns of proton-electron conductors La2-xCaxCe2O7-δ(0≤x≤0.2) after sintered 10 h at 1 500 ℃
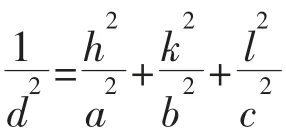
2.2 微观结构分析

图2 不同掺杂比例的质子导体La2-xCaxCe2O7-δ 表面SEM 图(2 000 倍)Fig.2 SEM images of the surface of La2-xCaxCe2O7-δ sintered at different doping ratios (2000 times)
图2 和图3 为1 500 ℃烧结温度下La2-xCaxCe2O7-δ的表面和断面的SEM 图。从图中可以明显看到,当x=0 时试样表面孔隙较多,不致密,且晶型较模糊;0≤x≤0.05 的烧结样品,表面和断面均不致密,有一定的闭气孔存在;当x≥0.1 时,烧结样品的表面非常致密。随着Ca 的掺杂量增加,试样微观组织结构逐渐致密,晶粒持续长大,平均粒径由x=0时的1~5 μm 增长到x=0.2 时的50 μm,单位面积内的晶界数量减少,晶粒饱满,晶型清晰。

图3 不同掺杂比例的质子导体La2-xCaxCe2O7-δ 断面SEM 图(2 000 倍)Fig.3 SEM images of the cross section of La2-xCaxCe2O7-δ sintered at different doping ratios (2000 times)
2.3 化学稳定性分析
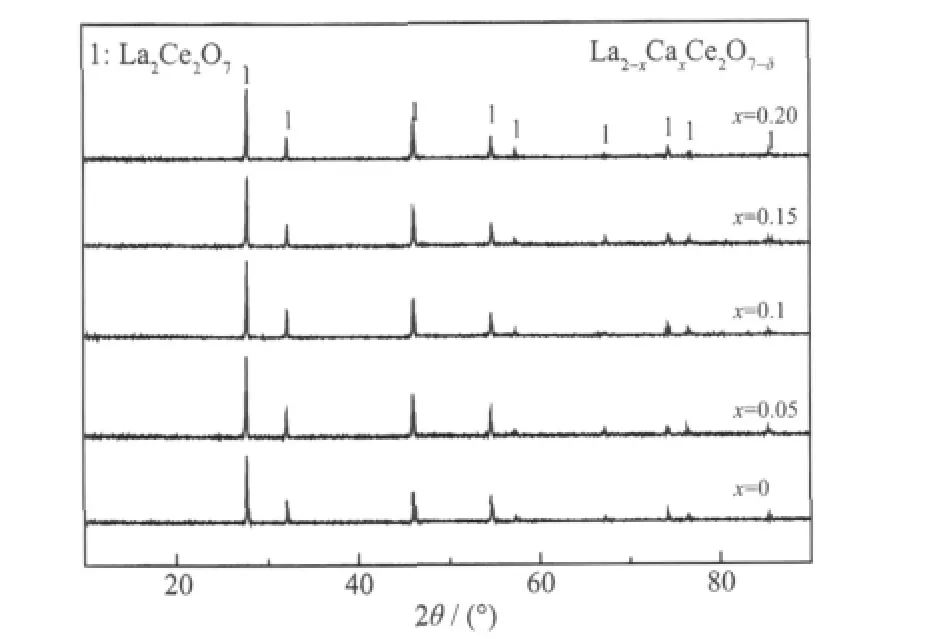
图4 1 500 ℃烧结的La2-xCaxCe2O7-δ 在CO2 气氛800 ℃处理10 h 后的XRD 图Fig.4 XRD patterns of La2-xCaxCe2O7-δ sintered at 1 500℃after exposed to flowing CO2 atmosphere at 800 ℃for 10 h
为了从实验中验证高温质子导体La2-xCaxCe2O7-δ在CO2气氛中的化学稳定性,将其置于100%流动CO2中800 ℃处理10 h。样品的颜色没有发生变化,始终为浅黄色,图4 是1 500 ℃烧结10 h 后的试样进行CO2化学稳定试验后的XRD 图。稳定性试验后XRD 图没有发生变化,没有杂质峰生成,说明质子导体La2-xCaxCe2O7-δ在CO2气氛中稳定。由图5 可知,各组成的样品在水蒸汽中也有良好的稳定性。
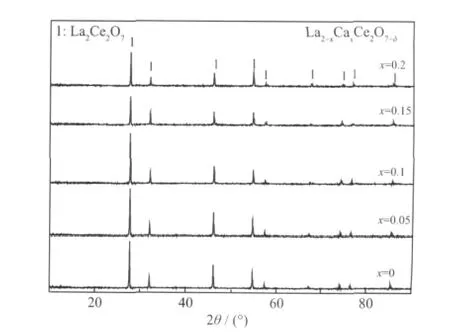
图5 1 500 ℃烧结的La2-xCaxCe2O7-δ 在水蒸气气氛下800 ℃处理10 h 后的XRD 图Fig.5 XRD patterns of La2-xCaxCe2O7-δ sintered at 1 500℃after exposed to flowing H2O atmosphere at 800 ℃for 10 h
2.4 阻抗谱分析
固体电解质的交流阻抗谱从高频至低频一般由四部分组成[17]:(1) 导线及接触电阻R0;(2) 晶粒电阻Rg及其电容Cg;(3) 晶界电阻Rgb及其电容Cgb;(4)电极反应电阻Rct及电极-电解质界面双电层电容Cdl,总电Rtotal=R0+Rg+Rgb+Rct。在给定的测量温度范围内,各部分对总电阻的贡献不同。低温时主要表现晶粒和晶界阻抗半圆,阻抗谱图由两个半圆和一条射线组成。当温度升高时,第一个晶粒半圆逐渐减小直至消失,主要由于低的晶粒电容超出了仪器频率测试范围[18]。第二个半圆变小,而射线逐渐有变成第三个半圆的趋势。根据砖层模型,第一个半圆对应晶粒阻抗,而第二、第三个半圆分别对应于晶界和界面反应阻抗[19]。
质子导体的电性能采用电化学交流阻抗谱测量,典型的阻抗谱如图6 所示。图6 为1 500 ℃烧结的La1.85Ca0.15Ce2O7-δ质 子 导 体 使 用 铂 浆 为 电 极 材 料在空气中600 ℃、650 ℃、700 ℃、750 ℃时的阻抗谱图。600 ℃时阻抗谱图由一部分晶粒阻抗半圆、晶界阻抗半圆和一条射线组成。随着温度的升高达到650 ℃,晶粒阻抗半圆逐渐变小直至消失,晶界阻抗半圆逐渐趋于完整,射线逐渐弯曲最后变成一个下沉的半圆。当温度达到750 ℃时,晶界阻抗半圆与界面反应阻抗半圆逐渐重合。
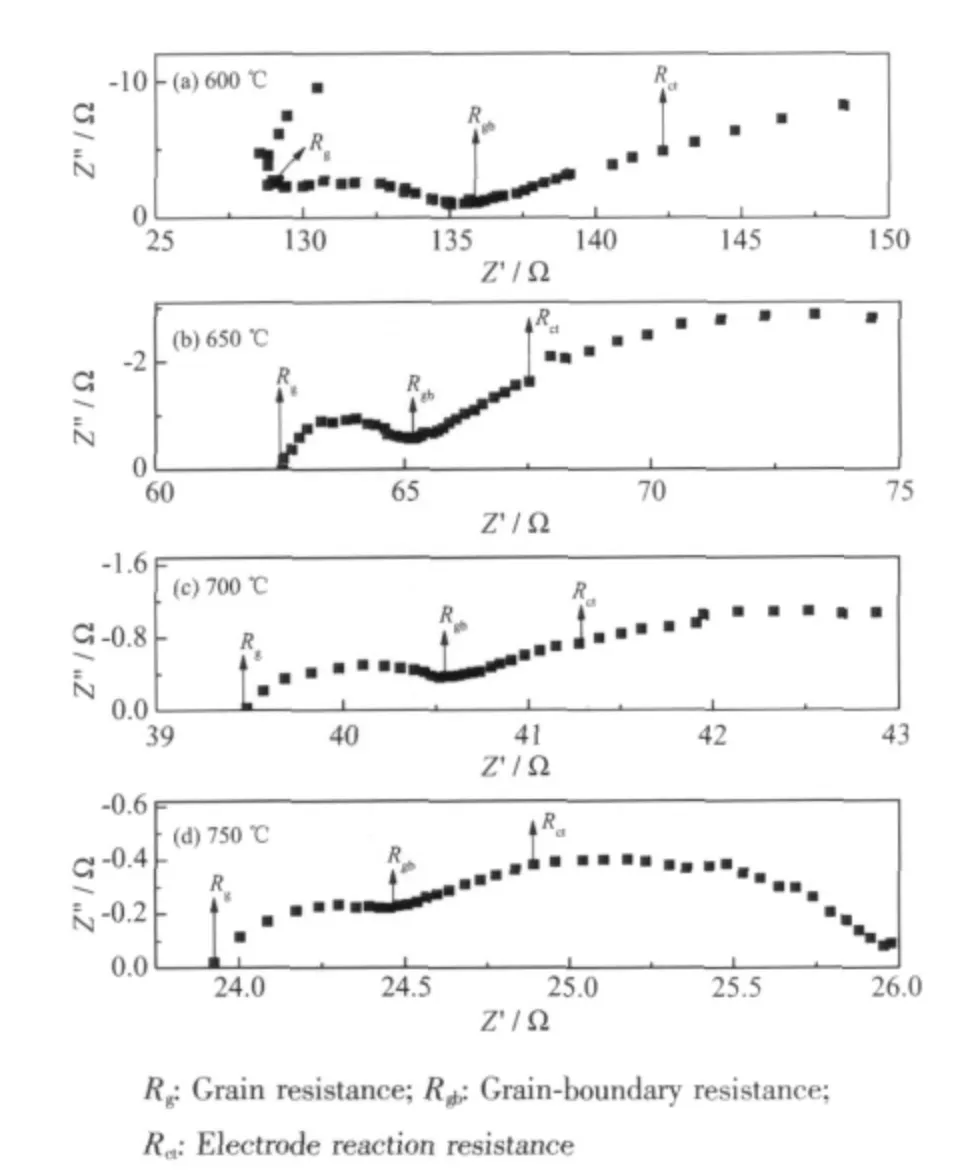
图6 空 气 气 氛 中La1.85Ca0.15Ce2O7-δ 在 不 同 温 度 下阻抗谱图Fig.6 AC Impedance spectra of La1.85Ca0.15Ce2O7 at different temperature in air
图7 可 知,1 500 ℃烧 结 的La1.85Ca0.15Ce2O7-δ质子导体使用铂浆为电极材料在湿润氢气气氛中550℃、600 ℃、650 ℃、750 ℃时的阻抗谱图。在氢气中低温时550 ℃时阻抗谱图由一部分晶粒阻抗和晶界阻抗半圆和一条射线组成。随着温度的升高达到600 ℃,晶粒阻抗半圆逐渐变小直至消失,晶界阻抗半圆逐渐趋于完整。当温度达到700 ℃时,晶粒阻抗半圆完全消失,阻抗谱由一个代表晶界阻抗的半圆和一条代表界面反应阻抗的射线组成。
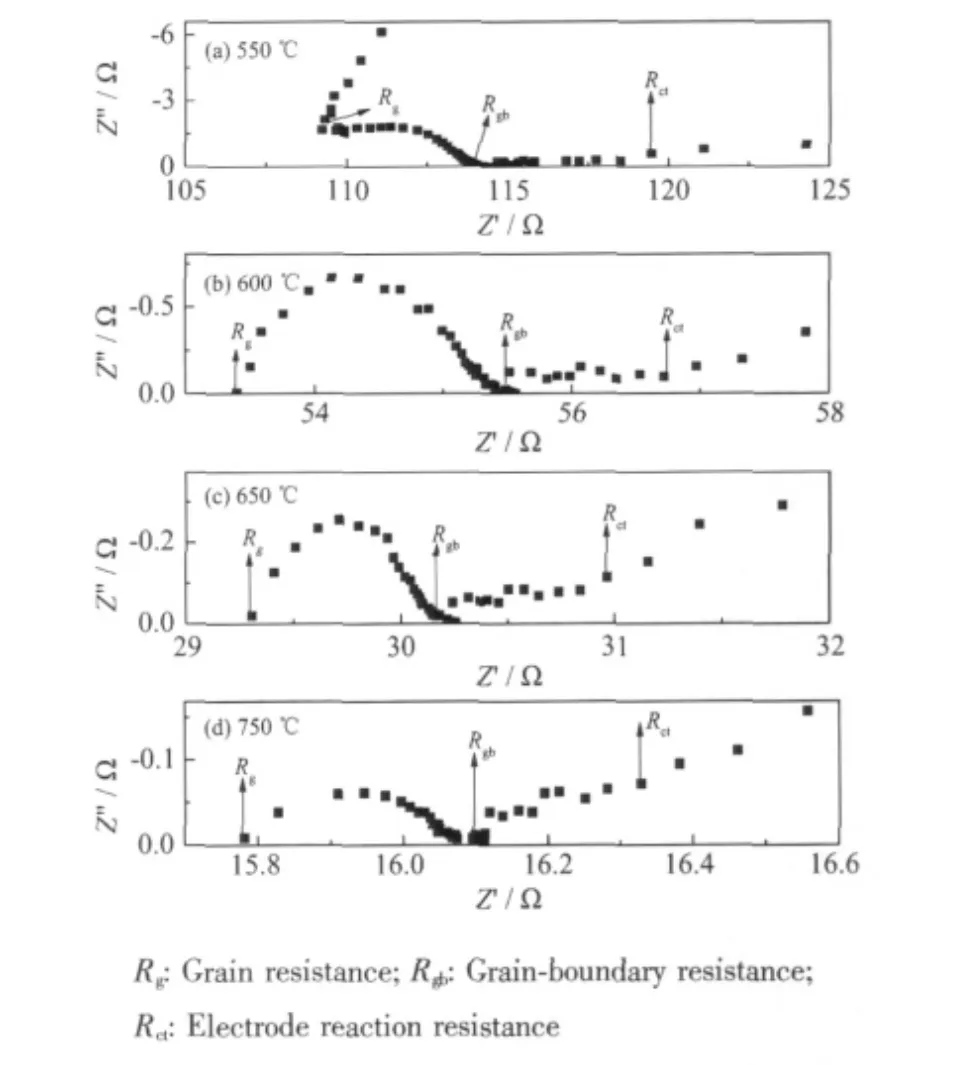
图7 湿 润 氢 气 气 氛 中La1.85Ca0.15Ce2O7-δ 在 不 同 温 度 下的阻抗谱图Fig.7 Impedance spectra of La1.85Ca0.15Ce2O7-δ at at different temperature in air
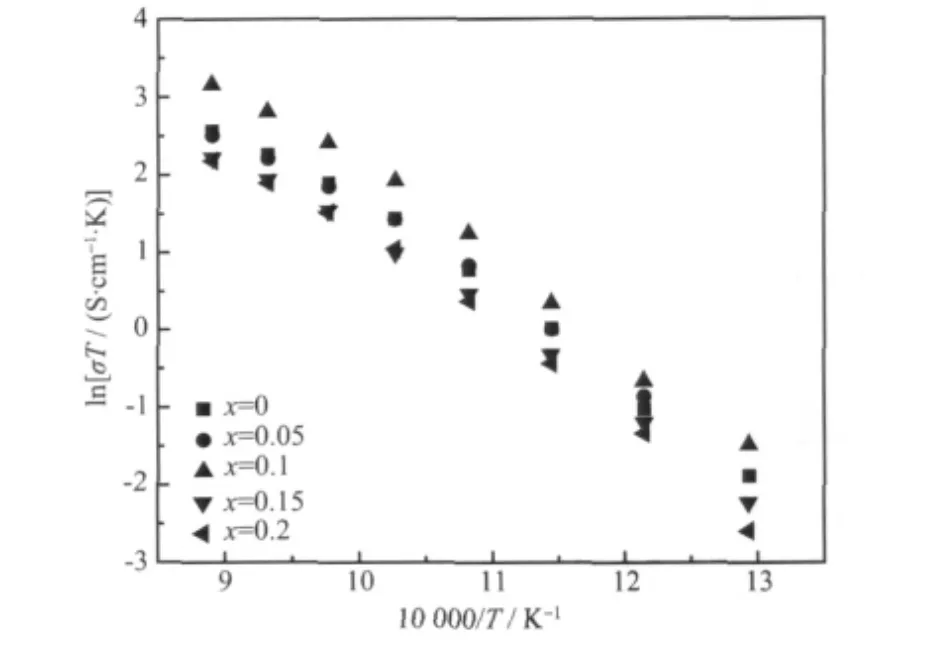
图8 La2-xCaxCe2O7-δ(0≤x≤0.2)在500~850 ℃、空气气氛下的Arrhenius 曲线Fig.8 Arrhenius plots of La2-xCaxCe2O7-δ(0≤x≤0.2) at 500~850 ℃in air
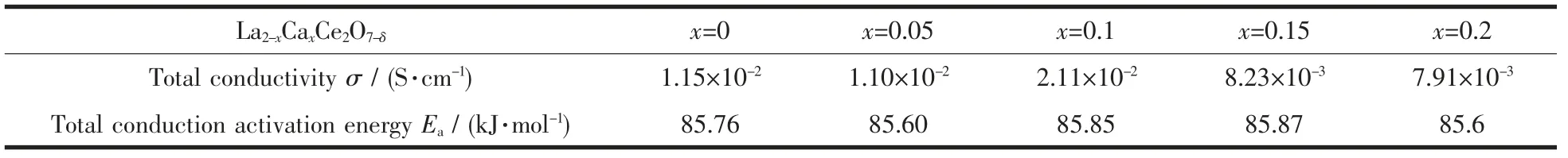
表2 La2-xCaxCe2O7-δ 在850 ℃、空气气氛下的总电导率和电导活化能Table 2 Activation energies and electrical conductivity of La2-xCaxCe2O7-δ at 850 ℃in air

表3 La2-xCaxCe2O7-δ 在850 ℃、湿润氢气气氛下的总电导率和电导活化能Table 3 Activation energies and electrical conductivity of La2-xCaxCe2O7-δ at 850 ℃in 4% H2/Ar
2.5 电导率及活化能计算
图8、 图9 分别为质子导体La2-xCaxCe2O7-δ在500~850 ℃、 空气和湿润氢气气氛下电导率与温度之间的关系曲线。La2-xCaxCe2O7-δ的电导率随着掺杂量的增加而发生变化。当x=0.1 时的电导率最大,850 ℃时在空气和湿润氢气气氛中分别为2.11×10-2S·cm-1和3.16×10-2S·cm-1。因此,Ca2+在La2Ce2O7中掺杂不仅可以抑制其结构相变,而且可以提高其电性能,为扩展质子导体La2Ce2O7的应用提供了可能。表2、 表3 分别为850 ℃时的总电导率和活化能。
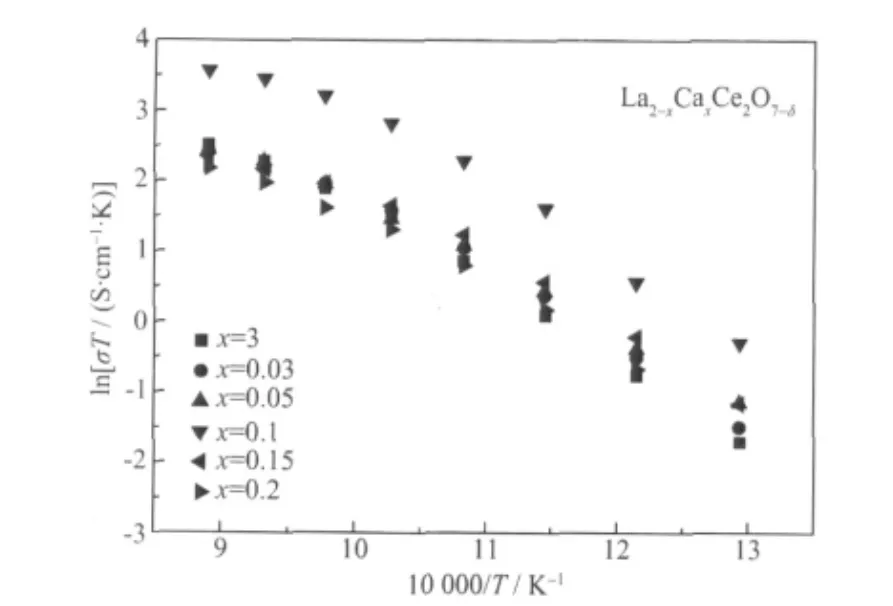
图9 La2-xCaxCe2O7-δ(0≤x≤0.2)在500~850℃、湿润氢气气氛下的Arrhenius 曲线Fig.9 Arrhenius plots of La2-xCaxCe2O7-δ(0≤x≤0.2) at 500~850 ℃in 4% H2/Ar
3 结 论
(1) 采用高温固相反应成功合成了高温质子导体La2-xCaxCe2O7-δ(0≤x≤0.2)材料,XRD 测试结果表明,试样经1 500 ℃烧结后匀形成萤石型结构。
(2) Ca 掺 杂 量 对La2-xCaxCe2O7-δ微 观 形 貌 的 影响研究表明,随着掺杂量的增加试样微观组织结构越来越致密。
(3) 质子导体La2-xCaxCe2O7-δ的电导率随着掺入Ca2+的增加,呈现先降低后增加再降低的趋势,当x=0.1 时,850 ℃时在空气和湿润氢气气氛中电导率分别为2.11×10-2S·cm-1、3.16×10-2S·cm-1,电导活化能分别为85.85 kJ·mol-1、84.93 kJ·mol-1。
(4) 高温质子导体La2-xCaxCe2O7-δ在CO2和H2O气氛中表现出良好的化学稳定性。
[1] Iwahara H, Esaka T, Uchida H, et al. Solid State Ionics,1981,3-4:359-363
[2] Iwahara H, Yajima T, Hibino T, et al. Solid State Ionics,1993,61(1/2/3):65-69
[3] Wilde P J, Catlow C R A. Solid State Ionics, 1998,112:173-183
[4] Bemhardt J W, Kevin W E, Catherine H, et al. Solid State Ionics, 2000,129:111-133
[5] Labrincha J A,Frade J R,Marques F M B. Solid State Ionics,1997,99:33-40
[6] Matsumoto H, Hamajima S, Yajima T, et al. J. Electrochem.Soc., 2001,148:252-254
[7] Omata T, Ikeda K, Tokashiki R, et al. Solid State Ionics,2004,167:389-397
[8] Lin B, Wang S L, Liu X Q, et al. J. Alloys Compd., 2009,478:355-357
[9] Erickson E E, Gray D, Taylor K, et al. Mater. Res. Bull.,2002,37:2077-2083
[10]Omata T, Okuda K, Tsugimoto S, et al. Solid State Ionics,1997,104:249-258
[11]Rhodes J M.Thesis for the Doctorate of University of Florida.2005.
[12]Wang J D, Xie Y H, Zhang Z F, et al. Mater. Res. Bull.,2005,40:1294-1302
[13]Tao Z T, Bi L, Fang S M, et al. J. Power Sources, 2011,196:5840-5843
[14]Yan L T, Sun W P, Bi L, et al. Int. J. Hydrogen Energy,2010,35:4508-4511
[15]Fang S M, Bi L, Yan L T, et al. J. Phys. Chem. C, 2010,114:10986-10991
[16]Tao Z T, Bi L, Fang S M, et al. J. Power Sources, 2011,196:5840-5843
[17]Xie K, Yan R Q, Liu X Q. Electrochem. Commun., 2009,11(8):1618-1622
[18]Potter A R, Baker R T. Solid State Ionics, 2006,177(19-25):1917-1924
[19]Bohn H G, Schober T. J. Am. Ceram. Soc., 2000,83(4):768-772
