7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮的合成及其与牛血清白蛋白的相互作用研究
2013-08-14杨绪红胡大为王晓东
杨绪红,胡大为,王晓东,刘 颖,於 智
(湖北科技学院核技术与化学生物学院,湖北 咸宁437100)
吖啶酮类化合物是一类具有良好生物活性的氮杂环化合物,具有杀菌、消炎、镇痛和抗癌等作用[1,2]。7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮(Y)是含有吖啶酮药效团的化合物之一,同时由于其羰基的邻位含有α-H,可以与其它药物基团进行分子对接,因此也是进一步合成新药物的优良中间体。
作者参照文献[3],以5-氯-2-氨基二苯甲酮与1,3-环己二酮在碘催化下合成7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮(Y)。通过IR、1HNMR、13CNMR、MS及元素分析对其结构进行了确证;并用荧光猝灭法在模拟人体生理条件下研究 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与牛血清白蛋白(BSA)的相互作用,得出两者相互作用的结合常数、结合位点数及热力学参数,拟为该类物质的合成及生物活性研究提供理论依据。7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮的合成路线见图1。
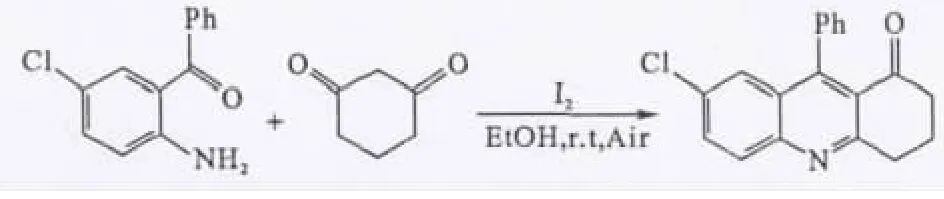
图1 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮的合成路线Fig.1 The synthetic route of 7-chloro-9-phenyl-3,4-dihydroacridin-1(2 H)-one
1 实验
1.1 试剂与仪器
5-氯-2-氨基二苯甲酮;1,3-环己二酮;牛血清白蛋白(BSA);三羟基甲氧基氨基甲烷(Tris试剂);其它试剂均为分析纯;实验用水为二次蒸馏水。
Shimadzu IRPrestige-21 型 红 外 光 谱 仪;JEOL-500MHz型核磁共振仪;VarioELⅢ型元素分析仪;HP5988A型质谱仪;YRT-3型熔点仪(温度计未经校正);JA5003型电子天平;F-4500型荧光光度计(带恒温系统);PH-3C型酸度计;CS501型超级恒温器。
1.2 方法
1.2.1 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮的合成
在50mL圆底烧瓶中加入1.1575g(5mmol)5-氯-2-氨基二苯甲酮、0.8338g(7.5mmol)1,3-环己二酮、10mL无水乙醇、0.0127g碘,在恒温35℃条件下磁力搅拌反应12h,减压脱除溶剂,将所得固体用无水乙醇重结晶,即得黄色产物,产率80%,熔点184~185℃。
1.2.2 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与 BSA相互作用的研究
参照文献[4]分别配制5.0×10-5mol·L-1BSA溶液及2.0×10-3mo1·L-17-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮溶液,于0~4 ℃保存。在模拟人体生理条件下(pH=7.4),固定BSA的量,激发波长为295 nm,测定 7-氯-9-苯 基-3,4-二 氢 吖 啶-1(2 H)-酮-BSA(Y-BSA)体系的荧光光谱,考察7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对BSA 的荧光猝灭情况;然后测定不同温 度 下 7-氯-9-苯 基-3,4-二 氢 吖 啶-1(2 H)-酮 对BSA的荧光猝灭情况,以确定荧光猝灭机理;最后计算7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与 BSA 相互作用的结合常数、结合位点数及热力学参数,确定作用力类型。
2 结果与讨论
2.1 产物结构表征
通过IR、1HNMR、13CNMR、MS及元素分析对产物结构进行确证。
1HNMR(CDCl3,500MHz),δ:8.0061~7.9877(d,J=9.2Hz,1H),7.6991~7.1529(m,7H),3.3726~3.3474(t,J1=6.3MHz,J2=6.4MHz),2.7233~2.7107(t,J1=6.3MHz,J2=6.85MHz),2.2641~2.2515(d,J=6.3MHz);13CNMR(CDCl3,125MHz),δ:197.86,162.26,150.61,147.12,136.95,132.71,132.51,130.27,128.45,128.01,127.99,126.84,124.52,77.42,77.17,76.92,40.70,34.63,21.36;IR(KBr),ν,cm-1:3068,3022,2953,1700,1601,1473,1385;MS(ESI),m/z:308([M+H]+);C19H14NOCl元素分析实测值(理论值):C 74.15(74.08),H 4.58(4.75),N 4.55(4.51)。所有数据解析均与目标化合物结构相符,证明成功合成了7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮。
2.2 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对 BSA 荧光光谱的影响(图2)
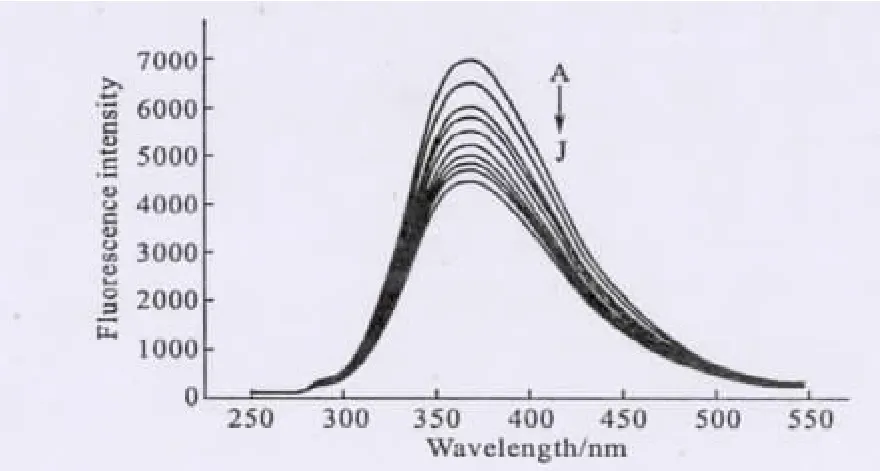
图2 7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对BSA荧光光谱的影响Fig.2 The fluorescence spectra of BSA in the presence of 7-chloro-9-phenyl-3,4-dihydroacridin-1(2 H)-one
由图2可知,BSA在375nm附近有较强的荧光峰,随着体系中7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮浓度的增大,BSA的内源荧光强度有规律地降低,而峰的形状保持不变,说明7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对 BSA 的荧光有猝灭作用。
2.3 荧光猝灭机理
荧光猝灭过程分动态猝灭过程与静态猝灭过程。动态猝灭过程中随温度的升高猝灭常数相应增大,静态猝灭过程中随温度的升高猝灭常数相应减小[5,6]。荧光猝灭遵循Stern-Volmer方程[7,8],即:

测定温度分别为298K、302K、306K、310K时7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对 BSA 的荧光猝灭情况,绘制Stern-Volmer曲线,见图3。
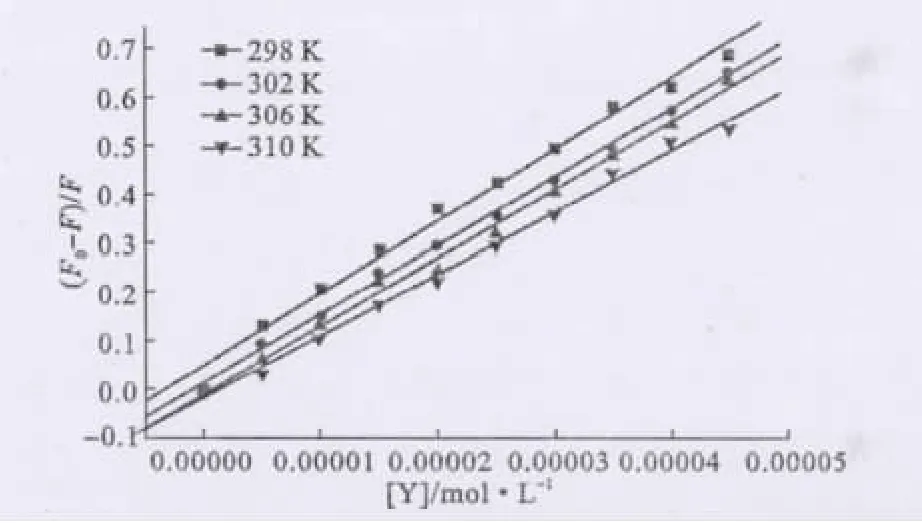
图3 不同温度下,Y-BSA体系的Stern-Volmer曲线Fig.3 The Stern-Volmer plots of Y-BSA system at different temperatures
根据式(1)计算pH=7.4时不同温度下的猝灭常数KSV,见表1。

表1 不同温度下的猝灭常数KSV/×105 L·mol-1Tab.1 The quenching constant KSVat different temperatures/×105 L·mol-1
由表1可知,随着温度的升高,KSV减小,表明7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对 BSA 的荧光猝灭过程为静态猝灭过程。
2.4 结合常数与结合位点数
7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与 BSA 的表观结合常数Kb和结合位点数n根据式(2)计算[9]:

绘制不同温度下的lg[(F0-F)/F]~lg[Y]曲线,见图4。
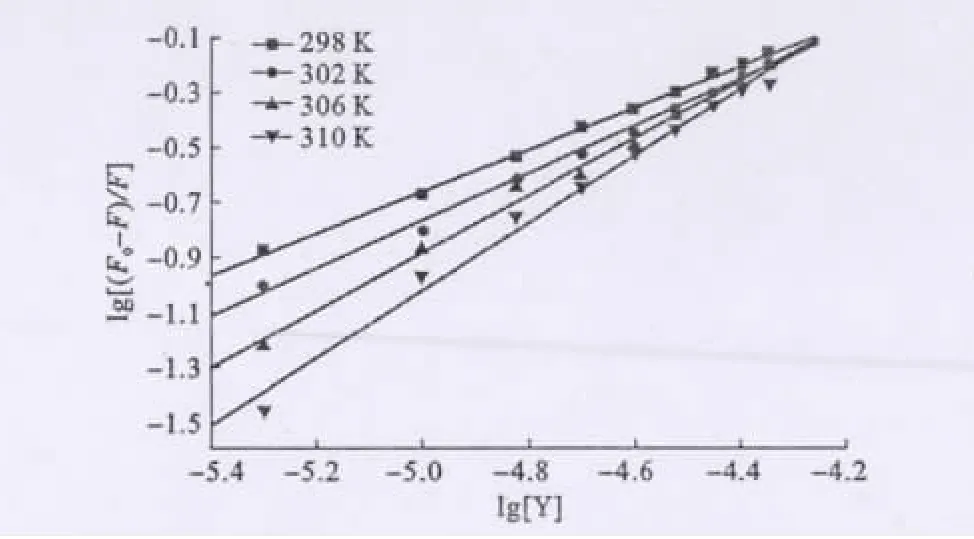
图4 不同温度下,Y-BSA体系的lg[(F0-F)/F]~lg[Y]曲线Fig.4 The lg[(F0-F)/F]~lg[Y]plots of Y-BSA system at different temperatures
依直线的斜率和截距求得化合物7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与 BSA 的表观结合常数 Kb和结合位点数n,见表2。
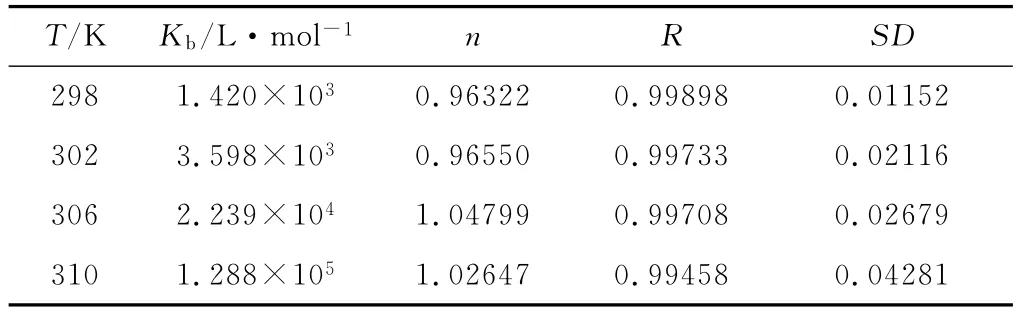
表2 结合常数Kb和结合位点数nTab.2The binding constant Kband the binding site n
由表2可知,在298K、302K、306K、310K下的平均结合常数为3.9044×104L·mol-1,结合位点数约为1,表明7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮分子与BSA分子以1∶1结合。
2.5 作用力类型
蛋白质与小分子之间的作用力类型可根据反应前后热力学常数焓变(ΔH)和熵变(ΔS)的正负来判断:ΔS>0、ΔH>0时,为疏水作用力;ΔS<0、ΔH<0时,为氢键和范德华力;ΔS>0、ΔH≈0时,为静电引力[10-12]。热力学参数可根据式(3)、式(4)计算:

绘制 Van′t Hoff曲线(lnK~1/T 曲线),见图5。
不同温度下的热力学参数ΔH、ΔG、ΔS见表3。
由表3可知,ΔH>0、ΔS>0,表明7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与BSA的作用力类型主要是疏水作用力。
3 结论
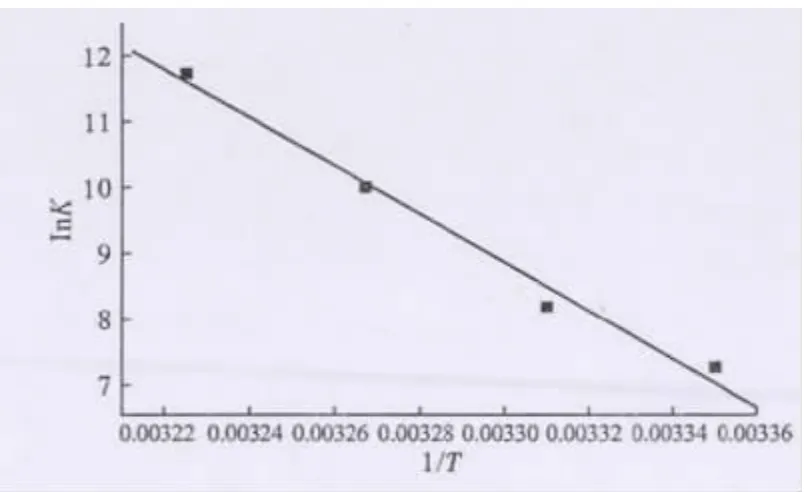
图5 Van′t Hoff曲线Fig.5 The Van′t Hoff plot

表3 不同温度下7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮与BSA作用的热力学参数Tab.3 The thermodynamic parameters for the interaction between 7-chloro-9-phenyl-3,4-dihydroacridin-1(2 H)-one and BSA at different temperatures
7-氯-9-苯基-3,4-二氢吖啶-1(2 H)-酮对牛血清白蛋白(BSA)具有良好的静态猝灭作用,其相互作用的结合常数为3.9044×104L·mol-1,结合位点数约为1,主要作用力类型为疏水作用力。
[1]欧阳杰,刘润南,王进军.吖啶酮类高效镇痛药物的研究(Ⅰ):6,7-亚甲二氧基-3-芳-1(2 H,4 H)吖啶酮的合成[J].吉林化工学院学报,1992,9(2):22-26.
[2]李少斌,赵会君,罗田伟,等.吖啶酮类化合物逆转肿瘤耐药的研究进展[J].时代教育:教育教学刊,2011,(10):7-8.
[3]Wu J,Xia H G,Gao K.Molecular iodine:A highly efficient catalyst in the synthesis of quinolines via Friedlnder annulation[J].Organic & Biomolecular Chemistry,2006,4:126-129.
[4]方强,汤从海,郭明,等.荧光猝灭法研究2,6-二(邻甲基苯亚甲基)环己酮与牛血清白蛋白的相互作用[J].凯里学院学报,2010,28(6):77-79.
[5]Laconic J R.Pdinciples of Fluorescence Spectroscopy[M].New-York:Plenum Press,1983:257.
[6]Hu Y J,Li W,Liu Y,et al.Fluorometric investigation of the interaction between methylene blue and human serum albumin[J].Journal of Pharmaceutical and Biomedical Analysis,2005,39(3-4):740-745.
[7]Hu Y J,Liu Y,Shen X S,et al.Studies on the interaction between 1-hexylcarbamoyl-5-fluorouracil and bovine serum albumin[J].Journal of Molecular Structure,2005,738(1-3):143-147.
[8]李锐,代本才,赵永德,等.光谱法在分子间非共价相互作用中的应用及进展[J].光谱学与光谱分析,2009,29(1):240-243.
[9]刘永明,李桂芝.荧光猝灭法研究依诺沙星和蛋白质的相互作用[J].应用化学,2004,21(6):621-624.
[10]Némethy G,Scheraga H A.Structure of water and hydrophobic bonding in proteins.Ⅰ.A model for the thermodynamic properties of liquid water[J].The Journal of Chemical Physics,1962,36(12):3382-3400.
[11]Timasheff S,Peeters H.Protein of Biological Fluids[M].Oxford:Pergamon Press,1972:511.
[12]Ross P D,Subramanian S.Thermodynamics of protein association reactions:Forces contributing to stability[J].Biochemistry,1981,20(11):3096-3102.
