贮藏温度对红肉脐橙(Citrus sinensis Osbeck)果实类胡萝卜素含量的影响
2013-08-07王长锋陶能国黄师荣
王长锋,陶能国*,黄师荣
(湘潭大学化工学院,湖南 湘潭 411105)
果实色泽是柑橘的主要外观品质,随着人们生活水平的提高,果实色泽已悄然成为消费者判断果品接受与否或者物有所值的重要参考[1]。类胡萝卜素是绝大多数柑橘品种的着色物质,其合成受品种、成熟度、采收期、贮藏方式、贮藏条件和环境因素等的综合影响[2-5]。医学研究表明,柑橘果实类胡萝卜素还具有清除人体有害自由基、增强人体免疫力、预防心血管疾病、防癌抗癌和预防维生素A缺乏症等功能[6]。因此,柑橘果实类胡萝卜素代谢已逐渐引起人们的浓厚兴趣。
红肉脐橙(Citrus sinensis Osbeck)是华盛顿脐橙的天然芽变,是迄今世界上唯一果肉因含番茄红素和β-胡萝卜素而着色粉红的脐橙品种,20世纪80年代发现于委内瑞拉,1990年由华中农业大学柑橘研究所从美国引种至我国,在湖北、湖南、浙江、江西和福建等我国柑橘主产区均有一定面积的栽培[1,7-8]。此外,红肉脐橙果实还含大量的线性类胡萝卜素(如八氢番茄红素等),加之果实类胡萝卜素代谢途径未产生突变,因而成为研究柑橘果实类胡萝卜素代谢的理想材料[9-11]。
本研究拟以红肉脐橙为材料,探讨常温和低温贮藏对柑橘果皮和果肉类胡萝卜素含量的影响,以期为通过调节贮藏温度改善柑橘果实色泽品质提供理论参考。
1 材料与方法
1.1 材料与试剂
红肉脐橙(C. sinensis Osbeck)果实取自华中农业大学柑橘研究所,果实于2009年12月26日采收。低温贮藏的样品直接放置于4℃恒温保鲜柜,常温处理的样品则置于20℃培养箱中保存,每80个果实为1小区,3次重复。从采收当天开始,每隔1周收集果皮和果肉,冷冻干燥后用液氮研磨成粉末备用。
甲醇、乙腈、MTBE(色谱纯) 美国Fisher公司;正己烷、丙酮、无水乙醇、氯化钠、氢氧化钾(分析纯) 湖南师大化学试剂厂;番茄红素、β-胡萝卜素标准品 美国Sigma公司;β-隐黄素、叶黄素、反式紫黄质、八氢番茄红素、花药黄质、α-胡萝卜素标准品 瑞士Carote Nature公司。
1.2 仪器与设备
Thermo 706超低温冰箱、FS60超声波振荡仪 美国Thermo Fisher Scientific公司;J-20XP离心机 美国Beckman公司;5301真空浓缩仪 德国Eppendorf公司;Direct-Q3超纯水制备设备 法国Millipore公司;U-2800紫外可见分光光度计 日本Hitachi公司;1525高效液相色谱仪 美国Waters公司。
1.3 类胡萝卜素提取
类胡萝卜素的提取参考Lee[7]方法稍有改进。分别称取0.5g左右果皮和果肉干样,加15mL提取剂(正己烷:丙酮:无水酒精=2:1:1,V/V,含0.1‰ BHT),超声波萃取30min后4000×g离心10min,沉淀用15mL提取剂重复提取2次至无色。合并上清液,用饱和NaCl水溶液反复洗3次至中性,吸取上层液,用正己烷定容至20mL,将上层液旋转蒸发至干,溶于2mL甲基叔丁基醚(MTBE)(含0.1‰ BHT),再加2mL 10% KOH-甲醇溶液避光条件下皂化10h。加4mL饱和NaCl水溶液和2mL MTBE(含0.1‰ BHT)使之更好的分层,洗走水层,再加3次5mL饱和NaCl水溶液洗至中性。将上清液旋转蒸发后用1mL MTBE(含0.1‰ BHT)溶解定容备用。
1.4 类胡萝卜素的HPLC分析
HPLC分析条件:2996PDA检测器,YMCC30色谱柱;流动相:A:乙腈:甲醇=3:1 (含0.0l% BHT,0.05% TEA),B:100% MTBE(含0.01% BHT);流速为lmL/min;上样体积为20μL,检测波长设定为450nm。梯度洗脱:0min,A:B(95:5);0~10min,A:B(95:5);10~19min,A:B(86:14);19~29min,A:B(75:25);29~54min,A:B(50:50);54~66min,A:B(26:74);67min,A:B(95:5)。
Empower软件控制及数据处理系统处理色谱结果。各组分含量以μg/g干质量(μg/g DW)表示,总类胡萝卜素含量以各鉴定组分的含量之和计算。番茄红素、β-胡萝卜素、β-隐黄素、叶黄素、反式紫黄质、八氢番茄红素、花药黄质和α-胡萝卜素含量根据相应的标准曲线计算;α-隐黄素和顺式紫黄质的含量参照β-隐黄素和反式紫黄质的标准曲线计算。
1.5 数据分析
每组有3次重复,采用常规的分析方法来标注标准偏差,数据分析采用SPSS16.0统计分析软件,ANOVA来分析显著性差异(P<0.05)。
2 结果与分析
2.1 红肉脐橙果实类胡萝卜素的组成
采用反相高效液相色谱(reversed phase-high performance liquid chromatography,RP-HPLC)技术,根据组分保留时间,比较标准品以及PDA检测器检测出的波谱特点,并参照前人文献[7,12],初步鉴定了红肉脐橙果皮和果肉中类胡萝卜素的各种组分(表1)。红肉脐橙果皮共鉴定组分15个,分别为反式紫黄质、顺式紫黄质、花药黄质、叶黄素、八氢番茄红素、玉米黄素、β-隐黄素、ζ-胡萝卜素、α-胡萝卜素和β-胡萝卜素等;红肉脐橙果肉类胡萝卜素共鉴定出组分16个,分别为反式紫黄质、顺式紫黄质、花药黄质、叶黄素、α-隐黄素、八氢番茄红素、玉米黄素、β-隐黄素、α-胡萝卜素、β-胡萝卜素、番茄红素顺式异构体和番茄红素等。
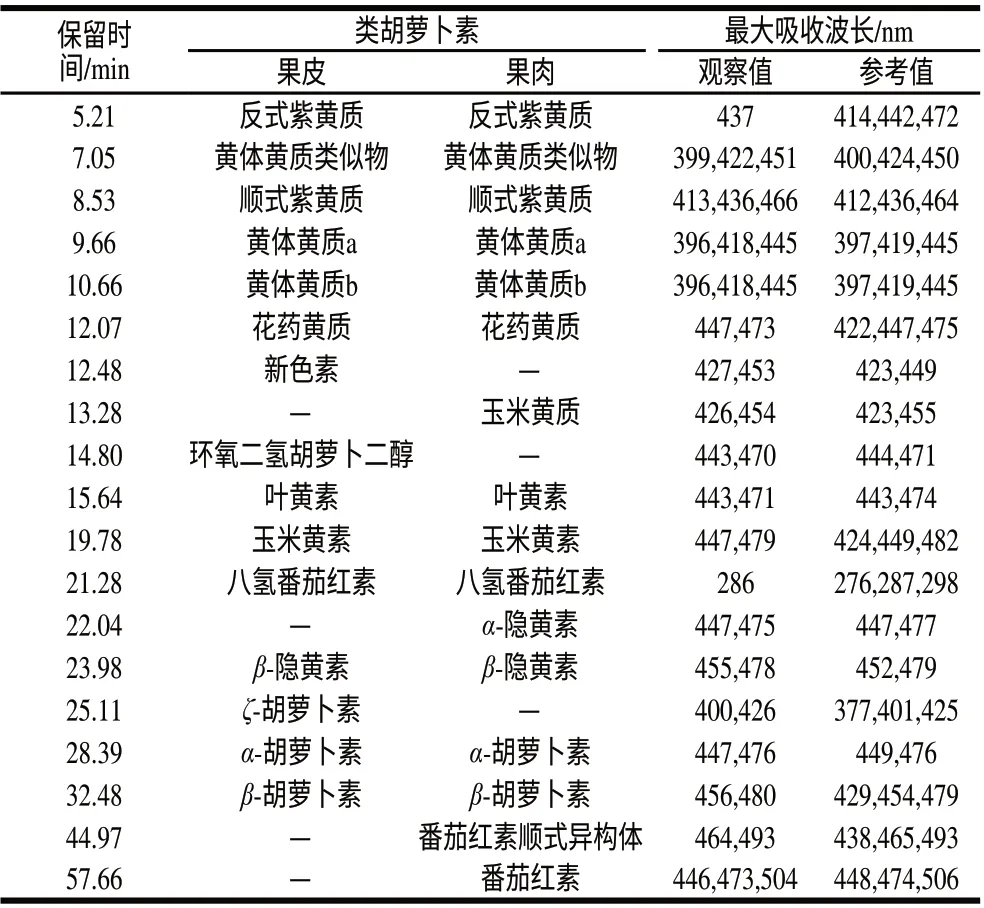
表 1 红肉脐橙果实类胡萝卜素组分的色谱和光谱特点Table 1 Chromatographic and spectral characteristics of the identifed carotenoids in ‘Cara Cara’ fruit
2.2 贮藏温度对红肉脐橙果皮类胡萝卜素组分的影响
从图1可以看出,贮藏的前5周内,常温有利于红肉脐橙果皮总类胡萝卜素和各类胡萝卜素组分的积累,随着贮藏时间延长,这种优势逐渐被低温取代。常温条件下,红肉脐橙果皮总类胡萝卜素和各组分含量呈现出现一个逐步上升的趋势,这种趋势随着贮藏时间的延长而减弱直至含量降低,且不同组分出现含量高峰的时间差别较大。其中,总类胡萝卜素、八氢番茄红素、β-胡萝卜素、α-胡萝卜素、花药黄质、反式紫黄质、顺式紫黄质于采后3周达到高峰,含量分别为(464.70±45.37)、(212.88±25.28)、(3.73±0.57)、(2.39±0.35)、(10.48±1.91)、(59.99±3.99)和(159.42±9.66)μg/g(以干质量计,下同);而玉米黄素和β-隐黄素的含量高峰则出现在采后第1周,含量分别为(1.39±0.18)μg/g和(14.15±2.83)μg/g;叶黄素的含量甚微,勉强能检测到。常温贮藏6周后,红肉脐橙果皮总类胡萝卜素和各类胡萝卜素含量基本保持稳定。对低温贮藏而言,红肉脐橙果皮总类胡萝卜素和各类胡萝卜素组分含量随贮藏时间延长逐渐增加。总类胡萝卜素、八氢番茄红素、α-胡萝卜素、β-隐黄素、反式紫黄质和顺式紫黄质含量于采后第9周达到峰值,分别为(327.18±58.59)、(123.63±19.43)、(1.78±0.20)、(42.45±6.45)、(28.47±6.48)μg/g和(120.64±23.69)μg/g;叶黄素、β-胡萝卜素、玉米黄素和花药黄质的峰值出现在采后第6周,含量分别为(1.11±0.22)、(1.91±0.13)、(1.60±0.19)μg/g和(5.10±0.54)μg/g;随着贮藏时间的延长,总类胡萝卜素和各组分含量基本保持不变。
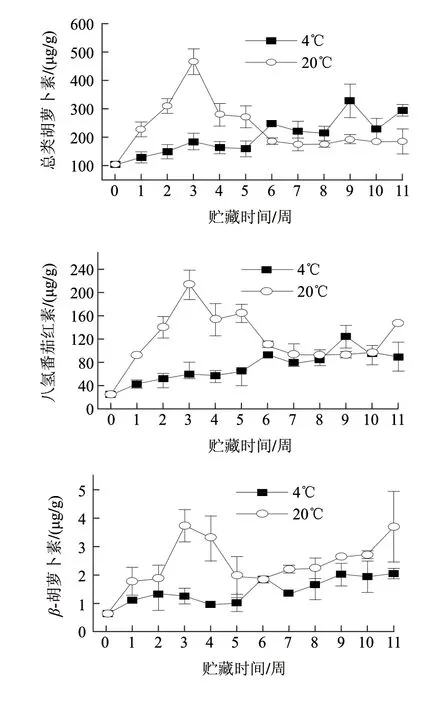
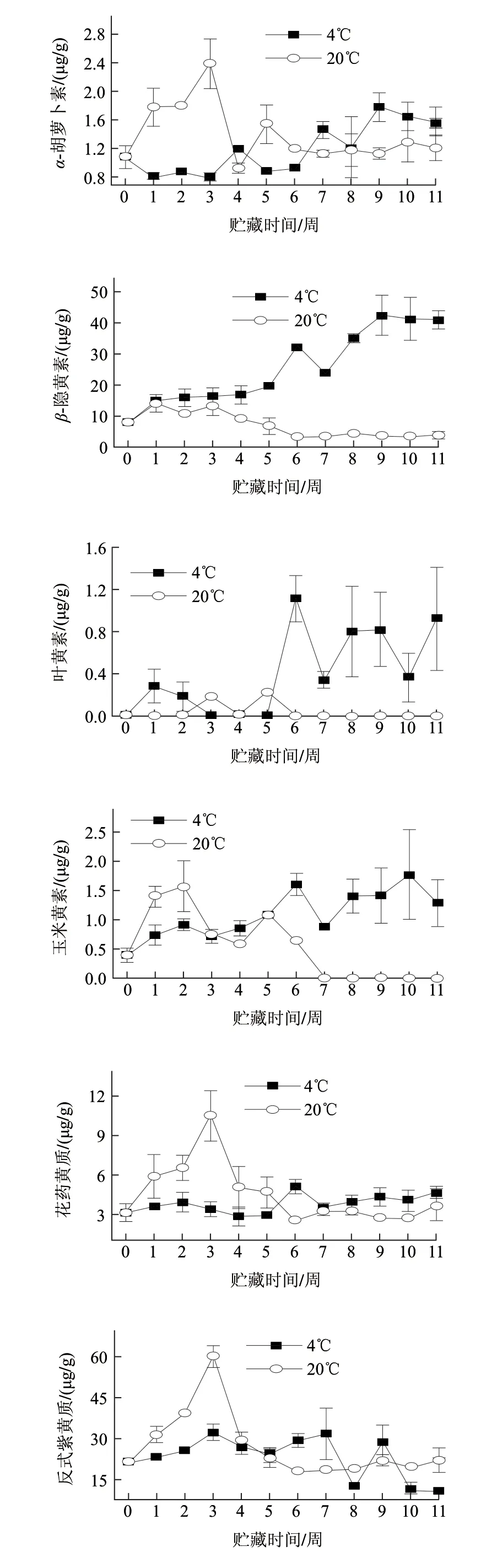

图 1 贮藏温度对红肉脐橙果皮类胡萝卜素含量影响Fig.1 Effect of storage temperature on carotenoid contents
2.3 贮藏温度对红肉脐橙果肉类胡萝卜素组分的影响
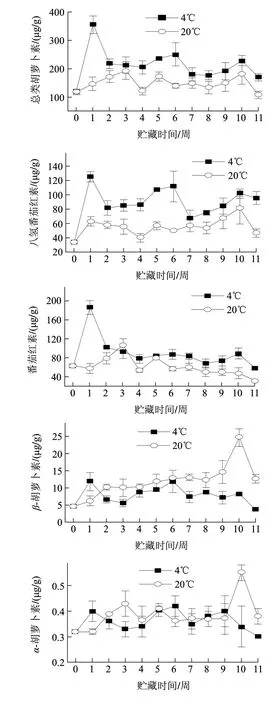

图 2 贮藏温度对红肉脐橙果肉类胡萝卜素含量影响Fig.2 Effect of storage temperature on carotenoid contents
从图2可以看出:低温有利于红肉脐橙果肉类胡萝卜素的积累。低温贮藏条件下,红肉脐橙果肉总类胡萝卜素、八氢番茄红素、番茄红素、α-胡萝卜素、β-胡萝卜素、β-隐黄素和叶黄素于采后第1周达到峰值,含量分别为(278.00±21.85)、(125.03±7.23)、(185.33±14.57)、(0.40±0.04)、(11.79±2.63)、(5.11±1.03)μg/g和(3.98±0.90)μg/g,且含量显著高于常温贮藏(P<0.05),随着贮藏时间延长,上述组分含量基本保持稳定。常温条件下,红肉脐橙果肉β-胡萝卜素、α-胡萝卜素、α-隐黄素、β-隐黄素和叶黄素含量缓慢上升,贮藏10周时达到峰值(24.56±2.56)、(0.55±0.03)、(3.71±0.05)、(3.55±0.21) 和(5.55±0.07)μg/g,随后下降至采收时水平;番茄红素含量于采后第3周达到峰值(105.88±14.03)μg/g,随后逐渐下降,至第11周时显著低于采收时含量。常温和低温贮藏的红肉脐橙果肉花药黄质含量变化趋势类似,贮藏3周时达到峰值(4.49±0.63)μg/g和(5.35±0.31)μg/g,且两者间含量无显著差异(P>0.05),随后逐渐降低。常温贮藏的红肉脐橙果肉顺式紫黄质和反式紫黄质出现两个小高峰,分别为贮藏第1周和第10周;而低温贮藏的红肉脐橙果肉顺式紫黄质和反式紫黄质两个高峰出现的时间则分别为第5周和第10周。
3 讨 论
温度是柑橘果实采后贮藏条件中对果实品质影响最大的环境因子[13]。类胡萝卜素对温度极其敏感,偏离最佳着色温度1℃都可以对果实着色产生显著影响[14]。对柑橘果实色泽而言,15~25℃的温度有利于果皮黄色类胡萝卜素的积累,但柑橘果肉中类胡萝卜素的含量基本保持稳定[15-17]。
本研究也表明,采后红肉脐橙果皮和果肉类胡萝卜素的代谢存在明显差别。常温(20℃)不仅促进红肉脐橙果皮玉米黄素和紫黄质的积累,而且还能促进八氢番茄红素等线性类胡萝卜素的积累,从而使总类胡萝卜素含量增加。这一结果与前人关于常温(20℃)通常有利于温州蜜柑黄色类胡萝卜素(如β-胡萝卜素、β-隐黄素、玉米黄素和紫黄质)的积累,促进柑橘果实着色的报道相似[16]。奇怪的是,红肉脐橙果皮β-隐黄素在贮藏1周时少量增加,随后保持较稳定的水平,随着贮藏时间延长至5周后又逐渐下降,显著低于采收时的含量(P<0.05)。出现这一现象可能与品种特性有关。Van Wyk等[18]研究发现, 20℃能导致Palmer脐橙果皮着色品质下降。常温贮藏的红肉脐橙果肉除β-胡萝卜素、叶黄素,α-隐黄素含量于采后第10周急剧上升外,其余类胡萝卜素含量只在贮藏前1周内小幅增加,随后保持较为稳定的水平。
与前人报道类似[16],在贮藏初期,低温(4℃)能基本保持红肉脐橙果皮总类胡萝卜素和各组分的含量,但随着贮藏时间的延长,各组分呈现缓慢增加的趋势,特别是八氢番茄红素和β-隐黄素的含量在采后5周后急剧增加;而低温(4℃)贮藏诱导红肉脐橙果肉八氢番茄红素、番茄红素、β-胡萝卜素、β-隐黄素、叶黄素和紫黄质等的积累。根据前人报道,番茄红素的最佳合成温度为15~25℃,5℃的低温能显著抑制番茄红素的合成[19]。因此,低温条件下红肉脐橙果肉番茄红素的积累说明形成番茄红素的上游途径开始大量启动。在植物类胡萝卜代谢途径中,八氢番茄红素的合成是关键步骤之一,受八氢番茄红素合成酶(PSY)基因的遗传控制,该基因的表达与柑橘果实类胡萝卜素含量呈明显的正相关[9-11,20]。从代谢途径分析,红肉脐橙八氢番茄红素含量增加可能与低温诱导PSY基因上调表达有关。这一假设与总类胡萝卜素含量和番茄红素下游代谢物(如β-胡萝卜素、β-隐黄素、叶黄素和紫黄质等)的增加相吻合。
4 结 论
本研究结果表明,贮藏温度对红肉脐橙果皮和果肉类胡萝卜素含量的影响存在组织特异性。常温(20℃)对红肉脐橙果皮着色的积极作用只维持在贮藏的前5周;低温(4℃)能基本保持贮藏初期果皮类胡萝卜素含量,但含量低于常温贮藏。除贮藏10周时β-胡萝卜素、叶黄素、α-隐黄素含量有一个小幅增加外,常温对红肉脐橙果肉类胡萝卜素总体影响不大;低温贮藏的红肉脐橙果肉类胡萝卜素含量于采后1周达到峰值,随后含量基本保持稳定。
[1] 徐娟.几个柑桔产区果实色泽评价及红肉脐橙(Citrus sinensis L. cv. Cara Cara)果肉呈色机理初探[D]. 武汉: 华中农业大学, 2002.
[2] FANCIULLINO A L, DHUIQUE-MAYER C, LURO F, et al. Carotenoid diversity in cultivated citrus is highly influenced by genetic factors[J]. Journal of Agricultural and Food Chemistry, 2006, 54(12): 4397-406.
[3] MOULY P P, GAYDOU E M, LAPIERRE L, et al. Differentiation of several geographical origins in single-strength Valencia orange juices using quantitative comparaison of carotenoid profiles[J]. Journal of Agricultural and Food Chemistry, 1999, 47(10): 4038-4045.
[4] MATSUMOTO H, IKOMA Y, KATO M, et al. Quantification of carotenoids in citrus fruit by LC-MS and comparison of patterns of seasonal changes for carotenoids among citrus varieties[J]. Journal of Agricultural and Food Chemistry, 2007, 55(6): 2356-2368.
[5] DHUIQUE-MAYER C, FANCIULLINO A L, DUBOIS C, et al. Effect of genotype and environment on citrus juice carotenoid content[J]. Journal of Agricultural and Food Chemistry, 2009, 57(19): 9160-9168.
[6] FRASER P D, BRAMLEY P M. The biosynthesis and nutritional uses of carotenoids[J]. Progress in Lipid Research, 2004, 43(3): 228-265.
[7] LEE H S. Characterization of carotenoids in juice of red navel orange (Cara Cara)[J]. Journal of Agricultural and Food Chemistry, 2001, 49(5): 2563-2568.
[8] XU Changjie, FRASER P D, WANG Weijie, et al. Differences in the carotenoid content of ordinary citrus and lycopene-accumulating mutants[J]. Journal of Agricultural and Food Chemistry, 2006, 54(15): 5474-5481.
[9] TAO Nengguo, HU ZhiYong, LIU Qin, et al. Expression of phytoene synthase gene (Psy) is enhanced during fruit ripening of Cara Cara navel orange (Citrus sinensis Osbeck)[J]. Plant Cell Reports, 2007, 26(6): 837-843.
[10] ALQUÉZAR B, RODRIGO M J, ZACARÍAS L. Regulation of carotenoid biosynthesis during fruit maturation in the red-fleshed orange mutant Cara Cara[J]. Photochemistry, 2008, 69(10): 1997-2007.
[11] FANCIULLINO A L, CERCÓS M, DHUIQUE-MAYER C, et al. Changes in carotenoid content and biosynthetic gene expression in juice sacs of four orange varieties (Citrus sinensis) differing in flesh fruit color[J]. Journal of Agricultural and Food Chemistry, 2008, 56(10): 3628-3638.
[12] LIU Qin, XU Juan, LIU Yongzhong, et al. A novel bud mutation that confers abnormal patterns of lycopene accumulation in sweet orange fruit (Citrus sinensis L. Osbeck)[J]. Journal of Experimental Botany, 2007, 58(15/16): 4161-4171.
[13] TIETEL Z, LEWINSOHN E, FALLIK, E. Importance of storage temperatures in maintaining flavor and quality of mandarins[J]. Postharvest Biology and Technology, 2012, 64(1): 175-182.
[14] YOUNG L B, ERICKSON L C. Influences of temperature on color change in Valencia oranges[J]. Proceedings of the American Society for Horticultural Science, 1961, 78: 197-200.
[15] WHEATON T A, STEWART I. Optimum temperature and ethylene concentration for postharvest development of carotenoid pigments in citrus[J]. Journal of the American Society for Horticultural Science, 1973, 98(2): 337-340.
[16] MATSUMOTO H, IKOMA Y, KATO M, et al. Effect of postharvest temperature and ethylene on carotenoid accumulation in the flavedo and juice sacs of Satsuma mandarin (Citrus unshiu Marc.) fruit[J]. Journal of Agricultural and Food Chemistry, 2009, 57(11): 4724-4732.
[17] RODRIGO M J, ZACARIAS L. Effect of postharvest ethylene treatment on carotenoid accumulation and the expression of carotenoid biosynthetic genes in the flavedo of orange (Citrus sinensis L. Osbeck) fruit[J]. Postharvest Biology and Technology, 2007, 43(1): 14-22.
[18] VAN WYK A A, HUYSAMER M, BARRY G H. Extended lowtemperature shipping adversely affects rind colour of ‘Palmer Navel’ sweet orange [Citrus sinensis (L.) Osb.] due to carotenoid degradation but can partially be mitigated by optimizing post-shipping holding temperature[J]. Postharvest Biology and Technology, 2009, 53(3): 109-116.
[19] JAVANMARDI J, KUBOTA C. Variation of lycopene, antioxidant activity, total soluble solids and weight loss of tomato during postharvest storage[J]. Postharvest Biology and Technology, 2006, 41(2): 151-155.
[20] KATO M, IKOMA Y, MATSUMOTO H, et al. Accumulation of carotenoids and expression of carotenoid biosynthetic genes during maturation in Citrus fruit[J]. Plant Physiology, 2004, 134(2): 824-837.
