基于化学传感体系的丙二酸阴离子比色识别研究*
2013-07-19汤立军唐炳涛
汤立军,赵 佳,唐炳涛
(1.渤海大学 化学系 辽宁省功能化合物的合成与应用重点实验室,辽宁 锦州 121013;2.大连理工大学 精细化工国家重点实验室,辽宁 大连 116024)
前 言
阴离子广泛存在于生物体系中,研究与开发能选择性识别特定阴离子的化学传感器受到了越来越多的关注[1~6]。在具有重要生物学意义的有机阴离子中,二元羧酸阴离子尤为引人注目,它们参与生物体内的代谢过程和能量储存,在各种生命过程中具有重要的作用[7~9],如丁二酸阴离子参与三羧酸循环[10],丙二酸和草酸阴离子能抑制琥珀酸脱氢酶的作用[11]。
纯水介质中阴离子的高选择性识别具有高度挑战性[12]。这是由于阴离子在水溶液中极易被溶剂化,水合能大,通常自身体积大、几何构型多样而且电荷密度低。近年来报道较多的光化学传感器大多利用胍基[13]、质子化氮杂冠醚[14]、咪唑[15]、脲[16]、吡啶阳离子[17]等作为阴离子键合基团设计合成,但通常由于受体水溶性差,与阴离子结合强度低等原因,绝大多数已报道的用于识别二元羧酸阴离子的光化学传感器都是在纯有机溶剂或者有机/水混合溶剂中应用的,这就降低了其实用价值。目前,在纯水介质中开展的二元羧酸阴离子的光化学传感识别研究尚不多见,仅有少数采用配位未饱和的过渡金属配合物型受体,基于指示剂置换法[18,19]而设计的光化学传感体系被报道[20~23]。
有关丙二酸阴离子光化学识别的研究尚不多见[24~27],且仅有的几例基本上都是在纯有机溶剂或有机/水混合体系中进行的,而在纯水介质中开展的识别研究工作尚未见报道。本文利用联二萘酚的分子骨架,设计合成了一种结构新颖的双核铜配合物(图式1)作为受体,并用该受体在纯水介质中开展了丙二酸阴离子的比色识别研究。
1 实验部分
1.1 主要试剂
(S)-2,2′-(1,1′-联萘-2,2′-二氧)-二乙酰氯(2)[28]和 2-(2′-(2-吡啶基)-乙基)氨基乙醇(3)[29]分别按文献方法合成,其它试剂和溶剂均为市售分析纯.
1.2 主要仪器
紫外可见分光光度计(SP-1900,上海光谱),核磁共振仪(400MHz,美国 Varian INOVA公司),液相色谱/质谱联用分析仪(Agilent1100,美国),显微熔点测定仪(北京泰克仪器有限公司)。
1.3 合成实验
配体 1 的合成:将 2(0.307g,0.7mmol)和三乙胺(0.2mL,1mmol)溶于 30mL干燥的 THF 中,搅拌下加入 3(0.152g,1mol),N2保护,室温搅拌 18h。旋干,用饱和的NaHCO3溶液冲洗固体,二氯甲烷萃取,柱层析分离后得产品0.145g,收率31%。熔点:152~154℃。1H NMR(400 MHz,CDCl3)δ 8.39(d,J=4.8 Hz,2H),7.93(dd,J=13.5,8.6 Hz,2H),7.85(d,J=7.7 Hz,2H),7.61(d,J=7.2 Hz,2H),7.43(dd,J=9.0,4.4Hz,2H),7.34 (d,J=7.2Hz,2H),7.22(d,J=7.3 Hz,3H),7.18-7.10(m,5H),4.72(t,J=10.7 Hz,2H),4.65 (d,J=13.2 Hz,2H),4.31 (dd,J=30.8,14.9Hz,4H),3.33 (dd,J=15.7,11.1Hz,4H),3.04(d,J=15.1 Hz,2H),2.92(dd,J=22.0,6.8 Hz,2H),1.26(s,2H)。ESI-MS(-)∶m/z669.0.
受体[Cu2(1)]4+的合成:将1(290mg,0.43mmol)和 CuCl2·2H2O(221.4mg,1.3mmol)溶于 30mL 无水乙醇中,搅拌,加热回流3h;冷却,过滤,用乙醇冲洗固体,晾干得固体 0.118g,收率 30%。ESI-MS(-)∶m/z939.0.
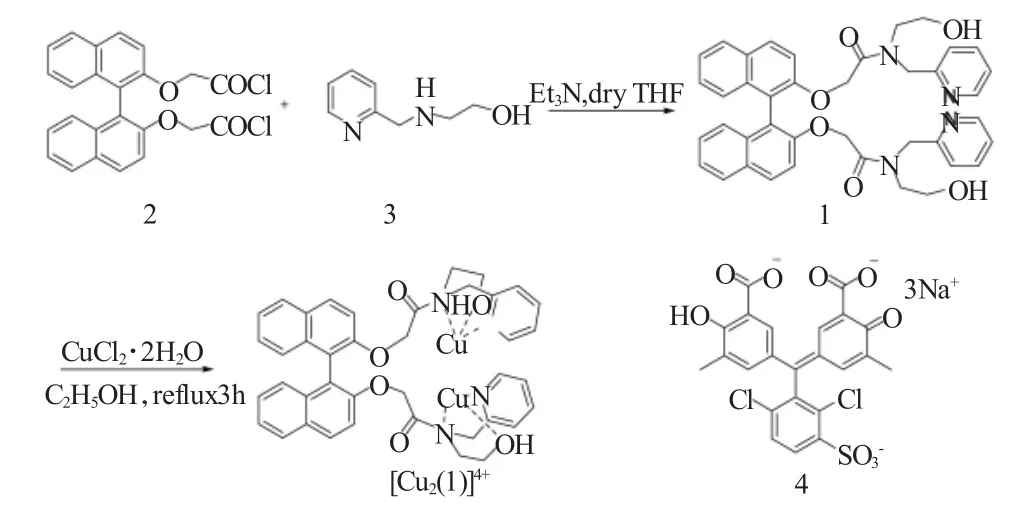
配体1及受体[Cu2(1)]4+的合成
1.4 光谱测试实验
1.4.1 受体对指示剂铬天青S(4)滴定
在铬天青S(4)的缓冲溶液(2.0×10-5M,HEPES 10mM,pH=7.0)中,分别加入不同体积的受体[Cu2(1)]4+的标准液(5.0×10-4M,HEPES 10mM,pH=7.0),控制加入的溶液体积不超过原受体溶液体积的3%。分别测试各试样的紫外光谱。
1.4.2 二元羧酸阴离子的识别
将各种二元羧酸阴离子的标准液(5.0×10-2M,HEPES 10mM,pH=7.0)分别加入到所确定的化学传感体系溶液中,测试各试样的紫外光谱。
1.4.3 丙二酸根对传感体系的滴定实验
向化学传感体系溶液中分别加入不同浓度的丙二酸阴离子,测试其紫外光谱。
1.4.4 其它二元羧酸阴离子对丙二酸根识别的干扰试验
向化学传感体系溶液中分别加入各种阴离子,然后再分别加入丙二酸根,测试每个试样的紫外光谱。
2 结果与讨论
2.1 化学传感体系的确定
在初步筛选实验的基础上,本文选择了铬天青S(4)作为构筑化学传感体系的指示剂。4的溶液为淡黄色,其最大吸收波长为424nm。随着向4(20μM)的溶液中逐渐增加受体[Cu2(1)]4+的浓度,在424nm处的吸光度逐渐降低,同时在592 nm处出现新的吸收峰并且吸光强度逐渐增大,溶液由黄色变为蓝色。当加入受体[Cu2(1)]4+为4的1倍时,溶液的紫外可见光谱不再发生明显变化,证明此时受体对指示剂的滴定已经达到饱和状态(图1)。由此确定使用1∶1物质的量比的受体-指示剂溶液作为化学传感体系。采用1∶1的结合模式的Benesi-Hildebrand方程[30]对滴定数据进行拟合,所得直线的线性相关系数为0.99,说明受体与指示剂以1∶1结合,表观结合常数为6.3×103M-1(图1内插图)。
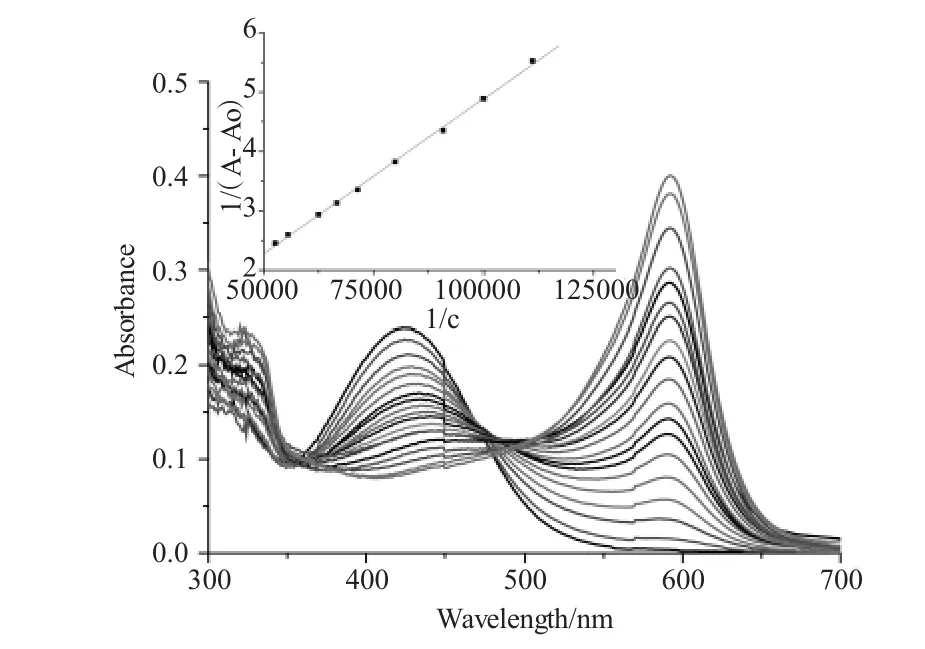
图1受体[Cu2(1]4+对指示剂铬天青S滴定的紫外-可见光谱变化Fig.1 Changes of Uv-vis absorption spectrum of indicator chromeazurol Supon titration by receptor[Cu2(1)]4+
2.2 化学传感体系对二元羧酸阴离子的选择性
化学传感体系(2.0×10-5M,HEPES 10mM,pH=7.0)对各种二元羧酸阴离子的选择性实验结果如图2所示。在相同的条件下,分别向化学传感体系溶液中加入10摩尔倍量(相对于化学传感体系)的各种二元羧酸阴离子(包括邻苯二甲酸,间苯二甲酸,对苯二甲酸,草酸,丙二酸,丁二酸,戊二酸,己二酸的相应阴离子),发现丙二酸阴离子能引起化学传感体系溶液的紫外可见光谱发生显著变化,592nm处的吸光度显著降低,而在424nm处的吸光度明显增强,溶液由蓝色变为黄绿色。其他二元羧酸阴离子对溶液的紫外可见光谱几乎没有显著影响。这表明只有丙二酸阴离子才能将指示剂从化学传感体系([Cu2(1)]4++铬天青S)中置换出来,也说明该化学传感体系对丙二酸阴离子具有很好的选择性。
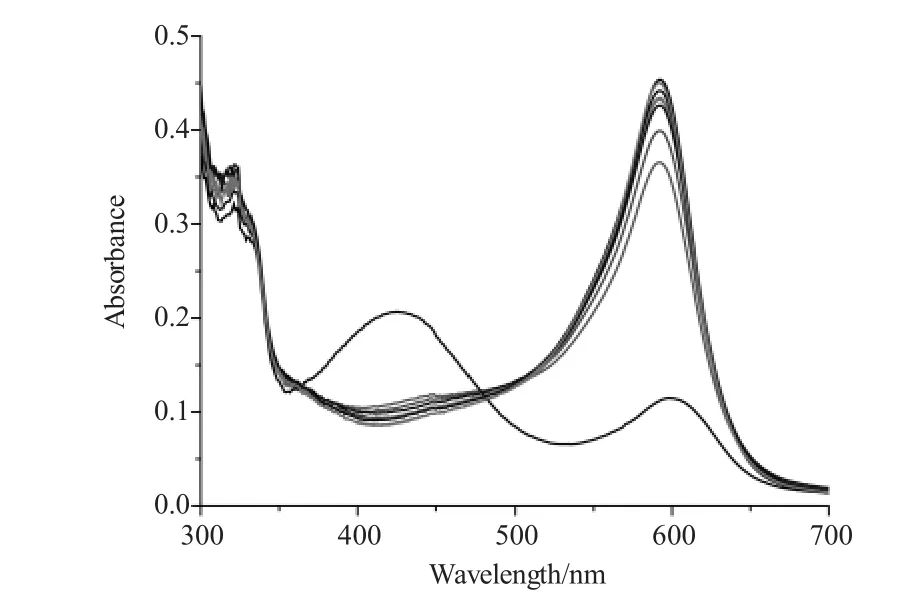
图2 各种二元羧酸阴离子对化学传感体系的紫外-可见光谱的影响Fig.2 Effects of various dicarboxylate on the Uv-vis spectrum of chemosensing ensemble
2.3 丙二酸阴离子对化学传感体系的滴定
为考察化学传感体系对丙二酸阴离子的传感性质,进行了丙二酸阴离子对化学传感体系的滴定实验(图3)。如图所示,当逐渐增加丙二酸阴离子的浓度后,化学传感体系溶液在592 nm处的吸光度逐渐降低,与此同时,在424 nm处的吸光度逐渐增强,当加入的丙二酸阴离子浓度为200μM时,滴定达到饱和。滴定实验结果表明所构筑的化学传感体系对丙二酸阴离子具有较好的传感性质。根据竞争键和平衡模型公式[31]对滴定数据进行拟合,得到一条直线,说明丙二酸阴离子与受体按照1∶1相结合,计算得出二者的表观结合常数为6.4×103M-1(图3内插图)。
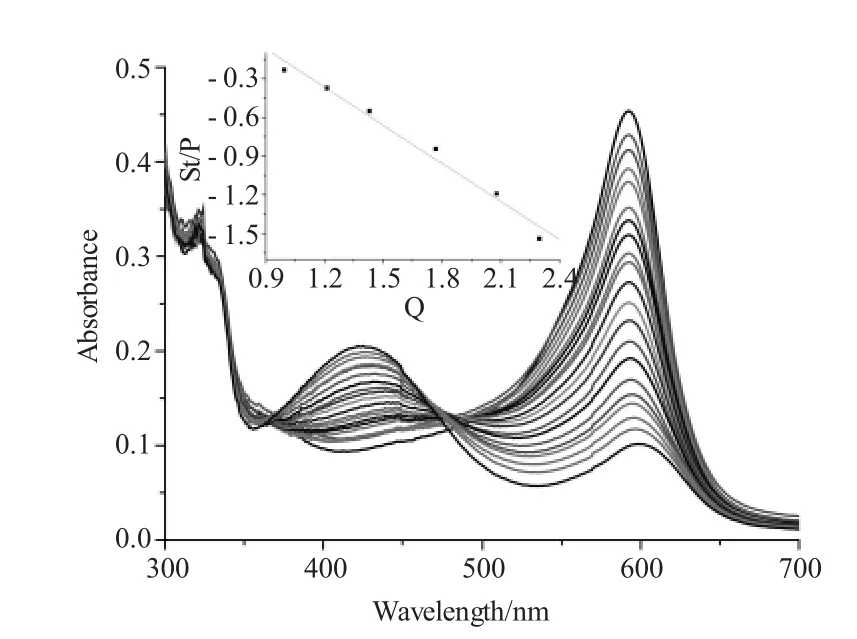
图3 丙二酸阴离子对化学传感体系溶液(20μM)滴定的紫外-可见光谱变化Fig.3 Changes of Uv-vis absorption spectrum of the chemosensing ensemble(20μM)upon titration bymalonate
2.4 其他阴离子对丙二酸根识别的影响
为考察其他二元羧酸阴离子对丙二酸阴离子识别的干扰情况,本文进行了竞争实验。在相同的条件下,在化学传感体系溶液中分别加入200μM的各种二元羧酸阴离子,如前所述,化学传感体系溶液的紫外-可见吸收光谱的均无显著变化。在此基础上,分别向各个试样溶液中继续加入200μM的丙二酸阴离子,所得溶液在592nm处的吸光度均显著降低,与单独加入丙二酸阴离子引起变化相似。这表明化学传感器对丙二酸阴离子的选择性识别基本不受其他共存的二元羧酸阴离子的干扰。
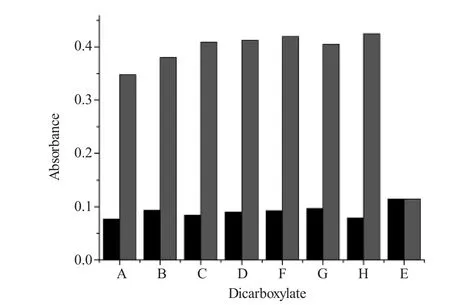
图4 其他二元羧酸阴离子对丙二酸根识别的影响Fig.4 Influences of other dicarboxylates on the recognition of malonate
3 结 论
设计合成了一种双核铜配合物[Cu2(1)]4+作为二元羧酸阴离子的受体,通过受体[Cu2(1)]4+对指示剂铬天青S的紫外-可见吸收光谱滴定实验确立了光化学传感体系(体系中铬天青S和1均为20 μM)。该化学传感体系在水溶液(HEPES 10mM,pH=7.0)中对丙二酸阴离子具有良好的选择性识别作用,此识别过程几乎不受其它二元羧酸阴离子的干扰。
[1]GALE P A.Structural and Molecular Recognition Studies with Acyclic Anion Receptors[J].Accounts of Chemical Research,2006,39(7):465~475.
[2]DAVIS A P.Anion binding and transport by steroid-based receptors[J].Coordination Chemistry Reviews,2006,250(23~24):2939~2951.
[3]SCHMIDTCHEN F P.Reflections on the construction of anion receptors:Is there a sign to resign from design[J].Coordination Chemistry Reviews,2006,250(23~24):2918~2928.
[4]KATAYEV E A,USTYNYUK Y ASESSLER J L.Receptors for tetrahedral oxyanions[J].Coordination Chemistry Reviews,2006,250(23~24):3004~3037.
[5]YOON J,KIM SK,SINGH N J,et al.Imidazolium receptors for the recognition of anions[J].Chemical Society Reviews,2006,35(4):355~360.
[6]MARTÍNEZ-MÁÑEZ R,SANCENÓN F.Fluorogenic and Chromogenic Chemosensors and Reagents for Anions[J].Chemical Reviews,2003,103(11):4419~4476.
[7]CARVALHO S,DELGADO R,FONSECA N,et al.Recognition of dicarboxylate anions by a ditopic hexaazamacrocycle containing bis-p-xylyl spacers[J].New Journal of Chemistry,2006,30(2):247.
[8]LIU S-Y,HE Y-B,WU J-L,et al.Calix[4]arenes containing thiourea and amide moieties:neutral receptors towards α,ω-dicarboxylate anions[J].Organic&Biomolecular Chemistry,2004,2(11):1582~1586.
[9]SINGH N,LEE GWJANG D O,p-tert-Butylcalix[4]arenebased fluororeceptor for the recognition of dicarboxylates[J].Tetrahedron,2008,64(7):1482~1486.
[10]MATEUS P,DELGADO R,BRAND O P,et al.Dicarboxylate Recognition by Two Macrobicyclic Receptors:Selectivity for Fumarate over Maleate[J].The Journal of Organic Chemistry,2012,77(10):4611~4621.
[11]GOUGOUX A,LEMIEUX GLAVOIE N.Maleate-induced bicarbonaturia in the dog:a carbonic anhydrase-independene effect[J].American Journal of Physiology-Legacy Content,1976,231(4):1010~1017.
[12]BEER P D,GALE P A.Anion Recognition and Sensing:The State of the Art and Future Perspectives[J].Angewandte Chemie International Edition,2001,40(3):486~516.
[13]RAKER J,GLASS T E.Selectivity via Cooperative Interactions:?Detection of Dicarboxylates in Water by a Pinwheel Chemosensor[J].The Journal of Organic Chemistry,2002,67(17):6113~6116.
[14]SANCEN N F,MART NEZ-M EZ R,MIRANDA M A,et al.Towards the Development of Colorimetric Probes to Discriminate between Isomeric Dicarboxylates[J].Angewandte Chemie,2003,115(6):671~674.
[15]KIM S K,KANG B-G,KOH H S,et al.A New Imidazolium Cavitand for the Recognition of Dicarboxylates[J].Organic Letters,2004,6(25):4655~4658.
[16]GUNNLAUGSSON T,LEONARD J PMURRAY N S.Highly Selective Colorimetric Naked-Eye Cu (II)Detection Using an Azobenzene Chemosensor[J].Organic Letters,2004,6(10):1557~1560.
[17]GHOSH K,SARKAR A R.Anthracene-based macrocyclic fluorescent chemosensor for selective sensing of dicarboxylate[J].Tetrahedron Letters,2009,50(1):85~88.
[18]WISKUR S L,AIT-HADDOU H,LAVIGNE JJ,et al.Teaching Old Indicators New Tricks[J].Accounts of Chemical Research,2001,34(12):963~972.
[19]汤立军,李叶,李明辉,等.指示剂置换法识别阴离子的研究进展[J].化学通报,2010,73(7):600~607.
[20]BOIOCCHI M,BONIZZONI M,FABBRIZZI L,et al.A Dimetallic Cage with a Long Ellipsoidal Cavity for the Fluorescent Detection of Dicarboxylate Anions in Water[J].Angewandte Chemie International Edition,2004,43(29):3847~3852.
[21]BOIOCCHI M,BONIZZONI M,MOLETTI A,et al.Linear recognition of dicarboxylates by ditopic macrocyclic complexes[J].New Journal of Chemistry,2007,31(3):352~356.
[22]TANG L J,PARK J,KIM H-J,et al.Tight Binding and Fluorescent Sensing of Oxalate in Water[J].Journal of the American Chemical Society,2008,130(38):12606~12607.
[23]TANG L J,LIU M H.A New Chemosensing Ensemble for Colorimetric Detection of Oxalate in Water[J].Bull.Korean Chem.Soc,2010,31(11):3159.
[24]YEN Y-P,HO K-W.Synthesis of colorimetric receptors for dicarboxylate anions:a unique color change formalonate[J].Tetrahedron Letters,2006,47(7):1193~1196.
[25]LIU Y,LIANG Z,LIX,et al.Enhanced Sensitivity and Selectivity of Chemosensor for Malonate by Anchoring on Gold Nanoparticles[J].Chinese Journal of Chemistry,2011,29(3):531~538.
[26]COSTERO A M,COLOMER JV,GIL S,et al.Fluorescent Cyclohexyl-Based Chemosensors for Selective Sensing of TMA Malonate in DMSO/Water [J].European Journal of Organic Chemistry,2009,2009(22):3673~3677.
[27]COSTERO A M,COLERA M,GAVINA P,et al.Fluorescent chemosensors based on cyclohexane:selective sensing of succinate and malonate versus their longer or shorter homologues[J].Tetrahedron,2008,64(30):7252~7257.
[28]GHOSH K,SEN T,PATRA A,et al.(rac)-1,1'-Binaphthyl-Based Simple Receptors Designed for Fluorometric Discrimination of Maleic and Fumaric Acids[J].The Journal of Physical Chemistry B,2011,115(26):8597~8608.
[29]LIG,QIAN X,YAN S,et al.Synthesis,Herbicidal Activity,and Structure-Bioactivity Relationship of Pyridyl-Containing 2-Phenyliminothiazolidines[J].Monatshefte für Chemie/Chemical Monthly,2008,139(2):169~178.
[30]BENESIH A,HILDEBRAND JH.A Spectrophotometric Investigation of the Interaction of Iodine with Aromatic Hydrocarbons[J].Journal of the American Chemical Society,1949,71(8):2703~2707.
[31]CONNORSK A,Binding constants:themeasurement ofmolecular complex stability[M].New York:Wiley,1987.
