GC法测定利鲁唑的含量
2013-07-01秦迎春秦卫红
秦迎春秦卫红
(1 湖南省张家界市食品药品检验所,湖南 张家界 427000;2 湖南省张家界市人民医院药剂科,湖南 张家界 427000)
GC法测定利鲁唑的含量
秦迎春1秦卫红2
(1 湖南省张家界市食品药品检验所,湖南 张家界 427000;2 湖南省张家界市人民医院药剂科,湖南 张家界 427000)
目的 采用气相色谱法(GC)测量利鲁唑原料中含有利鲁唑的比例,为临床应用提供理论依据。方法 本文使用了气相色谱法中的内标法,用来测量利鲁唑中的含量。其中色谱柱采用了DB-1弹性的毛细管柱,检测器使用了FID;而汽化室的温度保持在260℃,检测器的温度保持在260℃;柱温保持在230℃,载气使用高纯氮气流速控制在5.0mL/min,尾吹控制在30mL/min,分流比为1/5,采用咖啡因子作为内标物。结果 利鲁唑的含量在1.5~19.5μg/mL呈现了较好的线性关系(r=0.9998),平均的回收率达到了100.1%,其中的RSD达到了0.36%。结论 采用GC法对利鲁唑的含量进行测定,不但方便简便、准确、快速以及可靠,而且最终测出结果比较准确,能够有效测定利鲁唑含量。
含量;利鲁唑;GC法测定
利鲁唑(Riluzole,RLZ)是用来治疗ALS(肌萎缩侧索硬化症)新药,也是目前被认准治疗ALS唯一药物。从文献中可知,目前使用高效液相的色谱法测定该药物含量[1,2]。但是从使用效果来看还存在许多需要改进之处,因此本文结合相关资料后,采用GC法测定出利鲁唑的含量,通过实验体现出这种方法的优势和可行性。
1 仪器与试药
日本岛津的GC-2014气相色谱仪。利鲁唑对照品(自制的,高效液相的色谱法测定含量≥99.9%);咖啡因(中国药品生物制品检定所,纯度:90%);利鲁唑原料(鲁南贝体制药有限公司生产,批号:080502);无水乙醇等各种试剂,这些试剂都属于分析纯。
2 方法与结果
2.1 方法
2.1.1 色谱条件
本文采用了DB-1的弹性石英毛细管柱(30cm×0.53 mm,1.5μm);将汽化室的温度控制在260℃;柱温控制在230℃;载气使用高纯氮气流速控制在5.0mL/min,尾吹控制在30 mL/min,分流比为1/5,采用咖啡因子作为内标物。
2.1.2 样品溶液的制备
精密称取利鲁唑原料50.10mg,置100mL容器中,加无水乙醇进行溶解,最终配制出浓度是0.501mg/mL溶液。
2.1.3 对照品溶液的制备
精密称取干燥利鲁唑对照品50.00mg放置到100mL的量瓶中,加无水乙醇稀释到刻度,摇匀,得到浓度0.50mg/mL的储备溶液。
2.1.4 内标溶液的制备
精密称取咖啡因约100mg,放置到100mL的量瓶中并加入无水乙醇稀释到刻度上,摇匀即得。
2.1.5 考察线性关系
从配制好的对照溶液(浓度:0.5mg/ml)中精密吸取1.0、3.0、5.0、7.0、9.0、11.0、13 mL,分别置于100mL容量瓶中,加入无水乙醇稀释刻度,摇匀。精确吸取3μL,按“2.1项下”色谱条件进行测定,记录色谱图。根据色谱图利鲁唑和内标峰面积之比,横坐标X是对照品浓度(μg/mL),纵坐标Y表示吸光度,以内标峰面积与利鲁唑峰面积之比对利鲁唑浓度回归,得回归方程:y=3.4570x-0.2700,r=0.9998,结果表明利鲁唑在1.5~19.5μg/mL线性关系良好。GC色谱图如图1,其分离度符合规定。
2.1.6 空白试验考察线性
吸取无水乙醇3.0 μL按“2.1” 项下色谱条件进行测定,其空白图谱如图2所示,结果显示无水乙醇没有干扰到利鲁唑的含量。
2.1.7 测定校正因子
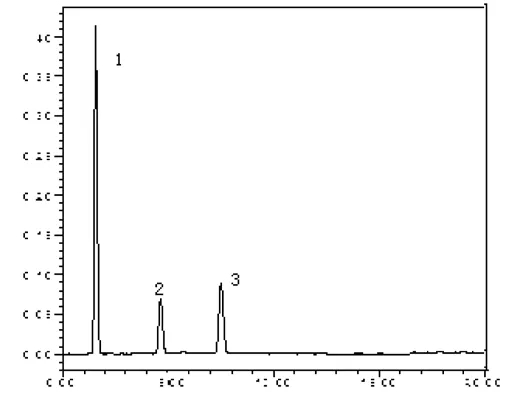
图1 GC色谱图
精密吸取对照品储备液3.0、5.0、7.0mL,分别放置到50mL的量瓶中,每个瓶中再加入内标溶液5 mL,用无水乙醇稀释到刻度。每一个浓度重复测定3次,得出其平均校正因子为1.06,RSD=0.32%。
2.1.8 精密度试验
精密吸取对照品的储备溶液中5mL,放置到50mL的量瓶中,并加入内标溶液5mL,用无水乙醇稀释到刻度并摇匀。吸取样品3μL,“2.1”项下色谱条件进行测定,重复6次,结果RSD为0.27%。
2.1.9 重复性试验
从利鲁唑的原料中称取5份样品,按“2.2”项下方法制备,“2.1”项下色谱条件进行测定,结果显示利鲁唑含量为RSD为1.3%,表明该方法重复性良好。
2.1.10 加样回收率试验
从已知含量为99.86%利鲁唑的原料吸取出9份样品,分别放置到50mL的量瓶之中,并且分别加入“2.3”项下储备溶液分别是3.0、4.0、5.0mL的溶液,再加入内标溶液5mL,使用无水乙醇进行稀释到量瓶的刻度上,均匀,过滤,吸取3.0μL,按“2.1”项下条件测定。
2.2 结果
对加样回收率采用了GC法进行试验之后,得出了计算回收率的结果,见表1。
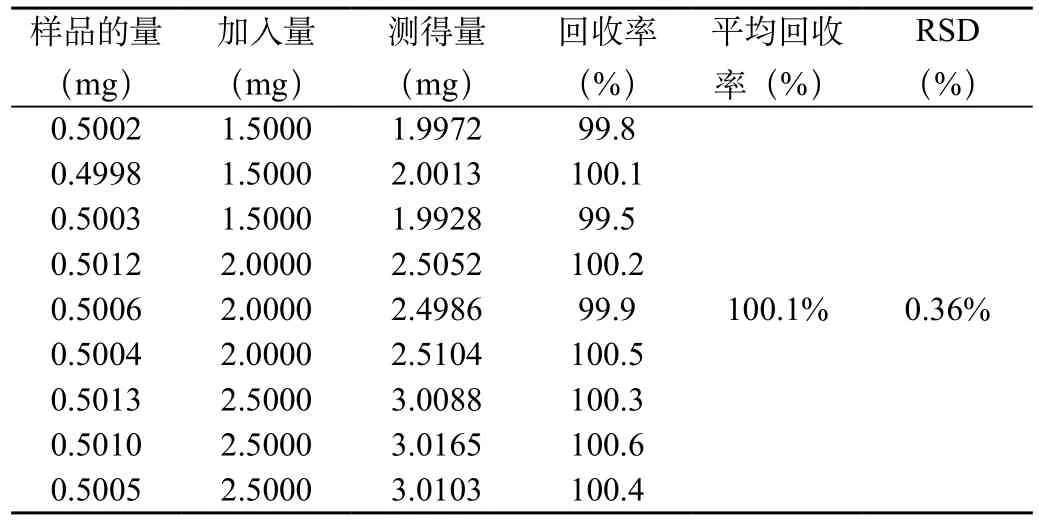
表1 所测定的回收率结果统计(n=3)
从上面2.2中配制的样品溶液中精密取出5mL,精密称取5mL内标溶液加入进去,均匀混合,并取出3μL注入到气相色谱仪中,按照上述测定色谱条件,采用内标法测量利鲁唑中的含量,对这3批样品进行测量之后结果如下,见表2。
3 讨 论
3.1 选择色谱柱

表2 测定样品结果
从各种文献结果可知,如果采用DB-624或HP-5毛细管柱测定,根本就不能够有效分离咖啡因与利鲁唑,但是使用了DB-1的毛细管柱最终结果完全不一样,有效且完全分离出了咖啡因和利鲁唑,并且基线比较稳定,柱效较好。
3.2 选择内标
通过对乙酰氨基酚、非娜西丁以及咖啡因进行试验,利鲁唑是不能够和非娜西丁分离,乙酰氨基酚能够和利鲁唑进行分离,但是稳定性比较差,但是咖啡因与利鲁唑之间进行分离效果比较明显,并且整个过程都具备较好稳定性。
3.3 该方法的优势
采用GC法测定利鲁唑含量,有效的避免了使用二类有毒溶剂的甲醇,而且整个测定过程分析都比较简单,柱效比较高,采用GC法测定平均回收率高达100.1%,RSD仅仅为0.36%,但是从文献张维斌2006年发表《反相高效液相色谱法测定利鲁唑片含量》可知,采用反相高效液相色谱法,平均回收率高达99.5%,RSD为0.71%。相比而言GC法最终所测定结果具备可靠的准确度,同时还能够有效控制柱本品质量。同时这种方法消耗样品量比较少。而且通过本研究发现应用GC法测定,柱效较高,并且分析简便、快速且结果准确可靠,能够有效控制本品的质量。从本试验中可以发现采用无水乙醇作为提取剂效果比较明显,之后再采用甲醇定容做紫外色谱分析。提取极少的原料就能够达到试验提取要求,这种提取方式不但灵敏度高而且降低了样品的杂质含量,确保了色谱柱能够连续分析大量的样品。本文构建出了利鲁唑样品的预处理方法与色谱条件操作,其属性比较强,准确度也比较高,已经被利鲁唑的代动力学以及生物等各种有效性研究广泛使用。
[1] 郑静,陈德俊.高效液相色谱法测定布洛芬片中布洛芬含量[J].中国药业,2007,16(23):34-36.
[2] 李凤兰,胡新海.HPLC法测定布洛芬片的含量[J].中外健康文摘,2010,7(4):92-94.
[3] 郭琦,傅强,潘永西,等.毛细管气相色谱法测定布洛芬胶囊的含量[J].中国药师,2009,12(7):56-59.
[4] 米振清,范剑.用HPLC法测定布洛芬片的含量[J].药学服务与研究,2009,9(2):119-122.
R914
B
1671-8194(2013)21-0105-02
