立体定向脑内核团毁损及深部电刺激术治疗帕金森病临床观察
2013-06-09夏卫东朱广廷赵长地
夏卫东 朱广廷 赵长地
(1济南大学山东省医学科学院医学与生命科学院,山东 济南250062;2济宁医学院附属济宁市第一人民医院,山东 济宁272011)
帕金森病(Parkinson's disease,PD)是常见的中枢神经系统慢性退行性疾病,左旋多巴制剂是治疗PD的标准药物,长期服用会出现运动并发症及药效降低,此时外科治疗往往是一种较好的治疗手段[1-4]。立体定向脑内核团毁损和脑深部电刺激术(deep brain stimulation,DBS)是治疗帕金森病的2种方法,手术成功的关键是术中靶点的精确定位。我科自2008年至2011年行45例核团毁损术,5例选取丘脑底核(subthalamic nucleus,STN)DBS,现总结如下。
1 资料与方法
1.1 一般资料
所有病例均为本院2008年12月至2011年12月收住院治疗的PD患者,其中男29例,女21例。年龄50~80岁,平均63岁。病程3~11a,平均6a。42例症状为双侧性,8例为单侧性。47例有震颤、僵直及运动迟缓,其中以震颤为主19例,以僵直和运动迟缓为主10例,混合型18例。3例仅有肢体僵直和运动迟缓。伴有抑郁症者4例,曾抗抑郁药物治疗。所有病例均经神经内科运动障碍疾病亚专业组副主任医师以上专家,按1984年全国锥体外系疾病讨论会制定的诊断标准确诊[5],并排除其他疾病引起的帕金森综合征,经多巴胺类药物系统治疗3a以上。病情按Hoehn和Yahr分级标准:Ⅱ级11例,Ⅲ级32例,Ⅳ级7例。毁损手术45例,DBS 5例。单侧丘脑腹外侧中间核(Vim)毁损术30例,单侧苍白球腹后内侧部(Gpi)毁损术13例,一侧Vim、对侧Gpi毁损2例。5例DBS均选取STN作为靶点,3例单侧手术,1例分期双侧手术,1例同期双侧手术。45例毁损术,其中CT定位26例,MRI(1.5T或3.0T)定位19例。5例DBS手术均MRI定位。
1.2 手术方法
术前停服多巴胺类药物,有些多巴胺受体(DA)激动剂如麦角乙脲(lisuride)会增加凝血时间,造成出血并发症,因此术前4~6周停药。对于半衰期较长的DA激动剂在术前应减量或暂停。局麻下安装定向仪头架,注意与前后联合(AC-PC)平面线体表投影平行。行CT或MRI薄层扫描,确定前联合(AC)、后联合(PC)及其连线(IC)。Vim靶点坐标设定在AC-PC层面,后联合前5~7mm,正中矢状线旁开13~15mm处。Gpi靶点坐标取IC中点前2mm,IC线下3~6mm,正中失状面外17~21mm处。STN靶点坐标取IC线下2~7mm,IC中点前0mm,正中失状位外侧12.5mm处。计算靶点坐标,将此坐标与CT/MRI图像直接测得的坐标相参考,并与标准脑图相验证,选取最合适的靶点坐标,再换算成头架坐标。局麻下额部钻孔,安装定向仪,调整好靶点坐标,通过导针用微推进器将微电极向靶点方向送入,自靶点上方10mm开始记录细胞电生理信号,根据微电极测得的结果确认靶点。更换射频电极,将射频电极送至验证后的靶点,通过电刺激进一步验证靶点准确,无肢体麻木、无力及视力视野改变后,先给予45℃60s的可逆性毁损,经再次证实靶点准确后给予75℃60s的不可逆性毁损。行DBS者,同样经微电极记录验证靶点后,将刺激电极送入靶点,经微刺激观察效果满意后,改全麻,逐一固定电极、导线和脉冲发生器(单侧Soleter 7426,双侧Kinter 7428)。术后3周开机程控,根据症状改善情况及副作用发生情况调整参数。
1.3 评价方法
采用帕金森评定量表(UPDRS)和日常生活能力量表(ADL)对患者进行“开”和“关”两状态的术前、术后共3次评分。“开”状态是指患者在服用左旋多巴制剂后药效达到最佳状态时的情况;“关”状态是指药效减退至最差时的情况。患者术前和术后左旋多巴制剂的剂量保持不变,评分在术前1周和术后1月、术后1a由不参与手术的有经验的神经科医师独立进行,症状改善率按如下公式计算:改善率=(术前评分-术后评分)/术前评分×100%。
效果评价标准:肢体的震颤、僵直完全消失为显效;症状明显缓解、但仍残留部分症状为有效;症状无改善为无效。
2 结果
2.1 PD患者手术前后UPDRS与ADL评分比较
与手术前比较,手术后1月UPDRS和ADL评分明显降低,差异有统计学意义(P<0.05)。见表1。
表1 PD患者手术前后UPDRS与ADL评分(分,±s)
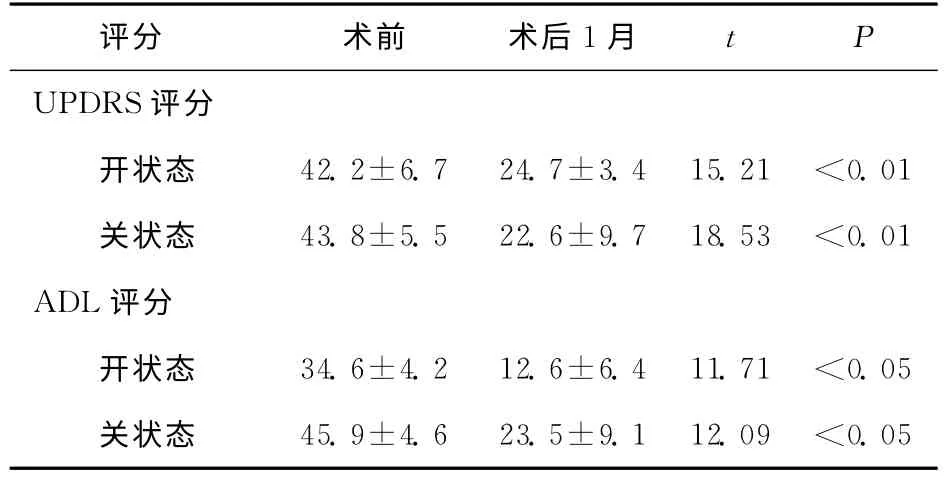
表1 PD患者手术前后UPDRS与ADL评分(分,±s)
t P UPDRS评分 术前 术后1月评分开状态 42.2±6.7 24.7±3.4 15.21<0.01关状态 43.8±5.5 22.6±9.7 18.53<0.01 ADL评分开状态 34.6±4.2 12.6±6.4 11.71<0.05关状态 45.9±4.6 23.5±9.1 12.09<0.05
2.2 术后症状改善情况
本组显效44例(88%),有效6例(12%),无效0例,总有效率100%。UPDRS评分:“开”状态下症状改善率52%,“关”状态下改善率72%。ADL评分:“开”状态下提高38%,“关”状态下提高49%。
2.3 术后随访情况
术后50例患者随诊至3a,8例(均为射频毁损术患者)不同程度复发,占17.8%。其中2例术后半年逐渐复发,另6例术后2~3a后逐渐复发。DBS者,术后调整参数,效果满意,无复发。1例射频毁损者术后2a因意外事故死亡。
2.4 并发症
肢体轻偏瘫2例,CT证实为靶点周围水肿波及内囊所致,经治疗后均短期内完全恢复。1例双侧毁损者二次术后出现一过性构音障碍,1月后完全恢复。无脑内出血及感染等其他并发症发生,无死亡。
3 讨论
对于确诊的帕金森病患者,早期应给予正规的药物治疗,但随着病情的进展,药物治疗效果会逐渐下降。对这类患者及药物治疗副作用较大难以耐受者,寻求积极的外科治疗也是十分必要的。目前立体定向手术治疗帕金森病主要包括射频毁损术和脑深部电刺激术。Vim、Gpi和STN是立体定向手术治疗帕金森病的3个常用靶点。Vim核毁损术或电刺激术能显著改善帕金森患者的震颤和肌僵直,但对运动减少症状效果差,是治疗以震颤为主的帕金森病的首选靶点。Gpi对震颤消除不完全,但对肌僵直、运动减少及药物引起的异动症效果满意[6]。所以近些年来许多立体定向外科医生对改靶点情有独钟。STN手术不但能够消除顽固性震颤、缓解运动迟缓、僵直、步态和药物诱导的运动功能紊乱,有些患者还可减少术后多巴胺的药量。目前,在临床上尤其DBS手术上逐渐得到广泛应用。STN的毁损术国内外也有报道[7],效果同样满意。
核团毁损术与脑深部电刺激术是目前临床应用最广泛的手术方式[8-9]。本研究采用DBS与STN毁损术观察PD患者的临床疗效。结果显示,手术后1个月患者的UPDRS与ADL评分明显降低,有效率100%,复发率较低,改善率较高。帕金森病脑部病变的基础是黑质多巴胺能细胞的减少,导致基底节与丘脑某些核团的电生理活动异常。现代神经外科治疗帕金森病是基于帕金森病患者Vim、GPi和STN核(团)过度活跃这样一个假说。手术目的是精确定位核(团)并减少其过度输出[10]。
无论是毁损术还是DBS手术,要想取得满意的临床效果,尽可能地减少手术带来的并发症,作者体会:1)严格掌握手术适应症,是提高手术疗效的重要因素。我们所有的手术患者均由神经内科运动障碍疾病专业组医生确诊,并经过内科药物正规治疗,严把疾病的诊断关。2)术中精确定位是成功的关键。如有条件,尽可能采用微电极记录技术,以确保靶点的准确,提高疗效、降低并发症的发生。3)术后继续服药及合理的锻炼康复。目前,该病尚无完全根治的办法,但手术能缓解症状、延缓疾病进展,改善患者的生活质量。所以,术后还要继续服用药物治疗,并进行积极的身体锻炼和各种康复训练。
[1] Benabid AL,Koudsie A,Pollak P,et al.Future prospects of brain stimulation[J].Neurol Res,2000,22(3):237-246.
[2] Starr PA,Christine CW,Theodosopoulos PV,et al.Implantation of deep brain stimulators into the subthalamic nucleus:technical approach and magnetic resonance imaging-verified lead locations[J].J Neurosurg,2002,97(2):370-387.
[3] Lozano AM.刘康永,郎黎琴,译.脑深部电刺激治疗帕金森病[J].中国神经精神疾病杂志,2002,28(1):1-7.
[4] 周晓平,胡小吾,王来兴,等.微电极导向立体定向手术治疗帕金森病[J].第二军医大学学报,2001,22(8):752-754.
[5] 张振馨.帕金森病的诊断[J].中华神经科杂志,2006,39(6):408-409.
[6] Seijo FJ,Alvarez-Vega MA,Gutierrez JC,et al.Complications in subthalamic nucleus stimulation surgery for treatment of Parkinson's disease.Review of 272procedures[J].Acta Neurochirurgica,2007,149(9):867-875.
[7] 曹依群,周晓平,张致峰,等.丘脑底核脑深部电刺激治疗帕金森病的功能显像研究[J].中华神经外科杂志,2006,9(22):564-566.
[8] Weaver FM,Follett K,Stern M,et al.Bilateral deep brain stimulation vs best medical therapy for patients with advanced Parkinson disease:a randomized controlled trail[J].JAMA,2009,301(1):63-73.
[9] 张世忠,张旺明,徐强,等.微电极导向核团毁损术和脑深部电刺激术治疗帕金森病的疗效分析[J].中华神经外科杂志,2006,22(12):264-269.
[10]Skandar EN,Cosgrove GR,Shinobu LA.Surgical treatment of Parkinson disease[J].JAMA,2001,286(24):3056-3060.
