甲型副伤寒杆菌pagC基因分布及其重组表达产物免疫保护作用
2013-05-31范欣丽葛玉梅孙爱华
张 佳,范欣丽,葛玉梅,严 杰,孙爱华
(1.温州医学院检验医学院和生命科学学院,浙江 温州 325035;2.浙江医学高等专科学校,浙江 杭州 310053;3.浙江大学医学院病原生物学系,浙江 杭州 310058)
伤寒沙门菌(Salmonella typhi)感染引起的伤寒以及甲型副伤寒沙门菌(S.paratyphi A)、肖氏沙门菌(S.schottmuelleri)和希氏沙门菌(S.hirschfeldii)感染引起的甲、乙和丙副伤寒是常见消化道传染病[1]。近年来我国不少地区甲副伤寒发病率显著增高,已替代伤寒成为优势病种[2-3]。近年北美、欧洲和东南亚地区甲副伤寒病例也显著增加甚至出现暴发流行[4-8]。目前用于预防伤寒和副伤寒的疫苗是用伤寒沙门菌荚膜多糖制备的Vi疫苗,但甲型副伤寒沙门菌无荚膜[1]。近年国内临床分离的甲型副伤寒沙门菌菌株耐药率为35% ~50%,远高于伤寒沙门菌[9-11]。因此,甲型副伤寒沙门菌无荚膜以及高耐药率被认为是近年甲型副伤寒高发的主要原因。
接种疫苗是预防和控制各种传染病最为有效和经济的措施,尤其在控制高耐药率病原菌感染相关传染病方面具有更为重要的意义。甲型副伤寒沙门菌是具有外膜的革兰阴性菌,外膜蛋白(outer membrane protein,OMP)通常是革兰阴性菌主要表面抗原成分。在甲型副伤寒沙门菌基因组中,至少有 20个 OMP编码基因[12],除 SpaO、OmpA 和 NmpC 外[13-15],其余OMP免疫原性和免疫保护作用未有研究报道。本研究中,我们构建了甲型副伤寒沙门菌外膜侵袭蛋白PagC编码基因原核表达系统,鉴定了重组表达产物rPagC的免疫原性,检测了我国甲型副伤寒杆菌临床菌株pagC基因携带率,采用小鼠感染模型初步了解了rPagC的免疫保护作用,以期为rPagC作为甲型副伤寒沙门菌基因工程疫苗的候选抗原提供依据。
1 材料与方法
1.1 菌株来源和培养 我国甲型副伤寒沙门菌参考标准株50001、35株分离自甲型副伤寒患者的甲型副伤寒沙门菌株由浙江大学医学院病原生物学系提供。采用营养肉汤(Oxoid)培养上述菌株。
1.2 血清标本来源 我国甲型副伤寒沙门菌参考标准株50001兔抗血清、68份甲型副伤寒患者血清及6份正常人血清由浙江大学医学院病原生物学系提供。
1.3 PCR及测序 采用 (Generay)提取甲型副伤寒沙门菌参考标准株50001、35株甲型副伤寒沙门菌临床菌株基因组DNA,紫外分光光度法测定其浓度和纯度[16]。根据报道的pagC基因序列(GenBank No.:CP000026)以及限制性核酸内切酶位点分析结果、原核表达载体pET42a(Novagen)多克隆位点,自行设计PCR引物并由上海Introvigen公司合成。引物序列如下:上游5'-GCG CAT ATG(Nde I)aaa aat att att tta tcc-3',下游5'-GCG CTC GAG(Xho I)GAA ACG GTA TCC AAC TCC GAC-3'。采用高保真PCR试剂盒(TaKaRa)扩增全长pagC基因序列片段。PCR 总体积 100 μl,内含 2.5 mol/L各dNTP、250 nmol/L上游及下游引物、2.5 U EX-Taq酶、100 ng DNA 模板和1×PCR缓冲液(pH 8.3)。PCR参数:94℃ 5 min;94℃30 s,50℃ 30 s,72℃ 90 s,30 个循环;72℃ 10 min。采用1 μg/ml溴乙锭预染色的1.5%琼脂糖凝胶电泳检测扩增产物,委托上海Introvigen公司测序。
1.4 原核表达系统构建 采用T-A克隆试剂盒(TaKaRa)将甲型副伤寒沙门菌参考标准株50001的pagC基因扩增片段克隆至pMD-19T载体中,形成 pMD-19TpagC后电转化入 E.coli DH5α(Invitrogen)并在LB培养液(Oxoid)中扩增,质粒提取试剂盒(Axygen)提取pMD-19TpagC后测序[16]。分别将pMD-19TpagC及原核表达载体pET42a用Nde I和 Xho I双酶切,回收的pagC基因片段与线性化pET42a用T4 DNA连接酶(TaKaRa)连接形成 pET42apagC。将pET42apagC转化入表达宿主菌 E.coli BL21DE3(Novagen)形成 E.coli BL21DE3pET42a-pagC,该工程菌在LB培养液中扩增后按上法提取质粒,然后再次测序。
1.5 rPagC表达和鉴定 采用含0.5 mmol/L IPTG(Sigma)的LB培养液,37℃震荡培养4 h,以诱导 E.coli BL21DE3pET42a-pagC表达 rPagC[16]。用10%分离胶的SDS-PAGE联合Bio-Rad凝胶图象分析系统检查rPagC表达情况并估计产量,采用Ni-NTA亲和层析柱(BioColor)提取rPagC。
1.6 免疫原性检测 将1 mg rPagC与弗氏完全佐剂混合后皮内免疫家兔4次,每次间隔一周,末次免疫后两周采集心血并分离血清,采用免疫双扩散法和ELISA检测抗血清的效价。分别以1∶1000 稀释的兔抗rPagC血清和甲型副伤寒沙门菌50001株全菌抗血清、1∶500稀释的5份甲型副伤寒患者血清为一抗,1∶3000 稀释的HRP标记羊抗兔IgG(Jackson ImmunoResearch)为二抗,采用 Western Blot检测rPagC的抗原性和免疫反应性。
1.7 ELISA 采用1 μg rPagC包被96孔酶标板4℃过夜,次日用 0.01 mol/L PBS(pH 7.4)洗板3次。以1∶1000 稀释的68份甲型副伤寒患者血清为一抗、1∶5000 稀释的HRP标记羊抗人IgG(Jackson ImmunoResearch)为二抗,采用ELISA检测各血清标本OD450值,若OD450值大于相同稀释度正常人血清OD450均值+3SD 者判为阳性[16]。
1.8 小鼠保护试验 将体重(20±2)g健康BALB/C小鼠分组,每组8只,各组小鼠腹腔注射不同浓度(CFU/ml)的甲型副伤寒沙门菌50001 株新鲜培养物 0.5 ml,观察 7 d,以获得100%最低致死量(MLD)。将BALB/C小鼠分为2组,每组15只,分别于颈背部皮下注射100 μg 或 200 μg rPagC 与 0.1 mg 氢氧化铝(Sigma)混合物进行免疫,间隔1周按上法再次免疫。末次免疫后2周,用2倍100%MLD的甲型副伤寒沙门菌50001株注射小鼠腹腔进行攻击,观察7 d内动物死亡情况。实验中以8只200 μg BSA(Sigma)与 0.1 mg 氢氧化铝混合物免疫的小鼠作为对照。
1.9 微量肥达试验 按上法将100 μg或200 μg rPagC与0.1 mg氢氧化铝(Sigma)混合物免疫小鼠。末次免疫后2周采集抗凝外周血,3000 r/min 4℃离心10 min后取上清,采用微量肥达试验检测上清标本的凝集效价[13]。实验中200 μg BSA与0.1 mg氢氧化铝免疫小鼠抗凝血上清为对照。
2 结果
2.1 PCR及测序结果 从甲型副伤寒沙门菌参考标准株50001、35株甲型副伤寒沙门菌临床菌株基因组DNA中均扩增出预期大小的pagC基因片段(图1)。测序及Blast软件分析结果显示,上述36株甲型副伤寒沙门菌株pagC基因与 GenBank中公布的 pagC基因(No.:CP000026)的核苷酸和氨基酸序列相似性分别为99.1%~100%和98.4%~100%。
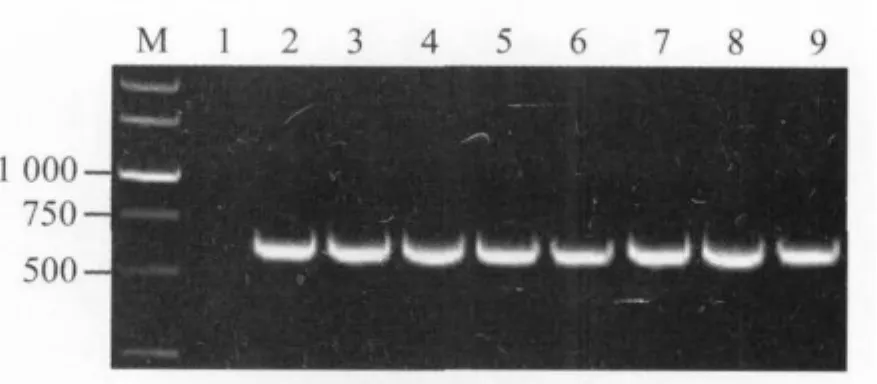
图1 甲型副伤寒沙门菌株pagC基因扩增片段Fig.1 Amplification fragments of pagC gene from Salmonella paratyphi A strains
2.2 rPagC表达和提纯效果 在 IPTG诱导下,E.coli BL21DE3pET42a-pagC能高效表达 rPagC,其表达量约占细菌总蛋白的35%。Ni-NTA亲和层析法提纯的rPagC经SDS-PAGE后在胶上显示为单一的蛋白条带(图2)。
2.3 rPagC抗原性和免疫反应性 rPagC免疫家兔后能产生高效价抗体,其免疫双扩散和ELISA 效价分别为1∶4和1∶8000 。Western blot结果证实,rPagC及甲型副伤寒沙门菌参考标准株50001兔抗血清、5份甲型副伤寒病人血清均能识别rPagC并产生阳性杂交信号(图3)。
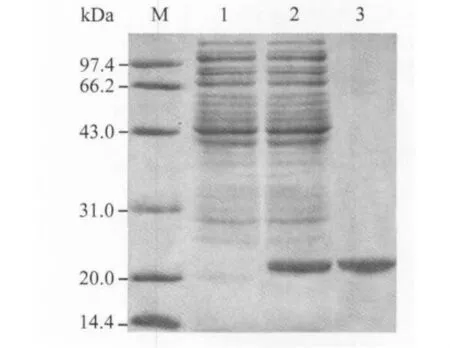
图2 rPagC蛋白表达和提纯效果Fig.2 Expression and purification effects of rPagC protein

图3 rPagC与不同血清标本Western Blot结果Fig.3 Western BlotresultofrPagC with different serum specimens
2.4 ELISA结果 6份正常人血清OD450均值+3SD为0.25(cut-off值)。68份甲型副伤寒患者血清标本中,97.1%(66/68)的ELISA结果阳性。
2.5 小鼠保护试验结果 甲型副伤寒沙门菌参考标准株50001对小鼠的100%MLD为5×107CFU。BSA免疫对照组小鼠用2倍MLD甲型副伤寒沙门菌参考标准株50001攻击后7 d内均死亡,100 μg 和 200 μg rPagC 对感染小鼠的免疫保护率分别为73.3%(11/15)和86.7%(13/15)(表1)。
2.6 微量肥达试验结果 rPagC免疫小鼠血清对伤寒沙门菌O抗原的凝集效价仅为0~1∶10,对伤寒沙门菌和甲型副伤寒沙门菌H抗原凝集效价高达1∶10~1∶40,但对肖氏沙门菌和希氏沙门菌H抗原凝集效价也较低(0~1∶10)。见表2。

表1 rPagC对小鼠免疫保护效果Table 1 Immunoprotective effect of rPagC in mice

表2 rPagC免疫小鼠微量血清肥达试验效价Table 2 Micro-Widal's test titers of serum specimens from rPagC-immunized mice
3 讨论
OMP是革兰阴性菌主要表面蛋白抗原[1,18]。早有文献报道,沙门菌 OMP 可有效地诱导机体产生淋巴细胞增殖反应[19-20],也可诱导患者或实验感染动物产生高效价抗体[20]。我们以往的研究结果也显示,甲型副伤寒沙门菌重组外膜蛋白rSpaO和rOmpA有免疫原性和免疫保护作用[13-15]。因此,我们选择甲型副伤寒沙门菌重组外膜蛋白rPagC作为基因工程疫苗抗原有一定依据。
蛋白抗原在不同来源菌株中分布广泛且序列保守,是确定其能否作为基因工程疫苗候选抗原的基本条件之一。我们的实验结果显示,分离自不同地区甲型副伤寒患者的35株甲型副伤寒沙门菌均携带pagC基因,且其核苷酸和氨基酸序列相似性分别高达99.1% ~100%和98.4% ~100%,表明pagC基因分布广泛且序列保守。
抗原的免疫原性分为抗原性和免疫反应性,具有良好的抗原性和免疫反应性是确定蛋白分子能否作为基因工程疫苗候选抗原的另一基本条件。我们的免疫双扩散和ELISA结果显示,rPagC免疫家兔后能产生高效价的特异性抗体;Western Blot结果显示,rPagC不仅能与其兔抗血清结合,也能与甲型副伤寒沙门菌全菌抗血清发生免疫反应;ELISA结果显示,97.1%(66/68)甲型副伤寒患者血清标本中存在rPagC抗体。上述实验结果表明,PagC具有良好的抗原性和免疫反应性。
动物保护试验是确定任何抗原分子能否作为基因工程疫苗候选抗原的关键步骤。我们的小鼠免疫保护试验结果显示,100 μg和200 μg rPagC对感染小鼠的免疫保护率分别高达73.3%和86.7%,明显高于以往报道的甲型副伤寒沙门菌重组外膜蛋白rOmpA的41.7%和58.3%、重组外膜蛋白rNmpC的41.7%和66.7%[14-15]。在肥达试验中,所谓伤寒或副伤寒沙门菌H抗原是未经加热处理的活菌抗原,加热后表面蛋白抗原被破坏,但脂多糖抗原耐热,称之为O抗原,由于伤寒或副伤寒沙门菌脂多糖完全相同,故在肥达试验中仅用伤寒沙门菌O抗原[14-15]。我们的微量肥达试验结果显示,rPagC免疫小鼠血清对伤寒沙门菌O抗原凝集效价仅为0~1∶10,对伤寒沙门菌和甲型副伤寒沙门菌H抗原凝集效价高达1∶10~1∶40。经过检索我们发现,伤寒沙门菌基因组中也含有 pagC 基因(GenBank accession No.:NC_003198),其氨基酸序列与甲型副伤寒沙门菌pagC 基因相似性高达(183/185)[22]。因此,rPagC免疫小鼠血清对伤寒沙门菌H抗原也有较高的凝集效价。由于95%以上伤寒和副伤寒由伤寒沙门菌或甲型副伤寒沙门菌感染所致[2-10],若采用rPagC作为甲型副伤寒沙门菌基因工程疫苗抗原,不仅可预防甲型副伤寒沙门菌感染,同时也对伤寒沙门菌有预防效果。
[1]YAN Jie(严 杰).Medical Microbiology(医学微生物学)[M].Second edition,Peijing:the Higher Education Press,China,2012,109-112.(in Chinese)
[2]WANG Haoqiu,PAN Jingcao,GE Yumei,et al(汪皓秋,潘劲草,葛玉梅,等).Molecular characteristics of Salmonella typhi and Salmonella paratyphi A isolates in Hangzhou area[J].Chinese Journal of Microbiology and Immunology(中华微生物学和免疫学杂志),2012,32(8):711-715.(in Chinese)
[3]YAN Meiying,LIANG Weili,LI Wei,et al(闫梅英,梁未丽,李伟,等).Epidemiological analysis of typhoid and paratyphoid cases in China during 1995 to 2004[J].Disease Control(疾病监测),2005,20(8):401-403.(in Chinese)
[4]WOODS C W,MURDOCH D R,ZIMMERMAN M D,et al.Emergence of Salmonella enterica serotype Paratyphi A as a major cause of enteric fever in Kathmandu[J].Nepal Trans R Soc Trop Med Hyg,2006,100(11):1063-1067.
[5]PANDIT A,ARJYAL A,PAUDYAL B,et al.A patient with paratyphoid A fever:an emerging problem in Asia and not always a benign disease[J].J Travel Med,,2008,15(5):364-365.
[6]WILDE H.Enteric fever due to Salmonella typhi andparatyphiA:A neglected and emerging problem [J].Vaccine,2007,25(29):5246-5247.
[7]FANGTHAM M, WILDE H. Emergence of Salmonella paratyphi A as a major cause of enteric fever:need for early detection,preventive measures,and effective vaccines [J].J Travel Med,2008,15(5):344-350.
[8]GUPTA S K,MEDALLA F,OMONDI M W,et al.Laboratory-based surveillance of paratyphoid fever in the United States:traveland antimicrobial resistance[J].Clin Infect Dis,2008,46(11):1656-1663.
[9]GUPTA S K,MEDALLA F,OMONDI MW,et al.Laboratory-based surveillance of paratyphoid fever in the United States:traveland antimicrobial resistance[J].Clin Infect Dis,2008,46(11):1656-1663.
[10]FANGTHAM M,WILDE H.Emergenceof Salmonella paratyphi A as a major cause of enteric fever:need for early detection,preventive measures,and effective vaccines [J].J Travel Med,2008,15(5):344-350.
[11]LU Lianqin,LUO Yong(俞连琴,骆 勇).Identification and drug sensitive test results of 122 Salmonella paratyphi A isolates[J].Chinese Journal of Nosocomiology(中华医院感染学杂志),2003,13(1):6-7.(in Chinese)
[12]McCLELLAND M,SANDERSON K E,CLIFTON S W,et al.Comparison of genome degradation in Paratyphi A and Thphi,human-restricted serovars of Salmonnella enterica taht cause typhoid [J].Nat Genet,2004,36(12):1268-1274.
[13]RUAN P,XIA X P,SUN D,et al.Recombinant SpaO and H1a as immunogens for protection of mice from lethal infection with Salmonella paratyphi A:Implications for rational design of typhoid fever vaccines [J].Vaccine,2008,26:6639-6644.
[14]JIANG Jinqin,RUAN Ping,DING Wei,et al(蒋锦琴,阮 萍,丁 威,等).Distribution of Salmonella paratyphi A ompA gene and immunological identification the recombinant expressed product[J].ChineseJournalof Microbiology and Immunology(中华微生物学和免疫学杂志),2010,30(1):1-5.(in Chinese)
[15]WU Ying,WANG Yanfang,YAN Jie,et al(吴颖,王艳芳,严 杰,等).Prokaryotic expression ofSalmonella paratyphiA nmpC gene and immunoprotective effect of the expressed product[J].Chinese Journal of Microbiology and Immunology(中华微生物学和免疫学杂志),2010,30(12):1118-1123.(in Chinese)
[16]SAMBROOK J,FRITSCH E F,MANIATIS T.Molecular Cloning:A LaboratoryManual[M].2nd edition,New York:Cold Sping Harbor Labooratory Press,1989,1.21-1.52,2.60-2.80,7.3-7.35,9.14-9.22.
[17]SUN A H,WANG Y,DU P,et al.A sensitive and specific IgM-ELISA for the serological diagnosis of human leptospirosis using a rLipL32/1-LipL21-OmpL1/2 fusion protein [J].Biomed Environ Sci,2011,24(3):291-299.
[18]BROOKS G F,BUTEL J S,MORSE S A.Medical Microbiology[M].22nd edition,Now York:McGraw-Hill Press,2001,217-228.
[19]GONZALEZ C R, ISIBASI A, ORTIZNAVARRETE V,et al.Lymphocytic proliferative response to outer membrane protein isolated from Samonella [J].J Microbiol Immunol,1993,37(10):793-799.
[20]McSORLEY S J,COOKSON B T,JENKINS M K,et al.Characterization of CD4+cell responses during natural infection with Salmonella typhimurium [J].J Immunol,2000,164(2):986-993.
[21]JEANNIN P,MAGISTRELLI G,GOESTSCH L,et al.Outer membrane protein A(OmpA):a new pathogen-associated molecular pattern that interacts with antigen presenting cells-impact on vaccine strategies[J].Vaccine,2002,20(1):23-27.
[22]PARKHILL J,DOUGAN G,JAMES K D,et al.Complete genome sequence of a multiple drug resistant Salmonella enterica serovar Typhi CT18[J].Nature,2001,413(6858):848-852.
