麸质蛋白过敏原ELISA定量测定能力验证研究*
2013-05-14武利庆高运华盛灵慧
王 洋 武利庆 高运华 盛灵慧 杨 彬 王 晶 杨 屹
(1.北京化工大学,北京 100029;2.中国计量科学研究院,北京 100013)
0 引言
食品过敏原属于食品安全性的范畴,食品过敏原多指那些能对特定人群产生过敏反应的食品中的蛋白质。据报道,90%以上的食品过敏是由蛋、奶、鱼、甲壳类、花生、大豆、坚果类及小麦这8类常见食物引起[1]。
小麦是人们日常饮食中的主要食物来源,也是主要的食物蛋白来源之一,小麦中蛋白含量占其总体的7%~15%。小麦致敏通常会影响皮肤、内脏和呼吸道的健康,引起运动激发过敏症、职业哮喘、鼻炎、接触性荨麻症、乳糜泻肠炎和麻风皮肤病等不适[2]。麸质蛋白是其主要的致敏成分,根据其在水醇溶液中的溶解情况,可以分为可溶性的醇溶蛋白和不可溶的麦谷蛋白[3]。醇溶蛋白一般是麸质蛋白含量的一半,所以,准确检测谷物中醇溶蛋白的含量,就可以得到其麸质蛋白的含量。
食品过敏原的体外检测方法有很多[4],ELISA法是其中之一,他具有灵敏度高、重复性好、易操作和应用广泛等优点,而且很多过敏原专用的ELISA试剂盒都已经实现商品化,成为应用最多的过敏原检测方法。其中,双抗夹心ELISA法和竞争ELISA法应用最为广泛,国内外已有很多关于双抗夹心ELISA法和竞争ELISA法定量检测食物中醇溶蛋白含量的报道[5-8]。
为了考察各个实验室采用ELISA方法检测食品过敏原数据的可比性,澳大利亚计量院组织了麸质蛋白定量检测国际能力验证。中国计量科学研究院参加了此次能力验证,实验采用的是双抗夹心ELISA法,用德国拜发的醇溶蛋白试剂盒测定了比对样品中的麸质蛋白含量并对测定结果的不确定度进行了评定。
1 实验部分
1.1 主要仪器与试剂
多功能酶标仪;离心机;天平;水浴;涡旋仪;排枪。
超纯水;异丙醇(色谱纯);乙醇(色谱纯);待测样品由澳大利亚计量院提供;麸质蛋白提取液和麸质蛋白检测试剂盒RIDASCREEN® Gliadin。
1.2 实验步骤
1)根据试剂盒提供的标准方法,待试剂盒平衡至室温后,将样品稀释液进行1:5稀释;二抗储备液进行1:11稀释;洗涤缓冲液进行1:10稀释,备用。
2)根据试剂盒提供的标准方法,准确称取0.25g样品,加入2.5mL提取液,60℃水浴15min。加入7.5mL 68%异丙醇,60℃恒温水浴10min;60℃水浴10min;2500g离心10min;取80μL上清液,加920μL样品稀释液,混匀待测。
3)在酶标板每孔加入100μL标准或样品溶液,室温孵育1小时;每孔用250μL洗涤液洗涤三次;每孔加入100μL酶-偶联物,室温反应40min;每孔用250μL洗涤液洗涤三次;每孔加入50μL底物和50μL显色剂,微微震荡板,室温暗反应40min;每孔加入100μL停止液,在450nm测定吸光度。
1.3 结果计算
试剂盒直接测定出的结果为提取稀释后溶液中的醇溶蛋白的含量,通过式(1)根据称取样品的质量、样品溶液体积和稀释倍数可计算出样品中的醇溶蛋白含量:
χGliadin=cGliadin×a×V/m
(1)
式中,cGliadin为稀释液中醇溶蛋白的含量;a为稀释倍数;V为样品溶液体积;m为称取的样品质量。
根据麸质蛋白由50%谷蛋白和50%醇溶谷蛋白组成,将测定出的醇溶蛋白含量乘以2即得到样品中麸质蛋白的含量:
χGluten=2χGliadin
(2)
2 结果与讨论
2.1 试剂盒的选择与评价
近年来,市场上已有多种商品化的麸质过敏原ELISA检测试剂盒销售,可在短时间内实现麸质过敏原的定性和半定量检测。但是,大多数是利用抗体与小麦中的Ω-醇溶谷蛋白片段反应,因而不能等量检测大麦或黑麦中的醇溶谷蛋白。经调研,最终选择了德国拜发公司的RIDASCREEN麸质提取检测试剂盒,该试剂盒符合食品法典修订标准并获得AOAC商品化试剂盒的认证,也是欧盟食品法典的强制执行方法。
为了保证样品分析结果的准确可靠,进行能力验证样品分析前,首先对试剂盒定量的准确性、重复性、定量限、检出限和线性范围等指标进行了评价和验证。以试剂盒自带的0ng/g、5ng/g、20ng/g、40ng/g麸质蛋白标准品绘制标准曲线,将10ng/g麸质蛋白标准品作为未知样,进行评价实验。评价实验连续进行3天,每天进行3次平行实验。计算10ng/g麸质蛋白标准品测定结果与标准值的误差作为准确度的指标;计算日内变异系数和日间变异系数作为重复性的指标;以3倍0ng/g麸质蛋白标准品吸光度计算检出限;以10倍0ng/g麸质蛋白标准品吸光度计算定量限。试剂盒的各评价参数见表1。可见该试剂盒对0~40ng/g范围内的麸质蛋白具有较好的定量能力,能够满足此次能力验证样品的测定要求。
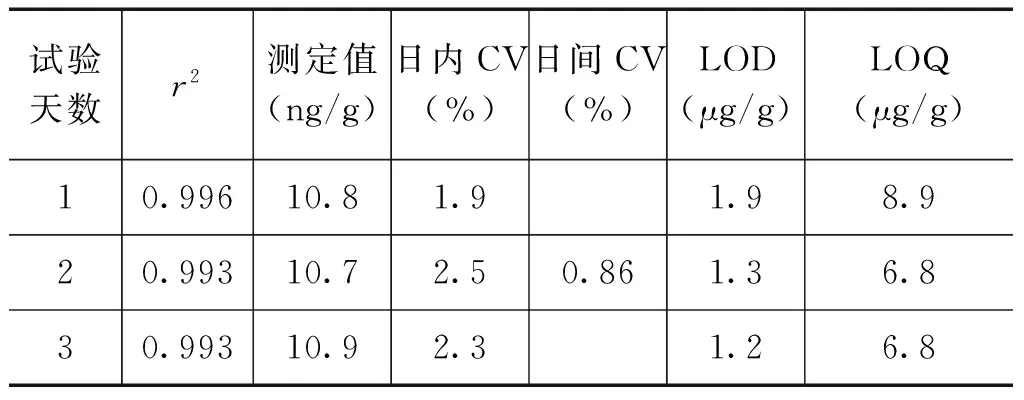
表1 试剂盒定量能力评价参数
2.2 能力验证样品中麸质蛋白含量的测定
此次能力验证共发放两个盲样,均为研磨后混合均匀的食品粉末,每个样品各50g。按照所述实验步骤完成样品的提取、测定,并按照1.3的方法计算样品中麸质蛋白的含量。每次实验时两个样品分别称取3个子样,每个子样平行测定3次,总共进行3次实验,结果如表2所示。从表2可以看出,盲样S1为高值样品,S2为低值样品,低值样品中的醇溶蛋白含量低于检出限。高值样品日内变异系数为3.13%~3.76%,日间变异系数为4.45%,如表3所示。

表2 比对样品中麸质蛋白含量的测定

表3高值样品中麸质蛋白含量测定结果
2.3 不确定度评价
本实验结果计算的数学模型为式(1)。根据数学模型,不确定度主要来自醇溶蛋白浓度的测定、稀释因子、加样体积和样品称量。
2.3.1 醇溶蛋白浓度测定
醇溶蛋白浓度测定的不确定度主要来源于方法的重复性、标准品和标准曲线拟合。醇溶蛋白一共测定了3组,每组测定了9个数据,共得到27个实验数据,最终结果为这27个数据的平均值。采用A类不确定度评定方法计算吸光度重复性的不确定度分量(n=27):
根据文献[9]计算标准曲线y=ax+b中斜率a和截距b的不确定度:
ua=0.77μg/g,ub=0.94μg/g
所以,由醇溶蛋白浓度测定带来的不确定度为:
2.3.2 稀释因子
在实验过程中,分别使用检定合格的100μL和1000μL的移液器移取80μL样品和920μL样品稀释液进行样品稀释。根据JJG 646—2006《移液器检定规程》,100μL和1000μL移液器的最大允许误差分别为±2.0%和±1.0%,按照均匀分布估计,由此带来的稀释因子的不确定度为:
2.3.3 样品溶液体积
样品溶液体积总共为10mL,由10mL的移液器分别移取2.5mL和7.5mL的液体得到,根据JJG 646—2006《移液器检定规程》,10mL移液器的最大允许误差分别为±0.6%,按照均匀分布估计,由此带来的样品体积的不确定度为:
2.3.4 样品称量
根据JJG 1036—2008《电子天平检定规程》,实验过程中采用6位数天平称量0.25g样品,其最大允许误差远远小于移液器引入的不确定度分量,因此,可忽略由样品称量引入的不确定度。
2.3.5 不确定度合成
标准合成不确定度为以上不确定度分量的合成:
取扩展因子k=2,对应于95%的置信概率,则扩展不确定度:
Urel=kuc,rel=0.24;U=0.24×18.9=4.5μg/g
最终测定结果为:(18.9±4.5)μg/g。
2.4 能力验证结果
此次能力验证由澳大利亚计量院主导,来自世界各国的共11家实验室参加了此次能力验证,其中有9个实验室上报了测定结果。所有实验室均采用ELISA方法进行测定,测定的目标蛋白均为醇溶蛋白,结果如表4和图1所示。
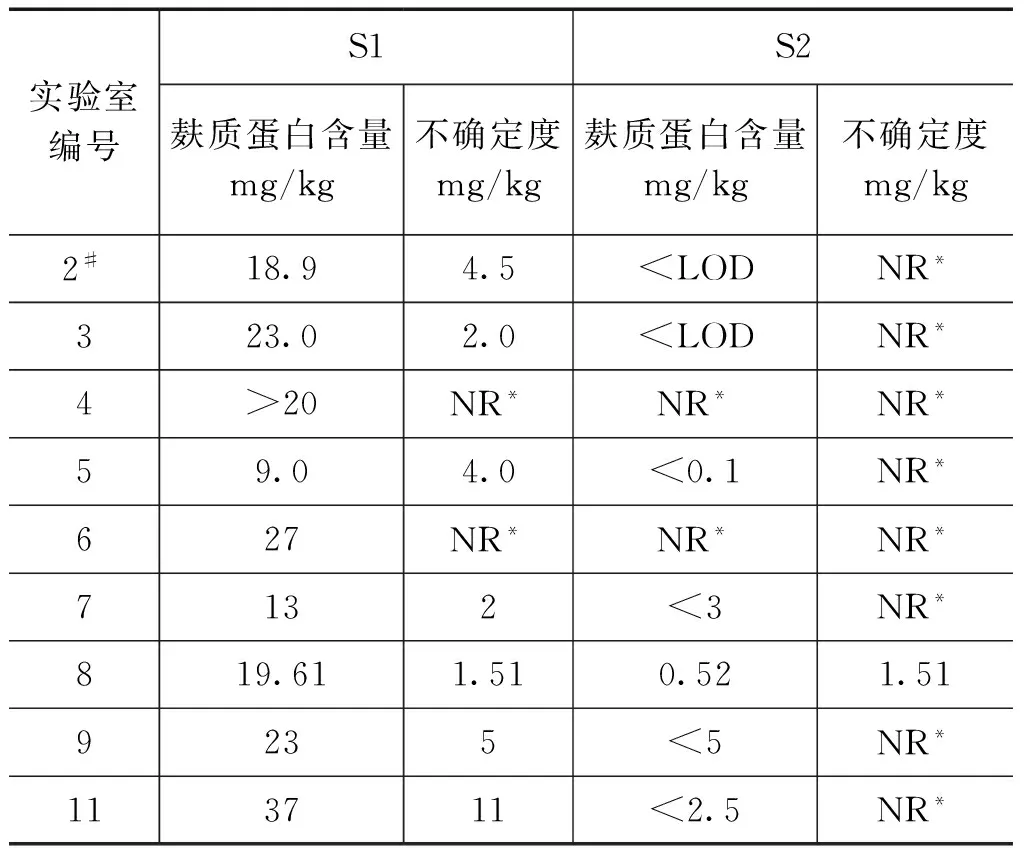
表4 各实验室样品测定结果
S2样品为空白样品,只要测定过程中没有污染,测定结果就不会出现问题,所有参加实验室都成功完成了S2样品的测定。S1为澳大利亚计量院的定值样品,定值结果为(17.6±2.6)mg/kg(见图1),所有参加实验室中只有中国计量科学研究院和8号实验室测定结果中心值落在样品定值结果范围内。

图1 S1样品中麸质蛋白含量测定结果
为了更加科学合理的对能力验证结果进行评价,澳大利亚计量院同时采用了z值和En值评价各家实验室的测定结果。z值和En值的计算公式分别如下:
(4)
(5)
式中,x为各参加实验室的测定结果;X为比对样品的赋值结果;σ为样品赋值结果的标准偏差,σ=X·CV;Ux为样品赋值结果的扩展不确定度;Uχ为测定结果的扩展不确定度。
若z≤2,说明结果可信;2

图2 z值分布图
若按z值评价(图2),中国计量科学研究院以及实验室3、5、7、8、9的z≤2,证明这些实验室的测定结果可靠;若按En值评价(图3),中国计量科学研究院以及实验室8、9的En≤1,说明这些实验室测定结果可靠。不论采用z值还是En值评价,中国计量科学研究院以及实验室8、9的结果都与澳大利亚计量院结果一致,通过了此次能力验证。此次食品过敏原能力验证数据表明中国计量科学研究院已具备准确测定食品中麸质蛋白过敏原的能力。

图3 En值分布图
3 结论
过敏原是当前食品安全面临的一大问题,快速、准确定量食品中的过敏原具有重要的意义。中国计量科学研究院参加澳大利亚计量院组织的本次过敏原国际能力验证,就是为了检验自身的食品过敏原检测能力。验证结果表明中国计量科学研究院的测定结果与主导实验室的结果等效,证明了中国计量科学研究院已具有较好的麸质蛋白过敏原定量测定能力。
[1] 聂凌鸿,周如金,宁正祥.食物过敏原研究进展[J].生命的化学,2002,22(5)
[2] 秦倩茹.抗卵清蛋白单克隆抗体的制备及卵清蛋白、醇溶蛋白ELISA检测方法的建立[D].中国海洋大学,2010
[3] Herbert W.Chemistry of gluten proteins[J].FoodMicrobiol,2007,24
[4] Taylor S L,Nordlee J.Methods for the detection of food allergens[J].FoodTechnol,1996,50(5)
[5] 孙秀兰,管露,单晓红,等.食品过敏原体外检测方法研究进展[J].东北农业大学学报,2012,43(2)
[6] María C.M.,Manuel L.,Alberto H.Comprehensive analysis of gluten in processed foods using a new extraction method and a competitive ELISA based on the R5 antibody [J].Talanta,2012,91
[7] 秦倩茹,高宏伟,马洪明.过敏原小麦醇溶蛋白的ELISA定量检测方法的建立[J].食品工业科技,2010,31(11)
[8] 邵碧英,傅碧忠,郑晶,等.烤鳗酱油中大豆、小麦过敏原的ELISA检测[J].中国酿造,2011(3)
[9] 刘庆,邵志新.回归分析的直线拟合不确定度探讨[J].中国测试,2009,35(3)
