甲烷水合固化过程反应热实验研究
2013-03-17陈文胜康宇
陈文胜,康宇
(黑龙江科技学院安全工程学院,哈尔滨150027)
0 引言
目前,我国对瓦斯(主要成分为甲烷)的利用率不高,致使大量瓦斯直接排空,由此导致能源浪费、环境污染。因此,进行煤矿瓦斯分离及综合利用研究十分必要。煤矿瓦斯混合气体中甲烷组分通过低耗高效的技术进行分离是瓦斯利用亟待解决的关键。2006年,吴强等基于瓦斯水合物生成条件温和(0℃以上即可加压合成)、含气率高(标况下,1体积水合物可储存164倍体积甲烷气体)、储存安全(常压、常温条件下,分解速度缓慢)等特性,提出了瓦斯水合固化分离及储存新方法[1]。
目前,研究者已通过理论与实验研究,证明了以水合物形式分离和储运煤矿瓦斯的可行性[2],而煤矿瓦斯水合物高效快速的生成是这种储运方式能否实施的前提。瓦斯水合固化过程除了受水合过程中物质传递的影响,还受水合过程中热量传递的控制。瓦斯水合过程是结晶放热过程,这就要求瓦斯在水合过程中要及时将反应热传递出去,因此,在瓦斯水合固化过程中需提供其必需的制冷量来提高生成效率,进行瓦斯水合过程中反应热的研究是解决这一问题的关键。因此,笔者根据甲烷水合物相平衡数据,结合推导出的反应热求解方程,对三种实验体系的反应热进行了求解。
1 数学模型
由于实验体系气相压力为高压状态,因此,采用考虑压缩系数的气体状态方程:

其中:p、V、T分别为压力、体积和温度,Z为气体压缩因子,则体系中两状态点1、2间的气体变化量由式(1)确定[3]:

反应体系中,状态点2的气体体积:
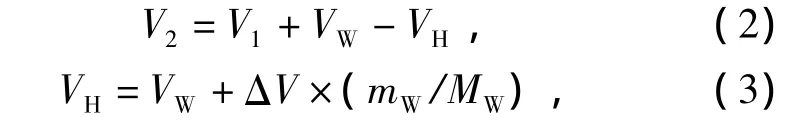
据式(2)、(3),可得状态点2的气体体积为

式中:VW——生成过程中水的变化量,cm3;
VH——反应过程中水合物生成量,cm3;
ΔV——反应过程中1 mol水转化成水合物空腔后的体积增加量,cm3;
mW——反应过程中消耗的水的质量,g;
MW——水的摩尔质量,g/mol。
Ⅰ型水合物(甲烷生成Ⅰ型水合物)空腔密度ρHⅠ为0.796 g/cm3,则有
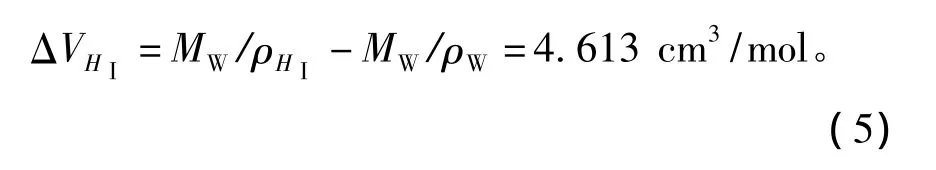
已知Ⅰ型水合物的水合数为5.75,水合物的气体填充率一般情况下达不到100%,故取系数1.2(相当于空腔填充率83.3%)来修正水合数,则:
对于Ⅰ型水合物,反应过程中消耗的水的摩尔变化量nWⅠ为
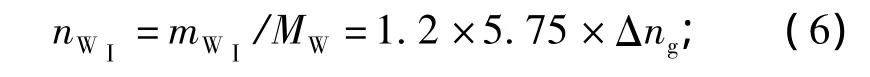
对于Ⅰ型水合物,由方程(4)~(6),可得状态点2的气体体积表达式为

对于Ⅰ型水合物,体系中两状态点间的气体变化量Δng,由方程(1)、(7)得
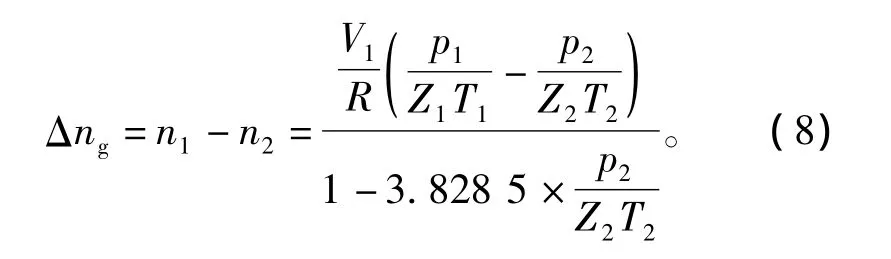
甲烷水合物反应热Q求解方程为

式中:q——单位摩尔量甲烷水合物反应热,kJ/mol。
若将气体和水生成水合物的过程看成是一个拟化学反应过程,那么可以用反应式(10)表示:
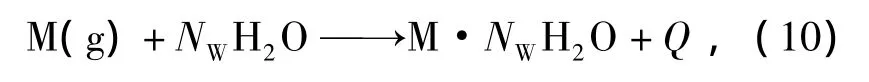
式中:M(g)——气体分子;
NW——水合数,即水合物结构中,水分子数和气体分子数之比。
水合物的生成过程是气体分子进入水分子以氢键结合成的笼型结构的吸附过程,是放热过程[4]。热量释放量与参与反应的客体分子(气体)和主体分子(液体)反应后生成的水合物量相关,水合物生成量多则热量释放多。Davidson[5]等对甲烷水合物进行研究得出甲烷气体的反应热为23.8 kJ/mol。
所以,联立方程(8)、(9)得出甲烷水合物反应热求解方程:
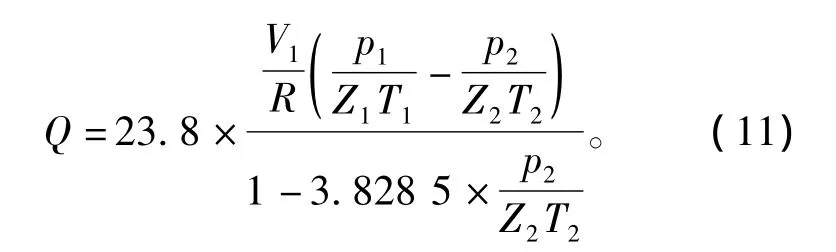
2 实验与结果分析
2.1 实验系统
用于实验的瓦斯水合分离实验装置(图1)主要包括水合固化器、恒温控制箱、气体压缩循环系统、数据采集系统等。该装置具备气体水合分离、瓦斯混合气组分在线分析等功能。
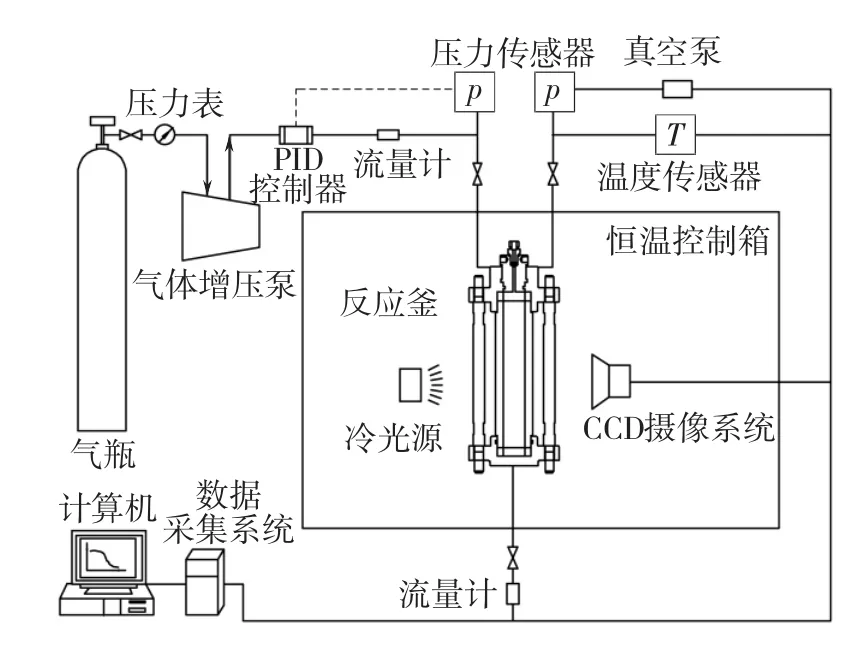
图1 瓦斯水合物高压实验设备系统Fig.1 Experimental set-up for high pressure test
利用该实验装置,在纯水体系Ⅰ、THF(1 mol/L)促进剂溶液体系Ⅱ和THF(1 mol/L)-SDS(0.1 mol/L)复配溶液体系Ⅲ中进行了甲烷水合固化过程反应热的实验研究,实验所用气体为体积分数为99.99%的纯甲烷。反应的初始温度、压力条件分别为1℃和5 MPa。
2.2 实验步骤
采用等温压力搜索法测定三种实验体系的水合物相平衡数据,具体步骤为:
(1)用蒸馏水清洗反应釜三次并吹干;
(2)配置复配溶液,放入制冷系统使溶液制冷至1℃,然后注入反应釜内;
(3)打开温度、压力数据采集系统,监测釜内温度、压力;
(4)充气管线与反应釜连接好后,利用真空泵对反应釜抽真空,至压力传感器指示值不再下降时结束;
(5)利用增压泵对釜内气体加压,至反应釜内气压达5 MPa;
(6)开启恒温箱,调节智能温控仪,将恒温箱温度调节到1℃;
(7)打开摄录系统,全过程观察釜内水合固化过程;
(8)当监测数据温度-压力-时间曲线在4 h内基本无变化时,认为水合反应结束。
2.3 实验结果及分析
通过数据采集系统得到实验过程压力随时间变化曲线,见图2。

图2 三种体系水合物生成压力与时间的关系曲线Fig.2 Relationship curves of pressure with time of hydrate formation in 3 systems
根据数据采集系统采集的水合反应过程中的数据,结合水合反应热求解方程(11),每间隔60 min计算出该时间范围水合反应热量,结果见表1。
从表1可以看出,在水合物生成结束前,相同的时间范围,纯甲烷水合固化过程产生的热量,体系Ⅲ>体系Ⅱ>体系Ⅰ。例如在1~60 min,体系Ⅱ产生的热量几乎是体系Ⅰ的两倍,体系Ⅲ产生的热量几乎是体系Ⅰ的三倍。究其原因,THF的添加,改善了甲烷水合物生成热力学条件,提高了水合物生成速率[6];THF-SDS的协同作用缩短了水合物生成诱导时间[7],提高了水合物生长速率,相同的时间范围内水合物的生成量多,产生的热量就多。

表1 不同时间区域水合反应产生热量Table 1 Caloric value of hydrate reaction in different time zone
3 结论
(1)建立了甲烷水合物反应热的计算模型,并对其进行了计算。
(2)促进剂的添加,缩短了水合物生成的诱导时间,改善了甲烷水合物生成热力学条件,提高了甲烷水合物的生成速率,导致水合过程中的反应热增多。
[1] 吴强,张保勇,孙登林,等.利用水合原理分离矿井瓦斯实验[J].煤炭学报,2009,34(3):361-365.
[2] 吴强,张保勇,王海桥.煤矿瓦斯固化防突及低浓度瓦斯固化分离新技术[J].黑龙江科技学院学报,2010,20(1):23-27.
[3] 吴强.矿井瓦斯水合机理实验研究[D].徐州:中国矿业大学,2005:94-96.
[4] 王如竹.吸附式制冷[D].北京:机械工业出版社,2002.
[5] JOHN L C.Natural gas hydrates:properties,occurrence and recovery[M].Boston:Butterworth,1983.
[6] 张保勇,吴强,朱玉梅.THF对低浓度瓦斯水合化分离热力学条件促进作用[J].中国矿业大学学报,2009,38(2):203-208.
[7] 吴强,张保勇.THF-SDS对矿井瓦斯水合分离影响研究[J].中国矿业大学学报,2010,39(4):484-489.
