情境中引发兴趣 探究中把握规律——苏教版化学2“乙醇”教学设计
2013-03-13高欣漫郑柳萍
高欣漫 郑柳萍
(福建师范大学化学与材料学院 福建 福州 350007)
一、教学背景分析
《乙醇》 是江苏教育出版社出版的高中课程标准实验教科书《化学2》(必修)专题3 第2 单元“食品中的有机化合物”第1 课时的内容。初中化学介绍了乙醇的化学式、俗称、物理性质、可燃性以及用途,但并未涉及乙醇的微观结构,官能团和除燃烧以外的化学性质。初中学生对乙醇的认识只停留在肤浅的表观阶段,需要进一步拓展认识。而本节课是在初中的基础上进一步学习乙醇的分子结构和化学性质,使学生构建“同一类有机物官能团决定其化学性质”的思维方法,为以后学习更复杂有机物奠定坚实的基础。
二、教学目标
1.知识与技能
(1)了解乙醇的物理性质。
(2)理解并掌握乙醇的分子组成和结构、乙醇的催化氧化和乙醛的催化氧化反应。
2.过程与方法
通过质疑、讨论解疑、对比实验等方法,培养由事物的表象解析事物的本质、判断、推理等能力。
3.情感态度和价值观
(1)感受我国源远流长的酒文化和古代劳动人民的勤劳智慧,增强民族自豪感。
(2)认识化学与人类生活密切关系,体验科学探究的艰辛和乐趣,激发学生学习化学的积极性。
三、教学重难点
重点:乙醇分子的结构和化学性质;
难点:乙醇分子结构的确定、乙醇催化氧化的理解。
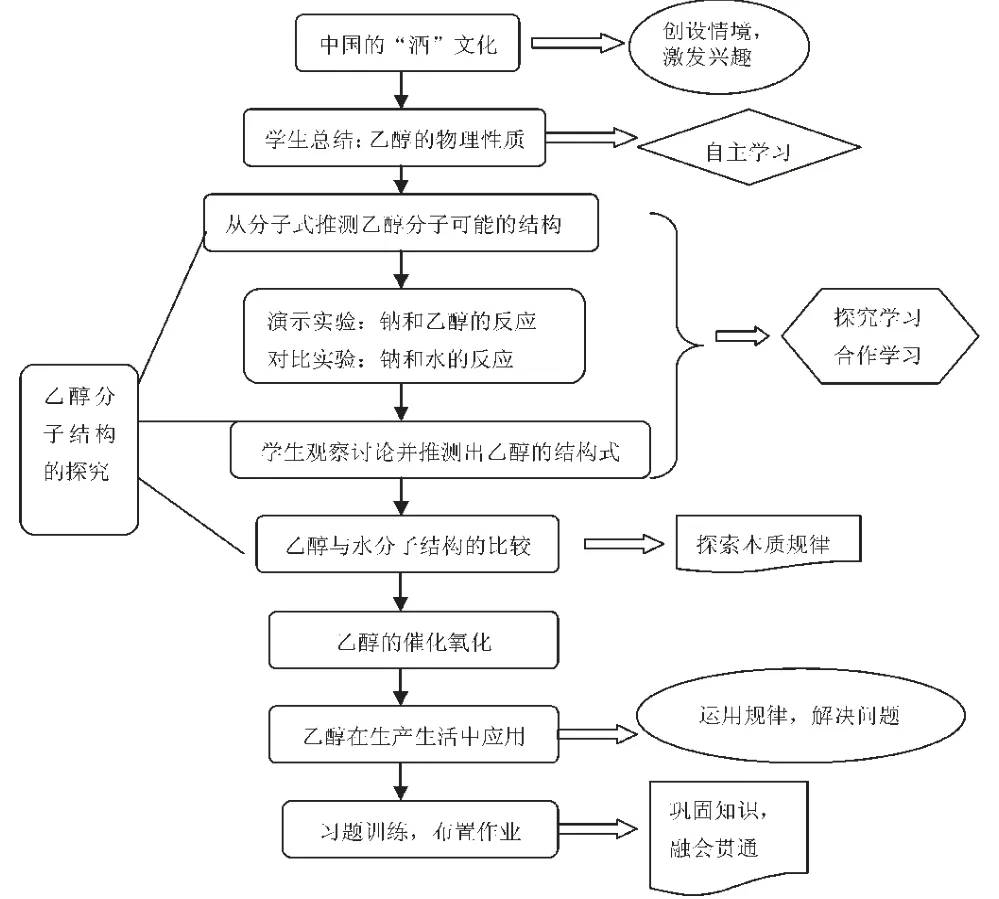
四、教学流程
五、关键性教学模块的分段解析
1.巧用中国源远流长的“诗酒文化”导课
[引入]中国自远古以来, 诗与酒就交织在一起,形成独具中国特色的“中国诗酒文化”。纵观诗酒文化发展史,酒醉诗美;诗借酒神采飞扬,酒借诗醇香飘溢。诗与酒,相映生辉,形成绚烂的文明景观。同学们,你们能举出和酒有关的古诗词吗?

图1 酒坛

图2 文人喝酒吟诗
[学生]纷纷响应:
(1)劝君更尽一杯酒,西出阳关无故人。——王维
(2)何以解忧,唯有杜康。——曹操
(3)借问酒家何处有? 牧童遥指杏花村。——杜牧
(4)白日放歌须纵酒,青春作伴好还乡。——杜甫
(5)今宵酒醒何处,杨柳岸、晓风残月。——柳永
……
(设计意图: 让学生课前收集关于酒的古诗词的资料,感受中国自古以来的诗酒文化。让课堂在师生热烈的讨论交流中开始,能显著地调动课堂气氛,激发学生的学习兴趣,让他们以更饱满的精神状态进入接下的课堂学习中。)
2.理论预测—实验探究,引导学生探究乙醇的分子结构:
[过渡]同学们,我们知道“结构决定性质”的化学学科思想, 那么乙醇的化学性质应与它的分子结构有关。乙醇(C2H6O)与乙烷(C2H6)的分子式只相差一个氧原子。而乙烷的分子构型为:
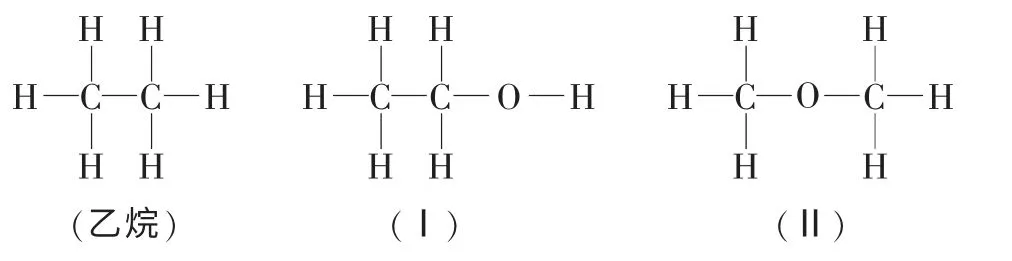
[设疑]根据乙烷分子的分子结构,同学们能否推测一下乙醇的分子结构式呢?
[板书]二、乙醇的分子结构
[学生]思考,讨论并得出结论。
(设计意图:学生分组合作学习,研究探讨乙醇的分子结构,培养他们独立思考的能力和合作精神,让学生在探究中把握有机物官能团和结构的本质规律。)
[过渡]究竟乙醇的分子结构是哪一种呢? 我们通过简单的实验来验证。
[实验探究]学生分组实验(教师指导)步骤如下:
(1)观察钠的保存方法;
(2) 取两支试管分别加入3~4mL 无水乙醇和水,再向两支试管中分别加入一小粒金属钠,观察实验现象;
(3)收集产生的气体,检验其是否可燃烧产生蓝色火焰。
[学生]观察并记录实验现象:
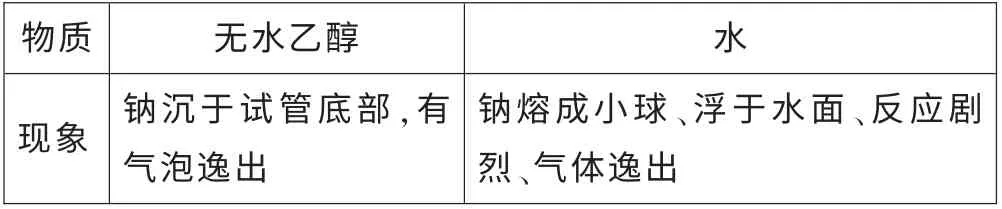
表1 无水乙醇、水与金属钠反应
经检验:该气体为氢气。
(设计意图:学生实验,培养其实验操作能力和观察思考能力。)
[讲解]大家注意:乙醇和金属钠反应比水和金属钠反应要缓和的多。
[引导]钠与乙醇、水反应时都产生氢气,说明钠能够置换出水和乙醇分子中的氢。由水分子的结构式为“H—O—H”, 可推测乙醇分子中存在与水分子相同的“O—H”键。
[学生质疑]也许是乙醇中与碳原子相连的氢被金属钠置换生成氢气呢?
[解疑]实验前我们观察过, 金属钠保存在什么中呢?
[学生]异口同声答:煤油!
[点拨]那煤油的主要成分是什么呢?
[讲解]钠长期保存在煤油中,而煤油是多种烷烃的混合物, 由此证明烷烃分子中与碳原子直接相连的氢(C—H) 不能被金属钠置换出来, 而是乙醇分子中羟基(—OH)上的氢原子被金属钠置换。
[得出结论]乙醇的分子结构是I 式。
[板书]分子式:C2H6O
结构简式:CH3CH2OH 或C2H5OH
官能团:—OH(羟基)
[提问]乙醇分子中羟基(—OH)上的氢原子与水分子中羟基—OH 上的氢原子相比哪个更活泼呢?
[回答]水分子中的。因为水与金属钠反应比乙醇与金属钠反应要剧烈得多。
[板书]三、乙醇的化学性质
1.乙醇与钠反应:
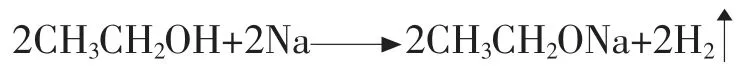
(设计意图:让学生学会根据实验事实推测结构,牢固建立“结构决定性质”的化学学科思想。)
3.指导学生动手实践,开展有关乙醇分子模型组装的趣味性活动
[学生探究活动]关于“乙醇分子结构”的探究活动:
(1)将学生分成2 人一组,教师向每组分发牙签10个、金桔2 个、冬枣1 颗、小西红柿6 颗,让学生根据前面学习的乙醇分子结构式来组装乙醇的水果实物模型。(牙签代表原子之间的共价键,金桔代表碳原子,冬枣代表氧原子,小西红柿代表氢原子。)
(2)学生组装完成后展示给全班同学并介绍自己的实物模型。

图3 水果实物模型
(3)待学生展示完毕后,教师点评并向学生展示乙醇分子的球棍模型和比例模型。
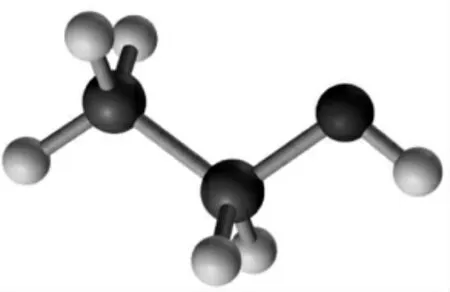
图4 乙醇的球棍模型

图5 乙醇的比例模型
[学生]观察乙醇的球棍模型并思考。
(设计意图:学生通过亲身体验、参与和合作探究学习,既体验了独立思考及动手操作的乐趣与魅力,又能更深刻把握乙醇分子结构的本质规律,在情境中引发兴趣,在探究中把握规律。)
4.联系实际,学习乙醇的催化氧化反应及产物
[情境导入]焊接银器、铜器时,表面会生成发黑的氧化膜,银匠说,可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初! 这实际上利用了乙醇另外一个重要性质——催化氧化生产乙醛。
[演示实验]向试管中加入3~4mL 无水乙醇, 浸入50℃左右热水中将铜丝烧热,迅速插入乙醇中,反复多次。
[学生]观察并感受铜丝颜色和乙醇气味的变化。
实验现象: 红热的铜丝,移离火焰变黑,迅速伸入乙醇中, 铜丝由黑变红, 同时产生刺激性气味。
[讲述]反应生成了乙醛。
[板书]2.乙醇的催化氧化:

图6 工人打造银饰
烧红的铜丝迅速插入乙醇中,反复多次。
图7 乙醇的催化氧化
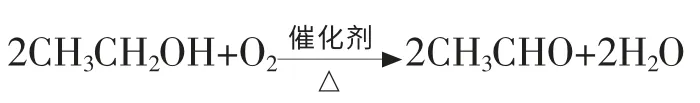
[补充]催化氧化的条件: 与-OH 相连的碳原子上要有氢原子(即羟基在末端的醇)。
(设计意图: 以银匠打造银饰的情景引入乙醛这种新的有机物,既增添了趣味性,激发了学生们的探究兴趣,又拓展了学生的知识,提高了将化学知识联系运用到生产生活中的能力,在情境中引发兴趣,在探究中把握规律。)
5.辨析有机物与无机物的氧化还原反应
[提问]有机物发生氧化还原反应的判断方法与以前学的无机物的氧化还原反应的判断方法一样吗?
[学生]不一样。以前学的无机物的氧化还原反应是在反应过程中有元素化合价变化。
[解疑]没错,一般有机物的氧化还原反应与无机物的氧化还原反应的判断不同, 把加氧或去氢叫氧化,加氢或去氧叫还原。而乙醇被催化氧化成乙醛,就是一个典型的去氢型氧化反应。
(设计意图:引导学生透过现象看本质,掌握乙醇和乙醛催化氧化反应的实质,区别有机物与无机物氧化还原反应的差异。)
6.联系生产生活,介绍乙醇的用途
[拓展视野]
(1)教师向学生介绍“乙醇的用途”:
乙醇有相当广泛的用途,除用作燃料,温度计,制造饮料和香精外,也是一种重要的有机化工原料,如用乙醇制造乙酸、乙醚等。乙醇又是一种有机溶剂,用于溶解树脂, 制造涂料。医疗上常用75%的酒精作消毒剂。
(2)教师指导学生阅读书本上“酒与酒精”的资料,了解工业酒精—甲醇的危害以及判断司机是否酒后驾车的化学原理。
(设计意图:使学生了解乙醇与社会生产、生活、学习、工作等等息息相关,知道工业酒精甲醇对人们身体健康的危害以及判断司机酒后驾车的化学原理,坚决抵制用甲醇配制饮料和酒, 损害他人健康的的不法行为,增强杜绝酒后驾车的观念。)
七、教学反思
教学设计的主线是 “在情境中引发学生对乙醇的学习兴趣, 在实验探究中把握乙醇的结构和性质的规律”。
1.开篇先让学生在吟诵关于酒的诗句中产生对乙醇这种物质的好奇心理,然后抓住教学最佳时机,趁热打铁进入新课的学习,然后在乙醇与金属钠反应的实验中进一步引导学生探究乙醇地分子结构。
2.紧接着为了让学生更好的理解乙醇的分子结构,进行了探究活动,让学生用牙签、小西红柿、葡萄等组装乙醇的实物模型,有效地激发了学生的学习兴趣,更加深刻地把握了乙醇结构的内在规律。
3.在乙醇被氧化的实验中,以银匠打造银饰的情景引入乙醛这种新的有机物,既增添了趣味性,又拓展了学生的知识面。
4.最后在介绍乙醇的用途时,教师引入了大量的事例, 让学生在丰富多彩的情境中结束了一节课的学习,让他们把学习到的化学知识和规律最终应用到生产生活实际中去,认识到化学是一门很实用的学科。
