苦杏仁苷凝胶制备工艺的研究
2013-03-06刘俊红卓玉珍李棣华张淑坤
刘俊红,卓玉珍,李棣华,张淑坤
(天津市南开医院,天津市中西医结合急腹症研究所,天津 300100)
苦杏仁苷凝胶制备工艺的研究
刘俊红,卓玉珍,李棣华,张淑坤
(天津市南开医院,天津市中西医结合急腹症研究所,天津 300100)
目的 筛选苦杏仁苷凝胶基质,确定制备工艺。方法 采用体外经皮渗透法,使用透皮扩散试验仪,用HPLC测定接受液中苦杏仁苷含量,以透皮速率为考察指标,通过正交试验筛选基质。结果 苦杏仁苷凝胶剂的优化处方组成为1%卡波姆、15%甘油、10%丙二醇、0.5%三乙醇胺。结论 该凝胶制备工艺简单,透皮效果好。
苦杏仁苷;凝胶;卡波姆;透皮吸收
苦杏仁苷(amygdalin)广泛存在于杏、桃、山楂等多种蔷薇科植物果实的种子中,尤其在苦杏仁中含量较多,大约在2%~3%。苦杏仁苷除具有止咳平喘作用外,还能预防和治疗因血黏稠度升高所致的脑缺血;治疗急性胰腺炎;增加皮肤组织微循环血流,促进伤口愈合等作用[1]。
苦杏仁苷口服后,会被肠道细菌产生的β-葡萄糖苷酶分解为氢氰酸和苯甲醛,氢氰酸既是有效成分也是有毒成分,少量对呼吸中枢可产生一定的抑制作用,使呼吸运动趋于安静而达到镇咳平喘的作用,如果大量服用苦杏仁苷,易产生氢氰酸中毒[2]。研究表明,苦杏仁苷静脉注射在小鼠、家兔及患者身上均未出现药物不良反应,从小鼠实验可见500 mg·kg-1静注苦杏仁苷,动物100%存活,而相同剂量灌胃,48 h内中毒死亡率竟达80%。说明苦杏仁苷的毒性与给药途径密切相关[3]。经皮给药系统可以使药物通过皮肤或黏膜的毛细血管直接进入血液循环,避免了胃肠道、消化液等因素的影响,减小不良反应,使用方便[4]。由于苦杏仁苷生物半衰期短,排泄快[5],本实验改变用药途径,拟制成通过透皮吸收而发挥作用的外用制剂——苦杏仁苷凝胶剂。
1 材料与仪器
1.1 动物
Wistar大鼠,♂,体质量200~250 g,由中国人民解放军军事医学科学院卫生学环境医学研究所动物实验中心提供,实验动物合格证号:SCXK(军)2009-003。
1.2 材料
苦杏仁苷提取物(南京泽朗医药公司,批号:ZL0902021A;含量:98.4%);苦杏仁苷对照品(中国药品生物制品检定所,批号:110820-200403,含量:98.8%);卡波姆-980NF(美国诺誉化工有限公司,批号:EC381CC244);丙三醇、丙二醇(湖南尔康制药有限公司,批号分别为20071014和20060321);三乙醇胺、对羟基苯甲酸乙酯、磷酸均为分析纯;甲醇为色谱纯。
1.3 仪器
TK-12B 型透皮扩散试验仪(上海锴凯科技贸易有限公司);SSI PC2000 型高效液相色谱仪(美国科学系统公司),EZChrom Elite Client/Server色谱工作站;AL104电子天平(梅特勒-托利多仪器有限公司);FE20型PH计(梅特勒-托利多仪器有限公司)。
2 方法与结果
2.1 体外透皮试验含量测定方法的建立
2.1.1 色谱条件 Alltech色谱柱(4.6 mm×150 mm,5 µm),流动相甲醇-0.1%磷酸水(20∶80),流速0.9 mL·min-1,检测波长210 nm,柱温35 ℃。
2.1.2 线性关系考察 取苦杏仁苷对照品0.06 g,精密称定,置10 mL量瓶中,加蒸馏水溶解稀释至刻度,摇匀,分别精密量取30,60,120 µL和2.5,5 mL置10 mL量瓶中,加蒸馏水溶解稀释至刻度,摇匀。精密吸取上述对照品溶液10 µL进样测定。以苦杏仁苷的质量为横坐标,峰面积为纵坐标,绘制标准曲线,计算回归方程Y=1.683 01× 106X-0.000 536 157,r=0.999 9,结果表明苦杏仁苷在0.019~6.400 µg内呈良好的线性关系。
2.1.3 仪器精密度试验 精密吸取苦杏仁苷凝胶剂样品溶液重复进样5次,记录峰面积,经计算RSD为3.0%,表明仪器精密度良好。
2.1.4 稳定性试验 分别于0,4,8,24,48 h,精密吸取苦杏仁苷凝胶剂样品溶液进样,记录峰面积,经计算RSD为1.11%,表明苦杏仁苷在48 h内稳定。
2.1.5 供试品溶液的制备 对于苦杏仁苷含量较低的凝胶剂样品,直接取接收液通过微孔滤膜;对于苦杏仁苷含量较高者,精密吸取原液1 mL加入10 mL量瓶,加蒸馏水稀释至刻度,摇匀,过微孔滤膜,即得。
2.1.6 加样回收试验 取苦杏仁苷凝胶,按“2.2”项下体外透皮吸收试验操作,6份,15 h后取样,作为样品原液,按“2.1.5”项下方法制备供试品溶液,按“2.1.1”项下色谱条件,依法测定含量;取上述已知含量的样品原液,精密量取1 mL,分别精密加入苦杏仁苷对照品原液0.25 mL及蒸馏水0.75 mL,混匀,再精密吸取混合液1 mL加入10 mL量瓶,加蒸馏水稀释至刻度,摇匀,过膜,精密吸取20 µL进样,依法测定,计算回收率为100.1%,RSD=1.74%。
2.1.7 专属性试验 除去苦杏仁苷配制空白凝胶,按“2.2”项下体外透皮吸收试验操作,15 h后取样,作为阴性对照液;按“2.1.5”项下方法制备供试品溶液,按“2.1.1”项下色谱条件,依法测定。结果阴性对照液在苦杏仁苷对应处没有相应的色谱峰,色谱图见图1。

图1 高效液相色谱图A-样品溶液;B-阴性样品;C-对照品;1-苦杏仁苷Fig 1 The HPLC chromatograms A-sample; B-blank; C-standard; 1-amygdalin
2.2 苦杏仁苷体外透皮试验
2.2.1 离体鼠皮的制备 取健康大鼠,♂,将大鼠麻醉后固定四肢,剪去腹部正中线两侧的鼠毛,再用电动剃须刀剃净绒毛后迅速剥皮,小心剔除皮下脂肪及组织,用滤纸擦拭干净,得离体鼠皮,放入冰箱(-20 ℃)冷冻保存,于1周内用完。
2.2.2 试验方法 采用TK-12B 型透皮扩散试验仪,将鼠皮从冰箱取出,放至室温,在接收池中放入磁力搅拌子,将鼠皮固定于扩散池与接收池之间,真皮面向接收池,接收液为蒸馏水。试验时,将精密称量的凝胶剂涂于处理好的鼠皮角质层,注满接收液,液面恰与皮肤真皮层接触,排除气泡。开动磁力搅拌器和恒温水浴,磁力搅拌转速设定为380 r·min-1,水浴温度(32±0.5)℃,扩散池容积6 mL,扩散面积为2.92 cm2。分别于1,3,5,7,9,24,32,48 h 取样,按“2.1.5”项下方法制备供试品溶液。取样时将接收池中的液体全部吸出,同时补加同样体积的新鲜接收液。
2.2.3 HPLC测定及数据处理 按“2.1.1”项下色谱条件,进样20 µL测定苦杏仁苷,计算透过量,并分别计算单位面积平均累积透过量Q,计算公式如下:
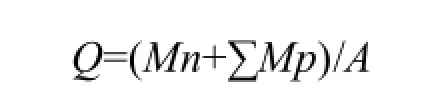
式中Q为t时刻的累积透过量(µg·cm-2);Mn为第n个取样点测得的药物透过量(µg);∑Mp为之前测得的药物透过量之和(µg);A为皮肤扩散面积。
以累积渗透量Q(μg·cm-2)为纵坐标,时间t(min)为横坐标作图,可以得到药物的累积渗透曲线。将累积渗透量Q对时间t进行回归,所得线性方程的斜率即为该条件下药物的稳态透皮速率J(μg·cm-2·h-1)。
2.3 正交试验
在初期已考察凝胶外观及理化性质基础上,设计制备所用的基质用量范围,如表1;采用4因素3水平,选用L9(34)正交表,见表2,以透皮速率为考察指标。按表2各试验号,将苦杏仁苷加适量蒸馏水溶解,加入卡波姆-980搅拌,放置2 h以上时间充分溶胀,再依次加丙三醇、丙二醇,对羟基苯甲酸乙酯乙醇液,最后滴加三乙醇胺,加蒸馏水至50 g,充分搅拌,即成凝胶剂。经过透皮吸收试验及HPLC测定及数据处理,得到各试验组稳态透皮速率,统计结果见表2,方差分析结果见表3。
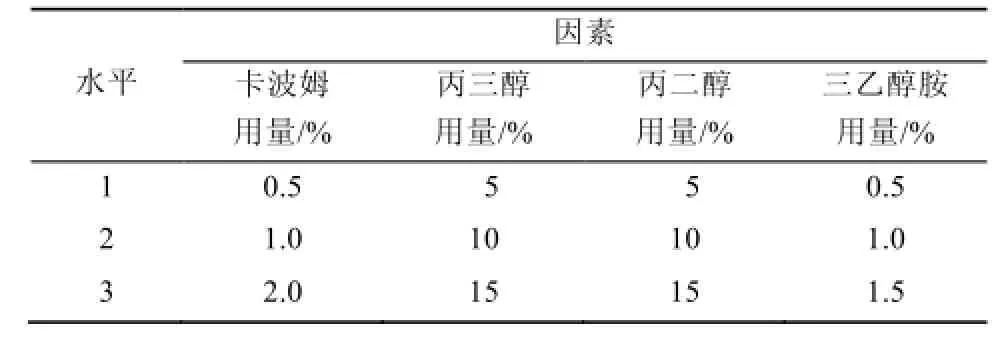
表1 因素水平表Tab 1 Level of experimental factors
由表2中极差R值大小显示,4个因素作用主次关系为A>C>B>D。方差分析结果表明,卡波姆用量及丙二醇用量有显著性差异(P<0.05),故选用A2B2C3D1工艺条件,即卡波姆用量1%,甘油用量10%,丙二醇用量15%,三乙醇胺用量0.5%。
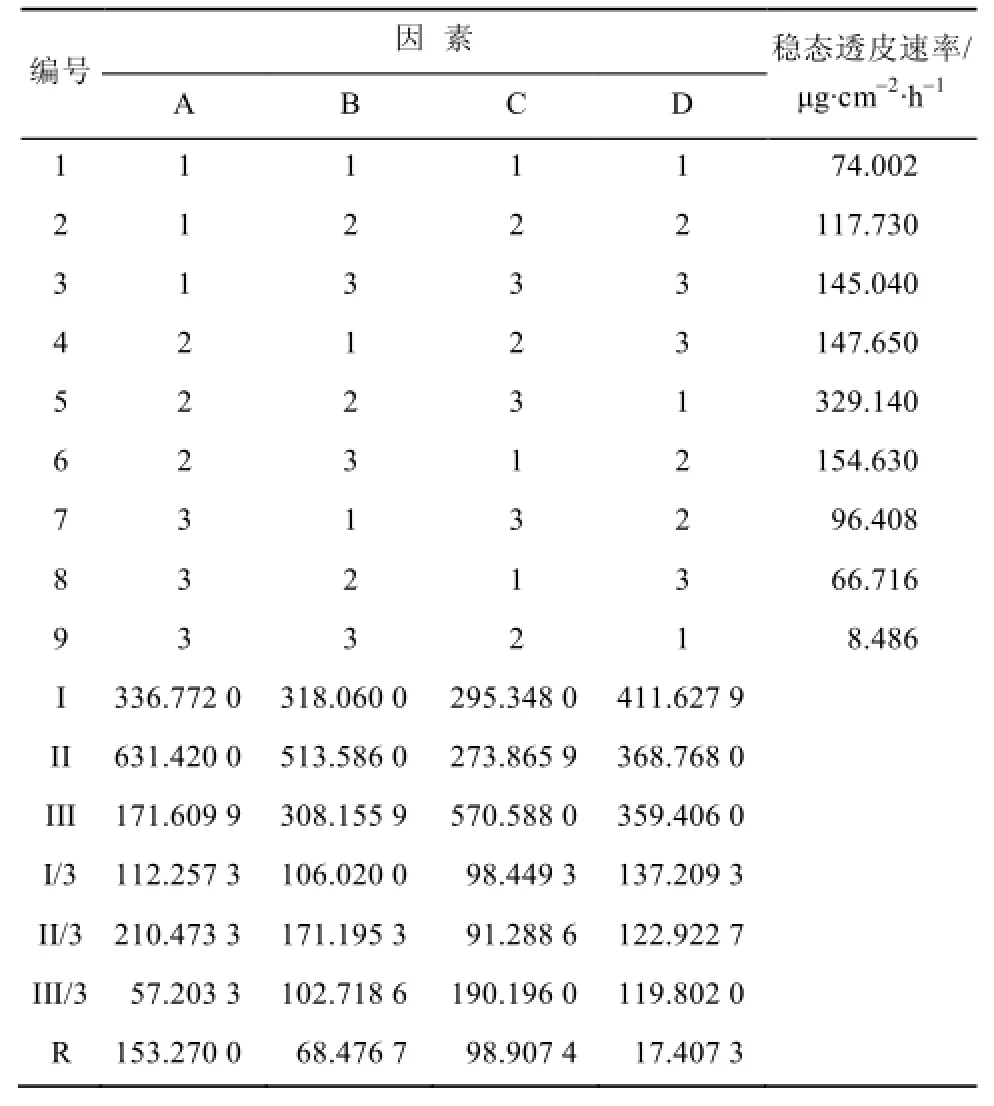
表2 L9(34)正交实验设计及结果表(n=3)Tab 2 Results of orthogonal experimental design(n=3)
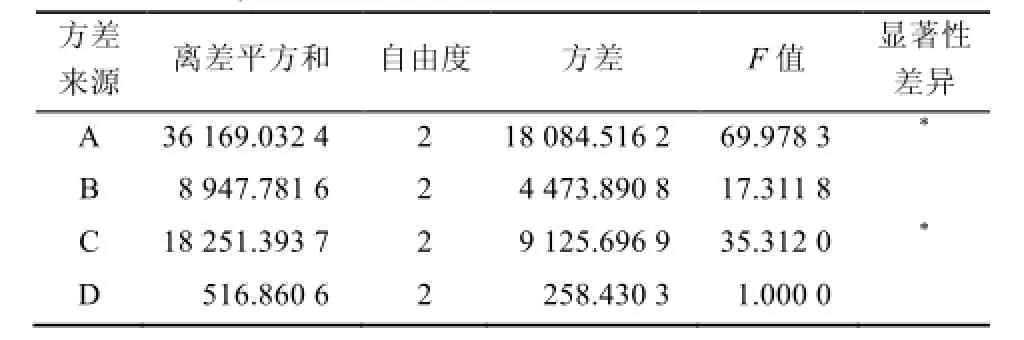
表3 方差分析表Tab 3 Analysis of variance
3 讨论
苦杏仁苷水溶性好,分子量较小,适于采用水溶性高分子材料为基质,配制成水溶性凝胶,与皮肤有较好的亲和性,能增强皮肤的水合作用,有利于药物的透皮吸收。经过试验证明氮酮和杏仁油对透皮吸收影响不大。因为丙二醇可渗入角质层并在其中形成积蓄,由此增加药物在角质层中的溶解性和分配性质,提高药物对皮肤的渗透性,对于苦杏仁苷,即使丙二醇单独作为促渗剂,透皮吸收效果也很好。前期工作已证明,注射苦杏仁苷能治疗急性胰腺炎;能预防和治疗因血黏稠度升高所致的脑缺血等作用;本课题小组经过药理实验证明本苦杏仁苷凝胶剂无皮肤局部刺激性和过敏性反应,具有活血、止痛作用,在保护胰腺外分泌功能和因脑缺血造成的脑含水量方面有确切疗效,现已得到专利授权。
REFERENCES
[1] WU X Z, WU X X, ZHAO L G, et al. Preparation of amygdalin and application in promoting blood circulation of heat, brain and pancreas: China ZL200610170297.1 [P]. 2007-07-04.
[2] ZHOU J H, WANG J M. Pharmacology of Chinese Materia Medica(中药药理学) [M]. Shanghai: Shanghai Science and Technology Press, 1986: 219.
[3] LI X M, LU W Q, QIN Z L, et al. Study on pharmacokinetics and toxicology of amygdalin [J]. New Drugs Clin Rem(新药与临床), 1986, 5(3): 141-143.
[4] LUO M C, WANG Z M, YANG Y. Preparation and evaluation of aciclovir thermosensitive gel [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2012, 29(9): 819-822.
[5] ZHANG G M, JIN B Q. Pharmacokinetics of amygdalin in rabbits [J]. Acta Phramacol Sin(中国药理学报), 1986, 7(5): 460-462.
Preparation of Amygdalin Gel
LIU Junhong, ZHUO Yuzhen, LI Dihua, ZHANG Shukun
(Tianjin Nankai Hospital, Tianjin Institute of Acute Abdomen in Integrated Traditional Chinese and Western Medicine, Tianjin 300100, China)
OBJECTIVE To screen amygdalin gel matrix to determine the preparation process. METHODS Using transdermal diffusion test instrument in vitro, the content of amygdalin in the received solution was determined by HPLC. Steady-state penetration rate was served as investigation indexes by orthogonal test. RESULTS Matrix dosage included 1%carbomer, 15% glycerin, 10%propylene glycol, 0.5% triethanolamine. CONCLUSION The preparation is simple, and the transdermal effect is good.
amygdalin; gel; carbomer; percutaneous permeation
R943
B
1007-7693(2013)10-1085-04
2013-02-19
国家自然科学基金项目(81102686)
刘俊红,女,副研究员 Tel: (022)27435360 E-mail: nlnbq@sina.com
