PVC体外循环管中TOTM溶出量的测定
2013-02-06广东省医疗器械质量监督检验所三水中心佛山528137
广东省医疗器械质量监督检验所三水中心(佛山 528137)
PVC 体外循环血路是尿毒症患者及肾病患者在血液透析时所必须使用的医疗器械产品。PVC室温下较硬且易碎,需要加入增塑剂以改善其柔韧性,目前最常用的增塑剂是邻苯二甲酸二异辛酯(简称DEHP)。研究表明,循环血路在使用过程中,增塑剂会溶出而进入人体[1]。动物试验研究表明DEHP 具有广泛的不良反应,明显表现为肝脏毒性和睾丸萎缩[2]。美国、日本建议在某些人群和一些特殊用途时不要使用含DEHP 的PVC医疗产品,欧盟更将其列入首批SVHCs(高度关注物质)名单中[3]。我国在《一次性使用输注器具产品注册技术审查指导原则》(简称《指导原则》)中也指出增塑剂不再局限于DEHP,更安全的医用增塑剂可以使用。
偏苯三酸三辛酯(简称TOTM/TEHTM)是目前DEHP 替代物之一,使用在PVC 体外循环血路中。虽然TOTM 具有生物体内代谢快,潜在毒性低[4,5],耐高温、低浸出[6]等优良特性,但《指导原则》中要求“非DEHP 增塑的PVC 医疗器械,需提交该增塑剂用于人体的安全风险分析报告”。本文拟通过模拟临床使用方式制备检验液,采用高效液相色谱测定循环血路中TOTM 的溶出量,并根据TOTM 的不良反应水平推导出其每日允许限量来评价使用TOTM 循环血路的安全性。
1.试验部分
1.1 实验仪器
LC-20AT 高效液相色谱仪(日本岛津,配PDA 检测器);
UV-2550 紫外分光光度计(日本岛津)
分析天平(精度为0.1mg);
液体比重天平
恒温水浴锅;
滚压式血泵/离心泵。
1.2 实验试剂和样品
无水乙醇:体积分数99.7%,密度ρ 为0.789g/ml~0.791g/ml;
浸提溶剂:用液体比重天平配置密度ρ 为(0.9373~0.9378)g/mL 的乙醇水混合液;
偏苯三酸三辛酯:优级纯,纯度98%,密度0.98g/cm3,折光率n20/D:1.485~1.487 ;
人工心肺机-体外循环血路样品(采用TOTM 为增塑剂)。

图1.TOTM紫外吸收谱图
1.3 色谱条件
色谱柱:岛津Inertsil ODS-SP C18 反相色谱柱(4.6×150mm,5µm, 配C18 保护柱)
检测器温度:40˚C;
检测波长:220nm;
流动相:甲醇;
流速:1ml/min;
进样量:10µL。
1.4 浸提溶剂
TOTM 是一种无色透明的油状液体,微溶于水, 25˚C 水中溶解度为0.13mg/L,可溶于醇、醚、酮等大多数有机溶剂。虽然体外循环血路与人体接触的是血液,但是由于血液来源受到限制,所以必须选用其他的浸提溶剂。本文参考DEHP 常用浸提介质—(0.9373~0.9378)g/mL 乙醇水溶液来浸提出TOTM。
1.5 样品前处理
根据产品的临床使用条件进行模拟试验来制备检验液。对于人工心肺机体外循环血路其临床使用时间一般为6h,本试验以12h 为检验液制备时间。取体外循环管路一套,按说明书的要求与泵连接,将管路的入液口和出液口插入到一个2L 的加盖容器中以形成一个密闭的回路。将2L 的浸提溶剂注入到容器中。然后将带有浸提介质的容器置入到37±1˚C 的水浴锅中。打开泵,将流速调至2L/min,使浸提溶液开始循环,在37±1˚C 下循环,取循环1h、3h、6h、12h 时的浸提液,作为供试液。
1.6 标准曲线
在乙醇中溶解0.1000gTOTM,用乙醇稀释至100ml,得溶液1,再精密移取1mL 溶液1 至10mL 容量瓶中,用浸提溶剂定容至10mL,制得10µg/mL TOTM 标准储备溶液。
分别精密移取TOTM 标准储备溶液0.5、0.5、1、2、5、10、25mLTOTM 标准储备液于100mL、50ml、50ml、50ml、50ml、50ml、50ml 容量瓶中,用浸提溶剂定容,配成浓度为0.05、0.1、0.2、0.5、1.0、2.0、5.0µg/mL 标准系列溶液,经0.45µm 过滤头过滤,按以上色谱条件进样,每个浓度重复测定三次,分别以峰面积平均值与各对应浓度绘制标准曲线。
1.7 含量测定方法
1.7.1 吸收波长的选择
以ρ 为(0.9373~0.9378)g/mL 的乙醇水混合液为参比,扫描TOTM 标准溶液在200nm~320nm的紫外吸收,图1 表明TOTM 在200nm~250nm之间吸收较强,选取220nm 为液相色谱PDA 检测波长。
1.7.2 TOTM 的含量测定
取浸提液,经0.45µm 过滤头过滤,得检验液,按以上色谱条件进行液相色谱分析,色谱图见图2,TOTM 出峰时间为5.600min。
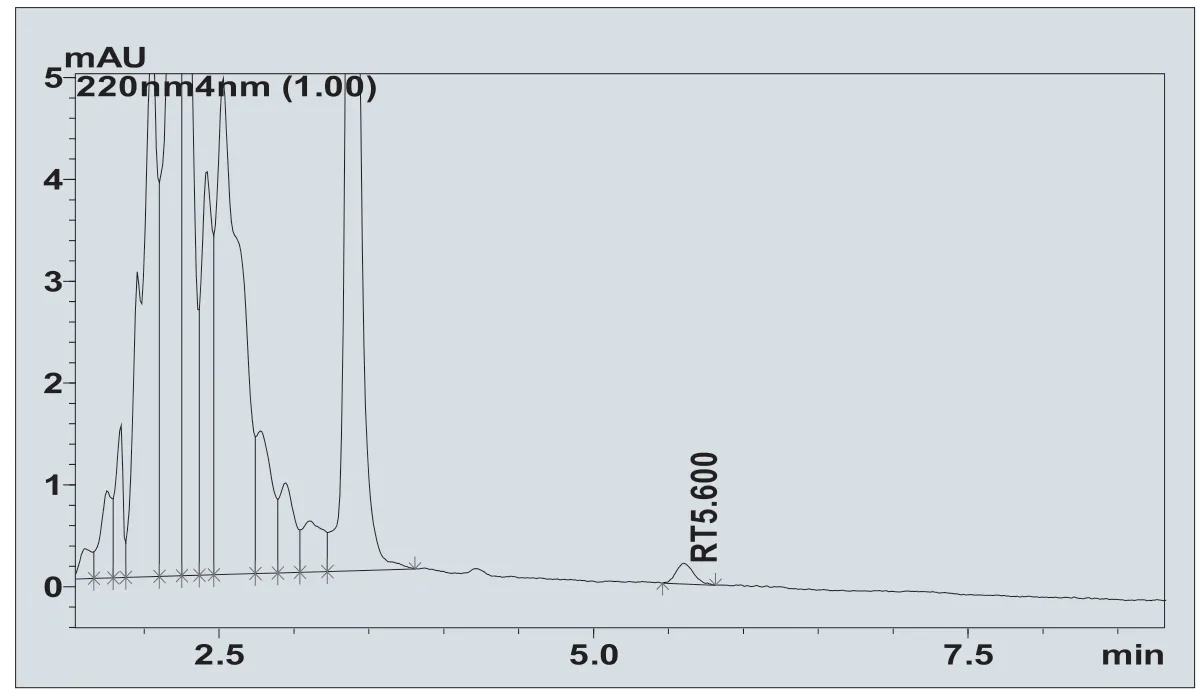
图2.TOTM液相色谱图
2.结果分析
2.1 方法学考察
2.1.1 线性范围及检测限
TOTM 在0.05~5.0µg/mL 范围内线性关系良好,回归方程为y=16959x+232.34,R2=0.9998。检测限为0.0110µg/mL。
2.1.2 加标回收率及精密度
被测样品中分别精密加入浓度为0.0600µg/mL、0.0800µg/mL、0.1000µg/mL 的TOTM 标准品溶液,按上述色谱条件测定,每个样品测试6次,计算平均回收率。表1 中结果表明该方法的准确度较高,回收率为95.9%~98.7%,RSD 为0.12%~0.35%。
2.2 TOTM 允许限量(AL)
根据日本OECD SIDS 数据[7],以大鼠试验,TOTM 的重复剂量毒性和生殖毒性(雄性)是最大的,其不良反应水平(NOAEL)都为100mg/kg bw/day,而雌性及后代的生殖毒性为1000mg/kg bw/day,因此一般以雄性生殖毒性来研究TOTM安全性研究的毒性特征。TOTM 允许限量依据GB/T16886.17-2005《医疗器械生物学评价 第17部分:可沥滤物允许限量的建立》进行推导。
2.2.1 可耐受摄入量(TI)

UF1— 表示人体间的个体差异,根据动物对毒性试剂的安全评估,选用缺省值10
UF2— 表示从替代物种数据的推导而不是人类数据,参考FDA 推导DEHP 时的值3
UF3— 表示实验数据的定性和相关性,本试验有缺乏支持性研究、终点评估中不适当动物模型的使用以及不适当的接触途径等不确定因子,因此设定为3。
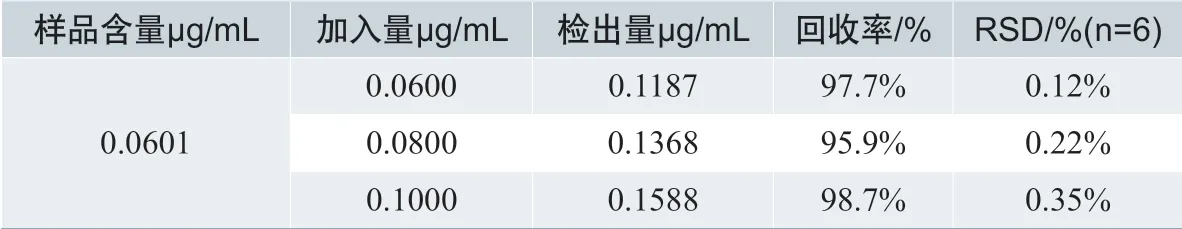
表1.回收率测定结果(n=6)


表2.各时间段TOTM 溶出量

图3.TOTM溶出量随时间的变化
2.2.2 TOTM 可耐受限量(TE)
TE=TI×m×UTF UTF=CEF×PEF
m— 医疗器械接触群体的体质量,成人默认值为70kg
CEF— 多器械接触因子,取缺省值0.2
PET— 比例接触因子,取缺省值1
TE=1.11 mg/kg bw/day×70 kg×0.2×1=15.54 mg/day
2.2.3 TOTM 允许限量的确立
允许限量即可沥滤物通过医疗器械接触进入人体时,认为每天可接受的最大量,即判断TOTM 的每天能接受的最大量。
AL=TE×BF
BF— 为受益因子,因体外循环管中TOTM的溶出量在技术和经济上都是可行的,因此不进行受益评价,受益因子设为1。
AL=TE=15.54 mg/ day
2.3 TOTM 溶出量分析
取1h、3h、6h、12h 时的供试液,按以上色谱条件检测, TOTM 浸出量随时间的变化见图3 所示。
由以上实验结果知,体外循环血路浸出浓度在0.0534~0.0601µg/mL 之间,可能是因为溶出量浓度较低,造成取样浓度不均匀,有以上的趋势图,总体溶出量还是呈比较平缓的上升趋势,浸提12h 的检验液TOTM 溶出量为0.0601µg/mL,2L 浸提液中TOTM 溶出总量可通过以下式计算可得:
总溶出量(mg)=0.0601µg/mL×2000 mL=120.2µg
由结果可以看出,浸提12h 后,体外循环管总溶出量为120.2µm,即人体可能接触到的TOTM 为0.1201mg/12h,远小于上述推导出的TOTM 允许限量15.54 mg/ day,在安全限量范围内。
3.总结
TOTM 作为一种新型的具有潜力的环保增塑剂,其大量的使用必然要求对其溶出量进行测定和安全性评估,本文采用高效液相色谱法测定TOTM 溶出量,具有准确性高、重复性好等优点。而TOTM 允许限量的建立涉及支持性研究、不适当动物模型等不确定因素,因此本文允许限量的建立仅适用于本试验产品。本试验中TOTM 溶出量是以乙醇水溶液为浸提介质,与临床使用血液作为浸提介质的差别还有待考究。另外,试验中浸提时溶剂的循环速度对溶出量有较大的影响,循环速度大小和溶出量的关系尚待进一步的研究。
[1]卢忠,胡相华,何小帆.在体外循环血路行业标准中增加常用化学粘合剂残留量检测的建议及检测方法设计.中国医疗器械信息 16,48-50(2010).
[2]FDA.Safety assessment of di(2-ethylhexyl)phthalate(DEHP)released from PVC medical devices.Center for Devices and Radiological Health,US Food and Drug Administration,Rockville.http://www.fda.gov/cdrh/ost/dehp-pvc.pdf(2001).
[3]杨晓冬.PVC 医疗器械中增塑剂DEHP 的安全性评价.中国医疗器械杂志 36,118-120(2012).
[4]K.Kambia,T.Dine,R.Azar,et .Comparative study of the leachability of di(2-ethylhexyl)phthalate and tri(2-ethylhexyl)trimellitate from haemodialysis tubing.International journal of pharmaceutics 229,139-146(2001).
[5]European commission.Opinion on the safety of medical devices containing DEHP-plasticized PVC or other plasticizers on neonates and other groups possible at risk.Health &Consumer Protection Directorate-General(2008).
[6]Raumedic AG.Migration of platicizers from PVC tubes into contact media.Fraunhofer Institute for Process Engineering and Packaging IVV,1-13(2010).
[7]OECD SIDS.SID Initial Assessment Report for SIAM14.UNEP PUBLICATIONS,1-118(2002).
