美国和日本核桃RAPD-PCR反应体系优化
2012-12-28KeithWoeste张存旭张硕新
赵 鹏 ,Keith E.Woeste,张存旭 ,程 飞 ,张硕新,蔡 靖
美国和日本核桃RAPD-PCR反应体系优化
赵 鹏1,2,3,Keith E.Woeste2,张存旭1,程 飞1,张硕新1,4,蔡 靖1,4
(1.西北农林科技大学 林学院,陕西 杨凌 712100 ;2.美国普渡大学 森林与自然资源系,美国农业部阔叶树种改良与更新中心, 西拉法叶市 印第安纳州 47907,美国;3.西北大学 生命科学学院,西部资源生物与现代生物技术教育部重点实验室,陕西 西安 710069;4.陕西秦岭森林生态系统国家野外科学观测研究站,陕西 宁陕 711600)
核桃属种质资源丰富,其中多数物种木材材质优良,果实可食,营养丰富,为重要的经济树种。以美国白核桃Juglans cinerea、日本核桃Juglans ailantifolia等为材料,通过改良CTAB方法,从嫩芽、新鲜叶片和干叶片中分别提取核桃基因组DNA,并以此DNA为模板对RAPD-PCR反应体系中的一些重要参数进行摸索和优化试验。结果表明,改良的CTAB法可有效去除细胞内多糖和多酚等杂质对模板DNA的污染, 大大提高DNA的数量和质量。优化适合于美国核桃、日本核桃和杂合核桃的RAPD-PCR反应体系为:在20 μL的PCR反应体系中, 含10 ng 模板DNA, 0.1 mg/mL 牛血清蛋白(BSA), 0.25 mmol/L dNTPs, 3.5 mmol/L Mg2+,1 μL 10×Taq DNA 聚合酶反应缓冲液, 0.5 U Taq聚合酶, 5.0 mmol/L RAPD引物。RAPD-PCR反应扩增程序为:92℃变性 3 min;93℃ 变性 1 min,35℃ 复性1 min,72℃延伸 1 min,35个循环;72℃后延伸10 min,置4℃ 保存。
美国白核桃;日本核桃;RAPD;优化
核桃属Juglans 是胡桃科Juglandaceae 的一个进化属[1], 该属成员多为重要的经济林树种, 不仅能生产营养价值高的食用核桃果仁,而且木材材质好、生长快[2]。核桃属植物在全球的栽培历史久远,种质资源极为丰富,约有21个种[3],是一个非常重要的用材和坚果经济树种之一[4]。美国白核桃J.cinerea,也叫白核桃、灰核桃、油核桃或柠檬核桃,是一种短期生长、耐寒、速生的用材和经济树种[2-3,5], 可以生产优良木材,果实可以食用并可榨油。20世纪70年代,该树种受到一种外来病菌Sirococcus clavigignenti-juglandacearum 的危害,已濒临灭绝[3]。日本核桃J.ailantifolia,又称为心核桃,源产于日本和库页岛[6],1870 年被引入美国[7-8]。美国黑核桃 J.nigra 通常也称为东方黑核桃或者美国核桃,为经济价值较高的用材树种[9],在我国栽培十分广泛。我国核桃属植物栽培历史也十分悠久,在长期进化与栽培过程中,表现出了一些特有的优良性状,如孤雌生殖、早实[10]、丰产和抗性强等。目前,我国主要栽培的核桃品种有以下6个种:分别是核桃J.regia、铁核桃J.sigillata、美国黑核桃J.nigra、麻核桃J.hopeiensis、胡桃楸J.mandshurica和野核桃J.catheayensis[1,11-12]。
随着分子生物学的发展,20世纪90年代后DNA分子标记开始广泛应用于植物分子遗传育种、分子进化等研究领域。DNA分子标记是DNA分子水平上遗传多态性的直接反应,表现为核苷酸的差异[13-14]。随机扩增多态性DNA 分子标记 (Randomly Amplified Polymorphic DNA) ,简称RAPD,常常呈共显性遗传[13]。应用RAPD分子标记技术进行物种品种鉴定,方法简单、快捷、可靠,不需要任何前期DNA模板信息[4,13,16]。国内外也曾报道有RAPD技术在核桃属植物核桃的研究和应用[10,15-16]。但是针对美国白核桃、美国黑核桃、日本核桃和杂种核桃的RAPD-PCR反应体系报道较少。DNA的提取和RAPD-PCR反应体系的优化,是对核桃属植物进行遗传育种等分子生物学研究必须首先解决的关键问题之一。 本研究的目的:(1)以美国白核桃、美国黑核桃、日本核桃和杂种核桃为试验材料,研究优化从叶片中提取基因组总DNA的方法和步骤。(2)进一步研究以上几个核桃属植物RAPD反应体系中各种组分的浓度、PCR反应的温度和反应程序等对PAPD-PCR扩增的影响效果,找出适合以上几个树种的RAPD-PCR反应体系的优化方案,从而为核桃属植物在分子水平开展的相关研究奠定良好基础。
1 材料与方法
1.1 试验材料
美国白核桃和杂种核桃试验样品来源于美国不同州和地区的马特尔(Martell)核桃遗传育种试验地;日本核桃采集于美国加州国家种质资源中心;美国黑核桃样品采集于印第安纳州巴特勒维尔(见表 1)。4月份从健康植株上采集嫩芽,5月份从健康植株上采集当年生新鲜嫩叶2~3片(单株),放入标记好的塑料袋中,用保温箱迅速运回实验室,保存于4℃ 冰箱中,备用。
1.2 试验方法
1.2.1 DNA的提取与分离方法
DNA的提取与分离参照Doyle and Doyle等人提出的CTAB法[17],并在此基础上进行了改良。称取约100 mg新鲜叶片,去除叶脉 (或者采用干叶片),放入2 mL screw-cap试管中,并加入2粒0.5 cm 大小的硬珠豆(Bio 101-Savant, Carlsbad, CA,USA),再加入 1 mL CTAB 提取缓冲液[18]。缓冲液包括 2% CTAB (hexadecyltrimethylammonium bromide), 50 mmol/L TrisCl, 20 mmol/L EDTA, pH值8.0, 1.4 mol/L NaCl, 0.4 mol/LLiCl, 2% PVP(polyvinylpyrrolidone), 2% SDS。 然 后 用 快 速离心机研磨,研磨之前迅速加入β-疏基乙醇(β-Mercaptoethanol,2%)。将样品在研磨机(Fast Prep 120,Bio 101-Savant, Carlsbad, CA) 转速为55的速度下混匀,40 s 3次,每次间隔期间将样品放到冰上冷却3 min。研磨之后,将样品放到65 ℃ 的杂交炉中匀速旋转,过夜后取出样品,加入400 μL氯仿并轻轻混匀,室温13 000 r/min离心5 min。取上清液置1.5 mL离心管中,加入450 μL 混合液(V苯酚∶ V氯仿∶ V异戊醇=25∶ 24∶ 1)后轻轻混匀,室温13 000 r/min 离心10 min。取上清液置1.5 mL离心管中,加入400 μL氯仿并轻轻混匀,室温13000 r/min离心5 min(重复2次)。再取上清液置1.5 mL离心管中,加入 90 %的冷却异丙醇(4 ℃)和 10 % 的醋酸钠(3 mol/L NaAc, pH 6.8)并轻轻混匀,室温19 000 r/min 离心15 min。去上清夜,加750 μL的70 % 乙醇洗2~3次,轻轻将乙醇液体倒掉,注意保留离心试管底部的白色结晶状物质,室温干燥后溶于TE 缓冲液(10 mmol/L of Tris, 1.0 mmol/L of EDTA, pH值 8.0)中, 在37℃水浴锅中放置40 min, 然后置于4℃冰箱保存。
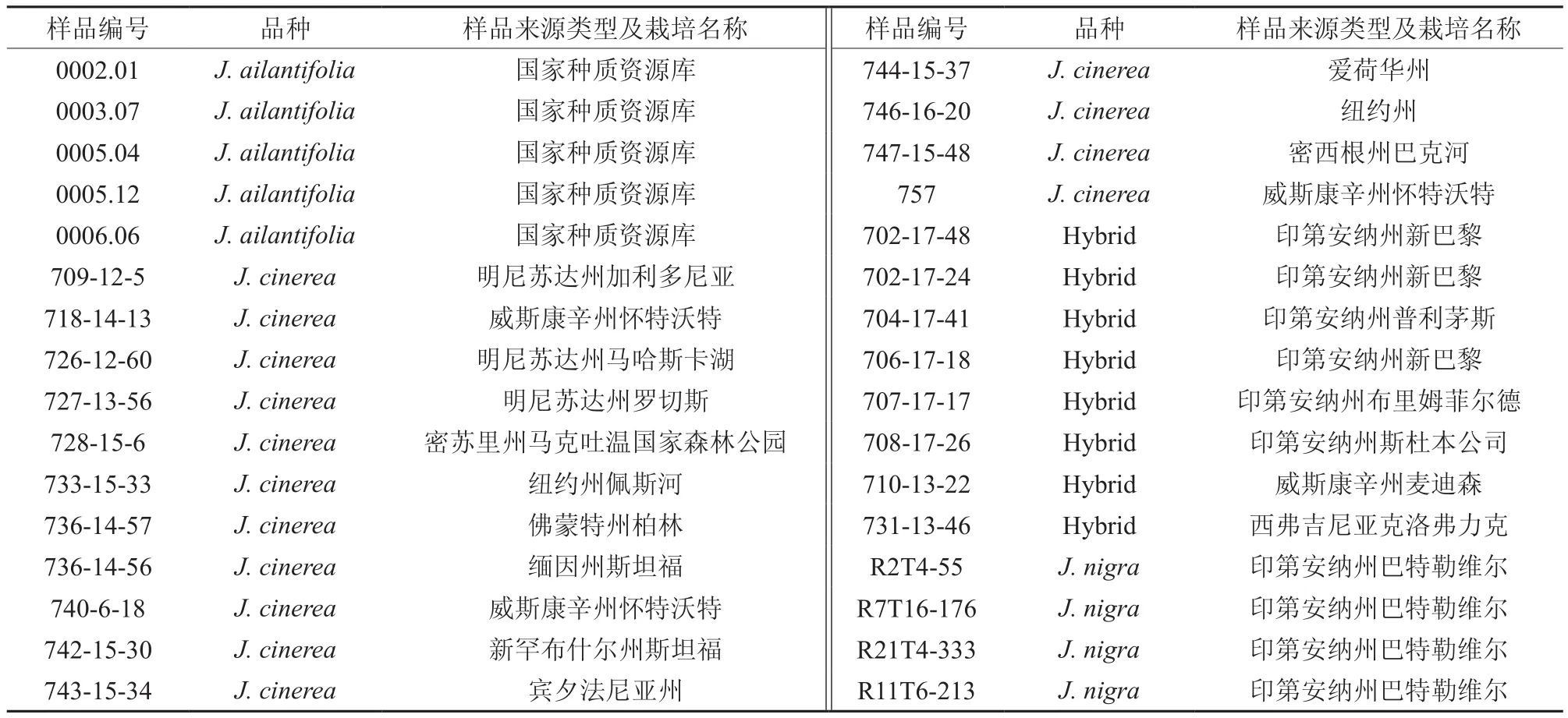
表 1 核桃样品与种质资源信息Table 1 Sample information and the sources of germplasm for this study
1.2.2 DNA检测方法
分别采用分光光度计和琼脂糖凝胶电泳检测DNA的浓度和纯度。TE缓冲液作为空白对照,用 NanoDrop-8000分 光 光 度 计 (Thermo Fisher Scientific, Wilmington, DE 19810, USA) 检测DNA质量和浓度。用含有5 mg/mL溴化乙锭的1.0 %琼脂糖凝胶电泳检测DNA质量。DNA在稀释至所需要的浓度后,保存于-20℃冰箱,初始浓度的基因组DNA置于-80℃冰箱中保存。
1.2.3 PCR 扩增和PCR产物的检测
PCR扩增引物为40个RAPD序列引物由Gene link 公司合成 (见表2)。PCR扩增反应以Williams等[12]和Woeste等[14]的反应体系为基础。Taq DNA 聚合酶反应缓冲液 [100 mmol/L Tris-HCl, pH 值8.8, 15 mmol/L MgCl2, 500 mmol/L KCl and 0.01% (w/v)gelatin] 购于 Stratagene 公司(La Jolla, California, USA), Taq DNA聚合酶、dNTPs和牛血清蛋白(Bovine Serum Albumin , BSA) 购于Promega 公 司(Madison ,Wisconsin, USA)。PCR 反应体系 20 μL,其中 dNTPs 0.2 mmol/L,BSA 0.5 mg/mL,TaqDNA聚合酶0.3 U,引物浓度为 0.8 μmol/L, Mg2+浓度为 1.5 mmol/L, DNA 模板质量浓度为5 ng/L。当一种反应成分进行浓度(用量)梯度变化实验时,其它反应成分浓度或者用量不变,通过比较不同处理对RAPD-PCR扩增结果的影响进行分析。PCR反应成分的处理因素和水平设计见表 3。 PCR 扩增程序为:94℃变性5 min;93℃变性 30 s,35℃退火30 s,72℃延伸45 s,35 个循环;72 ℃后延伸 10 min,置 4℃ 保存。
每个 PCR 产物 (10 μL) 与 0.5 μL 上样液 染 料 (40 % w/v sucrose, 15 % ddH2O和 30 %glycerol)混合上样,采用1×TAE缓冲液制成2.0%的凝胶琼脂糖电泳胶,加荧光嵌入染料溴化乙啶(Ethidium Bromide, EB)染色到电泳胶中,然后设置90 W 恒功率电泳,约1.5 h,溴酚蓝指示剂跑至接近胶底部时,终止电泳。用凝胶成像仪(75312 Bad Wildbad, Germany)检测PCR产物扩增,DNA 片段大小标准用100 bp ladder(Madison,Wisconsin, USA)。
2 结果与分析
2.1 提取核桃基因组DNA的改良CTAB方法
实验(见图1)表明,采用改良后的CTAB方法均适合于从老叶、新叶、干叶和嫩芽中获得高浓度和纯度的DNA,有效地降低多糖和酚类物对DNA的污染。改良后的CTAB法,从核桃新鲜叶片中所得到的DNA样品浓度高,平均为763.4 ng/μL,是大部分实验结果DNA提取浓度50 ng/μL的15倍左右;从干叶片中提取出来的DNA浓度平均为196.84 ng/μL,从嫩芽得到的DNA平均浓度为 2 980.4 ng/μL,分别是普通鲜叶片和干叶片的3.9倍和15.1倍。分别从新鲜叶片、干叶片和嫩芽中获得的高质量DNA均可以进一步用于分子生物和分子遗传学等方面的实验操作。DNA测定的A260/A280值平均为2.10,A260/A230值平均为2.04,符合基因组DNA的最佳范围值,说明改良后的CTAB法可应用于从核桃属植物新鲜叶片和干叶片中提取高质量和纯度的DNA。试验中,采用改良CTAB法,得到的DNA沉淀呈乳白色结晶状,加TE缓冲液易溶解,1 % 琼脂糖凝胶电泳检测时,点样孔无带,且主带非常明显 (见图 1)。

表 2 40个随机多态性DNA引物序列Table 2 Sequence of forty RAPD primers used in this study
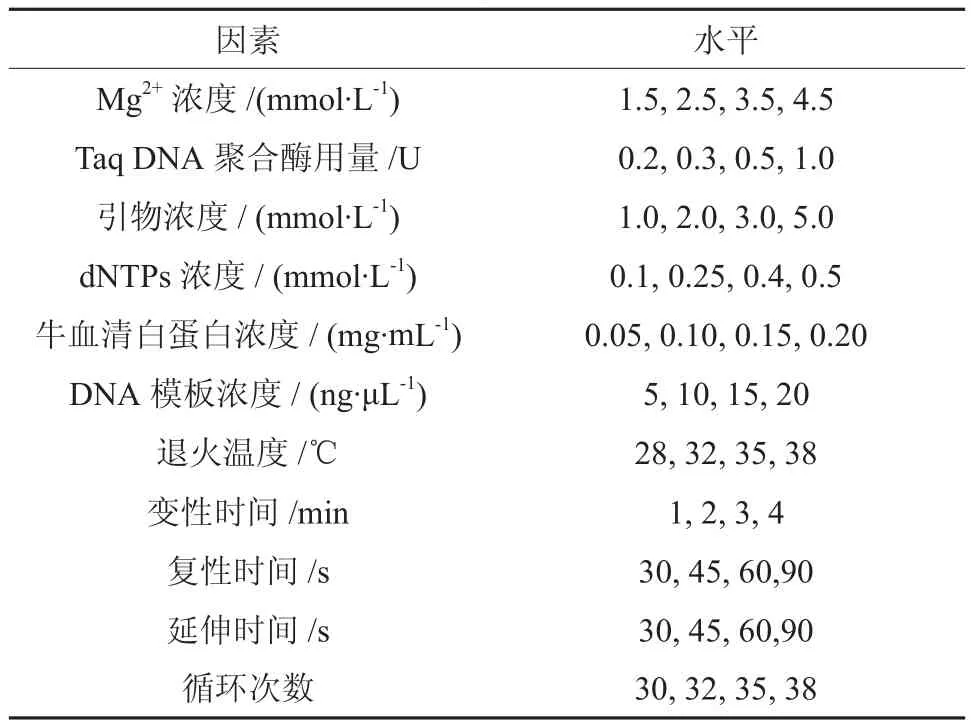
表 3 RAPD-PCR 反应体系的处理因素和水平设置Table 3 The design factor and level of RAPD-PCR reaction system

图1 改良CTAB法提取总DNA的电泳检测结果Fig.1 Agarose gel results of genomic DNA products using improved CTAB method
2.2 RAPD-PCR反应体系
2.2.1 Mg2+和TaqDNA聚合酶浓度的影响
当Mg2+浓度为1.5 mmol/L 和2.5 mmol/L,TaqDNA聚合酶浓度为4个设置的用量时,均产生少量DNA条带,PCR扩增效果不佳。从扩增结果可知,当Mg2+浓度梯度为3.5 mmol/L时,TaqDNA聚合酶浓度为0.5 U 组合时扩增DNA特异条带最为清晰,扩增多态性强且效果最好(见图 2)。

图2 不同Mg2+和TaqDNA聚合酶浓度条件下RAPD-PCR扩增产物结果Fig.2 Results of RAPD-PCR products using different Mg2+ concentration and different amount of Taq DNA polymerases
2.2.2 模板DNA和引物浓度的影响
引物浓度对RAPD-PCR扩增影响较大,引物浓度在1.0 mmol/L和2.0 mmol/L时没有任何PCR产物。模板DNA浓度对PCR扩增效果影响不大,对几个不同种的核桃和杂种核桃样品扩增试验结果为,DNA模板浓度为 10 ng/μL和引物浓度为5.0 mmol/L组合时得到的RPAD-PCR扩增产物效果最好。
2.2.3 BSA和dNTPs浓度的影响
结果表明,BSA浓度梯度对RAPD-PCR扩增影响并不显著。当BSA 浓度为0.10 mg/mL时,DNA特异条带最为清晰。在此基础上,dNTPs浓度为0.25 mmol/L时得到的PCR产物效果非常好。
2.2.4 反应扩增程序的影响
研究发现,2个RAPD引物组合进行PCR扩增时退火温度为35℃效果最好。对变性温度和时间筛选结果表明,在 93℃下1 min效果最为理想;退火时间和延伸时间也均为60 s时,扩增结果最好。热循环次数分别设置了30、32、35和38。结果表明,在35个循环下,扩增的条带多态性最好,如果降低循环次数,扩增条带多态性会降低。
经过对RAPD-PCR优化后,采用美国白核桃、美国黑核桃、日本核桃和杂种核桃的DNA样品分别进行了试验,均可以到很好的PCR扩增效果(见图 3)。
3 讨 论
3.1 基因组总DNA提取方法
DNA的提取是分子生物学研究的基础技术,近些年来一些新的或者改良的DNA提取纯化方法不断出现[19-20]。不同植物DNA提取方法往往有差异,特别是富含多糖及多酚类物质的果树叶片中提取DNA方法难度大于禾谷类及蔬菜类植物[21-22]。从核桃属植物叶片中用CATB法提取基因组总DNA主要有以下几个方面的改良和优点:一是,加入2粒硬珠豆在试管中,在快速离心机的研磨后,放到杂交炉中,设置65 ℃匀速摇晃过夜,使得细胞充分破裂,有利于提纯。二是,加入更多的SDS(2 %)能使裂解细胞变易,使染色体离析,蛋白变性,同时SDS与蛋白质和多糖结合成复合物,释放出核酸。这样就可以很好地裂解细胞,去除较多的糖类杂质。三是,适当加大β-巯基乙醇剂用量,能防止多酚污染。同时,用苯酚、氯仿、异戊醇的混合液(v/v,25∶24∶1)提纯步骤,可以提高DNA质量,因为异戊醇可以减少提取震荡过程中的气泡产生。四是,提取的每个步骤过程中,可加入50~100 μL的TE缓冲液,可以大大增加上清液的量,并且可以得到更多的DNA,获得的DNA纯度高、数量多,并能够满足各种分子生物学试验要求。CTAB法经过改良之后,操作简单,不需要太多的仪器。缺点是操作步骤相对繁琐。利用核桃的鲜叶片和干叶片对改良后的CTAB法进行了检测,提取DNA纯度和质量都很高。在CTAB中加入2 %的PVP可以有效去除多糖,并可与多酚结合形成复合物,从而有效避免多酚类化合物介导的DNA降解[19,23-24]。
3.2 RAPD-PCR反应体系的优化
在不同植物中, RAPD-PCR反应体系的优化试验报道很多,研究者大都认为RAPD技术很大程度上有着不稳定性,重现率低的缺点。Mathews等[25]证明RAPD可在草莓上多次重复相同的实验结果;吴燕民等[11]也通过相同的RAPD产物重复的结果证明铁核桃为核桃属中一个独立种。经过本试验结果表明,用相同的试剂和药品,在相同的反应体系和实验条件下,RAPD-PCR分析还是具有很高的重复性,这与王正加等[25]报道胡桃科山核桃的研究结果一致。
TaqDNA聚合酶是Mg2+依赖性酶,Mg2+浓度过高会抑制Taq酶的活性,过低对Taq酶的活化不够,影响扩增效果。本试验对美国白核桃、美国黑核桃、日本核桃及杂种核桃RAPD-PCR反应中Taq酶的用量为0.5 U,Mg2+最佳浓度为3.5 mmol/L。Mg2+浓度与其他研究结果Mg2+浓度为2.5~3.5 mmol/L接近[4,9-10],同时,大部分研究结果Taq酶的用量为0.4~1.0 U,而张美勇等[4]RAPD研究中Taq酶的用量为0.03 U,这可能与Taq酶的成分有关。经试验表明,引物浓度的高低会对RAPD扩增效果影响很大。引物浓度过高,会使非特异性谱带增加;反之,则导致扩增谱带明显减少。在核桃PCR反应体系的研究中,RAPD引物浓度的差异较大[4,16],本试验中对日本核桃、美国核桃和杂种核桃的RAPD引物浓度为5.0 mmol/L,PCR扩增效果佳,与Nicese等[26]的研究结果4.0 mmol/L接近。 DNA模板浓度和纯度对RAPD-PCR反应结果也有一定影响,DNA模板浓度一般大于10 ng, 而杨克强等[16]RAPD-PCR反应中用150 ng模板DNA也能获得较好的扩增结果。BSA 可以封闭乙酰对RAPD扩增反应的抑制作用[28],用于PCR可改善扩增结果的特异性与酶的稳定性,增加PCR产量及产物[29-30]。大部分研究的试验材料在RAPD-PCR反应体系中都没有加入BSA增效剂,但在本实验中,加入BSA后,RAPD-PCR扩增效果明显比不加要好,产物条带清晰,且量多。
3.3 RAPD-PCR反应条件的优化
预变性是指DNA在温度升到一定程度时双链打开,形成单链的过程。合适的预变性时间是PCR扩增成功的必要条件。本研究中,对几个核桃物种的预变性温度和时间分别是92 ℃,3 min。在其他核桃属植物研究中,山核桃为94 ℃,2~5 min[26];核桃为 95℃,5 min[4]、94℃,5 min[10]。大量研究结果表明,复性时间为1 min,张美勇等[4]80 s,Woeste等[31]30 s;延伸时间多为2 min,本试验中1 min延伸时间为最佳。退火温度是引物与模板DNA结合的关键。温度太高,背景虽然清晰,但条带数量明显减少;温度太低,非特异性谱带明显增加,甚至背景发亮。退火温度根据不同的RAPD引物可以适当调整,一般为35 ℃或者36 ℃为最佳。山核桃的最佳退火温度为38 ℃,30 s[26]。RPAP-PCR反应的程序多为40个循环以上,山核桃为38个循环[26],核桃为43、45、45个循环[4,11,32]。本试验结果表明,RAPD-PCR反应程序为35个循环下可以得到理想的扩增效果,这样可以节约时间。
致谢 :感谢Marcia Kremer,Charles Michler,Lisa Worthen,Janis Gosewehr,Hannah Bergeman,黄忠莲 (Julie) 对本实验研究的技术支持,James McKenna对试验材料的采集。
[1] 阴翠翠,尉亚辉,刘 昊,等.核桃属植物分子水平遗传多样性与基因工程研究进展[J].中国农业科技通报,2008,10(6):16- 22.
[2] Ostry M E, Pijut P M.Butternut: An Underused Resource in North America [J].HortTechnology,2000,10: 302- 306.
[3] Rink G, Juglans cinera L.butternut [M].In Silvics of North America.Vol.2.Hardwoods.Eds.Burns RM and Honkala BH.USDA For Serv,Washington D.C.,Agriculture Handbook,1990,654: 386- 390.
[4] 张美勇,上官凌飞,徐 颖,等.核桃RAPD引物筛选及品种间亲缘关系研究[J].中国农学通报,2010,26(2): 84- 90.
[5] Ross-Davis A,Woeste K E.Microsatellite markers for Juglans cinerea L.and their utility in other Juglandaceae species[J].Conserv.Genet.,2008,9(2): 465- 469.
[6] Krussmann G.Manual of Cultivated Broad-leaved Tree and Shrubs [M].Vol.II.Portland, Oregon: Timber Press.(First pulished in German in 1977; in UK by Batsford in 1986) 1985.
[7] Manning W E.The classification within the Juglandaceae [J].Annals of the Missouri Botanical Garden, 1978,1058- 1087.
[8] Ostry M.Sirococcus clavigignenti-juglandacearum on Heartnut(Juglans ailantifolia var.cordiformis) [J].Plant Disease,1997,81(12): 1461- 1461.
[9] Harlow W M, Harrar E S,White F M.Textbook of dendrology, 6th ed [M].New York:McGraw-Hill Book Company, 1979: 510.
[10] 王国安,张虎平,虎海防,等.适于核桃的RAPD_PCR反应体系的建立[J].新疆农业科学,2004,41(1): 61- 64.
[11] 吴燕民,裴 东,奚生柯,等.运用RAPD对核桃属种间亲缘关系的研究[J].园艺学报,2000,27(001): 17- 22.
[12] 刘湘林,付艳华,吴海鹰,等.南方核桃栽培技术体系的研究[J].中南林业科技大学学报,2011,31(8): 35-39.
[13] Williams J G K, Kubelik A R, Livak K J, et al.DNA polymorphisms amplified by arbitrary primers are useful as genetic markers[J].Nucl.Acid.Res., 1990, 18(22): 6531.
[14] 郝 烔,渠云芳.DNA分子标记在作物育种中的应用[J].山西农业科学,2009,37(003): 81- 85.
[15] Woeste K,McGranahan G H,Bernatzky R.Randomly amplified polymorphic DNA loci from a walnut backcross[(Juglans hindsii×J.regia)×J.regia] [J].J.Am.Soc.Hortic.Sci.,1996,121: 358- 361.
[16] 杨克强,马 明,孙彩玲,等.核桃早实基因的RAPD标记及其序列分析研究[J].中国农业科学,40(9): 2021- 2027.
[17] Doyle J J,Doyle J L.A rapid DNA isolation procedure for small quantities of fresh leaf tissue [J].Phytochem.Bull,1987,19(1):11- 15.
[18] Lefort F, Douglas G C.An efficient micro-method of DNA isolation from mature leaves of four hardwood tree species Acer,Fraxinus,Prunus and Quercus[J].Ann.For.Sci.,1999, 56 (3): 259- 263.
[19] 易庆平,罗正荣,张青林.植物总基因组DNA 提取纯化方法综述[J].安徽农业科学,2007,35(25) :7789 - 7791.
[20] 汤文开,谭 新,张 辉,等.一种快速简单高效提取植物DNA的方法[J].华中师范大学学报,2007,41(003): 447-449.
[21] 张虎平,牛建新,王国安,等.适于核桃基因标记的DNA提取方法[J].生物技术,2003,13(5):18- 19.
[22] 王景雪,孙 毅,高武军.一种简便实用的植物总DNA提取方法[J].山西大学学报:自然科学版,2000,23(3): 271- 272.
[23] Kim C, Lee C, Shin J, et al.A simple and rapid method for isolation of high quality genomic DNA from fruit trees and conifers using PVP[J].Nucl.Acid.Res., 1997,25(5): 1085.
[24] Mathews H,Wagoner W, Kellogg J,et al.Genetic transformation of strawberry: stable integration of a gene to control biosynthesis of ethylene[J].In Vitro Cell Dev-PL,1995, 31(1): 36- 43.
[25] 王卓伟,余茂德,鲁 成.PVP在桑叶总DNA提取中的应用[J].西南农业大学学报,2001,23(001): 62- 62.
[26] 王正加,黄坚钦,郭传友,等.山核桃RAPD反应体系的优化[J].浙江林学院学报,2003,20(004): 429- 433.
[27] Nicese F P,Hormaza J I,McGranhan G H.Molecular characterization and genetic resources among walnut (Juglans regia L.) genotypes based on RAPD markers [J].Euphytica,1998,101(2):199-206.
[28] 边才苗,李钧敏,金则新,等.牛血清白蛋白在植物RAPD分析中的作用[J].遗传,2002,24(3): 279- 282.
[29] Forbes B A,Hicks K E.Substances interfering with direct detection of Mycobacterium tuberculosis in clinical specimens by PCR: effects of bovine serum albumin[J].J.Clin.Microbiol.,1996,34(9): 2125.
[30] Kreader C A.Relief of amplification inhibition in PCR with bovine serum albumin or T4 gene 32 protein[J].Appl.Environ.Microb.,1996,62(3): 1102.
[31] Woeste K,McGranhan G,Bernatzky R.The identification and characterization of a genetic marker linked to hypersensitivity to the cherry leafroll virus in walnut[J].Mol.Breeding,1996,2(3):261-266.
[32] 王国安,张虎平,虎海防,等.核桃早实性状相关联的RAPD标记[J].果树学报, 2004,21(5):485-487.
Optimization of RAPD-PCR reaction system for American and Japanese walnut
ZHAO Peng1,2,3, WOESTE E.Keith2, ZHANG Cun-xu1, CHENG Fei1, ZHANG Shuo-xin1,4, CAI Jing1
(1.College of Forestry, Northwest Agriculture & Forestry University, Yangling 712100, Shaanxi, China; 2.USDA Forest Service Hardwood Tree Improvement and Regeneration Center, Dept.of Forestry and Natural Resources, Purdue University, West Lafayette,IN 47907, USA; 3.Key Laboratory of Resource Biology and Biotechnology in Western China, Ministry of Education, College of Life Science, Northwest University, Xi’an 710069, Shannxi, China; 4.Qinling National Forest Ecosystem Research Station, Ningshan 711600, Shaanxi, China)
Germplasm resources for the genus Juglans (Juglandaceae) are rich, and the genus contains many tree species, commonly called walnuts, that are valued for their high quality timber and nuts.The CTAB method was improved to extract genomic DNA from walnut buds, fresh and dried leaves.Using the obtained DNA as templates, the important parameters influencing the application of RAPD-PCR for walnut species were optimized.The results indicate that the modified CTAB method more effectively removed most of the polysaccharides in the cytoplasm and inhibited the formation of oxidized polyphenolic compounds, compared with the traditional CTAB method.The optimal RAPD-PCR reaction conditions for Juglans cinerea , Juglans ailantifolia , J.nigra, and species hybrids included, in a total volume 20 μL, 1μL of 10 ng/μL DNA, 2 μL of 10×Taq DNA polymerase reaction buffer (1.5 mmol/L Mg2+),2.5 μL of 200 mmol/L dNTPs (0.25 mmol/L), 2 μL of 1mg/mL BSA (bovine serum albumin, 0.1 mg/mL), 2 μL of 25 mmol MgCl2(2.5 mmol), 4 μL of 50 mmol RAPD decamer primer pair, 0.5 units Taq polymerase, and 5.0 μL sterilized distilled water.Thermal cycling conditions were as follows: denaturation 3 min at 92℃ ; 35 cycles of 1 min at 92℃ , 1 min at 35℃ , 2 min at 72℃ ; and a final extension of 10 min at 72℃ at the end of the amplification.
butternut;heartnut;RAPD;optimization
2011-10-21
国家“十二五”科技支撑计划课题“高效可持续农林复合系统构建及调控技术研究”(2011BAD38B0202);西北大学科研启动基金(PR11055);美国印第安纳州自然保护局核桃遗传与保护研究项目(#2041-0006)
赵 鹏(1980- ),男,陕西榆林人,讲师,博士,主要从事植物分子进化和分子生态学研究
蔡 靖(1968- ),女,陕西子洲人,副教授,博士,研究方向:植物生理生态和森林生态;E-mail:cjcaijing@163.com
S792.13
A
1673-923X(2012)03-0129-07
[本文编校:谢荣秀]
