等离子体诱导乙烯吡啶修饰多壁碳纳米管富集放射性核素60Co(Ⅱ)
2012-12-25任雪梅赵桂霞杨世通邵大冬谭小丽
任雪梅,杨 鑫,赵桂霞,杨世通,胡 君,邵大冬,谭小丽
中国科学院 等离子体物理研究所,安徽 合肥 230031
随着核能的发展和放射性同位素的利用,产生了大量放射性废水,严重威胁生态环境的安全,因此放射性废水的处理日益受到人们的重视。吸附法因其工艺简单、成本低廉、可净化高含盐量(大于10g/L)的放射性废水等特点受到研究者的青睐[1]。目前,高富集量的复合吸附剂的研发是吸附法运用中的热点。在1991年日本教授Iijima发现了碳纳米管(MWCNTs)之后[2],碳纳米管由于其优越的物理化学性质在多个学科领域受到广泛关注。高的比表面(150~3 000m2/g)[3]决定了碳纳米管可以作为多种有机和无机污染物的吸附剂。例如Rao等[4]对碳纳米管和氧化碳纳米管吸附二价重金属离子(Cd2+、Cu2+、Ni2+、Pb2+、Zn2+)的技术可行性进行了综述;Yang和Xing[5]对碳纳米管吸附有机物进行了综述。然而因为疏水性和惰性,碳纳米管在水溶液中容易团聚限制了它的实际应用。碳纳米管的表面改性不仅能改善其分散性,同时能引入不同种类的官能团,提高吸附性能。
一般来说,碳纳米管功能化的方法有以下几种:通过各种化学试剂进行化学修饰[6-7];用聚合物包裹碳纳米管[8];通过等离子体在碳纳米管上接枝上聚合物链[9]。传统的化学修饰方法使用大量的化学试剂,在修饰过程中产生大量的化学试剂污染物,容易造成二次污染。而等离子体修饰方法可以在不破坏碳纳米管整体性质的情况下,将目标官能团直接修饰在碳纳米管表面,并且待修饰目标官能团不需要通常化学方法所需的保护措施,因此在修饰过程中可以避免大量化学溶剂的使用[10]。等离子体表面修饰方法作为一种新型、高效、环保的手段受到重视。
乙烯吡啶(VP)是一种功能化的单体,因为吡啶环中的氮原子是强的电子给予者,同时吡啶环还能与含氨基、羧基、羟基等官能团的非金属表面作用[11],所以被视为一种单官能团表面改性剂,用于在非金属表面固定和富集各种金属离子。本工作拟利用等离子体诱导技术在碳纳米管上修饰乙烯吡啶(表示为碳纳米管-乙烯吡啶,MWCNTs-g-VP),并将制备得到的碳纳米管-乙烯吡啶用于放射性核素60Co(Ⅱ)的富集,目的是评估该新型复合材料用于废水中放射性核素富集的可行性。
1 实验部分
1.1 试剂及碳纳米管-乙烯吡啶的制备
60Co(Ⅱ),中国原子能科学研究院;MWCNTs,自制;NaCl、HCl、NaOH和VP均为市售分析纯,并且使用前未做任何纯化处理。
等离子体反应装置见文献[10]。将3.0g MWCNTs放入250mL三口反应烧瓶中,密封,开机械泵抽真空(约6.0Pa),然后通氮气至反应器压强达10Pa,如此反复3次,最后将反应瓶中的气压维持在10Pa。然后打开电感耦合等离子体(ICP)电源进行等离子体放电,对MWCNTs表面进行等离子体处理40min(制得等离子体处理MWCNTs材料)。放电完毕后将待接枝单体乙烯吡啶迅速放入反应烧瓶中,在80℃的恒温水浴振荡器中反应24h。反应结束后,将反应产物用适当有机溶剂(如乙醇)充分洗涤、过滤,以除去未反应的单体和生成的均聚物。最后将产物在80℃干燥,制得等离子体诱导修饰MWCNTs复合材料(碳纳米管-乙烯吡啶,MWCNTs-g-VP)。碳纳米管-乙烯吡啶合成原理及性能表征见Ren等[12]的报道。
1.2 主要仪器
AL204型电光分析天平,感量0.000 1g,上海梅特勒-托利多仪器有限公司;pH-3B型精密pH计,上海精密科学仪器有限公司;HY-4调速多用振荡器,江苏金坛市荣华仪器制造有限公司;LG10-2.4A型高速离心机,北京雷勒尔离心机有限公司;3100TR/AB液体闪烁计数器,美国Packard公司。
1.3 实验方法
碳纳米管-乙烯吡啶对Co(Ⅱ)吸附实验步骤如下:向聚乙烯离心管中加入一定量的碳纳米管-乙烯吡啶复合材料的悬浮液与设定离子强度的电解质溶液预平衡24h,然后加入设定浓度的Co(Ⅱ)和放射性示踪剂60Co(Ⅱ)溶液,用极少量的HCl或NaOH调节体系的pH至所需值。然后将混合均匀的悬浮液于T=283K下在振荡器上振荡24h达到平衡后,以9 000r/min离心分离固液相。
离子强度对碳纳米管-乙烯吡啶吸附Co(Ⅱ)的影响的吸附实验步骤如下:向聚乙烯离心管中加入一定量的碳纳米管-乙烯吡啶复合材料的悬浮液与不同离子强度的NaCl溶液(0~0.15mol/L)预平衡24h,然后加入设定浓度的Co(Ⅱ)和放射性示踪剂60Co(Ⅱ)溶液,用极少量的HCl或NaOH调节体系的pH至固定值。然后将混合均匀的悬浮液于T=283K下在振荡器上振荡24h达到平衡后,以9 000r/min离心分离固液相。
实验中使用的60Co(Ⅱ)为放射性示踪剂,用液体闪烁计数器测其计数。碳纳米管-乙烯吡啶吸附Co(Ⅱ)的量从吸附初始和平衡后两者的差值计算得到。所有实验数据均为3次实验的平均值,数据相对误差约为5%。
用吸附率(Y)和分配系数(Kd)来表示Co(Ⅱ)的富集,计算公式分别为:
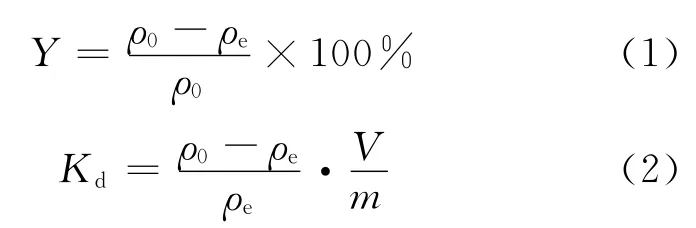
式中:ρ0,Co(Ⅱ)在溶液中的初始质量浓度,mg/L;ρe,Co(Ⅱ)在溶液中平衡后的质量浓度,mg/L;V,悬浮液的体积,L;m,MWCNTs的质量,g。
2 结果和讨论
2.1 pH值对吸附的影响
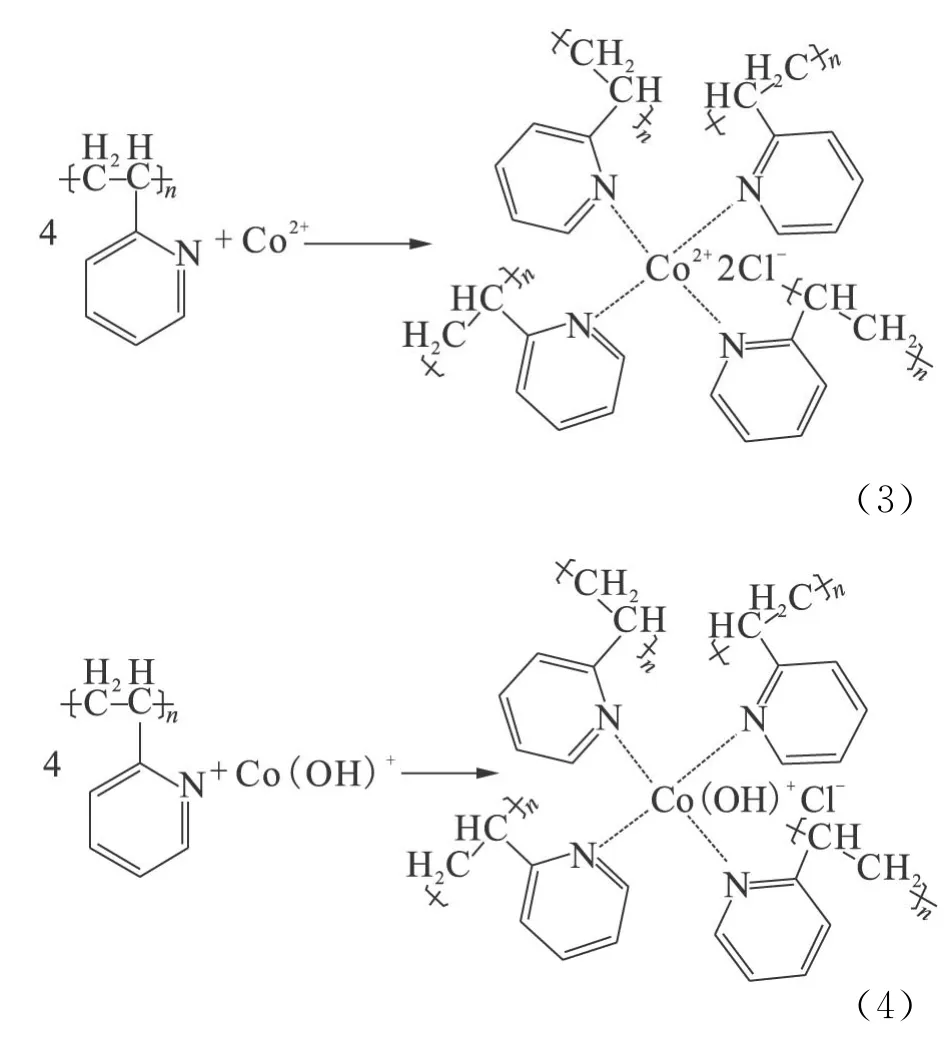
为了评估修饰上的乙烯吡啶对碳纳米管吸附量的影响,对比了碳纳米管改性前后对Co(Ⅱ)的富集率。pH是控制富集过程的一个重要因素,因为改变溶液的pH值会影响吸附剂的表面性质同时会影响放射性核素的水解、络合和沉淀。pH值对碳纳米管-乙烯吡啶和碳纳米管富集Co(Ⅱ)的影响示于图1。由图1可知,pH对Co(Ⅱ)的富集有重要影响,Co(Ⅱ)在两种材料上的富集率均随pH升高而增加。碳纳米管的零电荷点约为5[13],在pH<5时,碳纳米管的表面带正电荷,由于静电斥力的作用,带正电的钴离子不易被吸附,同时溶液中的H+与钴离子竞争吸附位,故在低pH值下碳纳米管对Co(Ⅱ)的富集率较低。而碳纳米管-乙烯吡啶由于乙烯吡啶的引入不仅改善了碳纳米管的分散性,同时还提高了官能团的含量,修饰在碳纳米管表面上的乙烯吡啶中含有的官能团,能通过式(3)和(4)与Co(Ⅱ)形成络合物[14]。因此在低pH值下,碳纳米管-乙烯吡啶对Co(Ⅱ)的富集率远远高于碳纳米管。随着pH值的增加,表面位去质子化伴随着钴离子的水解,碳纳米管和碳纳米管-乙烯吡啶对Co(Ⅱ)的富集率均增加。从钴的形态分布图[15]可以看出,在pH=8.5~11,钴的主要形态是Co(OH)+和Co(OH)2,它们均易吸附在带负电荷的材料表面,故钴的富集率达到最大。因此在高pH值下,2种材料对钴的富集率区别不大。

图1 pH值对碳纳米管-乙烯吡啶和碳纳米管富集Co(Ⅱ)的影响Fig.1 Effect of pH on the preconcentration of Co(Ⅱ)by MWCNTs-g-VP and MWCNTs
2.2 吸附等温线
常温下Co(Ⅱ)在碳纳米管上的吸附等温线示于图2。分别采用Langmuir[16]和Freundlich[17]模型对实验数据进行拟合。2种模型表达式如下:

式中:Cs,富集到碳纳米管-乙烯吡啶上的Co(Ⅱ)量,mg/g;Cmax,平衡时的最大吸附量,mg/g;KL,Langmuir模型常数;KF和n,Freundlich模型常数。
由2个模型计算得到的各参数值列入表1。以拟合的相关系数r作为评价标准可以看出,Langmuir模型最适合用来拟合Co(Ⅱ)在碳纳米管-乙烯吡啶上的富集。通过Langmuir模型拟合得出碳纳米管-乙烯吡啶对Co(Ⅱ)单层最大吸附容量为13.9mg/g。

图2 MWCNTs-g-VP富集Co(Ⅱ)的吸附等温线Fig.2 Sorption isotherm of Co(Ⅱ)by MWCNTs-g-VP pH=7.50±0.02,ρsolid=0.6g/L,c(NaCl)=0.01mol/L,T=283K
吸附容量决定了从给定的溶液中定量富集吸附质时吸附剂的用量[18]。表2列出了通过Langmuir模型计算得到的不同材料对Co(Ⅱ)的最大吸附容量。由表2可知,碳纳米管-乙烯吡啶对Co(Ⅱ)的单层吸附容量高于大多数吸附剂,说明碳纳米管-乙烯吡啶可以用于溶液中放射性核素60Co(Ⅱ)的富集。

表1 Langmuir和Freundlich模型参数Table 1 Langmuir and Freundlich parameters of Co(Ⅱ)preconcentration on MWCNTs-g- VP

表2 不同材料对Co(Ⅱ)吸附量的比较Table 2 Comparison of Co(Ⅱ)sorption capacity by various sorbents
2.3 吸附剂浓度对吸附的影响
吸附剂浓度对碳纳米管-乙烯吡啶富集Co(Ⅱ)和Kd值的影响示于图3。由图3可知:Co(Ⅱ)的富集率随吸附剂浓度的增加而增加;随着吸附剂浓度的增加,可用的吸附位增加,因此在高吸附剂浓度下,Co(Ⅱ)的富集率更高;Kd值在整个吸附剂浓度范围内无变化,这与分配系数的物理化学特性一致,即Kd值在低固液比时与吸附剂浓度无关[24]。

图3 吸附剂浓度对碳纳米管-乙烯吡啶富集Co(Ⅱ)的影响Fig.3 Effect of solid content on the preconcentration of Co(Ⅱ)by MWCNTs-g-VP
2.4 离子强度对吸附的影响
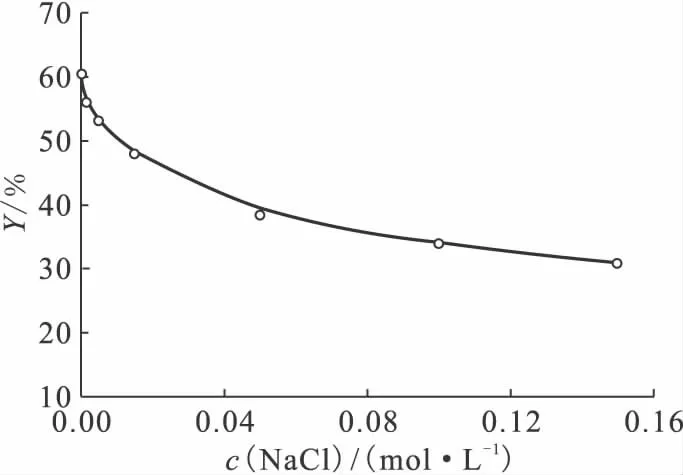
图4 NaCl对碳纳米管-乙烯吡啶富集Co(Ⅱ)的影响Fig.4 Effect of the concentrations of NaCl on the preconcentration of Co(Ⅱ)by MWCNTs-g-VP
离子强度对碳纳米管-乙烯吡啶富集Co(Ⅱ)的影响示于图4。由图4可知,随着离子强度的增加,碳纳米管-乙烯吡啶对Co(Ⅱ)的富集率下降,说明在此富集过程中存在外层络合作用,此结果与Shao等[9]的研究一致。随着离子强度的增加,由于盐的引入产生表面电荷的屏蔽效应将导致放射性核素与固体表面的静电作用(吸引或排斥)减小[25]。同 时Na+的存在,将 与Co(Ⅱ)竞争吸附位,导致Co(Ⅱ)的有效吸附位减少,降低Co(Ⅱ)的富集率。离子强度对Co(Ⅱ)在碳纳米管-乙烯吡啶上的富集有影响,说明存在外层络合物。
3 结 论
通过对碳纳米管进行功能化处理制备得到的碳纳米管-乙烯吡啶复合材料对Co(Ⅱ)具有良好的富集效果。基于本工作的实验结果,可得出以下结论:
(1)Co(Ⅱ)在碳纳米管-乙烯吡啶上的富集受pH值和离子强度的影响,说明吸附机理包括外层络合和内层络合;
(2)乙烯吡啶的引入不仅能改善碳纳米管的分散性,还能提高官能团的含量,使得改性后碳纳米管对Co(Ⅱ)的富集率远远高于改性前;
(3)Langmuir吸附模型拟合实验数据比Freundlich模型好,根据Langmuir模型推算,1g碳纳米管-乙烯吡啶可以富集13.9mg钴。与其他吸附材料相比,碳纳米管-乙烯吡啶具有相对较高的吸附性能,适用于放射性废水中放射性核素的预富集和固化处理。
[1]李瑞东,侯立安,张志利,等.碳纳米管-环糊精复合材料对Eu(Ⅲ)的吸附[J].原子能科学技术,2010,44(9):1 043-1 046.
[2]Iijima S.Helical Microtubules of Graphitic Carbon[J].Nature,1991,354:56-58.
[3]Hussain C M,Saridara C,Mitra S.Modifying the Sorption Properties of Multi-Walled Carbon Nanotubes via Covalent Functionalization[J].Analyst,2009,134:1 928-1 933.
[4]Rao G P,Lu C,Su F.Sorption of Divalent Metal Ions From Aqueous Solution by Carbon Nanotubes:a Review[J].Sep Purif Technol,2007,58:224-231.
[5]Yang K,Xing B.Adsorption of Organic Compounds by Carbon Nanomaterials in Aqueous Phase:Polanyi Theory and Its Application[J].Chem Rev,2010,110:5 989-6 008.
[6]Lu C,Chiu H.Chemical Modification of Multi-Walled Carbon Nanotubes for Sorption of Zn2+From Aqueous Solution[J].Chem Eng J,2008,139:462-468.
[7]刘淑娟,李金英,罗明标,等.纯化及羧化多壁碳纳米管吸附铀的研究[J].核化学与放射化学,2011,33(5):285-290.
[8]Tan Z Q,Abe H,Naito M,et al.Arrangement of Palladium Nanoparticles Templated by Supramolecular Self-Assembly of SDS Wrapped on Single-Walled Carbon Nanotubes[J].Chem Commun,2010,46:4 363-4 365.
[9]Shao D D,Ren X M,Hu J,et al.Preconcentration of Pb2+From Aqueous Solution Using Poly(Acrylamide)and Poly(N,N-Dimethylacrylamide)Grafted Multiwalled Carbon Nanotubes[J].Colloids Surf A,2010,360:74-84.
[10]Shao D,Jiang Z,Wang X.SDBS Modified XC-72 Carbon for the Removal of Pb(Ⅱ)From Aqueous Solutions[J].Plasma Processes Polym,2010(7):552-560.
[11]Malynych S,Luzinov I,Chumanov G.Poly(Vinyl Pyridine)as a Universal Surface Modifier for Immobilization of Nanoparticles[J].J Phys Chem B,2002,106:280-1 285.
[12]Ren X M,Shao D D,Zhao G X,et al.Plasma Induced Multiwalled Carbon Nanotube Grafted With 2-Vinylpyridine for Preconcentration of Pb(Ⅱ)From Aqueous Solutions[J].Plasma Process Polym,2011(8):589-598.
[13]Xu D,Tan X L,Chen C C,et al.Removal of Pb(Ⅱ)From Aqueous Solution by Oxidized Multi-Walled Carbon Nanotubes[J].J Hazard Mater,2008,154:407-416.
[14]Allender C J,Castell O K,Davies P R,et al.A Glimpse of the Inner Workings of the Template Site[J].Chem Comm,2009(2):165-167.
[15]Guo Z Q,Li Y,Zhang S W,et al.Enhanced Sorption of Radiocobalt From Water by Bi(Ⅲ)Modified Montmorillonite:a Novel Adsorbent[J].J Hazard Mater,2011,192:168-175.
[16]Langmuir I.The Adsorption of Gases on Plane Sur-faces of Glass,Mica and Platinum[J].J Am Chem Soc,1918,40:1 361-1 403.
[17]Freundlich H.Concerning Adsorption in Solutions[J].Z Phys Chem,1906,57:385-470.
[18]Stafiej A,Pyrzynska K.Adsorption of Heavy Metal Ions With Carbon Nanotubes[J].Sep Purif Technol,2007,58:49-52.
[19]Jaramillo J,Gomez-Serrano V,Alvarez P M.Enhanced Adsorption of Metal Ions Onto Functionalized Granular Activated Carbons Prepared From Cherry Stones[J].J Hazard Mater,2009,161:670-676.
[20]Al-Degs Y S,El-Barghouthi M I,Issa A A,et al.Sorption of Zn(Ⅱ),Pb(Ⅱ),and Co(Ⅱ)Using Natural Sorbents:Equilibrium and Kinetic Studies[J].Water Res,2006,40:2 645-2 658.
[21]Tan L Q,Jin Y L,Chen J,et al.Sorption of Radiocobalt(Ⅱ)From Aqueous Solutions to Na-Attapulgite[J].J Radioanal Nucl Chem,2011,289:601-610.
[22]Padala A N,Bhaskarapillai A,Velmurugan S,et al.Sorption Behaviour of Co(Ⅱ)and Cu(Ⅱ)on Chitosan in Presence of Nitrilotriacetic Acid[J].J Hazard Mater,2011,191:110-117.
[23]Liu M,Chen C,Hu J,et al.Synthesis of Magnetite/Graphene Oxide Composite and Application for Cobalt(Ⅱ)Removal[J].J Phys Chem C,2011,115:25 234-25 240.
[24]邵大东,许笛,王所伟,等.pH值和离子强度对放射性核素镍在MX-80黏土上的吸附影响和模型研究[J].中国科学,2008,38:1 025-1 034.
[25]López-Ramón V,Moreno-Castilla C,Rivera-Utrilla J,et al.Ionic Strength Effects in Aqueous Phase Adsorption of Metal Ions on Activated Carbons[J].Carbon,2003,41:2020-2022.
