车用锂离子电池能量密度影响因素研究进展
2012-12-23莫愁陈吉清兰凤崇
莫愁,陈吉清,兰凤崇
(华南理工大学机械与汽车工程学院,广东广州510640)
0 引言
由于环保与能源的压力,发展电动汽车替代传统燃油汽车作为交通运输工具是目前必然趋势。2009 年前电动汽车动力源的主流是镍氢电池[1],目前电动汽车产业界用得更多的是锂离子电池。电动汽车电池要求高的能量密度、功率密度,低的价格,长的寿命,良好的使用安全性和环境安全性[2],目前锂离子电池这些性能远未能满足需要,这是电动汽车还是未能商业化的原因之一,尤其是电池能量密度不能满足要求是商业化瓶颈之一。
锂离子电池能量密度较低,要使电动汽车续驶里程满足要求,必须配置较大电池组,这些电池组占用了更多的有用空间,同时增加了整备重量,减少了有效载重质量,这增加的重量反过来又降低了汽车的动力性和续行里程。同时,这较大的电池组重量对汽车的轴荷分配必然产生影响,必须准确计算,否则会影响汽车的牵引性、操纵稳定性等[3]。影响锂离子电池能量密度的因素众多,目前国内外各相关研究组织都在加大力度致力于这个领域的工作。
1 电池材料与结构
电池反应物质的选择确定了电池的理论容量、电动势,确定了电池的理论能量密度,由于极化电压的存在、电池内阻的存在、活性物质利用不完全、电池非反应物质的存在等原因,实际能量密度必然小于理论能量密度,两者关系如下[4]:
式中:W'为实际能量密度;
W'0为理论能量密度;
ηu为电压效率;
ηr为反应效率;
ηm为质量效率。
其中的W'0由下式确定:
式中:E 为电池电动势,V;
∑qi为参与反应的物质的电化当量总和,g/Ah。
1.1 正极材料
由式(2)可知,提高电池电动势,可以提高锂离子电池的理论能量密度。目前业界大多用相对于锂0 ~1 V 的碳材料作为锂离子电池的负极,要提高电池电动势就要着力提高正极电位,要使电池电动势在3 V 以上,正极材料必须使用4 V 级别的材料。正极电位与晶格能、离子化能、锂离子溶液的溶剂化能有关,其中晶格能影响最大,因此电池电动势主要由正极结晶结构决定[5-6]。理论上采用电化当量更小的正极材料可以得到更高的理论能量密度,但达到理论能量密度的程度受到反应原理、材料结构、制造工艺、制造成本、环保和安全等因素制约。
LiCoO2理论比容量274 mAh/g,实验室实际比容量135 ~140 mAh/g,其存在的主要问题是存在安全隐患,有毒,价格较高,这些缺陷注定它不能长期作为锂离子材料。LiNiO2理论比容量274 mAh/g,性能与LiCoO2接近,实验室实际比容量达190 ~210 mAh/g,但制备困难,可逆容量下降快,安全性差,商业化前景不好。LiMn2O4理论比容量为148 mAh/g,实验室实际比容量100 ~115 mAh/g,有着价格低、无毒的优点,由于其中的Mn3+易于溶解,导致其容量衰减快,循环性能差,这是目前业界需要解决的主要问题。LiCoO2、LiNiO2和LiMn2O4作为正极材料各有优缺点,将三种金属氧化物集合成一种化合物从而组合三者的优点是制备更优秀的材料的一种思路,LiNi1/3Co1/3Mn1/3O2理论比容量为278 mAh/g,实验室实际比容量155 ~165 mAh/g,存在的问题主要是循环稳定性、振实密度还有待提高,空气存储性能差,Yabuuchi[7]用制得的LiNi1/3Co1/3Mn1/3O2作正极组装的电池在75 ℃时能量达到225 mAh/g,但随温度升高,充放电的库仑效率即下降,这意味着电解液里有副反应发生。正交橄榄石型LiFePO4理论比容量达170 mAh/g,实验室实际比容量130 ~140 mAh/g,其性能稳定、寿命长、安全性高、环保性好、价格低,是目前业界认为综合性能最好、最有应用前景的材料,由于反应发生在LiFePO4和FePO4之间,Li+在迁出/嵌入过程中受扩散影响控制,不能完全参加反应[8],另外,Fe2+容易被氧化,工艺难度较大、体积容量较小也是需要解决的问题。目前改善LiFePO4的性能方法是提高电导率和振实密度,Z H Chen 等[9]合成的含碳质量分数为3.5%的LiFePO4在0.1 C 下放电,常温下容量可达160 mAh/g,接近其理论容量;清华大学核能与新能源技术研究院采用控制结晶碳热还原新工艺,利用硝酸铁、磷酸、氨水、碳酸锂、蔗糖等廉价的普通工业原料制备的球形磷酸铁锂,表观密度可达1.35 ~1.45 g/cm3,压实密度可达2.1 ~2.4 g/cm3。表1 比较了几种已商业化锂离子电池的比容量。
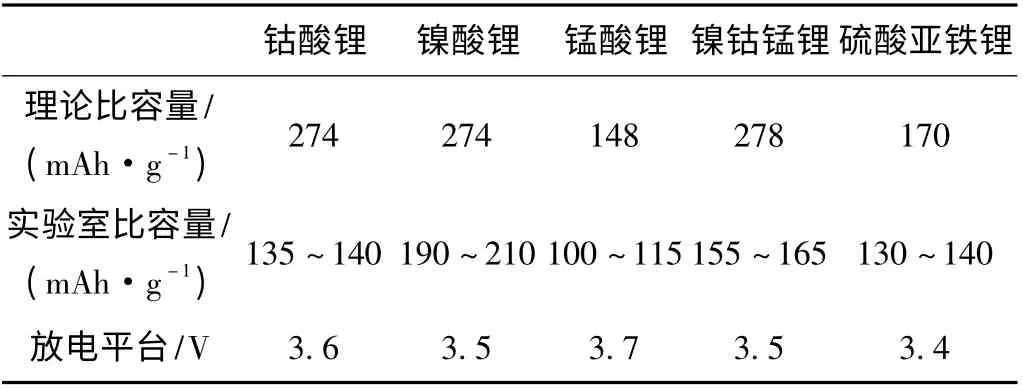
表1 几种锂离子比容量
1.2 负极材料
理论上凡是能嵌入锂离子的物质都可以作为锂离子电池的负极,储锂能力是确定电池能量密度的关键因素。目前业界的主流是用碳素材料作负极,其化学组成通常用LixC (0 <x <1)表示,已商业化应用的碳素材料有石墨和焦炭。目前常用的LiC6理论比容量为372 mAh/g,有报道实验室实际比容量达350 mAh/g[10]。难石墨化碳有较高的储锂能力,甲醛酚醛树脂在温度<800 ℃裂解得到的非晶体半导体材料多并苯(PAS)其容量高达800 mAh/g[11],但是这类材料与水分、CO2、O2等接触会使循环性能下降,导致难以商业化[12]。材料纳米化可以提高储锂能力,吴国涛、唐致远、尤今跨等[13]研究出容量达525 mAh/g 的纳米碳管材料,但是这类材料存在制备工艺繁杂、纳米颗粒易团聚、高倍率充放电容量和循环性能差的问题[14]。
1.3 电解液
锂离子电池用电解液的电导率一般只有0.01 S/cm 甚至更低,是酸性电池和碱性电池的几百分之一,因此锂离子电池在大电流放电时来不及从电解液中补充Li+,会发生电压下降。提高电导率是提高电池能量的途径之一,对电解质的改性或寻找替代电解质、对溶剂优化都没有取得突破性的进展,通过增加添加剂,比如电极碳包覆和掺杂金属、金属离子或稀土元素可以得到好的效果。包覆碳后,不仅材料的电导率得到提高,而且比表面积也相应增大,有利于材料与电解质充分接触,从而改善微粒内层锂离子的迁出/嵌入性能,进而提高材料的充放电容量和循环性能[15]。表面包覆导电材料仅是提高粒子间导电性,对材料进行掺杂则可以从内部改变导电性,曲涛等[16]采用固相法掺杂稀土元素Y 合成的Li0.99Y0.01FePO4,室温初始放电容量为129.9 mAh/g,循环15 次后仍保持初始容量的98.5%,电化学性能得到明显改善。
1.4 隔膜
隔膜的主要评价指标是孔隙率、浸润性和热安全性,其中的孔隙率通过影响电导率来影响电池的能量密度。隔膜核心生产技术是造孔工艺,目前主要问题是隔膜的厚度、强度和孔隙率等得不到整体兼顾。提高孔隙率能有效提高电导率,Xiao,Zhang 等[17-18]对聚合物组分进行了改进,以静电纺丝法制备了PVdF/PMMA/PVDF 三层结构聚合物膜,使室温下电导率达1.93 mS/cm,并具有良好的机械稳定性。在隔膜表面涂覆多孔结构的复合物涂层可以改善浸润性且不会让电解液进入隔膜微孔,Zhang 等[19]用CaCO3和少量的聚四氟乙烯制备了新型无机锂离子电池用隔膜,20 ℃下电导率为2.5 ~4 mS/cm。
1.5 原理与结构
锂离子电池的充放电过程,实际就是锂离子在正负电极间的迁入和迁出、嵌入和脱嵌过程,此过程伴随着与锂离子等当量电子的迁移。这个过程必然存在极化现象,也就存在着极化电压,极化电压升高,电池能量下降。影响电极极化的因素很多,电解液组成、温度、电极材料、电解液流动状况等因素对电极极化(过电位)都有影响。目前还没有精确的数学表达式能描述这些因素对极化电压的影响,仅有一些实验数据总结出来的经验关系式。张宾等[20]对几种型号的锂离子电池做了测试,在2C 放电电流能量密度有某些下降,放电电流越大、持续时间越久,趋势越明显,如图1 所示,认为极化过电位会随着电流的增大而增大,在电池的使用过程中,以小的电流输出会得到大的能量密度。
调整电池的正负极材料重量比例和减少封装膜可以提高质量效率,进而提高能量密度,叶飞[21]将以工业上比较成熟的LiCoO2作为正极、商业BTR 碳材作为负极的锂离子电池的负极富余量由33%降为17%、封装膜比重由17%降为11%后电池的能量密度由110 Wh/kg 升为131 Wh/kg。
2 电池内阻
内阻是电池运行状态重要特性参数之一,同时它表征着电池寿命,其大小衡量电子和离子在电极间传输难易程度,是影响电池放电效能的重要性因素[22]。内阻初始大小主要受电池的材料、制造工艺、电池结构等因素的影响,使用过程中受多种因素影响。温度对电池的能量有着重要影响,影响途径有多种,主要通过影响电池内阻来影响能量,温度变化可引起阻抗变量和化学反应的变化,而内阻的变化反过来又影响温度的变化。温度对锂离子电池的能量密度影响情况,大体而言,常温最利于其能量的发挥,低于10 ℃和高于45 ℃时内阻升高,低于10 ℃时升高趋势比高于45 ℃时更明显[23],而电池工作时大多时间温度在40 ℃以上。内阻随SOC 下降而呈升高趋势,低于30%时,升高趋势明显。能量密度随内阻的升高而下降。图2 显示了某3.7 V/10 Ah 锰酸锂电池内阻与温度、SOC 的关系,其中R 为电池内阻,R0为电池标称内阻(25 ℃,0%SOC)。
一个二次电池出厂时的内阻比较小,一般只有毫欧甚至微欧级别,多次充放电后,电池内部化学物质活性降低,内阻会逐渐增加,直至电量无法正常释放出来,所以对使用过程中逐渐增大的内阻的控制很重要,事实上,内阻除了影响电池放电性能外,也是影响电池一致性的主要因素之一。电池温度是影响内阻的关键因素,所以,提高电池的热管理水平对电池性能发挥非常重要,主要途径有提高电池的热稳定性和实施过充保护[24]。在电解液中添加一些高沸点、高闪点和溶剂和阻燃剂可以改善电池的安全性,比如一氟代甲基碳酸乙烯酯(CH2-FC)等[25]、硅烷和硼酸酯等[26]。选择颗粒大小适当、热稳定性好的正极材料,提高负极上的SEI 膜是提高钾离子电池热稳定性的重要方法[27]。
3 电池一致性
锂离子电池单体电压都不超过4 V,而为了提高电动机的效率,工作时需要几十、上百节电池串联,由于制造过程中工艺上的问题和材质的不均匀,这些电池单体之间的初始电压、内部阻抗、放电容量和工作温度必然存在差异,这个一致性问题影响电池组能量密度的提高。王震坡、麻友良等[28-29]研究认为,使用时,由于电池组中各个电池的所处位置温度、通风条件、充放电过程等差别的影响,在一定程度上增加了电池的电压、内阻及容量等参数的不一致,其中温度的影响较大。电池的材料存在差异,工作过程中必然形成温度差异,如上所述,锂离子电池的一个特点是内部阻抗是温度的函数,使用过程中每个电池单体温度变化情况不一致引起制造时就存在的不一致现象更加明显。
电池管理策略中[30],为保护电池,每节电池单体都会预定义电压最小值和最大值,只要每一单体电池均保持在过压和欠压断开范围之间,则该电池组便能够放电和充电,如果某一电池单体达到上述任何一个阈值,则整个电池组便会关闭,从而使其他本可以继续充放电的电池停止工作。由于电池的不一致性存在,必然导致电池电能无法充分充电和无法完全利用的情况存在。要提高电池一致性,目前方法一是在封装前对每个电池单体进行筛选[31],选择参数满足设定范围的电池单体,这样可避免电池组在使用初期出现的一致性问题,二是在使用过程中对每一个电池单体实施监控,这是锂电池真正能商业化的必要管理措施[32],当检测到某个电池单体参数低于设定目标时对其进行更换,从而整体保持电池组的较高的一致性、安全性和较高能量密度。
4 电池安全性
锂离子电池起火或爆炸的诱导原因是管理系统失效、散热能力不足[33]。过充电使负极表面沉积有金属锂,锂活性非常高,极易与氧气发生反应,且是比热最高的金属,而金属锂的表面电沉积极易形成“枝晶”,会刺穿隔膜,使正负极短路,导致电池迅速发热,导致起火或爆炸。有机溶剂遇高温、隔膜分解也是电池起火或爆炸的因素。
在不同连接方式组成的锂离子电池组中,内阻差异越大,电池组的安全性能越差[34]。有的电池平衡策略,比如只对电池组总电压进行保护、不加电池单体电压监控的策略,会出现总电压在策略范围内,而电池单体却过压或欠压的情况,这对安全性有较大影响,因此,为了提高锂离子电池组整体的安全性能,电池内阻应尽可能一致。通过添加剂实现电池过充的内部保护是简单、低成本和有效的方法,目前一是氧化还原保护法,在电解液中加入添加剂,该添加剂在超过额定电压后在电池正负极间反复进行氧化还原反应,以此来消除超压对电池的损害;二是电聚合保护法,在电池内部添加某种聚合物,电池充电到一定电势时,阴极表面生成的导电聚合物膜造成了电池内部微短路,可使电池自放电至安全状态[35]。
5 总结与展望
自1991 年被索尼公司发明以来,锂离子电池发展到今天已有20 年的历史,无数科研人员力图通过种种途径提升它的能量密度,主要有通过优化材料的合成工艺、材料纳米化以提高正负极的嵌锂容量,通过添加导电材料以提高电导率、减低极化电压,以此来提高电池的性能,也有开发替代材料的研究,期间也有某些材料在实验室几乎得到理论比容量的报道,但商业化生产条件无法等同实验条件,目前商业化生产的各种锂离子电池的能量密度仅有实验室的1/5 左右。在影响锂离子电池能量密度的关键因素未取得突破时,提高电池的管理水平、尽可能利用电池能量是提高电动汽车水平的有效途径。
能量是电压与容量乘积的产物,目前常见的各种锂离子电池输出电压都在3 ~4 V 之间,即使电极容量得以提高到理论值,电池能量密度也仅是汽油、柴油的十几分之一,锂离子电池汽车所有性能要达到传统燃油车水平是不可能的。相比传统燃料,锂离子电池有着更多引起爆炸的因素,从这个角度看,电动车辆有着更大的安全隐患,尤其是在目前电池安全管理技术不足够先进的情况下更是如此。目前电池成本居高不下的原因之一是量产电池一致性差,如果一致性标准高,电池的废品率也会升高,分摊到合格电池的成本也必然随之升高,反之,如果一致性标准较低,则废品率较低,电池的成本也较低,但电池组的整体能量也随之降低,同时也会增加安全隐患。提高电池能量密度必须综合考虑多种制约因素,寻找一个合理的折衷,尤其要把安全因素放在首要位置。为了电动汽车动力性、经济性、续行里程等目标,除了着眼电池的技术水平外,还可以通过车辆轻量化、提高电机效率、制动能量回收、优化内燃机效率和提高能源管理水平等途径实现。锂离子电池是动力源的中期目标,未来的发展趋势是燃料电池等性能更好的动力能源。
【1】马学美,崔毅.动力锂离子电池技术发展趋势和投资策略研究[J].华南理工大学学报:社会科学版,2011,13(1):5-8.
【2】崔胜民.新能源汽车技术[M]. 北京:北京大学出版社,2009:34.
【3】张春化,边耀璋,祁东辉.汽车新能源能量密度及有关问题[J].西安公路交通大学学报,2000,20(3):82-85.
【4】郭炳焜,李新海,杨松青. 化学电源- 电池原理及制作技术[M].长沙:中南理工大学出版社,2009:19-31.
【5】Corson D W. High power battery system for hybrid vehicles[J].Power Sources,2002(105):110 -113.
【6】钟俊辉.锂离子电池及其材料[J].电池,1996(2):91-95.
【7】Yabuuchi N,Ohzuku T.Electrochemical behaviors of Lithium LiNi1/3Co1/3Mn1/3O2in lithium batteries at elevated temperatures[J].Power Sources,2005,146:636.
【8】冯国彪,邓宏.锂离子电池正极材料磷酸铁锂研究进展[J]. 无机盐工业,2011(3):14 -17.
【9】Chen Z H,Dahn J R.Reducing carbon in/C composite electrodes to maximize specific energy,volumetric energy and tap density[J].J.Eletrochem.Soc.,2002,149(9):A1184-A1189.
【10】Ohta N,Nagaoka K,Hoshi K,et al.Carbon coated graphite for anode of lithium ion rechargeable batteries:graphite substrates for carbon coating[J].J Power Sources,2009,194(2):985 -990.
【11】Zheng T.High capacity carbon preperated from phenoric resin for cathode of lithium ion battery[J]. J. Eletrochem. Soc.,1995,14(5):211-214.
【12】Wang Shujun,Zhao Feiming. Study of the carbonized product of furfuralcohol resin as the electrode materials of lithium ion batteries(2)-the testing of the electrochemical performance of the lithium ion cells assembled with the resin carbon materials[J]. New carbon materials,2000,15(4):44-48.
【13】殷雪峰,刘贵昌.锂离子电池炭负极材料研究现状与发展[J].碳素技术,2004,23(3):37 -41.
【14】陈西知,吴秋芳,马新胜. 纳米材料在锂离子电池正极材料中应用的研究进展[J].材料导报,2010,24(11):38-44.
【15】周骏,李琪,乔庆东.提高锂离子电池正极材料LiFePO4电导率的方法[J].化工科技,2011,19(2):55 -58.
【16】曲涛,田彦文,钟参石,等. 钾离子电池正极材料Li0.99Y0.01Fe-PO4的制备[J].功能材料,2005,36(5):694 -696.
【17】Xiao Q,Li Z,Gao D,et al.A novel sandwiched membrane as polymer electrolyte for application in lithium ion battery[J]. J Membrane Sci,2009,326(2):260.
【18】Zhang H,Zhang P,Li Z,et al. A novel sandwiched membrane as polymer electrolyte for lithium ion battery[J]. Electrochem commun,2007,9(7):1700.
【19】Zhang S S,Xu K,et al.Alkaline composite film as a separator for rechargeable lithium batteries[J].Solid State Electrochem,2003,7(8):492.
【20】张宾,何勇灵,陈全世. 电动汽车用锂离子电池的能量功率特性分析[J].电源技术,2010,34(10):1076 -1079.
【21】叶飞.异型聚合物锂离子电池制备工艺及提高能量密度的研究[D].北京:国防科技大学,2008:62.
【22】朱梅,徐献芝,吴飞.动力电池研发的关键性因素探索[J]. 电源技术,2010,(12):1239 -1241.
【23】张志杰,李茂德. 锂离子电池内阻变化对电池温升影响分析[J].电源技术,2010,34(2):128 -130.
【24】Tobishima S,Yarnaki J.A consideration of lithium cell safety[J].Power Sources,1999,81/82:882 -886.
【25】Yokoyama K,Sasamo T,Hiwara A.Fluorine substituted cyclic carbonate electrolytic solution and battery containing the same:US,6010806[P].2000 -01-04.
【26】Narang S C,Ventura S C,Dougherty B J,et al. Nor-flammable/self-extinguishing electrolytes for batteries:US,5830600[P].1998 -11-03.
【27】唐致远,陈玉红,卢星河,等.锂离子电池安全性的研究[J].电池,2006(1):74-76.
【28】王震坡,孙逢春,张承宁. 电动汽车动力蓄电池组不一致性统计分析[J].电源技术,2003,27(5):438 -441.
【29】麻友良,陈全世.混合动力电动汽车用蓄电池不一致的影响分析[J].汽车电器,2001(2):5 -7.
【30】王贵明,王金懿.电动汽车及其性能优化[M].北京:机械工业出版社,2010:109 -116.
【31】何鹏林,乔月.多芯锂离子电池组的一致性与安全性[J]. 电池,2010,40(3):161-163.
【32】周宏湖.以创新提升锂动力电池能量密度:景佑能源科技有限公司采访记[J].制造技术与材料,2011(11):40.
【33】程新群. 化学电源[M]. 北京:化学工业出版社,2008:174 -177.
【34】于申军,周永超,李贺,陈志奎.内阻差异对锂离子电池组安全性能的影响[J].化工学报,2010(11):2960 -2963.
【35】Xiao L F,Ai X P,Cao Y L,et al.Electrochemical behavior of biphenyl as polymerizable additive for overcharge protection of lithium ion batteries[J].Electrochemical Acta,2004,49(24):4189-4196.
