芳羧酸功能化的聚砜与Tb(III)形成的高分子-稀土配合物的结构与荧光发射性能
2012-12-21张瑞霞高保娇位霄鹏
张瑞霞 高保娇 位霄鹏
(中北大学化学工程系,太原030051)
芳羧酸功能化的聚砜与Tb(III)形成的高分子-稀土配合物的结构与荧光发射性能
张瑞霞 高保娇*位霄鹏
(中北大学化学工程系,太原030051)
通过大分子反应将苯甲酸(BA)键合在聚砜(PSF)侧链,制得芳羧酸功能化的聚砜(PSFBA).以PSFBA为大分子配基,以邻菲啰啉(Phen)为小分子配体,与Tb(III)配位,分别制备了二元配合物PSFBA-Tb(III)与三元配合物PSFBA-Tb(III)-Phen,采用傅里叶变换红外(FTIR)光谱和紫外(UV)吸收光谱对配合物进行了表征,深入研究了配合物(溶液与薄膜)的荧光发射性能及热稳定性与结构的关系.研究结果表明,以PSFBA为大分子配基所形成的高分子-稀土配合物,均能发射出很强的Tb(III)特征荧光,即键合在PSFBA侧链的配基BA能有效地敏化Tb(III)的荧光发射.二元配合物PSFBA-Tb(III)的表观饱和配位数为10,即当二元配合物具有PSF-(BA)5-Tb(III)的结构时,BA对Tb(III)的配位表观上达到饱和,此时二元配合物具有最强的荧光发射.按n(Phen): n(Tb(III))=1的比例将Phen加入二元配合物PSF-(BA)5-Tb(III)溶液中进行补充配位,所制备的三元配合物PSF-(BA)5-Tb(III)-(Phen)1与惯用比例的三元配合物PSF-(BA)1-Tb(III)-(Phen)3或PSF-(BA)1-Tb(III)-(Phen)2相比,不仅荧光发射强度高,而且热稳定性能好,是一种高性能的场致发光材料.
聚砜;苯甲酸;高分子-稀土配合物;敏化作用;光致发光
1 引言
光致发光稀土配合物荧光单色性好、发光强度高、量子效率高,是一类性能独特的发光材料.在这类材料中,键合型聚合物-稀土配合物发光材料兼具有稀土配合物优异的场致发光性能与高分子化合物良好的力学性能与易于加工成型的特点,还可使发光材料内部呈均相特性,是一种高性能稀土发光材料,1-3尤其在电致发光器件的制备方面,键合型聚合物-稀土发光材料显示出明显的优点,具有良好的发展前景.4,5
关于键合型聚合物-稀土配合物发光材料,一方面报道还较少,另一方面在已报道的体系中,尚存在两个问题:(1)聚合物基质多为聚苯乙烯、聚甲基丙烯酸等通用性聚合物,这些聚合物玻璃化转变温度较低(80-120°C),热稳定性与力学性能均较差,6,7不能满足电致发光器件的需要;(2)聚合物侧链上的配基多为脂肪羧基(主要来自于单体丙烯酸或甲基丙烯酸),羧基只起对稀土离子配合的作用,而对稀土离子的荧光发射无敏化作用,只有加入具有敏化作用的小分子配体协同配位,才能形成聚合物-稀土发光材料.8,9上述缺点在很大程度上局限了键合型聚合物-稀土配合物发光材料的性能.
鉴于聚砜(PSF)是一种具有优良力学性能与热稳定性的聚合物,10,11而芳香羧酸配体对稀土离子兼具有配位与敏化双功能作用,12,13为克服键合型聚合物-稀土配合物发光材料目前尚存在的上述局限,本课题组在前期的研究中,以聚砜为基质,通过大分子反应,将对稀土离子具有双功能作用的苯甲酸(BA)引入其侧链,制得了芳香羧酸功能化的聚砜PSFBA,重点研究了PSFBA的制备与表征.14本文则深入研究PSFBA与Tb(III)离子所形成的高分子-稀土配合物的光致发光性能,包括单一配基的二元配合物PSFBA-Tb(III)与两种配基的三元配合物PSFBA-Tb(III)-Phen的荧光发射特性.深入探讨了配合物的发光性能及热稳定性与其结构的关系,提出了诸如“表观饱和配位数”和“补充配位效应”等新概念.可以预期,含芳羧酸配基的聚砜与稀土离子所形成的配合物,在场致发光尤其在电致发光材料的制备领域,将具有潜在的应用前景,类似的研究尚未见文献报道.
2 实验部分
2.1 试剂与仪器
聚砜(PSF,Mˉr=67000,上海塑料工业联合公司曙光化工厂),工业级;对氯甲基苯甲酸(CMBA,江苏磐希化工有限公司),工业级;无水四氯化锡(天津市元立化工有限公司),分析纯;二甲基乙酰胺(DMAC,天津市博迪化工股份有限公司,使用前用无水硫酸镁干燥处理),分析纯;N,N-二甲基甲酰胺(DMF,天津市博迪化工股份有限公司),分析纯;邻菲啰啉(Phen,天津市大茂化学试剂厂),分析纯;七氧化四铽(Tb4O7,国药集团化学试剂有限公司),分析纯;其余试剂均为市售分析纯试剂.
1700型傅里叶变换红外光谱仪(FTIR,美国Perkin-Elmer公司);UV-2602型紫外-可见分光光度计(上海尤尼柯公司);DRX300型核磁共振仪(瑞士Bruker公司);HITACHIF-2500荧光光度计(日本日立公司);ZCT-A型热重分析仪(北京精仪高科仪器有限公司).
2.2 改性聚砜PSFBA的制备及表征
按文献14所述的过程制备与表征改性聚砜PSFBA,典型的步骤如下.在装有电动搅拌器、冷凝回流管及温度计的四口瓶中,加入50 mL DMAC与0.66 g PSF,使PSF充分溶解,再加入2.56 g对氯甲基苯甲酸CMBA与0.18 mL无水四氯化锡,于70°C恒温及搅拌的条件下,使CMBA与PSF之间的Friedel-Crafts烷基化反应进行15 h.结束反应后,以乙醇为沉淀剂,将产物沉出,用稀盐酸洗涤,以除去四氯化锡,再用乙醇和蒸馏水交替洗涤,真空干燥至恒重,即得侧链键合苯甲酸(BA)配基的改性聚砜PSFBA.通过红外光谱与核磁共振氢谱的测定,14对PSFBA的化学结构进行表征,并采用紫外分光光度法测定功能聚合物PSFBA大分子链中BA的键合量,14本研究使用的PSFBA,其BA的键合量为2.45 mmol·g-1.
2.3 高分子-稀土配合物的制备及表征
2.3.1 二元配合物PSFBA-Tb(III)的制备
将10 mmol Tb4O7溶于50 mL 1:1(V/V)盐酸,加热至溶液呈透明后冷却,加入2 mL过氧化氢溶液(15%),搅拌1 h,加热浓缩至有晶粒开始产生,冷却体系,析出大量晶体,再置于真空烘箱中(35°C)烘干,即得三氯化铽结晶(TbCl3·6H2O).15称取0.3 g PSFBA(BA的量为0.735 mmol)溶解于50 mL DMF中,并用NaOH溶液调节pH=6-7,再加入0.0915 g三氯化铽晶体(0.245 mmol),在水浴50°C搅拌条件下使配合反应进行8 h(上述溶液体系中,大分子链BAPSF上的配基BA与Tb(III)离子的摩尔比为3: 1).配位反应结束后以乙醇为沉淀剂,沉淀出聚合物,用乙醇和蒸馏水洗涤,真空干燥,即得高分子-稀土二元配合物PSF-(BA)3-Tb(III)(对于键合型高分子-稀土配合物,一般以准确的投料比表示其组成).6,15改变配基BA与Tb(III)离子的摩尔比,也制备了其它结构的二元配合物.
2.3.2 三元配合物PSFBA-Tb(III)-Phen的制备
以邻菲罗啉为小分子第二配基,分别采用两种配比(中心离子:大分子链上配基:小分子第二配体的摩尔比为1:1:2及1:1:3),制备了两种三元配合物:PSF-(BA)1-Tb(III)-(Phen)2与 PSF-(BA)1-Tb(III)-(Phen)3.以PSF-(BA)1-Tb(III)-(Phen)2的制备为例,说明三元配合物的制备过程:准确称取0.0972 g(0.49 mmol)的邻菲罗啉,置于50 mL的锥形瓶中,再加入25 mL DMF,磁力搅拌下溶解,并用NaOH溶液调节pH= 6-7,加入0.0915 g(0.245 mmol)三氯化铽晶体,在水浴50°C磁力搅拌条件下使配合反应进行4 h.再称取0.1 g(0.245 mmol)的功能聚合物PSFBA,置于50 mL的锥形瓶中,加入25 mL DMF,使聚合物充分溶解,并用NaOH溶液调节pH=6-7;将此溶液加入上述溶液中,在水浴50°C磁力搅拌条件下使配位反应进行8 h.配位反应结束后,以乙醇为沉淀剂,沉淀出聚合物,用乙醇和蒸馏水洗涤,真空干燥,即得三元配合物PSF-(BA)1-Tb(III)-(Phen)2.
2.3.3 配合物的表征及热稳定性能测定
用KBr压片法测定二元配合物PSFBA-Tb(III)与三元配合物PSFBA-Tb(III)-Phen的FTIR光谱,证实它们的化学结构;采用热重(TG)分析仪,测定改性聚合物PSFBA、二元配合物与三元配合物的热失重曲线(空气氛围,升温速率为10°C·min-1),考察它们的热稳定性.
2.4 配合物谱学性能的测定
2.4.1 紫外吸收光谱的测定
以DMF为溶剂,配制PSFBA、二元配合物与三元配合物的溶液,使用UV-Vis分光光度计测定三种物质在DMF中的紫外吸收光谱.
2.4.2 荧光发射光谱的测定
以DMF为溶剂,分别配制三氯化铽、二元配合物和三元配合物的溶液,使用荧光光谱仪,以最佳激发峰(先以Tb(III)离子545 nm处的特征发射扫描两种配合物的激发光谱,测得最佳激发峰均在295 nm处)测定各溶液中诸物质的荧光发射光谱.
分别将二元配合物和三元配合物溶于氯仿中,在培养皿中流延成膜,置于温度为40°C的烘箱中,除去溶剂,干燥成膜,分别制得二元配合物与三元配合物的薄膜(膜的厚度约为60 μm),测定薄膜的荧光发射光谱.
3 结果与讨论
3.1 溶液中形成的二元配合物PSF-(BA)n-Tb(III)
的化学结构
本研究在Lewis酸催化剂的存在下,先使氯甲基苯甲酸与聚砜发生Friedel-Crafts烷基化反应,生成侧链键合苯甲酸配基的改性聚砜PSFBA,其化学结构如示意图1所示;然后使PSFBA与Tb(III)离子在溶剂DMF中进行配位反应,制得高分子-稀土配合物PSFBA-Tb(III)溶液,最后使用沉淀剂将配合物从溶液中析出.作者认为,有一个重要概念需要特别指出(虽然以往的文献6,7中一般并未指明):凡是高分子-稀土配合物溶液研究体系,体系中的高分子溶液应该均为稀溶液,溶液中的高分子线团是彼此分离的,大分子链上的配基与稀土离子之间的配位属分子内的配合作用,即同一条大分子链上的配基与稀土离子之间发生的配合作用,否则就会发生以稀土离子为交联桥的大分子之间的交联现象,16溶液就会变得浑浊,就不能称其为配合物溶液.在本研究体系中,当溶液中大分子PSFBA侧链上的配基BA与Tb(III)离子以一定的摩尔比进行配合反应时,所得到的高分子-稀土配合物PSF-(BA)n-Tb(III)应该具有示意图1所示的化学结构.
3.2 配合物的红外光谱

示意图1 改性聚砜PSFBA和二元配合物PSF-(BA)n-Tb(III)化学结构的图式表示Scheme 1 Schematic expression of structures of PSFBAand binary complex PSF-(BA)n-Tb(III)
图1给出了PSFBA,二元配合物PSF-(BA)3-Tb(III)及三元配合物PSF-(BA)1-Tb(III)-(Phen)2的FTIR光谱.在改性聚砜PSFBA的谱图中,除显示聚砜的全部特征吸收外,在1710 cm-1处的峰为配基BA羧羰基C=O的伸缩振动特征吸收峰,3420 cm-1处的峰为羧羟基的伸缩振动特征吸收.而在二元配合物PSF-(BA)3-Tb(III)的谱图中,BA羧羰基C=O于 1710 cm-1处的伸缩振动吸收峰消失,而在1536和 1406 cm-1处出现了羧基的反对称伸缩振动吸收峰和对称伸缩振动吸收峰,说明配基BA羧基的两个氧原子均与Tb(III)离子发生了配位作用,即BA的羧基以双齿配基的形式与Tb(III)离子发生了鳌合配位,17,18形成了二元高分子-稀土配合物;在二元配合物的谱图中,于418和456 cm-1处还出现了Tb-O键的伸缩振动吸收峰.同样,在三元配合物PSF-(BA)1-Tb(III)-(Phen)2的谱图中,BA羧羰基C=O的伸缩振动吸收峰消失,在1540和1405 cm-1处出现了羧基的反对称伸缩振动吸收峰和对称伸缩振动吸收峰,在456和418 cm-1处也出现了Tb-O键的伸缩振动吸收峰;另外,还在1560 cm-1处出现了红移后的Phen分子中C=N键的特征吸收峰.上述变化充分证实,PSFBA大分子链上BA的羧基协同Phen与Tb(III)离子发生了配位鳌合,形成三元配合物PSF-(BA)1-Tb(III)-(Phen)2.
3.3 配合物的紫外吸收光谱
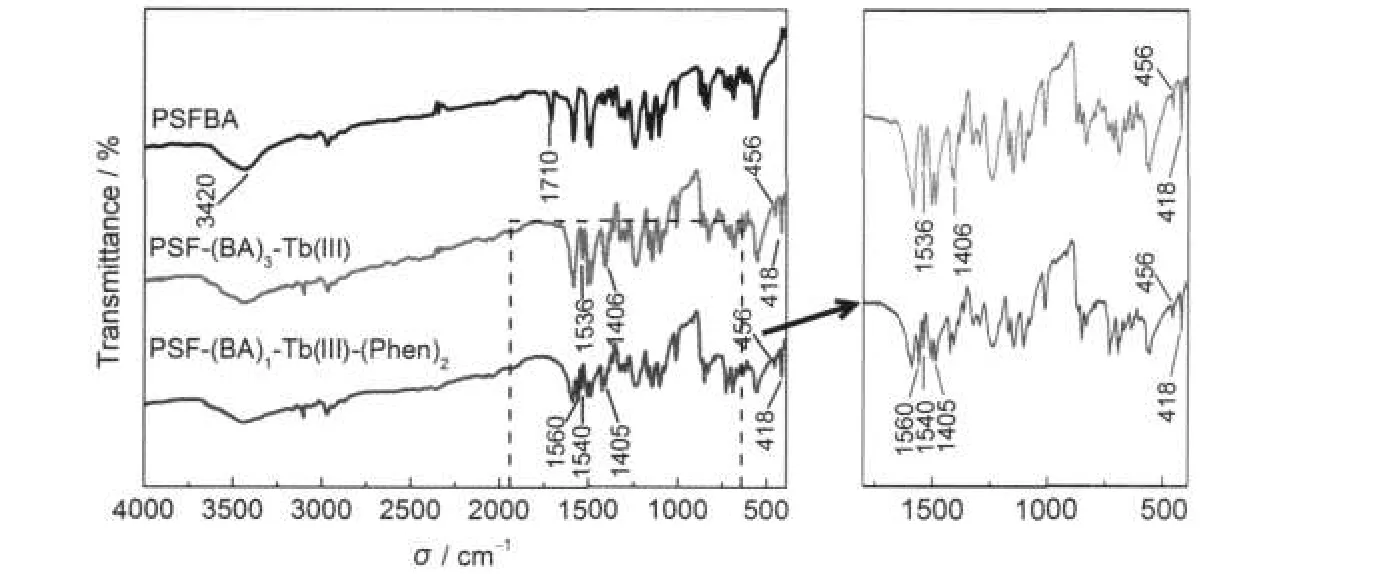
图1 PSFBA与配合物PSF-(BA)3-Tb(III)和PSF-(BA)1-Tb(III)-(Phen)2的FTIR光谱图Fig.1 FTIR spectra of PSFBAand complexes PSF-(BA)3-Tb(III)and PSF-(BA)1-Tb(III)-(Phen)2
图2给出了改性聚砜PSFBA,Phen,二元配合物PSF-(BA)3-Tb(III)及三元配合物PSF-(BA)1-Tb(III)-(Phen)2的紫外吸收光谱.
从图2可以看到,改性聚砜PSFBA,在265-315 nm范围具有强的紫外吸收,292 nm附近具有最强的吸收峰,归属于PSFBA分子结构中苯环和羰基的π→π*电子跃迁;自由配体Phen在294和321 nm处有两个特征吸收峰,分别归属于Phen的π→π*跃迁和n→π*跃迁.
当聚合物PSFBA与Tb(III)离子配位形成二元配合物后,紫外吸收峰的形状与PSFBA十分相似,也具有强的紫外吸收,只是特征吸收峰略有红移(292 nm→295 nm),进一步表明大分子配体PSFBA与Tb(III)离子之间形成了稳定的配合物结构; Tb(III)离子在紫外区吸收很弱,故上述谱图数据还说明二元配合物的紫外吸收来自于大分子配体PSFBA,与中心离子基本无关,配合物的发光主要是配基BA对Tb(III)离子能量传递的结果.
在三元配合物的紫外吸收光谱中,于297和323 nm处有两个最大吸收波长,前者是Phen的部分谱带与PSFBA的吸收峰重叠所致,后者则归属Phen的第二个特征吸收带.显然,与PSFBA及自由配体Phen的吸收光谱相比,三元配合物的紫外吸收峰发生了明显的红移,这是由于配基BA及Phen通过O、N原子与Tb(III)离子配位后,形成多个螯合环,使中心离子周围的π电子云密度变大,共轭体系增大,电子离域化程度增加,跃迁能量降低,从而产生红移现象.上述谱图数据对比的结果充分表明,Tb(III)离子与两种配体之间已配位成键,说明三元配合物的紫外吸收来自于大分子配体PSFBA与Phen的协同吸收(Tb(III)离子在紫外区吸收很弱),配合物的发光是两种配基对Tb(III)离子的能量传递所致.
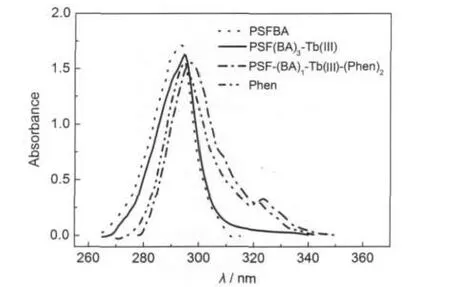
图2 PSFBA,Phen与配合物PSF-(BA)3-Tb(III)和PSF-(BA)1-Tb(III)-(Phen)2的紫外吸收光谱Fig.2 UV absorption spectra of PSFBA,Phen,and complexes PSF-(BA)3-Tb(III)and PSF-(BA)1-Tb(III)-(Phen)2 solvent:N,N-dimethyl formamide(DMF)
3.4 二元配合物PSFBA-Tb(III)的荧光发射光谱
3.4.1 PSF-(BA)3-Tb(III)的荧光发射光谱
以545 nm为发射波长,测定了二元配合物PSF-(BA)3-Tb(III)在DMF溶液中激发光谱,确定了最佳激发波长为295 nm,以此为激发波长,测定配合物PSF-(BA)3-Tb(III)在DMF溶液中的荧光发射光谱,同时也测定TbCl3在DMF溶液中的荧光发射光谱(两种溶液中的Tb(III)离子浓度相同),测定结果如图3(A)所示,图3(B)则为二元配合物PSF-(BA)3-Tb(III)薄膜的荧光发射光谱.
从图3可以看出:(1)二元配合物PSF-(BA)3-Tb(III)与TbCl3的发射谱带的位置与形状相同,表明配合物发射出Tb(III)离子的特征荧光,谱图中主要显示出490 nm处的5D4→7F6跃迁、545 nm处的5D4→7F5跃迁、585 nm处的5D4→7F4跃迁及623 nm处的5D4→7F3跃迁所导致的发射;(2)配合物的发射峰既窄(色纯度高)又强,在本研究条件下(Tb(III)离子浓度为9.8×10-5mol·L-1),溶液中二元配合物PSF-(BA)3-Tb(III)的荧光强度远比TbCl3强,提高约30倍;(3)二元配合物PSF-(BA)3-Tb(III)的薄膜具有强的荧光发射.
稀土离子本身的发光效率是很低的,上述实验事实充分显示,芳羧酸功能化的聚砜PSFBA侧链上的BA配基对稀土离子的荧光发射产生了显著的光吸收-分子内能量转移作用(Antenna效应),即配基BA吸收能量后,由三重态以非辐射方式将能量传递给Tb(III)离子,然后受激的Tb(III)离子再以辐射方式跃迁到基态能级,从而发射出Tb(III)离子的特征荧光,配基BA的敏化作用使得二元配合物的荧光发射远强于TbCl3的荧光发射,这与文献19,20中报道的小分子芳羧酸作为配基的稀土配合物的情形十分相似.上述实验事实也表明,配基BA的三重激发态能量与Tb(III)离子的最低激发态能级之间存在着良好的匹配关系,因为配基三重激发态能量与稀土离子最低激发态能级的高度匹配,是有效发生分子内能量传递的必要条件.18,19
3.4.2 荧光发射强度对配基BA数量的依赖性及

图3 二元配合物PSF-(BA)3-Tb(III)和TbCl3的激发与荧光发射光谱Fig.3 Fluorescence excitation and emission spectra of binary complex PSF-(BA)3-Tb(III)and TbCl3 (A)solution:solvent,DMF;concentration of Tb(III),9.8×10-5mol·L-1;(B)film of PSF-(BA)3-Tb(III)
表观饱和配位数在以往的高分子-稀土发光配合物研究中,小分子配体的协同配位以及发光强度对稀土离子浓度的依赖性(即稀土离子的浓度猝灭问题)总是人们研究的两个中心议题.作者认为,对于含有敏化发光配基的大分子链与稀土离子所形成的发光配合物,考察研究表观饱和配位数是一个更为重要的问题,对于制备具有高性能的强场致发光固体(或膜)材料来说,表观饱和配位数应该是一个很重要的参数,因为只有确定表观饱和配位数,才会将固体发光材料中所加入的小分子物质的量降至最少,这将有利于提高固体发光材料的综合性能(发光性能与热性能).关于“表观饱和配位数”的概念的提出以及相关理论的分析见下文的讨论.
固定溶液中Tb(III)离子的浓度,改变功能聚合物PSFBA的浓度,从而改变溶液中配基BA与Tb(III)离子的摩尔比,从而制得不同摩尔比的二元配合物PSF-(BA)n-Tb(III)的溶液,测定诸二元配合物溶液的荧光发射,得到图4.
图4中显示:(1)当溶液中聚合物PSFBA的浓度较小时,配合物的荧光发射很弱;(2)随着配基BA与Tb(III)离子的摩尔比(n(BA):n(Tb(III)))的不断增大,配合物的荧光发射强度不断增强;(3)当摩尔比增至5:1时,荧光发射强度达最大值,再继续增大摩尔比,如n(BA):n(Tb(III))=6:1时,荧光发射强度与摩尔比为5:1时的相同,不再改变.对上述实验事实作如下解释.当溶液中配基BA与Tb(III)离子的摩尔比较小时,由于Tb(III)离子的配位数远未达到饱和,故分子内能量转移的程度很弱,配合物的荧光发射强度很弱;随着BA与Tb(III)离子的摩尔比增大,与Tb(III)离子配位的配基数目增多,分子内的能量转移加强,荧光发射强度增强;当Tb(III)离子的配位数达到饱和时,二元配合物PSF-(BA)n-Tb(III)分子内的能量转移也达到极限,产生最大的荧光发射强度,此时再增大BA与Tb(III)离子的摩尔比,对配合物的荧光发射强度不再发生影响.图4显示,当n(BA):n(Tb(III))=5:1时,Tb(III)离子的配位数表观上达到饱和,即二元配合物的表观饱和配位数为10 (BA为双齿螯合基团),此时二元配合物的结构为PSF-(BA)5-Tb(III).
为什么称为“表观饱和配位数”呢?如前所述,在高分子-稀土离子配合物溶液体系中,功能聚合物PSFBA的大分子链呈彼此分离的无规线团状, Tb(III)离子与配基BA的配位是分子内的配合作用.但是,受大分子链弯曲张力的限制以及受空间位阻的影响,21大分子链上的配基与稀土离子配位时,不能像小分子配基那样,按照配合物空间结构的需要自由地配位,因此,即使溶液中聚合物PSFBA的浓度较大,大分子链上的配基也不能实现全部地与稀土离子配位,21其结果是:一方面稀土离子周围的配位点总会产生缺位现象(缺位位点被水分子占据,见示意图1),另一方面,大分子链上的配基有剩余现象.因此,当溶液中聚合物PSFBA的浓度增大到n(BA):n(Tb(III))=5:1时,所显示出的饱和配位数10应该是“表观饱和配位数”.
3.5 三元配合物的荧光发射光谱
3.5.1 小分子配体对二元配合物PSF-(BA)5-Tb(III)的补充配位效应
在二元配合物PSF-(BA)5-Tb(III)的溶液中,添加小分子配体Phen,且逐渐增大Phen的量,以改变两种配基的比例,形成三元配合物PSF-(BA)5-Tb(III)-(Phen)m,测定各种比例下三元配合物溶液的荧光发射强度,得到图5.

图4 配基BA与Tb(III)摩尔比不同时二元配合物PSF-(BA)n-Tb(III)的荧光发射光谱Fig.4 Fluorescence emission spectra of binary complexes PSF-(BA)n-Tb(III)at different mole ratios of ligand BAto Tb(III) solvent:DMF;concentration of Tb(III):9.8×10-5mol·L-1
由图5可见,随着小分子配体Phen的加入,三元配合物PSF-(BA)5-Tb(III)-(Phen)m的荧光发射强度在增强;当n(Phen):n(Tb(III))增加至1:1时,形成三元配合物PSF-(BA)5-Tb(III)-(Phen)1,此时配合物的荧光发射强度达到最大;若再继续加入Phen,配合物的荧光发射几乎不再改变.对上述实验事实作如下解释.
如前所述,在二元配合物PSF-(BA)5-Tb(III)的溶液中,Tb(III)离子周围的配基BA只是表观上达饱和,实际上由于受聚合物链弯曲张力的影响,Tb(III)离子周围仍有空位(配位水占据),当加入小分子配体Phen后,配位水会被取代,空位被Phen占据,会产生如下的补充配位效应:由于第二配体的加入,中心离子周围的共轭体系变大,两种配体的协同作用使配合物的光能吸收和分子内能量传递的能力增强;22,23另一方面,配位水分子的被取代,有效地避免了羟基-OH振动带来的荧光猝灭,24,25两种作用的结果都会导致配合物荧光发射的增强.但是,由于二元配合物PSF-(BA)5-Tb(III)分子中Tb(III)离子周围的配基已基本趋于饱和,故只需稍加补充Phen (按n(Phen):n(Tb(III))=1:1加入Phen,即增加2个配基),形成三元配合物PSF-(BA)5-Tb(III)-(Phen)1,即可使Tb(III)离子周围的配基达到完全饱和,此时再继续增加Phen的用量,对Tb(III)离子的荧光发射将不再发挥敏化作用,配合物的荧光发射强度将不再变化.该实验现象同时也说明,由于配基BA以双齿配基的形式与Tb(III)离子螯合配位,螯合效应使配位结构较为稳定,小分子配体Phen只起到补充配位的作用,并没有取代已发生配位的BA.
3.5.2 两类三元配合物发光性能与热性能比较

图5 在三元配合物PSF-(BA)5-Tb(III)-(Phen)m中邻菲啰啉的补充配位效应Fig.5 Supplementation coordination effect of phenanthroline in ternary complexes PSF-(BA)5-Tb(III)-(Phen)m solvent:DMF;concentration of Tb(III):9.8×10-5mol·L-1
除具有上述结构的三元配合物PSF-(BA)5-Tb(III)-(Phen)1外,本研究还固定第一配体与第二配体比例(n(BA):n(Phen)=1:2,n(BA):n(Phen)=1:3),制备了另一类三元配合物PSF-(BA)1-Tb(III)-(Phen)2和PSF-(BA)1-Tb(III)-(Phen)3(见2.3.2节),这是文献中惯用的方法及比例.在保持Tb(III)离子浓度相同(9.8×10-5mol·L-1)的条件下,配制了两类三元配合物的溶液,测定了荧光发射光谱,如图6A所示;也分别制备了两类三元配合物的薄膜,薄膜的荧光发射光谱示于图6B.
由图6可以看出,在BA与Tb(III)离子达到表观饱和配位的基础上再加入Phen补充配位,所制备的第一类三元配合物PSF-(BA)5-Tb(III)-(Phen)1,其荧光发射强度要高于第二类三元配合物PSF-(BA)1-Tb(III)-(Phen)2和PSF-(BA)1-Tb(III)-(Phen)3,其原因已在3.5.1节进行了分析,在于Tb(III)离子周围的配基达到完全饱和配位,两种配基的协同配位以及配位水分子的消除.第二类三元配合物的荧光发射强度都较低,且前者的荧光发射强度更低,其可能的原因在于:一方面Tb(III)离子周围的配基未达到饱和配位,另一方面Tb(III)离子周围可能存在有引起荧光猝灭的配位水分子.总之,对于含有敏化发光配基BA的大分子PSFBA与稀土离子所形成的配合物,当配基BA对Tb(III)离子的配位达到表观饱和时,再加入少量小分子配基补充配位,所形成的三元配合物PSF-(BA)5-Tb(III)-(Phen)1具有最强的荧光发射性能.

图6 两类三元配合物的荧光发射光谱Fig.6 Fluorescence spectra of two kinds of ternary complexes(A)solution:solvent,DMF;concentration of Tb(III), 9.8×10-5mol·L-1;(B)film
对于场致发光材料尤其是电致光材料而言,热稳定性是另一个重要的性能,本研究采用热重分析仪,测定了两类三元配合物的TG曲线,考察了它们的热稳定性,图7给出了测定结果.图7显示,三元配合物的热分解可基本划分为四个阶段:室温-150°C,水分子(配位水)的挥发;150-475°C, Phen的分解;475-525°C,配基BA从高分子链上的断裂分解;525-635°C,高分子PSF的分解.从图7的TG曲线可以清楚地看到:(1)第一类三元配合物PSF-(BA)5-Tb(III)-(Phen)1在150°C以前没有失重现象发生,表明其结构中不含配位水分子,而第二类三元配合物在150°C前均有明显失重,即均含有配位水,且PSF-(BA)1-Tb(III)-(Phen)2比PSF-(BA)1-Tb(III)-(Phen)3含有更多的配位水,此实验事实印证了前面关于配位水的理论分析;(2)第一类三元配合物PSF-(BA)5-Tb(III)-(Phen)1仅在475°C发生明显失重,表现出良好的热稳定性,而第二类三元配合物在较低的温度即发生明显失重,PSF-(BA)1-Tb(III)-(Phen)3明显失重的温度为220°C,PSF-(BA)1-Tb(III)-(Phen)2明显失重的温度为390°C,显示出差的热稳定性.显然,小分子配体加入量越少,三元配合物的热稳定性越好.因此,对于含有敏化发光配基BA的大分子PSFBA与稀土离子所形成的配合物,当配基BA对Tb(III)离子的配位达到表观饱和,然后再加入少量小分子配基补充配位,所形成三元配合物PSF-(BA)5-Tb(III)-(Phen)1具有最好的热稳定性.

图7 两类三元配合物的热失重谱图Fig.7 TG thermograms of two kinds of ternary complexes
综上所述,三元配合物 PSF-(BA)5-Tb(III)-(Phen)1既具有优良的荧光发射性能,也具有很高的热稳定性,再加上聚砜PSF良好的力学性能与成膜性能,可以预期,该高分子-稀土配合物是一种高性能的场致发光材料.
4 结论
用芳羧酸功能化的聚砜PSFBA与Tb(III)离子配位,并以Phen为第二配体,分别合成了二元配合物PSFBA-Tb(III)与三元配合物PSFBA-Tb(III)-Phen,深入研究了配合物的荧光发射性能与配合物结构之间的关系.大分子链上的配基BA对Tb(III)离子的荧光发射具有强的敏化作用,配合物均能发射出强的Tb(III)离子特征荧光.对于二元配合物PSFBA-Tb(III),Tb(III)离子的表观饱和配位数为10,即二元配合物具有PSF-(BA)5-Tb(III)的组成时,配基BA对Tb(III)离子的配位表观上达到饱和,此时二元配合物具有最大的荧光发射.在二元配合物PSF-(BA)5-Tb(III)溶液中,当按n(Phen):n(Tb(III))=1的比例加入Phen时,形成三元配合物PSF-(BA)5-Tb(III)-(Phen)1.与惯用的其它比例的三元配合物相比,三元配合物PSF-(BA)5-Tb(III)-(Phen)1中所加入的小分子配体Phen最少,但荧光发射强度最强,热稳定性最好.
(1) Setua,S.;Menon,D.;Asok,A.;Nair,S.;Koyakutty,M. Biomaterials 2010,31,714.
(2)Qiu,G.M.;Yan,C.H.;Guo,C.F.;Wang,W.W.;Zhang,M. J.Rare Earths 2007,25,5.
(3) Li,D.G.;Zhu,J.;Cheng,Z.P.;Zhang,W.;Zhu,X.L.React. Funct.Polym.2009,69,240.
(4) Guo,L.;Wu,S.Z.;Zeng,F.;Zhao,J.Q.Eur.Polym.J.2006, 42,1670.
(5) Hu,S.;Liu,L.;Zhang,W.;Wen,S.P.;Jin,R.G.;Li,X.L. J.Rare Earths 2006,24,14.
(6) Liu,D.;Wang,Z.G.Polymer 2008,49,4960.
(7) Liu,D.;Wang,Z.G.;Yu,H.;You,J.Eur.Polym.J.2009,45, 2260.
(8) Suo,Q.L.;Lu,F.;Shi,J.W.;Hong,H.L.;Luo,J.P.J.Rare Earths 2009,27,28.
(9)Yan,C.H.;Xu,C.J.;Hu,H.H.;Wang,R.;Zhang,M.;Qiu,G. M.J.Rare Earths 2009,27,761.
(10) Nechifor,G.;Voicu,S.I.;Nechifor,A.C.;Garea,S. Desalination 2009,241,342.
(11) Devrim,Y.;Erkan,S.;Bac,N.;Eroğlu,I.Int.J.Hydrog.Energy 2009,34,3467.
(12)Azab,H.A.;El-Korashy,S.A.;Anwar,Z.M.;Hussein,B.H. M.;Khairy,G.M.Spectrochim.Acta A 2010,75,21.
(13) Maji,S.;Viswanathan,K.S.J.Lumin.2008,128,1255.
(14) Zhang,R.X.;Gao,B.J.;Du,J.M.Chem.Bull.in press. [张瑞霞,高保娇,杜俊玫.化学通报,印刷中.]
(15)Yan,C.H.;Hu,H.H.;Xu,C.J.;Zhu,W.;Zhang,M.;Bu,X.R. J.Photochem.Photobiol.A:Chem.2009,204,19.
(16) McCurdie,M.P.;Belfiore,L.A.Polymer 1999,40,2889.
(17) Liang,X.;Jia,X.Q.;Yang,Y.;Hou,L.P.Eur.Polym.J.2010, 46,1100.
(18)Yan,B.;Zhou,B.J.Photochem.Photobiol.A:Chem.2005,171, 181.
(19) Liu,T.H.;Duan,G.J.;Zhang,Y.P.;Fang,J.;Zeng,Z.Z. Spectrochim.Acta A 2009,74,843.
(20) Pei,J.;Geng,X.T.;Yan,J.B.;Zhang,Y.H.;Zhao,Y.;Wang,Y. Y.;Sun,B.J.Alloy.Compd.2006,426,363.
(21)Nagai,A.;Takahashi,A.;Komatsu,T.;Nakagawa,T.Polym.J. 1988,20,609.
(22) Liu,X.Y.;Hu,Y.L.;Wang,B.Y.;Su,Z.X.Synth.Met.2009, 159,1557.
(23) Zhang,Y.H.;Hao,Y.Z.;Pei,J.;Li,Y.P.;Sun,B.;Ren,J.J. Spectroscopy and Spectral Analysis 2011,31,145. [张彦辉,郝彦忠,裴 娟,李英品,孙 宝,任聚杰.光谱学与光谱分析, 2011,31,145.]
(24) Marmodée,B.;de Klerk,J.S.;Ariese,F.;Gooijer,C.;Kumke, M.U.Anal.Chim.Acta 2009,652,285.
(25)Du,C.X.;Wang,Z.Q.;Xin,Q.;Wu,Y.J.;Li,W.L.Acta Chim. Sin.2004,62,2265.[杜晨霞,王志强,辛 琦,吴养洁,李文连.化学学报,2004,62,2265.]
October 9,2011;Revised:November 14,2011;Published on Web:November 17,2011.
Structure and Florescence Emission Properties of a Polymer-Rare Earth Complex Composed of Aryl Carboxylic Acid-Functionalized Polysulfone and Tb(III)
ZHANG Rui-Xia GAO Bao-Jiao*WEI Xiao-Peng
(Department of Chemical Engineering,North University of China,Taiyuan 030051,P.R.China)
Benzoic acid(BA)was bonded to the side chains of polysulfone(PSF)via a polymer reaction, giving aryl carboxylic acid-functionalized polysulfone(PSFBA).The binary complex PSFBA-Tb(III)and ternary complex PSFBA-Tb(III)-phenanthroline(Phen)were prepared by the coordination of Tb(III)to PSFBA using PSFBA as a macromolecular ligand and Phen as a smaller ligand.The chemical structures of the complexes were characterized by Fourier transform infrared(FTIR)and UV absorption spectroscopies. The relationships between the structure and properties,including the fluorescence emission properties,of the complexes in solution and films were investigated,as well as their thermal stability.All of the polymerrare earth complexes containing PSFBA exhibited very strong characteristic fluorescence emission from Tb(III),namely,BA bonded to the side chains of PSFBA can effectively sensitize Tb(III).The apparent saturated coordination number of PSFBA-Tb(III)is 10,which implies that the coordination of BA to Tb(III) reaches saturation and maximum fluorescence is achieved for the complex PSF-(BA)5-Tb(III).The ternary complex PSF-(BA)5-Tb(III)-(Phen)1,which is prepared by adding Phen to a solution of PSF-(BA)5-Tb(III), possesses the strongest fluorescence emission and excellent thermal stability compared with ternary complexes PSF-(BA)1-Tb(III)-(Phen)3and PSF-(BA)1-Tb(III)-(Phen)2,which were prepared using the conventional ratios of reagents.
Polysulfone;Benzoic acid;Polymer-rare earth complex;Sensibilization; Photoluminescence
10.3866/PKU.WHXB201111171
*Corresponding author.Email:gaobaojiao@126.com;Tel:+86-351-3924795.
The project was supported by the Natural Science Foundation of Shanxi Province,China(201002100843).
山西省自然科学基金(201002100843)资助项目
O641;O631
