滇姜花中倍半萜成分的研究*
2012-12-01赵映梅邹海舰朱培芳薛咏梅
赵映梅,邹海舰,朱培芳,薛咏梅,马 莎,赵 庆△
(1.昆明市呈贡区人民医院,云南昆明 650500;2.云南中医学院,云南昆明 650500)
滇姜花 (Hedychium yunnanenseGangep.)为姜科姜花属植物,主产于云南昆明、禄春、孟连,四川、广西也有分布。生长于海拔1 700~2 200m的山坡林下。花期8-9月,果期10-11月[1]。我们曾对滇姜花根茎的化学成分作过研究,分离得到多个化学成分[2-9];并对部分二萜成分进行了体外细胞毒活性和小鼠体内抗肿瘤活性筛选,部分二萜成分具有显著的活性[4,8-9]。初步预试还表明,其中的倍半萜成分还具有抗真菌活性。
1 实验仪器与材料
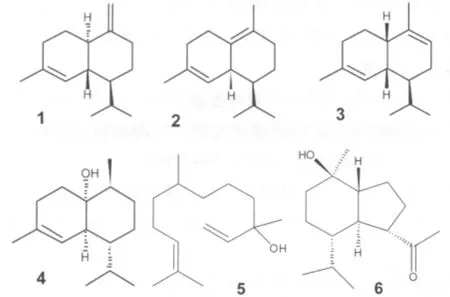
为进一步研究滇姜花的化学成分,我们又从采集于昆明市的滇姜花 (H.yunnanense)根茎中共分离鉴定了6个倍半萜类化合物,分别为:γ-杜松烯 (1),δ-杜松烯 (2),α-muurolene(3),epicubenol(4),橙花叔醇 (5),oplopanone(6)。其中,化合物1~4为杜松烷型倍半萜,化合物5为金合欢烷型倍半萜,化合物6为oplopane型倍半萜。所有6个化合物均为首次从该植物分离得到。
核磁共振氢谱、碳谱由Bruker AM-400型核磁共振仪测定。柱层析用的硅胶硅胶为青岛海洋化工厂生产。薄层色谱用青岛海洋化工厂生产的硅胶G板和硅胶H板,薄层显色方法为:喷洒10%硫酸-乙醇溶液,在105℃下烘烤至显色明显。Ag-NO3-硅胶系自己制备:将5%的硝酸银溶液100mL与80g 200~300目硅胶混合均匀后,在常温下挥干,再在烘箱中于105℃下烘烤30min即得。
滇姜花根茎样品采于云南省昆明市,植物标本由中国科学院昆明植物研究所童绍全研究员鉴定为Hedychium yunnanenseGangep.,保存于中国科学院昆明植物研究所植物化学实验室。
2 提取和分离
取滇姜花根茎样品4.0kg用95%乙醇回流提取3次。乙醇提取物 (410g)分别用石油醚、乙酸乙酯提取3次。石油醚提取部分 (230g)经硅胶柱层析分离,石油醚-乙酸乙酯梯度洗脱,得到6个馏分 (Fr.A~F)。馏分A(Fr.A)再反复经硅胶柱层析、石油醚-乙酸乙酯梯度洗脱,Ag-NO3-硅胶柱层析、石油醚-乙酸乙酯梯度洗脱,得到6个化合物。各化合物的产率如下。1∶90mg,2 和 3∶115mg,4∶87mg,5∶66mg,6∶87mg。
3 结构鉴定
γ-cadinene(1):colorless oil;EIMS m/z(%):204[M]+(21),203(100),149(69),123(60),109(67),95(86),57(95);1H NMR(400MHz,CDCl3):1.68(3H,s),0.75(3H,s),0.94(3H,s),4.67(1H,d,J=1.3Hz),4.55(1H,d,J=1.3Hz),5.57(1H,br.s);13C NMR(100MHz,CDCl3):15.1(q),21.6(q),23.9(q),103.2(t),36.3(t),30.5(t),26.5(t),25.8(t),122.4(d),46.9(d),45.1(d),43.5(d),26.7(d),153.2(s),134.7(s).以上数据与文献报道的γ-cadinene数据一致[10]。
δ - cadinene(2):13C NMR(100MHz,CDCl3):129.9(C -1),26.8(C -2),32.0(C -3),134.2(C-4),124.7(C -5),39.5(C -6),45.4(C -7),21.2(C -8),32.4(C -9),124.4(C -10),26.7(C-11),15.7(C -12),21.7(C -13),23.6(C -14),18.5(C-15).以上数据与文献报道的δ-cadinene数据一致[11]。
α -muurolene(3):13C NMR(100MHz,CDCl3):39.1(C -1),24.5(C -2),30.5(C -3),134.4(C -4),124.2(C -5),36.7(C -6),41.0(C -7),24.7(C -8),121.5(C -9),136.3(C -10),26.6(C -11),15.8(C -12),21.4(C -13),23.9(C -14),21.8(C-15).以上数据与文献报道的α-muurolene 数据一致[10,12]。
Epicubenol(4):colorless oil;1H NMR(400MHz,CDCl3):5.45(1H,br.d,J=3.8Hz,H - 5),1.70(3H,s,H - 14),0.96(3H,d,J=6.57Hz,H - 15),0.87(3H,d,J=6.95Hz,H - 13),0.80(3H,d,J=6.92Hz,H -12),1.05(1H,m,H -8β),1.10(1H,m,H -9α),1.17(1H,m,H -7),1.54(1H,m,H -9β),1.57(1H,m,H -8α),1.61(1H,m,H -10),1.63(2H,m,H -2),1.68(1H,m,H -6),1.97(1H,m,H -11),2.05(1H,m,H -3α),2.08(1H,m,H -3β);13C NMR(100MHz,CDCl3):15.2(C - 13),21.6(C -12),23.5(C -14),26.9(C -15),22.0(C-2),24.0(C -8),26.7(C -3),31.1(C -9),26.4(C -11),41.9(C -6),48.0(C -7),49.2(C -10),122.1(C -5),72.7(C -1),133.8(C -4).以上数据与文献报道的epicubenol数据一致[13]。
橙花叔醇(5):colorlessoil;1H NMR(400MHz,CDCl3):5.79(1H,dd,J=10.8,17.2Hz),5.08(1H,d,J=17.2Hz),4.93(1H,d,J=10.8Hz),1.56(3H,s),1.48(6H,s),1.15(3H,s);13C NMR(100MHz,CDCl3):25.4(q),17.3(q),15.6(q),27.0(q),22.4(t),26.4(t),39.5(t),41.9(t),73.0(s),131.2(s),135.1(s),124.0(d),124.0(d),144.7(d),111.3(t).以上数据与文献报道的橙花叔醇数据一致[14]。
oplopanone(6):whitepowder;13C NMR(100MHz,CDCl3):15.6(C -12),20.3(C -14),21.9(C -13),23.0(C -8),25.3C -2),28.6(C -3),29.47(C -15),29.49(C -11),42.0(C -9),46.7(C -7),49.4(C -1),55.7(C -6),57.0(C -5),73.0(C-10),211.5(C-4).以上数据与文献报道的oplopanone 数据一致[15]。
3 结果与讨论
化合物1~6均为首次从该植物中分离得到。AgNO3-硅胶柱层析法常用于分离一些难以用常规硅胶柱层析法分离的烯键异构体。在本文中,化合物1、2和3的烯键位置不同,采用该法就可得到很好的分离。
[1]中国科学院昆明植物研究所.云南植物志[M].北京:科学出版社,1997:549-560.
[2]赵庆,郝小江,陈耀祖,等.滇姜花新二萜成分的研究[J].高等学校化学学报,1995,16(1):64-68.
[3]赵庆,郝小江,陈耀祖,等.滇姜花的倍半萜成分[J].云南植物研究,1995,17(2):201-203.
[4]赵庆,邹澄,郝小江,等.滇姜花抗肿瘤活性二萜及其光敏氧化反应的研究[J].植物学报,1999,41(5):528-530.
[5]邹澄,赵庆,郝小江,等.滇姜花中的新二萜成分-滇姜花素 D[J].云南植物研究,1999,21(2):253-256.
[6]赵庆,邹澄,郝小江,等.滇姜花中的新二萜成分-滇姜花戊素[J].云南植物研究,2000,22(1):116-118.
[7]赵庆,郝小江,邹澄,等.滇姜花中的两个新成分[J].天然产物研究与开发,2008,20(5):761-764.
[8]赵庆,贺小琼,郝小江,等.滇姜花二萜成分的抗肿瘤活性研究[J].天然产物研究与开发,2010,22:395-397.
[9]赵声定,马莎,赵庆,等.三个二萜成分的抗肿瘤活性研究[J].云南中医学院学报,2010,33(3):33-34,50.
[10] Nils B,Wilfried A K.The role of germacrene D as a precursor in sesquiterpene biosynthesis:investigations of acid catalyzed,photochemically and thermally induced rearrangements[J].Phytochemistry,2000,155:141 -168.
[11] Barrfro A F,Sanchez JF,Oltra JE,et al.Oxygenated sesquiterpenes from the wood of Juniperus oxycedrus[J].Phytochemistry,1991,30(5):1551 -1554.
[12] Hiroshi H,Yasuhiko T,Nobuhiro F.Terpenoids with antifouling activity against barnacle larvae from the marine sponge Acunthella cavernosa[J].Tetrahedron,1996,52(7):2359-2368.
[13] Kensuke N,Kazuyoshi K,Masaru F,et al.Biosynthesis of(+)-cubenene and(+)-epicubenol by cell-free extracts of cultured cells of Heteroscyphus planus and cyclization of[2H] farnesyl diphosphates[M].J.Chem.Soc.Perkin.Trans.I,1995:1935 -1939.
[14]吴寿金,赵泰,秦永琪.现代中草药化学[M].北京:中国医药科技出版社,2002:734.
[15] Su W C,Fang J M,Cheng Y S.Sesquiterpenes from Leaves of Cryptomeria japonica[J].Phytochemistry,1995,39(3):603-607.
