神经介入治疗:生物电极
2012-11-27张冠石
张冠石
本刊编辑部,北京 100022
0 前言
神经介入治疗是一个通过使用人工模拟的生物电信号来干预人体神经系统,从而增强、抑制或修正神经反射的过程。将人工电信号导入人体时,要用到由良导体组成的电极。随着神经介入技术的发展,这种治疗技术的精确性和准确性都在不断提高,而实现这些技术进步的关键也在于新型电极设计和制造工艺的改良。
生物电极在神经介入治疗中的功能主要是接收和传导信号。针对不同的使用范围和目的,研究人员开发制作了不同材质和结构的电极。最初的生物电极主要由惰性金属制成,这些材料稳定性高、生物相容性好,而随着高分子和纳米材料的发展,科研人员开始考查各种新型材料作为生物电极原材料的可能性,并且已经获得了一定的进展。
1 原理:双电层模型(Gouy-Chapman-Stern,GCS)
生物电极在神经介入治疗中所扮演的角色,是连接信号发生器和人体并将人工生物电信号导入人体的介质和介面。电流在电极内部的传导遵循库仑定律,在进入人体之后则按照一定的规律去影响活体细胞的生物膜电位,从而生成或调整神经系统或肌肉内的神经脉冲。
在将人工电信号导入人体的过程中,由于人体内细胞和组织液的电学特性与金属电极有所不同,因此了解电极-组织液介面的物理和化学性质就尤为重要。金属电极中,电荷的移动是由电子在金属能带中的迁移现象完成的,而在本质为胶体溶液的组织液中,电荷以带电胶体粒子为载体分散在体系中,而且随着带电粒子的移动而移动。两者之间,电荷不能直接形成交换,而是通过电极-组织液介面上的一系列物理和化学过程形成的电荷移动完成电信号传导。
为了阐述胶体溶液和金属介质之间的电学属性,Helmholtz于1879年提出了该介面的平板模型,也就是双电层模型的雏形。之后,1910年和1913年,Gouy和Chapman分别修正了平板模型,建立了Gouy-Chapman扩散双电层模型。1924年,Stern又提出了Stern模型,基本确立了双电层理论的相关内容[1-5]。
胶体溶液中的电荷是以带电胶体粒子的形式分散在体系中。正负电荷总量相等,以保证溶液的电中性。在金属电极中,电荷的流动以电子流的形式生成。如果金属部分电子聚集,那么在金属-组织液介面上的组织液一侧,受到负电荷吸引,会有带正电的胶体颗粒聚集,形成一层带正电的致密层(Stern层),而在致密层外面还会有富集负电胶体颗粒的扩散层[6],见图1。

图1 双电层结构的模型
由于致密层溶液中电荷在空间中分布不均匀,这层溶液实际上体现出了一定的电容特性。再加上电荷的扩散效应,得出双电层的电学模型,见图2。
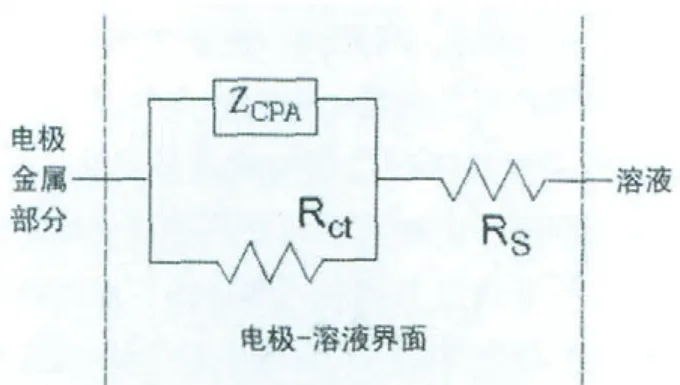
图2 双电层结构的电学模型
在该模型中,ZCPA是介面电容导致的阻抗[7]:

其中CI是介面的电容。在GCS模型中[8],介面电容可以由致密层电容CH和扩散层电容CG计算得出:

致密层电容与双电层厚度、双电层和普通溶液渗透性有关,而扩散层电容则与电极电压、胶体颗粒所带电荷等条件有关。
2 传统的电极设计
2.1 配合导电胶使用的银电极
传统的皮外电极是银电极(Ag/AgCl)[9],这种电极通常作为标准电极用于电化学测量过程中。经过长时间的科研测量和实际应用,标准Ag/AgCl电极的各项属性数据均已准确测出,其工作原理也已非常清楚。在正确的操作流程下,这种电极配合导电性良好的高分子胶能够给出非常完美的临床结果。
Ag/AgCl电极最常见结构是一颗镀银的盘状电极,后部与导线相连。现在市面上这种电极产品普及度很高,而且价格适宜,是皮外电极最常见的品类。皮外采集心电信号(ECG)、肌电信号(EMG)、脑电信号(EEG)和眼球电信号(EOG)等均使用这种电极[10-12]。
由于人体皮肤有大量沟回并有毛发等附着结构,在皮外采集生物电信号的过程中,这些附着结构将会在电极和皮肤之间带入空气,从而影响到收集的信号强度。因此一般情况下,电信号的皮外采集过程需要导电胶来传导电信号,排除电极与皮肤之间的空气等干扰因素。导电胶主要由各种网状导电高分子组成,包括聚氧化乙烯、聚乙烯吡咯烷酮(PVP)等。
2.2 干式电极
与使用导电胶的Ag/AgCl电极相反,干式电极在使用时不需要涂抹额外的导电液体。一般情况下,只需要略微润湿皮肤,干式电极就可以在短时间内获得与使用导电胶的电极质量相仿的生物电信号[13]。
干式电极根据工作原理可以分为两种:① 利用汗液等导电液体连接人体与电极,降低皮肤的电阻,从而接收记录人体电信号;② 刺入皮肤,跳过电阻较大的角质层而直接从真皮层测量记录生物电信号。
最初的干式电极是由导电金属板组成[14],使用时需要润湿皮肤或者利用汗液的导电作用。最常见的就是用于各种快速测量仪器,比如跑步机的心律测量。这种干式电极的最大优势是便于使用,不需要固定和涂抹胶体,缺点是不能固定于某处长期测量,因此在临床上作用比较受限。另一种干式电极则是由弹性橡胶掺杂碳纤维组成。该设计扩大了干式电极的舒适性和易用性,并且由于可以更好地贴近皮肤,该电极的信号质量也有所提高。
除了贴在皮肤上之外,另一种使电极降低对导电胶依赖的手段是跳过电阻较高的皮肤角质层[15-18]。人类皮肤角质层厚度约为10~40 mm,因此可以使用经过精密加工的微型针头电极来采集皮下的电信号。这种电极会导致病人轻微的炎症和刺痛感。
2.3 植入式电极
在绝大多数情况下,植入式电极被用于人机交互系统中,尤其是被用于脑机接口中。植入式电极按功能可以分为两类:信号收集类和激发类。两类电极在设计和材料方面并没有太大的区别。
植入式电极,尤其是用于脑机接口的品类,由于其接触的是人体最敏感的部分——神经组织,因此在设计和制作的过程中,对结构和材料有着很高的要求。植入式电极常用的触电材料是导电性优良、化学活性极弱的贵金属,比如金、铂、铱等,电极表面以陶瓷、聚酰亚胺等绝缘材料密封并保证生物相容性。
在设计方面,由于定位精确性的需要,单个植入电极的尺寸往往被控制在几十至几百μm范围内。这样做的目的是使每一个电极触点可以准确对应单个或少数几个神经元细胞或神经纤维,记录信息或输出刺激信号。正常情况下,电极距离目标细胞越近,距离其他细胞越远,信号的质量越高而噪音越小。
为了优化生物电信号的接收和发送,降低不良反应,并促进神经元细胞体和神经纤维在电极触点上的生长,研究人员尝试使用不同的大分子修饰电极,并取得了一定的成效:使用有消炎作用的多肽修饰电极触点来减轻炎症反应;使用高分子和氨基酸修饰电极来降低排异反应。
3 最新进展
3.1 无接触电极
无接触电极是一种新型的皮外电极,该电极的特点在于不必与人体皮肤接触,不需要传统的双电层机制进行电荷交换,并可以在不接触皮肤、毛发等附着物的情况下测量人体电信号。
无接触电极可以在不形成双电层的情况下测量人体电信号,是因为该系统利用了皮肤和电极表面两个导体层和二者之间的空气以及其他物质构成的绝缘层,组成了一个电容体系。该体系的电容很小(10pF级别)而电阻很大(大于108Ω),因此隔绝了电荷交换的可能,而完全由电容感应来侦测人体内电信号的产生和变化。电极部分侦测到的微弱信号将通过信号放大器放大并输出至处理器中。
1994年Prance和合作者首次开发了一组无接触电极系统[19],该系统由25颗ECG电极组成,可以在3 mm内收集人体电信号。该系统的电阻和电容分别为1016Ω以及10-17F。2000年,Prance和他的研究小组利用德州仪器公司的INA116信号放大器开发了上述产品的改进型[20]。
无接触电极的出现使得人体电信号的获取更加方便,而且病人的舒适程度也有所增加。随着技术的改进,有的公司逐步将电极嵌入到病床、椅子、床垫等日常用品中,实现了对脱离电极的病人实施监护等目的。
3.2 多通道电极
随着医疗技术的发展,在一个单独的位点所能达到的信息收集和神经刺激效果已经不能满足医疗手段的需求,而且单次植入操作也难以保证电极位置的精确性,因此多通道电极应运而生。
标准的多通道电极包含大约60只电极触点(8×8或6×10)。电极触点的尺寸约在10~30μm之间,材料为导电性良好的金属材料。常见的多通道电极包括Michigan电极组和Utah电极组,二者均以硅晶为基底,以金属丝为导电部分。
环状神经电极是另一种多通道电极,它的特别之处在于将多通道的电极触点集成在一片可折叠的绝缘材料上。环状神经电极的主要用途是利用人工电信号刺激神经纤维。通常情况下1根神经纤维包括大量的神经,每1根神经负责不同的功能,因此在需要有选择性地刺激其中1根而保持其他的神经不变的时候,就需要在该神经所在的神经纤维表面施加电刺激。
使用环状电极时,医生将找出需要针对的神经纤维,将环状电极沿外围固定一圈,保持电极触点与神经纤维的良好接触。然后通过每一个电极通道向神经纤维传递电信号,并通过观察患者反应确定每一颗触点的效果。结合所获得的数据和结果,医生可以编码电极各个通道之间的编码方式来优化神经刺激效果。
3.3 电磁感应(脑电波)
传统的脑电信号(EEG)测量方法是通过一组皮外电极多点测量脑部电信号。然而常用的电极组需要覆盖在患者头部,这给测量带来了一定的不便,并容易受到病人肌肉电信号和细微动作的影响。因此研究人员针对脑电波的电学特性开发了一种通过电磁感应测量大脑电信号的系统。
楞次定律证明闭合电路中电流的变化会形成一个激发磁场,该磁场会阻碍感应电流的磁通量变化。在人脑中,存在着大量的空间方向垂直于颅骨的神经元细胞,这些细胞内的信号传导是通过电流形式实现的,而这些电流的产生、改变和消失均会遵循楞次定律引起空间内磁场的改变。因此,在颅骨外侧的垂直平面上配置导电线圈,就可以捕捉到激发磁场的变化并量化地测量电信号强度。通过在不同位点放置导电线圈并测量电信号强度,即可获取脑电波信号。
4 结论
医用电极作为连接神经介入类医疗器械和患者身体的重要介质,在神经介入治疗过程中扮演着极为重要的角色。其材质、尺寸和结构设计均会影响人体和医疗器械之间的互动效果,因此必须针对特定的病症和作用位置进行深入的优化。
随着各种功能高分子和纳米科技的发展以及微机电技术(MEMS)的进步,医用电极的制作材质选择范围将得到进一步的拓展,其尺寸将进一步缩减,而电学性质和生物相容性将进一步提高,从而为需要神经介入治疗的患者带来更大的便利。
[1]David C Grahame.The electrical double layer and the theory of electrocapillarity[J].Chem Rev,1947,41(3):441-501.
[2]James A Davis,Robert O James,James O Leckie.Surface ionization and complexation at the oxide/water interface:I. computation of electrical double layer properties in simple electrolytes[J].J Colloid and Interface Science,1978,63(3):480-499.
[3]Anthony M Dymond.Characteristics of the metal-tissue interface of stimulation electrodes[J].IEEE Transactions on Biomedical Engineering,1976,23(4):274-280.
[4]Peter Van Gerwen,Wim Laureyn,Wim Laureys,et al.Nanoscaled interdigitated electrode arrays for biochemical sensors[J].Sensors and Actuators B:Chemical,1998,45(1-2):73-80.
[5]Franks W,Schenker I,Schmutz,et al.Impedance characterization and modeling of electrodes for biomedical applications[J].IEEE Transactions on Biomedical Engineering,2005,52(7):1295-1302.
[6]W Franks,F Heer,I McKay,et al.CMOS monolithic microelectrode array for stimulation and recording of natural neural networks[J].Biosensors and Bioelectronics,2004,20(2):358-366.
[7]E T McAdams,A Lackermeier, J A McLaughlin,et al.The linear and nonlinear electrical properties of the electrode electrolyte interface[J].Biosensors Bioelectron,1995,10(1-2):67-74.
[8]A J Bard,L R Faulkner.Electrochemical methods[M].New York:Wiley,2001.
[9]C Fonseca,A Martins da Silva.A novel dry active electrode for EEG recording[J].IEEE Transactions on Biomedical Engineering,2007,54(1):162-168.
[10]W Portnoy,R David,L Akers.Biomedical electrode technology[M].New York:Academic,1974.
[11]S Nishimura,Y Tomita,T. Horiuchi.Clinical application of an active electrode using an operational amplifier[J].IEEE Trans Biomed Eng,1992,39(10):1090-1099.
[12]A Taheri,R Knight,R Smith.A dry electrode for EEG recording[J].Electroencephalogr Clin Neurophysiol,1994,90(5):376-383.
[13]Yu Mike Chi,Gert Cauwenberghs.Dry-contact and noncontact biopotential electrodes:methodological review[J].IEEE Reviews in Biomedical Engineering,2010,(3):106-119.
[14]L Geddes,M Valentinuzzi.Temporal changes in electrode impedance while recording the electrocardiogram with "dry" electrodes[J].Ann Biomed Eng,1973,1(3):356-367.
[15]G Gargiulo,P Bifulco,R Calvo,et al.Mobile biomedical sensing with dry electrodes[A].2008 Fourth International Conference on Intelligent Sensors,Sensor Nertworks and Information Processing[C].Sydney:ISSNIP,2008:261-266.
[16]M Mestrovic,R Helmer,L Kyratzis,et al.Preliminary study of dry knitted fabric electrodes for physiological monitoring[A].Proc 3rd Int Conf Intelligent Sensors,Sensor Networks Information[C].Melbourne:ISSNI,2007:601-606.
[17]J Yoo,L Yan,S Lee,et al.An attachable ECG sensor bandage with planar-fashionable circuit board[A].Proc Int Symp Wearable Computers[C].Linz:ISWC,2009:145-146.
[18]M Ishijima.Monitoring of electrocardiograms in bed without utilizing body surface electrodes[J].IEEE Trans Biomed Eng,1993,40(6):593-594.
[19]A Clippingdale,R J Clark,C Watkins.Ultrahigh impedance capacitively coupled heart imaging array[J].Rev Scientific Instruments,1994,65(1):269-270.
[20]R J Prance,A Debray,TD Clark,et al.An ultra-low-noise electrical-potential probe for human-body scanning[J].Measure Sci Technol,2000,11(3):291.
