HCFC-141b水合物海水淡化试验研究
2012-11-23喻志广祁影霞刘业凤张华
喻志广,祁影霞,刘业凤,张华
(上海理工大学,上海 200093)
0 引言
海水淡化技术,近年来发展迅猛,当今海水淡化三大主流技术分别是多级闪蒸(MSF)、低温多效(MED)和反渗透(RO)[1]。我国目前的海水淡化方法主要包括蒸馏法、膜法、结晶法、溶剂萃取法和离子交换法等,然而这些方法分别存在能耗大,成本高,结垢情况严重等局限性, 需要开发更加经济环保的方法[2,3]。
水合物法海水淡化是利用较易生成水合物的小分子物质与海水中的纯水生成水合物晶体,固液分离后,固体水合物分解即可得到淡水。水合物法海水淡化技术的最大优点是能耗低、设备简单、紧凑[3-5];在水或盐水中溶解度低;无毒,价廉易得,无爆炸危险;显示了良好的应用前景。水合物技术的应用研究,经过几十年的发展,已经形成基于水合物形成和分解且具有重要工业应用前景的特有技术,在海水淡化、汽车燃料等诸多领域得到广泛应用,部分技术已进入中试阶段或实现小规模工业化[6]。水合物法海水淡化技术是研究最早、授予专利较多的水合物技术。20世纪40年代,Parker等就利用水合物技术从海水中提得到淡水,但是这一技术直到进入21世纪后被人们重视[1,3]。根据计算,生产1 m3淡水仅需2.64 kWh的电能[5,7]。Bradshaw等使用HCFC-141b和C2H4进行了海水淡化的初步研究,用 XRD和拉曼测试了盐水中生成的水合物成分,说明水合物具有很好的析盐能力,显示了水合物法海水淡化的良好应用前景,但是他们的实验没有涉及分离过程[7,8]。由上述海水淡化研究进展知,对于水合物法的研究很有限,不利促进该技术的发展。本文以 HCFC-141b水合物为研究对象,设计海水淡化试验系统装置和实验过程,研究水合物生成、分离和分解及前后溶液盐度的变化,分析实验结果,提出问题和建议,为水合物法海水淡化技术的研究奠定基础。
1 实验装置
实验仪器和样品具体主要包括:反应釜系统及磁力搅拌器;温度传感器:采用铂热电阻Pt100,A级;压力传感器:范围0~10MPa,精度等级:0.3%;数据采集系统:采用HP公司生产的Agilent34970A数据采集仪;恒温水浴:温度范围为-20~+100 ℃,波动度为±0.05 ℃,流量为13 L/min;盐度计:量程为1.0~50.0ppt 和0.1~5.00%两档,分辨率分别为0.1ppt和0.01%,使用温度-10~80 ℃;试剂:HCFC-141b,纯度≥99.5%;实验用水为去离子水(自制);NaCl(分析纯);分析天平(型号ALC-3100.2),精度0.01g;氮气瓶,纯度≥99.99%。

图1 实验装置系统
2 实验方法
实验方法如下:
1) 首先用去离子水配制溶液浓度分别为3.00%、
2.00%、1.00%和0.14%的NaCl溶液300.00g,并用盐度计进行实际盐度测定,记录数据;
2) 称量30.00 g , HCFC-141b溶液;
3) 在实验前用去离子水清洗反应釜,然后加入上述两种溶液,密封反应釜,进气、出气阀门打开,用氮气清扫釜内的空气,待常压之后关闭各阀门;
4) 启动恒温水浴系统,设定操作温度为实验温度,并等到水浴温度平衡在实验温度时进入下一步;
5) 把反应釜放到恒温水浴中,并固定好;装好温度传感器,测其内部反应物温度;
6) 在反应釜上安装好磁力搅拌机,打开电源,设定电压为20 V(大致转速为300-400转/分钟);
7) 打开Agilent34970A数据采集仪, 采集的数据通过串行口输入电脑进行显示,并将采集的数据储存,实验完后对数据进行处理;
8) 待其反应充分完成后,关闭相应仪器,分离生成的固体浆状HCFC-141b水合物,并将生成物与剩余溶液密封到干净的容器装置内,等待生成的水合物分解;
9) 待水合物分解完全后,用盐度计分别测定分解后溶液和未反应溶液的盐度,并记录数据;
10) 整理实验台,进行下一组实验。
3 实验水合物反应结果
3.1 水合物生成过程
在含盐溶液中,利用搅拌系统可以加快反应速度[9],常压下,通过搅拌,混合溶液温度不断降低,在温度降到5 ℃左右时,反应釜内混合液体的透明度明显有所下降,可以判定有HCFC-141b水合物形成,随着温度近一步下降,水合物逐渐增多,可以看出大量浆状水合物形成。但反应完成后,停止搅拌,可以看出反应并不能完全进行,底部始终有部分HCFC-141b未参加反应,上部溶液大量存在。根据文献[5,8],常压下HCFC-141b在去离子水和质量分数2%~5%的氯化钠溶液中的形成温度为2~6 ℃。在本试验中,常压下HCFC-141b在去离子水和质量分数2%和3%的氯化钠溶液中水合物大量生成的温度在2 ℃左右;而在1%和0.14%的氯化钠溶液中大量生成的温度都在0~1 ℃;降温过程中反应釜内的体系温度变化走势见图2。
3.2 水合物分离
待其反应充分完成后,取出并打开反应釜,将釜内反应物全部倒入特制过滤装置,用密质过滤布快速过滤掉未反应溶液,并保存未反应溶液;再将分离出的固体浆状HCFC-141b水合物用事先制备好的同温度下的蒸馏水稍稍冲洗;最后将生成物与剩余溶液密封到干净的容器内,等待生成的水合物分解。
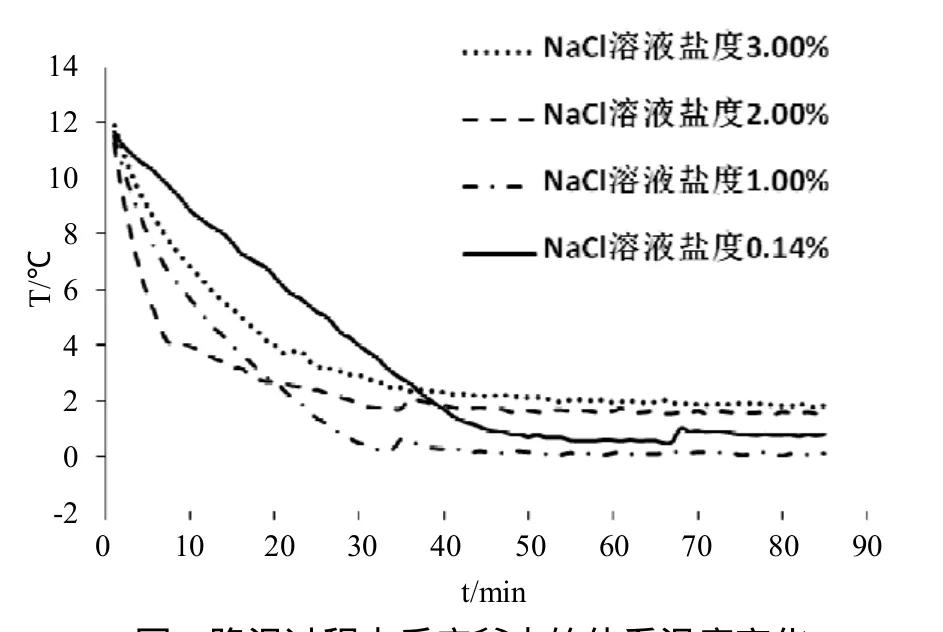
图2 降温过程中反应釜内的体系温度变化
3.3 水溶液在水合物反应前后盐度变化
待水合物分解完全后,用盐度计分别测定分解后溶液和未反应溶液的盐度,并记录数据。见表1。
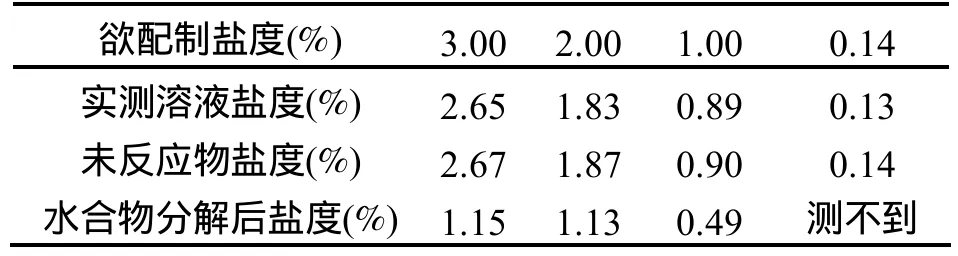
表1 溶液在水合物反应前后的盐度变化
4 水合物实验结果分析
由图2和表1的实验结果分析可知:
1) 图2为以HCFC-141b水合反应时的温度对反应时间关系曲线, 简称为水合曲线。在图2中, 在时段20 min~40 min中出现的是水合物形成峰。由于搅拌[9],反应界面很大,随着温度下降,当体系中有了晶核, HCFC-141b与水的水合反应便可以很快发生,大量水合物形成时放热足以使体系温度突然上升;但此峰高并不很明显,这是因为虽然搅拌促进水合物快速大量生成,但水在混合液中所占比例大,通过搅拌所产生的热量也快速分散传递出去,体系向环境放热故温度升到一定程度后又下降。
2) 随着水合物的生成,溶液盐度会增加,通过测量水合物形成后剩余溶液的盐度和水合物分解后的盐度,可以定性分析水合物在生成过程中的排盐机理,即是,在水合物生成的过程中,盐水中的水分子与HCFC-141b结合形成水合物,而盐水中的盐分仍留在溶液中。由表1中可以看出,水溶液的盐度在通过水合物的生成和分解后,已有显著降低。但从以上初步结果来看,还远未达到饮用水标准。另外,未反应物的盐度并没有显著上升,是因为水溶液所占比例大,反应后盐度并没明显变化。
根据文献[5],HCFC-141b在盐水中生成水合物的过程中,盐水的浓度对水合物生成的过冷度有一定影响,浓度太低或太高都对过冷度影响不大,质量分数1.0%的氯化钠可以有效减小过冷度。从本实验知,在水合物生成过程中加入了搅拌,使水合物、HCFC-141b、水三者充分混合, 形成混悬液, 加快了对流扩散,使反应物质相对接触面增大,此时盐水的浓度对水合物生成的过冷度有一定影响,质量分数1.0%~2.0%的氯化钠可有所减小水合物开始生成时的过冷度,可以有效增加水合物形成速度,缩短水合物生成时间。
3) 此外,水合物的分离和HCFC-141b的分离也是一个影响盐度变化的关键环节,合理的分离方法和易操作的分离装置,将对最后结果产生影响;分离水合物结晶时,应当适当洗去结晶上附着的浓盐水并在合适的条件下熔化该结晶水合物;所得的水合物分解后的混合液以及浓盐溶液都要进行分离HCFC-141b,因为HCFC-141b基本不导电,影响盐度计对溶液盐度的测量,并且要尽可能地回收水合剂HCFC-141b,减少污染;为此,我们除了用密质过滤布快速分离水合物,并用同温度的去离子水冲洗固体水合物结晶外,还让水合物分解后的混合液和浓盐溶液充分静沉,使HCFC-141b沉于底部,与上层水溶液分层,再依次从上层取出淡水、浓盐溶液进行相应盐度测量,底层液态HCFC-141b进行回收。
5 结论
1)在HCFC-141b水合物生成过程中加入了搅拌,此时盐水的浓度对水合物生成的过冷度有一定影响,质量分数1.0%~2.0%的氯化钠可有所减小水合物开始生成时的过冷度,可以有效增加水合物形成速度,缩短水合物生成时间。水合物分解后的水溶液测量后发现盐度明显降低,即采用水合物的生成和分解可以实现海水淡化的目的。
2)在实验操作上,通过搅拌,加快了对流扩散,使反应物质接触相对面积增大,并将水合物相变产生的热量及时散发出去, 这促进了水合物生快速形成;注重了操作细节,适当用同温度的去离子水冲洗水合物上附着的浓盐水,并对水合物分解后的混合液和浓盐溶液进行分离HCFC-141b,以此来减小对盐度测量的影响。在试验装置上,根据水合物的特点设计了水合物法海水淡化的试验装置和分离装置,使水合物法海水淡化流程和结果更合理;不足是仍没有实现自动化分离。所以建议设计的分离装置应简易,并能实现分离自动化;此外,在HCFC-141b与盐水分离回收时,可以考虑利用物质沸点的差异来进行分离,并实现连续回收再利用,减少污染。
3)在水合物法海水淡化的过程中,盐水中的水分子与HCFC-141b结合形成水合物,而盐水中的盐分仍留在溶液中,这是水合物脱盐的基础;水合物自然生成速率缓慢,故水合物技术的应用关键是提高水合物生成速率;加入搅拌,增加反应界面,强化传热是提高水合物生成速率的一个途径。所以,若进行淡水量产,要选择合适的工质,使其满足在较易到达的压力和温度下生成水合物,并能提高水合物的生成速度,且能很好地分离;开发设计的装置和分离技术要能使淡水进入量产。
[1] 汤成伟,刘道平,李刚.水合物法海水淡化技术[C]. 中国工程热物理学会 2008多相流学术会议论文集.青岛:中国工程热物理学会.2008:NO.086064.
[2] 朱玉兰.海水淡化技术的研究进展[J].能源研究与信息,2010, 2(26):72-73.
[3] 任宏波,相凤奎,张磊,等.水合物法海水淡化技术应用进展[J].海洋地质前沿, 2011, 27(6):74-78.
[4] 龙臻,李栋梁,梁德青.一种新型水合物法海水淡化系统能耗及经济性分析[J].水处理技术,2010,36(8):67-70.
[5] 李栋梁,龙臻,梁德青.水合冷冻法海水淡化研究[J].水处理技术,2010,36(6):65-68.
[6] 宋琦,王树立,武雪红,等.水合物技术应用与展望[J]. 油气储运,2009, 28(9):5-9.
[7] David Wolman. Hydrates, Hydrates Everywhere: A geophysicist revisits a provocatively simple-and previously unworkable-process for extracting freshwater from the sea[J]. Discover, 2004, 25(10).
[8] Bradshaw R W, Simmons B A, Majzoub E H, et al.Clathrate hydrates for production of potable water[J].Mater Res Soc Symp Proc. , 2006,930:1-6.
[9] 吕秋楠,陈朝阳,李小森. 气体水合物快速生成强化技术与方法研究进展[J]. 化工进展, 2011 ,30(1):74-79.
