己二酸铵对7075-T6铝合金硫酸阳极氧化的影响
2012-11-23刘建华李永星李松梅孙玉静
刘建华,李永星,于 美,李松梅,孙玉静
(1. 北京航空航天大学 材料科学与工程学院 空天先进材料与服役教育部重点实验室,北京 100191;2. 国家知识产权局 专利审查协作中心,北京 100088)
己二酸铵对7075-T6铝合金硫酸阳极氧化的影响
刘建华1,李永星1,于 美1,李松梅1,孙玉静2
(1. 北京航空航天大学 材料科学与工程学院 空天先进材料与服役教育部重点实验室,北京 100191;2. 国家知识产权局 专利审查协作中心,北京 100088)
研究硫酸电解液中添加己二酸铵对7075-T6铝合金阳极氧化的影响,采用场发射扫描电子显微镜(FE-SEM)对7075-T6铝合金在不添加和添加己二酸铵的硫酸电解液中制备的阳极氧化膜表面的微观形貌进行分析,采用线性阳极极化研究7075-T6铝合金在两种电解液中的极化行为。利用动电位极化技术和电化学阻抗谱(EIS)研究两种电解液中制备的阳极氧化膜的耐腐蚀性能。结果表明:硫酸电解液中添加己二酸铵可以通过降低电流密度来改善氧化膜的结构,减少氧化膜缺陷,降低微孔孔径,提高阻挡层厚度,从而降低氧化膜的自腐蚀电流密度,提高氧化膜耐腐蚀性能。
7075-T6铝合金;己二酸铵;阳极氧化;电化学阻抗谱
7×××铝合金由于其优异的比强度和良好的机械性能,在航空航天工业中得到广泛应用。然而,航空铝合金由于不同冶金相形成的微电偶使这些合金易于在含有氯离子的潮湿环境中以点蚀和晶间腐蚀的形式发生局部腐蚀[1-4]。为了提高铝合金的耐腐蚀性能,通常采用电解液对其进行阳极氧化处理。其中硫酸阳极氧化和铬酸阳极氧化得到广泛应用,但硫酸阳极氧化对铝合金疲劳性能影响较大,铬酸中的Cr(Ⅵ)被列为对人体危害最大的化学物质之一,是国际公认的致癌金属物之一[5]。因而,近年来国内外学者致力于无铬阳极氧化工艺的研究[6-11]。MOUTARLIER等[6-8]通过在硫酸中添加钼酸盐或高锰酸盐使氧化膜阻挡层厚度增加,膜层耐腐蚀性能得到提高。刘怡和刘凤霞[9]研究在硫酸电解液中添加有机缓蚀剂对氧化膜的影响。结果表明:在硫酸电解液中添加乳酸、酒石酸、苹果酸、乙酸钠和柠檬酸钠等物质,可以提高氧化膜的生长速度,增加氧化膜的厚度。CURIONI等[10]研究酒石酸对2024-T3铝合金阳极氧化及其氧化膜耐腐蚀性能的影响。结果表明:硫酸电解中添加酒石酸不会影响氧化膜的生长机理,会降低氧化膜的生长速率,减少槽液对氧化膜的侵蚀,提高氧化膜的耐腐蚀性能。美国波音公司的WONG等[11]于1990年开发出硼酸-硫酸阳极氧化工艺,并应用于实际生产。采用这种工艺制备的氧化膜更加致密,耐蚀性更高。以上研究说明,在硫酸电解液中加入合适的添加剂可以有效地提高铝合金阳极氧化膜的性能。
己二酸铵在电解电容工业中被广泛用来制备阻挡型氧化膜,其阴离子会进入氧化膜,影响氧化膜的介电性能[12]。本研究室对电压加载下己二酸铵对2024-T3铝合金阳极氧化膜的封闭进行了研究,发现己二酸铵可以有效地修补阻挡层的缺陷,具有良好的封闭效果[13]。在此基础上,本文作者研究硫酸电解液中添加己二酸铵对7075-T6铝合阳极氧化的影响。采用场发射扫描电子显微镜(FE-SEM)对阳极氧化膜的微观形貌进行了分析。采用线性阳极极化技术对铝合金在添加和不添加己二酸铵的硫酸电解液中的氧化行为进行了研究。利用电化学阻抗谱(EIS)对添加和不添加己二酸铵的硫酸电解液中制备的氧化膜耐腐蚀性能进行了研究。探讨硫酸电解液中添加己二酸铵对7075-T6铝合阳极氧化膜微观结构、生长过程及其耐腐蚀性能的影响。
1 实验
1.1 实验材料
实验材料为 7075-T6铝合金板材和工业纯铝(Al含量不低于99.6%,质量分数),尺寸为100 mm×50 mm×2.5 mm,7075-T6铝合金成分见表1。
1.2 铝合金的阳极氧化
将试样用水磨砂纸打磨至1000号,去离子水超声波清洗10 min;随后采用温度为60 ℃的NaOH溶液(40 g/L)碱洗 1 min,室温下用硝酸(30%,质量分数)出光 1 min,每一步处理之后用去离子水冲洗,冷风吹干,备用。
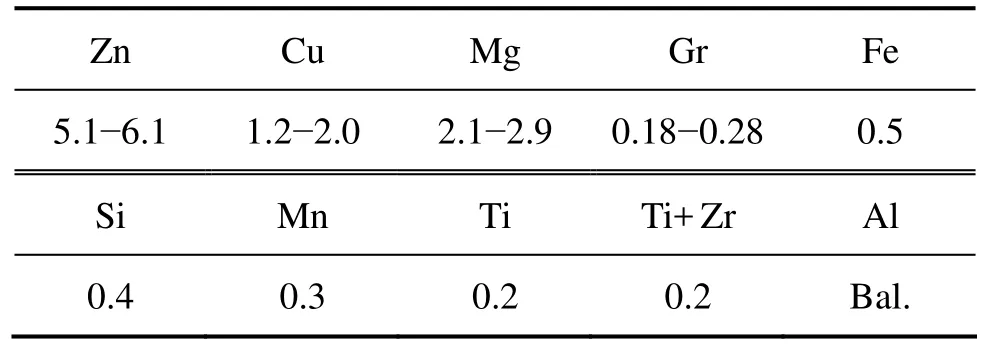
表1 7075-T6铝合金的组成Table1 Composition of 7075-T6 aluminum alloy (mass fraction, %)
对7075-T6铝合金分别在硫酸(0.46 mol/L)和添加己二酸铵(0.1 mol/L)的硫酸(0.46 mol/L)电解液中进行阳极氧化,起始电压为0 V,以3 V/min的速度逐渐升压到15 V(vs SCE)后,进行恒电压阳极氧化20 min,温度为室温((25±1) ℃)。阳极氧化结束后,取出,用去离子水冲洗1 min,冷风吹干保存。
1.3 微观形貌分析
采用场发射扫描电子显微镜(S-4800 FE-SEM,Hitachi, Japan)对添加和不添加己二酸铵的硫酸电解液中制备的阳极氧化膜表面微观形貌进行分析。
1.4 电化学实验
阳极氧化行为研究采用PARSTAT 2273电化学工作站(Princeton application research,ametek,American)对经过前处理的纯铝试样和7075-T6铝合金试样分别在硫酸(0.46 mol/L)和添加己二酸铵(0.1 mol/L)的硫酸(0.46 mol/L)电解液中进行线性阳极极化。试片为阳极,面积为7 cm2,饱和甘汞电极(SCE)为参比电极,铂电极为阴极;温度为室温((25±1) ℃);线性阳极极化从开路电位(OCP) 到7 V(vs SCE)停止,升压速率为1.5 V/min。
耐腐蚀性能测试采用传统三电极体系在电化学工作站上进行,实验介质为氯化钠水溶液(3.5%,质量分数),测试温度为室温((25±1) ℃),工作电极测试面积为1 cm2,饱和甘汞电极(SCE)为参比电极,铂电极为辅助电极;动电位极化曲线扫速为1 mV/s,测试范围从开路电位(OCP)下-0.5 V(vs SCE)到 0.8 V(vs SCE)。电化学阻抗谱(EIS)测试频率范围0.01 Hz~100 kHz,测试信号为幅值10 mV的正弦波,对两种电解液中制备的试样在氯化钠水溶液(3.5%,质量分数)浸泡不同时间(1 h、1 d、3 d)进行EIS测试,交流阻抗谱图采用ZsimPwin软件进行电学元件拟合。
2 结果与分析
2.1 阳极氧化膜微观形貌分析
图1所示为7075-T6铝合金在不添加和添加己二酸铵的硫酸电解液中制备的阳极氧化膜表面 FE-SEM像。从图 1(a)和(b)可以看出,7075-T6铝合金在两种电解液中制备的阳极氧化膜都存在随机分布、形状不一的缺陷,这是由于铝合金中的粗大合金相颗粒在阳极氧化过程中发生优先溶解或脱落造成的,特别是含Cu颗粒会在阳极氧化过程中发生Cu的富集、导致氧气产生,对氧化膜的生长非常不利[14-16]。但图1(b)阳极氧化膜较为平整致密、缺陷较少,说明在硫酸中加入己二酸铵可以减少氧化膜表面缺陷,提高氧化膜的致密度。图 1(c)和(d)分别为图 1(a)和(b)的高倍FE-SEM 照片。从图中看出,添加己二酸铵的硫酸电解液制备的阳极氧化膜更致密,微孔尺寸更小。这可能是由于两方面原因:一方面,阳极氧化过程中己二酸根离子进入氧化膜,改变了氧化膜的介电性能,限制了Al3+从氧化膜向电解液的迁移速率,减少了多孔层生长过程中孔内Al3+向电解液的迁移,从而降低微孔孔径。另一方面,加入己二酸铵,降低了电解液酸度,可以减少由于电解液对氧化膜的溶解造成的微孔孔径扩大。
2.2 阳极氧化行为
线性阳极极化可以用来研究纯铝及铝合金的阳极氧化行为[10,17-19]。为了进一步深入研究硫酸电解液中添加己二酸铵对 7075-T6铝合金阳极氧化行为的影响,采用线性阳极极化研究纯铝及7075-T6铝合金在添加和不含己二酸铵的硫酸电解液中的阳极氧化行为。
图2所示为纯铝和7075-T6铝合金在添加和不添加己二酸铵的硫酸电解液中的伏安曲线。从图 2(a)中看出,电流随电压的变化分为3个阶段(在图中用竖线标示)。第1阶段从开路电位到0 V(vs SCE),极化电流随着电压的升高而逐渐增大,这主要与初始的离子传导过程有关[20];第 2阶段,开始阶段出现一个平台,表明表面生成阻挡型氧化膜,并且逐渐增厚[19-20]。
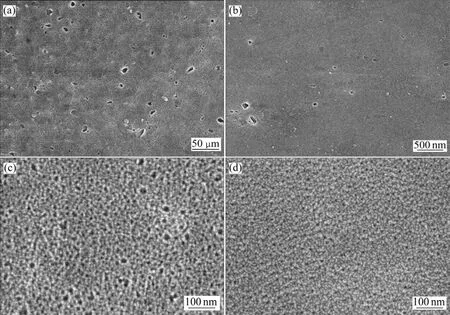
图1 7075-T6铝合金在硫酸和添加己二酸铵的硫酸电解液中制备的阳极氧化膜表面FE-SEM像Fig.1 FE-SEM images of anodic oxide films of 7075-T6 aluminium alloy formed in sulphuric((a), (c)) and ammonium adipate/sulphuric media((b), (d))
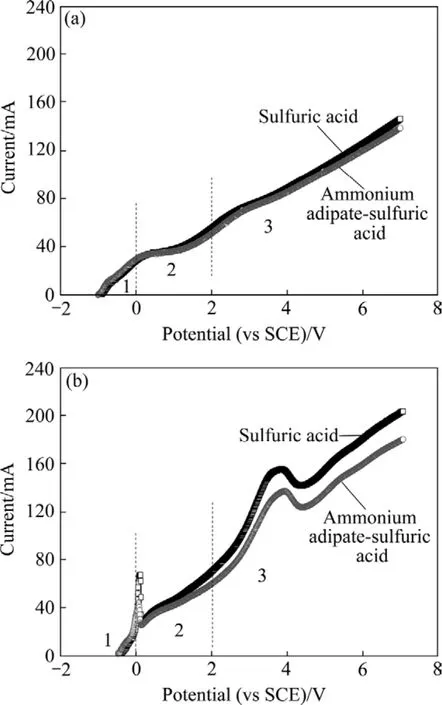
图2 纯铝(99.6%)和7075-T6铝合金在硫酸和添加己二酸铵的硫酸电解液中的伏安曲线Fig.2 V—I curves of 99.6% aluminum(a) and 7075-T6 aluminum alloy(b) in sulfuric acid with and without ammonium adipate
1 V(vs SCE)之后是一个过渡区域,是阻挡层随着电压的升高逐渐增厚,多孔层萌生的过程[21]。第3阶段,电压高于2 V(vs SCE)之后,电流随着电压的升高而增大,是多孔层稳定生长过程[20]。从图2(a)纯铝的伏安曲线可以看出,硫酸电解液中添加己二酸铵,伏安曲线略有下降,没有出现较大变化,说明己二酸铵不会改变纯铝在硫酸电解液中阳极氧化行为。从图2(b)看出,7075-T6铝合金伏安曲线与纯铝伏安曲线变化规律一致,也分为3个阶段。不同之处在于7075-T6铝合金中添加的合金相颗粒在氧化过程中会发生电流集中,因此,在0 V(vs SCE)出现第一个尖峰,在2 V(vs SCE)到5 V(vs SCE)之间出现第二个较宽的峰。而纯铝中不含合金相,所以没有出现电流的峰值。从图2中纯铝和7075-T6铝合金第2和第3阶段的伏安曲线可以看出,硫酸电解液中添加己二酸铵后,从多孔层的萌生开始电流密度相对降低。而 HOUSER等[21]和GRÉGORY等[22]的研究表明,阳极氧化过程中阴离子会进入氧化膜。电流密度相对降低可能是因为阳极氧化过程中己二酸根离子进入阻挡层,改变了氧化膜的介电性能[12]。从而影响了Al3+传导过程,限制了多孔层萌生和发展过程中Al3+从氧化膜向电解液的迁移,最终倾向于形成微孔尺寸更小的氧化膜。图2(b)第一个尖峰是由于含Mg合金相(如S相Al2CuMg)的活性溶解造成的[18,23],因为含Mg合金相的氧化吉布斯自由能小于 Al的氧化吉布斯自由能,阳极极化过程中发生优先氧化溶解,从而出现电流的峰值;第二个宽峰是由于含Cu合金相(如Al7Cu2Fe和(Al,Cu)6(Fe,Cu)等)发生氧化,并伴随着氧气的产生造成的电流集中,出现较宽的峰值[10,17-19]。这是由于含铜合金相惰性较高,发生氧化需要的吉布斯自由能高于Al氧化的吉布斯自由能,在氧化膜与铝合金基体之间会发生 Cu的富集,富集到一定程度,随着极化电压的升高,Cu会发生氧化进入氧化膜,并伴随着氧气的产生,这一过程对氧化膜的结构和形貌有巨大的影响[23-24]。硫酸电解液中添加己二酸铵后,7075-T6铝合金极化电流降低,同时合金相颗粒氧化引起的电流峰值降低:第一个电流峰值从7.5 mA降低为5.5 mA,第二个电流峰值从16 mA降低为13 mA。因此可以得出结论,硫酸电解液中添加己二酸铵可以降低纯铝氧化电流,降低7075-T6铝合金合金相颗粒氧化电流,降低合金颗粒相氧化对氧化膜的不利影响,有利于形成缺陷较少,微孔孔径较小的氧化膜。
2.3 阳极氧化膜耐腐蚀性能
图3所示为7075-T6铝合金在添加和不添加己二酸铵的硫酸电解液中制备的阳极氧化膜在氯化钠水溶液(3.5%,质量分数)中的动电位极化曲线。从图 3中看出,与硫酸电解液制备的阳极氧化膜比较,添加己二酸铵的硫酸电解液中制备的阳极氧化膜自腐蚀电流密度降低一个数量级,耐腐蚀性能较优。说明硫酸电解液中添加己二酸铵可以提高阳极氧化膜的耐腐蚀性能。为了进一步研究硫酸电解液中添加己二酸铵提高氧化膜的耐腐蚀性能的原因,进行了电化学阻抗谱测试。
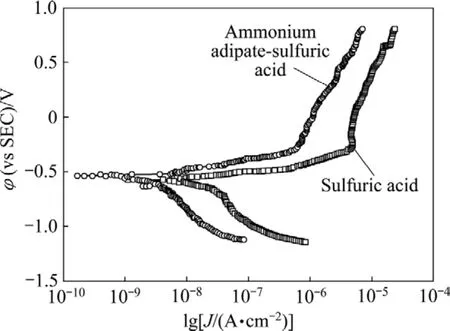
图3 7075-T6铝合金在硫酸和己二酸铵-硫酸电解液中制备的阳极氧化膜在氯化钠溶液中的动电位极化曲线Fig.3 Potentiodynamic polarization curves of anodic film of 7075-T6 aluminum alloy formed in sulphuric, ammonium adipate/sulphuric media in NaCl solution
图4 所示为7075-T6铝合金在添加和不添加己二酸铵的硫酸电解液中制备的阳极氧化膜在氯化钠水溶液(3.5%)中浸泡1 h、1 d、3 d测得的EIS谱。EIS谱的高频部分反映阳极氧化膜多孔层的电容和溶液的电阻,低频部分反映阻挡层的电容和电阻,而中频部分则反映多孔层的电阻[7-8]。从图4中看出,浸泡1 h和浸泡1 d的图中只在低频区出现一个容抗弧,这是由于未封闭的铝合金阳极氧化膜在浸泡过程中,氯化钠溶液中很容易进入多孔层,由于电解液的高导电性导致无法检测到多孔层的信息,只能检测到阻挡层信息[8]。随着浸泡时间的延长,容抗弧不断缩小,说明阳极氧化膜的阻挡层在氯化钠溶液中发生了腐蚀降解。浸泡到3 d时出现一个新的容抗弧,同时氧化膜表面出现点蚀,表明腐蚀介质已经进入到基体与氧化膜之间,造成基体发生腐蚀[25]。氧化膜在浸泡 1 h、1 d,3 d过程中,图4(b)中的容抗弧比图4(a)中的容抗弧大,说明添加己二酸铵的硫酸电解液中制备的氧化膜耐腐蚀性能好,这与图1(b)和(d)中硫酸电解液中添加己二酸铵后制备的氧化膜缺陷更少,多孔层更加致密,腐蚀介质不容易穿透直接相关。
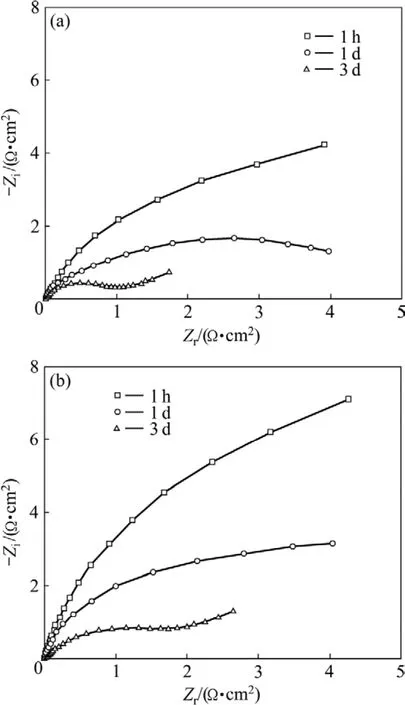
图4 7075-T6铝合金在硫酸和己二酸铵-硫酸电解液中制备的阳极氧化膜在氯化钠溶液中浸泡不同时间测得的电化学阻抗谱图Fig.4 Nyquist plots of anodic films after 7075-T6 aluminium alloy immersed in sulphuric(a) and ammonium adipate/sulphuric media(b) for different times
对于图4中氧化膜浸泡1 h和2 d的阻抗谱,通常采用等效电路图5(a),浸泡3 d后出现Warburg阻抗则采用等效电路图5(b),其中,Re代表电解液电阻,Rs代表多孔层微孔中的溶液电阻,Qpw代表多孔层孔壁的电容,Rb代表阻挡层电阻,Qb代表阻挡层电容,RW代表Warburg阻抗。因为未封闭的阳极氧化膜主要考察阻挡层的信息,所以将Rb和Qb的拟合结果列于表2。
从表2中看出,浸泡1 h后,添加己二酸铵的硫酸电解液制备的阳极氧化膜Rb值(3.007×104Ω·cm2),比不含己二酸铵的硫酸电解液制备的阳极氧化膜 Rb值(1.241×104Ω·cm2)高出一倍以上,表明硫酸电解液中添加己二酸铵后得到的氧化膜阻挡层阻抗值得到提高。浸泡过程中添加己二酸铵的硫酸电解液制备的阳极氧化膜Rb值降低较慢,可能存在两方面原因:一方面由于多孔层微孔孔径较小,减小了阻挡层和氯化钠电解液的接触面积,可以降低腐蚀介质对阻挡层的侵蚀;另一方面,可能氧化膜中残留的己二酸根在潮湿的环境中会与水合氧化铝或腐蚀产物反应,生成(Al—OOC—R)难溶物[26-27],减缓腐蚀的进行。因而添加己二酸铵的硫酸电解液制备的7075-T6铝合金阳极氧化膜的耐腐蚀性能更好。
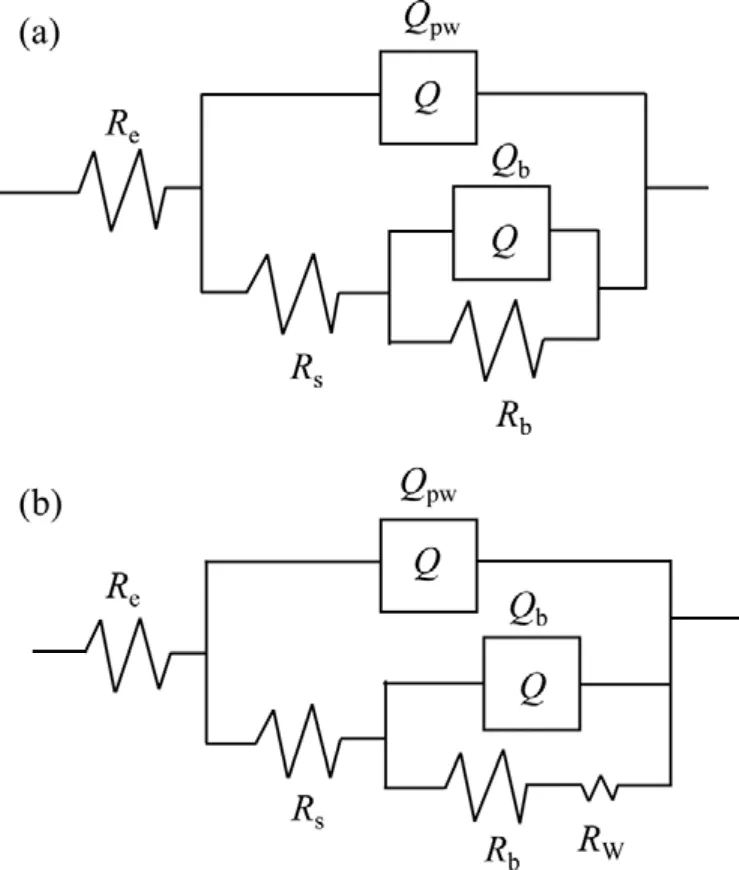
图5 7075-T6铝合金阳极氧化膜在3.5% NaCl溶液中的浸泡1 h、1 d和3 d的等效电路模型Fig.5 Equivalent circuits of anodic films of 7075-T6 aluminium alloy immersed in 3.5% NaCl solution for 1 h and 1 d(a) and 3 d(b)

表2 图3阻抗谱的拟合结果Table2 Fitted results of nyquist plots in Fig.3
表2中看出添加己二酸铵的硫酸电解液制备的阳极氧化膜阻挡层的容抗 Qb从 3.1×10-5Ω-1·cm-2降低为 1.24×10-5Ω-1·cm-2,而 Qb与阻挡层的厚度 Db有以下关系[28]:

式中:S为测试电极面积;εo为真空介电常数;εr为氧化铝介电常数。可见,Qb与 Db呈反比关系,说明添加己二酸铵的硫酸电解液制备的阳极氧化膜Db增大,即阻挡层厚度增加,优化阳极氧化膜的结构,从而表现出较高的耐腐蚀性能。
3 结论
1) 添加己二酸铵的硫酸电解液制备的7075-T6铝合金阳极氧化膜缺陷空穴较少,微孔尺寸较小。说明硫酸电解液中添加己二酸铵有利于减少氧化膜缺陷,降低微孔孔径,提高氧化膜耐腐蚀性能。
2) 纯铝和7075-T6铝合金的线性阳极极化结果表明,硫酸电解液中添加己二酸铵可以降低纯铝氧化电流,降低7075-T6铝合中金合金相颗粒氧化电流,降低合金相颗粒相氧化对氧化膜的不利影响,有利于形成缺陷较少、微孔孔径较小的氧化膜。
3) 电化学测试表明,硫酸电解液中添加己二酸铵后制备的7075-T6铝合金阳极氧化膜的自腐蚀电流密度降低一个数量级,阻挡层阻抗值得到了提高,从3.007×104Ω·cm2提高到 1.241×104Ω·cm2,同时阻挡层厚度也得到了提高,因而具有较好的耐腐蚀性能。
REFERENCES
[1] BIRBILIS N, CAVANAUGH M K, BUCHHEIT R G.Electrochemical behavior and localized corrosion associated with Al7Cu2Fe particles in aluminum alloy 7075-T651[J].Corrosion Science, 2006, 48(12): 4202-4215.
[2] GUILLAUMIN V, MANKOWSKI G. Localized corrosion of 6056 T6 aluminium alloy in chloride media[J]. Corrosion Science, 2000, 42(1): 105-125.
[3] GUILLAUMIN V, MANKOWSKI G. Localized corrosion of 2024 T351 aluminium alloy in chloride media[J]. Corrosion Science, 1999, 41(3): 421-438.
[4] ZHANG Wei-long, FRANKEL G S. Transitions between pitting and intergranular corrosion in AA2024[J]. Electrochimica Acta,2003, 48(9): 1193-1210.
[5] EARL G. Chromium[J]. Metal Finishing, 1997, 95(3): 59-61.
[6] MOUTARLIER V, GIGANDET M P, PAGETTI J, RICQ L.Molybdate/sulfuric acid anodizing of 2024-aluminium alloy:Influence of inhibitor concentration on film growth and on corrosion resistance[J]. Surface and Coatings Technology, 2003,173(1): 87-95.
[7] MOUTARLIER V, GIGANDET M P, PAGETTI J, LINGET S.Influence of molybdate species added to sulphuric acid on composition and morphology of the anodic layers formed on 2024 aluminium alloy[J]. Thin Solid Films, 2005, 483(1/2):197-204.
[8] MOUTARLIER V, GIGANDET M P, NORMAND B,PAGETTI J. EIS characterisation of anodic films formed on 2024 aluminium alloy in sulphuric acid containing molybdate or permanganate species[J]. Corrosion Science, 2005, 47(4):937-951.
[9] 刘 怡, 刘凤霞. 工业纯铝硬质阳极氧化的工艺研究[J]. 表面技术, 2006, 35(6): 35-37.LIU Yi, LIU Feng-xia. Technological study on hard anode oxidation of industrial pure aluminum[J]. Surface Technology,2006, 35(6): 35-37.
[10] CURIONI M, SKELDON P, KOROLEVA E, THOMPSON G E,FERGUSON J. Role of tartaric acid on the anodizing and corrosion behavior of AA 2024 T3 aluminum alloy[J]. Journal of The Electrochemical Society, 2009, 156(4): C147-C153.
[11] WONG Chun-ming, MOJI Y. Method for anodizing aluminum:United States Patent, 4894127[P]. 1990-01-06.
[12] ONO S, WADA C, ASOH H. Structure and property of anodic barrier films formed on aluminum in low voltage range[J].Electrochimica Acta, 2005, 50(25/26): 5103-5110.
[13] 李永星, 于 美, 刘建华, 李松梅, 陈高红. 电压加载下己二酸铵对2024-T3铝合金阳极氧化膜的封闭研究[J]. 航空学报,2011, 32(7): 1326-1335.LI Yong-xing, YU Mei, LIU Jian-hua, LI Song-mei, CHEN Gao-hong. Sealing of ammonium adipate on anodic film of aluminium alloy 2024-T3 under voltage loading[J]. Acta Aeronautica et Astronautica Sinica, 2011, 32(7): 1326-1335.
[14] ZHOU X, THOMPSON G E, SKELDON P, WOOD G C,SHIMIZU K, HABAZAKI H. Anodic oxidation of an Al-2wt%Cu alloy: Effect of grain orientation[J]. Corrosion Science, 1999,41(6): 1089-1094.
[15] 刘建华, 李 明, 李松梅, 詹中伟. 挤压成型对 LC4CS铝合金棒材阳极氧化膜结构的影响[J]. 航空学报, 2009, 30(2):368-370.LIU Jian-hua, LI Ming, LI Song-mei, ZHAN Zhong-wei. Effect of extrusion on microstructure of anodic oxide films formed on LC4CS aluminium alloy bars[J]. Acta Aeronautica et Astronautica Sinica, 2009, 30(2): 368-370.
[16] LIU Jian-hua, LI Ming, LI Song-mei, HUANG Min. Effect of microstructure of anodic oxide formation in sulfuric acid[J].International Journal of Minerals, Metallurgy and Materials,2009, 16(4): 432-438.
[17] SAENZ DE MIERA M, CURIONI M, SKELDON P,THOMPSON G E. Modelling the anodizing behaviour of aluminium alloys in sulphuric acid through alloy analogues[J].Corrosion Science, 2008, 50(12): 3410-3415.
[18] SAENZ DE MIERA M, CURIONI M, SKELDON P,THOMPSON G E. The behaviour of second phase particles during anodizing of aluminium alloys[J]. Corrosion Science,2010, 52(7): 2489-2497.
[19] CURIONI M, SAENZ DE MIERA M, SKELDON P,THOMPSON G E, FERGUSON J. Macroscopic and local filming behavior of AA2024 T3 aluminum alloy during anodizing in sulfuric acid electrolyte[J]. Journal of the Electrochemical Society, 2008, 155(8): C387-C395.
[20] CURIONI M, SKELDON P, THOMPSON G E. Anodizing of aluminum under nonsteady conditions[J]. Journal of the Electrochemical Society, 2009, 156(12): C407-C413.
[21] HOUSER J E, HEBERT K R. Modeling the potential distribution in porous anodic alumina films during steady-state growth[J]. Journal of the Electrochemical Society, 2006, 153(12):B566-B573.
[22] GRÉGORY B, NADINE P, CATHERINE D, MARTINE V,STEPHANE S. FESEM and EIS study of sealed AA2024 T3 anodized in sulfuric acid electrolytes: Influence of tartaric acid[J].Journal of the Electrochemical Society, 2008, 155(11):C521-C529.
[23] GARCIA-VERGARA S J, EL KHAZMI K, SKELDON P,THOMPSON G E. Influence of copper on the morphology of porous anodic alumina[J]. Corrosion Science, 2006, 48(10):2937-2946.
[24] IGLESIAS-RUBIANES L, GARCIA-VERGARA S J,SKELDON P, THOMPSON G E, FERGUSON J, BENEKE M.Cyclic oxidation processes during anodizing of Al-Cu alloys[J].Electrochimica Acta, 2007, 52(24): 7148-7157.
[25] LEI Wen, WANG Ya-ming, ZHOU Yu, OUYANG Jia-hu, GUO Li-xin, JIA De-chang. Corrosion evaluation of microarc oxidation coatings formed on 2024aluminium alloy[J]. Corrosion Science, 2010, 52(8): 2687-2696.
[26] KEVIN D, DOBSON, JAMES MC QUILLAN A. In situ infrared spectroscopic analysis of the adsorption of aliphatic carboxylic acids to TiO2, ZrO2, Al2O3and Ta2O5from aqueous solutions[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 1999, 55(7/8): 1395-1405.
[27] LANDRY C C, PAPPÉ N, MASON M R, APBLETT A W,TYLER A N, MACINNES A N, BARRON A R. From minerals to materials: Synthesis of alumoxanes from the reaction of boehmite with carboxylic acids[J]. Journal of Materials Chemistry, 1995, 5(2): 331-338.
[28] SUAY J J, GIMENEZ E, RODRIGUEZ T, HABBIB K, SAURA J J. Characterization of anodized and sealed aluminium by EIS[J].Corrosion Science, 2003, 45(3): 611-624.
Effects of ammonium adipate on sulphuric acid anodizing of 7075-T6 aluminum alloy
LIU Jian-hua1, LI Yong-xing1, YU Mei1, LI Song-mei1, SUN Yu-jing2
(1. Key Laboratory of Aerospace Materials and Performance, Ministry of Education, School of Materials Science and Engineering, Beihang University, Beijing 100191, China;2. State Intellectual Property Office of Patent Examination Collaborating Centre, Beijing 100088, China)
The effect of ammonium adipate on the sulphuric acid anodizing of 7075-T6 aluminum alloy was studied. The surface morphologies of anodic oxide films formed in the sulphuric acid solutions with and without ammonium adipate were studied by using field emission scanning electron microscopy (FE-SEM). The anodizing behavior of 7075-T6 aluminum alloy was investigated under linear polarization conditions in sulphuric acid anodizing solutions with and without of ammonium adipate. The potentiodynamic polarization and electrochemical impedance spectroscopy (EIS)were used to study the corrosion resistance of the anodic oxide films formed in the presence and absence of ammonium adipate. The results show that the ammonium adipate in sulfuric acid solution can reduce the cavity defects of the films,decrease the pores diameter, reduce the corrosion current density, enhance the thickness of the barrier layer and improve the corrosion resistance of anodic oxide films by decreasing the current density.
7075-T6 aluminum alloy; ammonium adipate; anodizing; electrochemical impedance spectrascopy
TG174.42
A
1004-0609(2012)01-0324-07
2011-11-30;
2011-03-08
刘建华,教授,博士;电话:010-82317103;E-mail: liujh@buaa.edu.cn
(编辑 李艳红)
