砷锑价态对铜电解液中砷锑铋脱除率的影响
2012-07-31郑雅杰周文科彭映林马玉天
郑雅杰,周文科,彭映林,马玉天
(1. 中南大学 冶金科学与工程学院,湖南 长沙,410083;2. 金川集团有限公司 精炼厂,甘肃 金昌,737100)
铜电解精炼过程中,阳极铜中的As,Sb和Bi杂质,以一定分配比进入铜电解液并逐渐积累。它们不仅会在阴极上沉积,而且会形成漂浮阳极泥,影响阴极铜质量。因此,As,Sb和Bi杂质的脱除是铜电解液净化的主要目标。生产中多采用电积法[1]脱除As,Sb和Bi等杂质,但电积法能耗高,产生黑铜渣,并有剧毒 AsH3气体放出[2-3]。萃取法[4]、离子交换法[5]和共沉淀法等[6-7]也用于铜电解液净化,但因其处理成本高,效果单一,只能作为铜电解液净化的辅助工艺。研究表明:As,Sb和Bi在铜电解液中主要以H3AsO4,HAsO2,AsO+,HSb(OH)6,SbO+和 Bi3+等形式存在。本文作者在研究 As(Ⅲ)净化铜电解液基础上[8-10],利用 SO2还原铜电解液,并调整电解液中 As(Ⅴ)与As(T),Sb(Ⅴ)与 Sb(T)的物质的量的比,蒸发浓缩使电解液中As,Sb和Bi杂质生成相应大分子沉淀,可实现电解液中As,Sb和Bi杂质的良好脱除[11]。
1 实验
1.1 实验步骤
取 500 mL铜电解液(国内某冶炼厂提供)于三颈瓶中,化学组成如表 1所示。根据实验需要,加入As2O5(AR)和Sb2O3(AR),加热搅拌溶解后, 通入SO2还原,然后加入 As2O5(AR)以及采用 Sb2O5与硫酸反应制得的 HSb(OH)6溶液调整电解液中 As(Ⅴ)与As(T),Sb(Ⅴ)与 Sb(T)的物质的量的比,加热浓缩电解液至一定体积后,冷却至10 ℃下结晶,过滤,并对滤液及结晶产物进行分析。其工艺流程如图1所示。
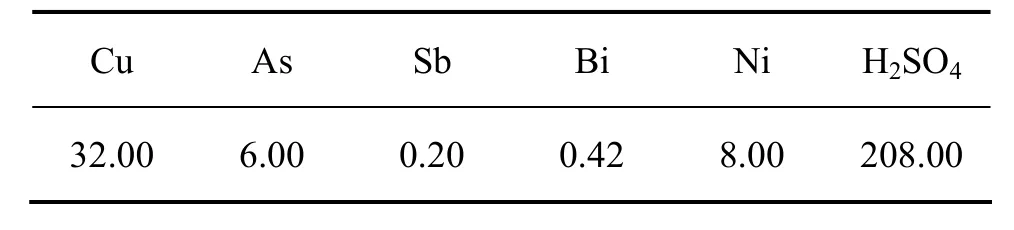
表1 铜电解液化学组成(质量浓度)Table 1 Compositions of copper electrolyte g/L
1.2 分析与检测
实验采用硫酸铈-溴酸钾滴定法分析 As(Ⅲ)和Sb(Ⅲ)的质量浓度,电感耦合等离子光谱仪(Intrepid II XSP)分析Cu,As,Sb和Bi的质量浓度。用X线衍射仪(XRD)(日本理学,Cu Kα,50 kV,300 Ma)分析结晶产物物相,用X荧光分析(XRF)仪(菲利浦24)分析结晶产物成分。
铜电解液中Cu,As,Sb和Bi的脱除率(r)按如下式计算:
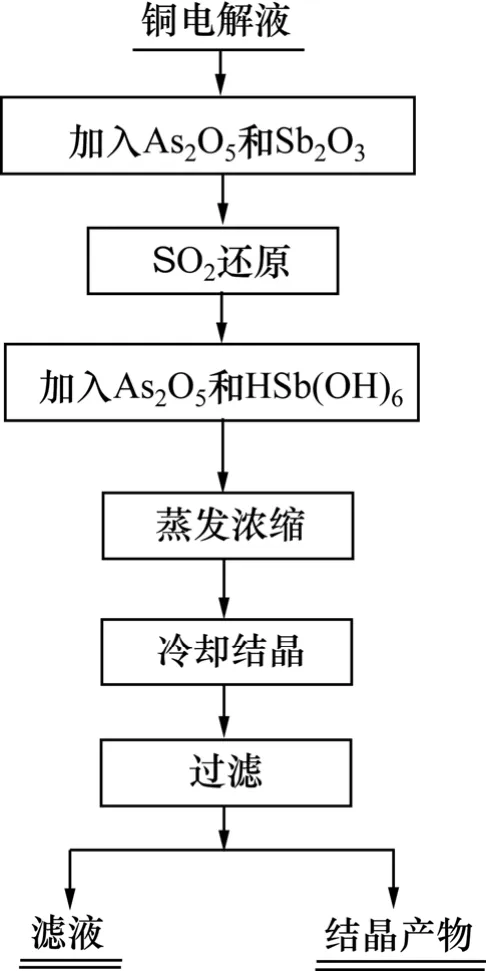
图1 铜电解液净化工艺流程图Fig.1 Process of copper electrolyte purification
式中:0ρ为电解液中Cu,As,Sb和Bi的质量浓度,g/L;1ρ为电解液浓缩结晶后Cu,As,Sb和Bi的质量浓度,g/L;V0为电解液体积,L;V1为电解液浓缩结晶后体积,L。
2 结果与讨论
2.1 浓缩体积比对铜电解液中As,Sb和Bi杂质脱除率的影响
实验取铜电解液500 mL,化学组成如表1所示,加入 Sb2O3调整电解液中 Sb(T)的质量浓度为 0.75 g/L,通入SO2还原,反应温度为25 ℃,反应时间为2 h,电解液中 n(Sb(Ⅲ))/n(Sb(T))和 n(As(Ⅲ))/n(As(T))分别为0.95。加热蒸发铜电解液至一定体积,浓缩体积比对铜电解液中As,Sb和Bi脱除率的影响如图2所示,浓缩体积比为蒸发浓缩前电解液体积与浓缩后电解液体积比。
由图2可知:铜电解液中As,Sb和Bi杂质脱除率随浓缩体积比增加而增加。当浓缩体积比从1.0增加至3.3时,As,Sb和Bi的脱除率分别从0增加至77%,26%和87%。当浓缩体积比为2.5时,电解液中As,Sb和Bi的脱除率分别为75%,20%和78%。
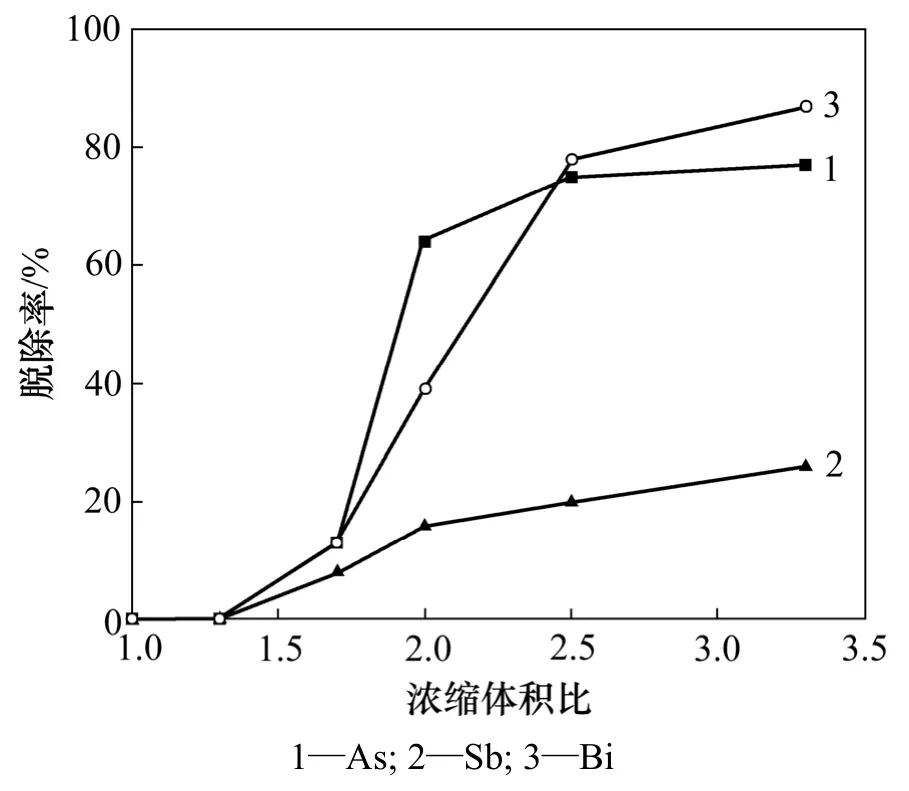
图2 浓缩体积比对铜电解液中As,Sb和Bi脱除率的影响Fig.2 Influence of ratio of initial volume to final volume on removal rates of As, Sb and Bi in copper electrolyte

表2 浓缩体积比对铜电解液中H2SO4质量浓度和Cu脱除率的影响Table 2 Influence of ratio of initial volume to final volume on concentration of H2SO4 and removal rate of Cu in copper electrolyte
由表2可知:当浓缩体积比从1.0增加至3.3时,H2SO4的质量浓度从208 g/L增加至645 g/L,Cu的脱除率从0增加到88%。当浓缩体积比为3.3时,结晶产物黏度增大,其中 H2SO4和Ni的含量增加[12]。因此,适宜的浓缩体积比为2.5。
电解液经 SO2还原后,As(Ⅴ)还原成As(Ⅲ),As(Ⅲ)在酸性溶液中的溶解度远低于As(Ⅴ)[13],且随H2SO4质量浓度增加而降低[14]。电解液蒸发浓缩过程中,硫酸质量浓度的增加及 CuSO4·5H2O晶体的形成,有利于HAsO2脱水生成 As2O3,使As得以脱除。其反应如下所示:
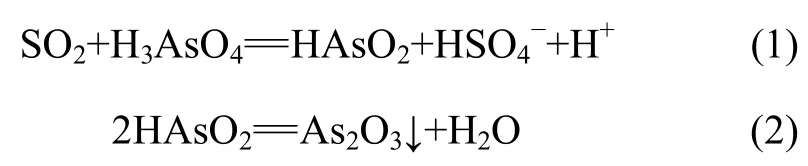
As2O3结晶过程,晶核的形成是控制步骤,CuSO4·5H2O 等结晶物的形成能显著降低 As2O3的晶核形成能,促使As2O3结晶析出。在SO2还原作用下,Bi3+生成 BiO 和(Bi2O3)4·3SO3[15],在由于浓缩过程中CuSO4·5H2O及As2O3的吸附及共沉淀作用,使得电解液中以各种形态存在的Sb和Bi杂质得以脱除。
2.2 As(T)质量浓度对铜电解液中As,Sb和Bi杂质脱除率的影响
上述其他实验条件不变,加入As2O5调节电解液中 As(T)的质量浓度,通入 SO2充分还原,n(As(Ⅲ))/n(As(T))为0.95,浓缩体积比为2.5时,电解液中As(T)的质量浓度对As,Sb和Bi脱除率的影响如图3所示。
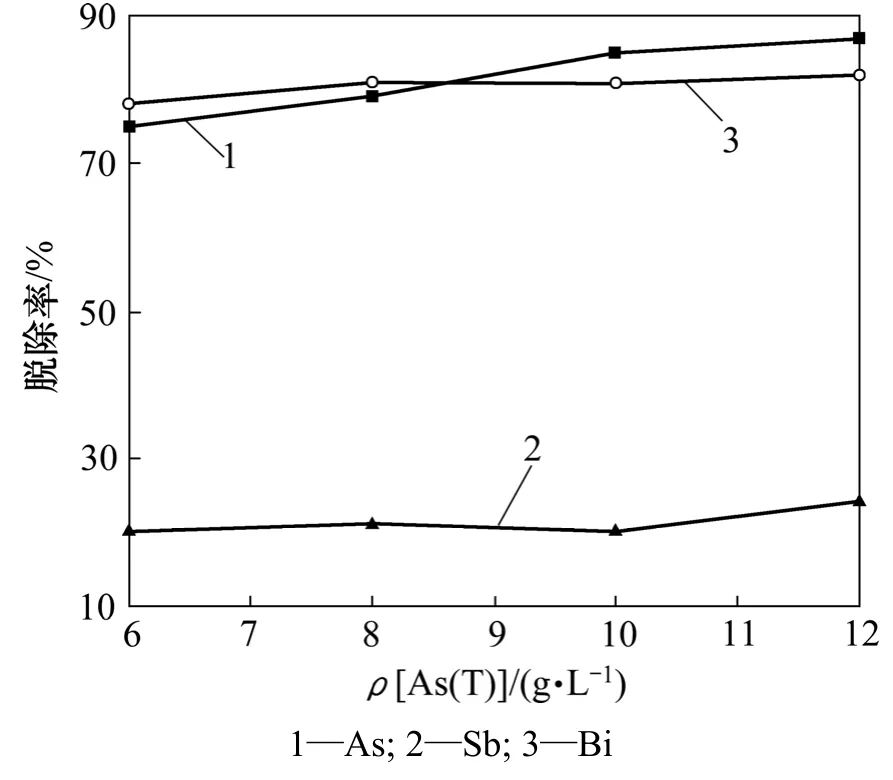
图3 As(T)的质量浓度对铜电解液中As,Sb和Bi脱除率的影响Fig.3 Influence of As(T) concentration on removal rates of As, Sb and Bi in copper electrolyte
由图3可知:As脱除率随铜电解液中As(T)质量浓度的增加而增加,当总砷质量浓度达到10 g/L时,As脱除率达到85%。As(T)质量浓度对电解液中Sb和Bi的脱除率影响不大。
在一定温度和硫酸质量浓度条件下,As(Ⅲ)在电解液中溶解度一定。As(Ⅲ)含量升高,As脱除率升高。
2.3 n(As(Ⅴ))/ n(As(T))对铜电解液中 As,Sb和 Bi杂质脱除率的影响
上述其他条件不变,电解液浓缩体积比为2.5,当电解液中 As(T)质量浓度为 10 g/L时,n(As(Ⅴ))/n(As(T))对电解液中As,Sb和Bi脱除率的影响如图4所示。
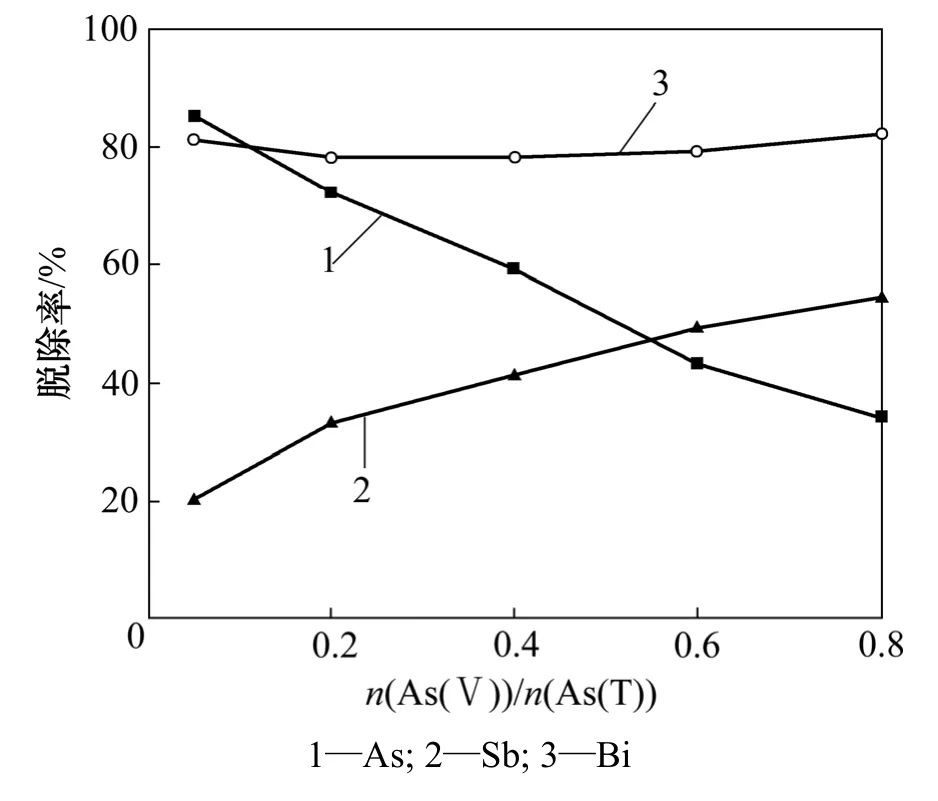
图4 n(As(Ⅴ))/n(As(T))对铜电解液中As,Sb和Bi脱除率的影响Fig.4 Influence of n(As(Ⅴ))/n(As(T)) on removal rates of As,Sb and Bi in copper electrolyte
由图4可知:As脱除率随n(As(Ⅴ))/n(As(T))升高而降低,Sb脱除率随n(As(Ⅴ))/n(As(T))升高而升高。当电解液中n(As(Ⅴ))/n(As(T))从0.05升高至0.8时,As的脱除率由85%降低至34%,Sb的脱除率由20%升高至54%,Bi脱除率均达到80%。
电解液中As(Ⅲ)减少,产生的As2O3结晶减少,As脱除率降低。而在As(T)质量浓度不变的情况下,As(Ⅲ)含量减少,As(Ⅴ)含量增多,电解液中 As(Ⅴ)增多促使SbO+与AsO43-反应[16],使Sb脱除率升高,相关反应如下:
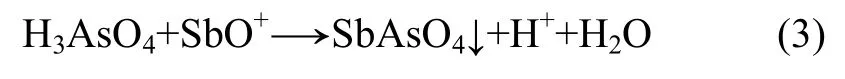
综合考虑电解液中As,Sb和Bi脱除情况,适宜的 n(As(Ⅴ))/n(As(T))为 0.4。
2.4 n(Sb(Ⅴ))/n(Sb(T))对铜电解液中 As,Sb和 Bi杂质脱除率的影响
以上其他条件不变,保持铜电解液中 n(As(Ⅴ))/n(As(T))为 0.4,n(Sb(Ⅴ))/n(Sb(T))对电解液中 As,Sb和Bi脱除率的影响如图5所示。
由图 5可知:As脱除率不随 n(Sb(Ⅴ))/n(Sb(T))变化,Sb脱除率随电解液中n(Sb(Ⅴ))/n(Sb(T))增大而增大。当n(Sb(Ⅴ))/n(Sb(T))从0增加到0.6时,Sb脱除率从 41%增加至 70%,n(Sb(Ⅴ))/n(Sb(T))达到 0.2时,Bi脱除率达到90%以上。
电解液中 Sb和 Bi脱除率升高,主要是因为As(Ⅲ),As(Ⅴ),Sb(Ⅲ),Sb(Ⅴ)和 Bi(Ⅲ)相互作用生成了锑酸盐、砷锑酸盐及亚砷锑酸锑等大分子沉淀物质。浓缩过程中,CuSO4·5H2O和As2O3结晶的形成会促使这些物质吸附共沉淀,有利于As,Sb和Bi杂质的脱除。其反应机理为[17-18]:
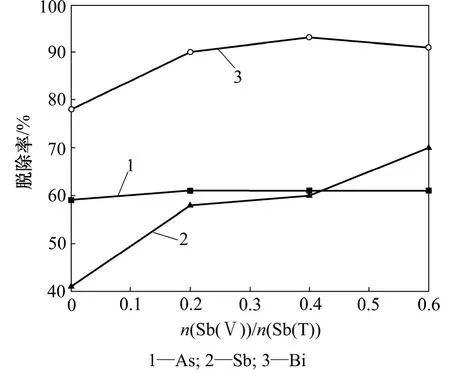
图5 n(Sb(Ⅴ))/n(Sb(T))对铜电解液中As,Sb和Bi脱除率的影响Fig.5 Influence of n(Sb(Ⅴ))/n(Sb(T)) on removal rates of As,Sb and Bi in copper electrolyte
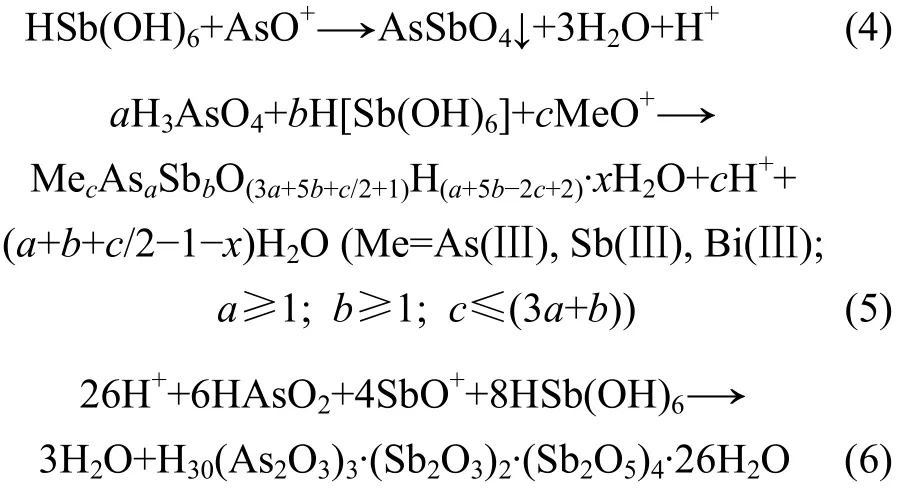
综合考虑电解液中As,Sb和Bi的脱除情况,调节铜电解液中n(As(Ⅴ))/n(As(T))和n(Sb(Ⅴ))/n(Sb(T))分别为0.4,浓缩结晶,已经能够有效地脱除电解液中As,Sb和Bi等杂质。
根据上述实验结果,取3 L铜电解液进行实验室放大实验,加入 As2O5和 Sb2O3,加热搅拌溶解后,通入 SO2还原,然后加入 As2O5及 HSb(OH)6溶液调整铜电解液中n(As(Ⅴ))/n(As(T))和n(Sb(Ⅴ))/n(Sb(T))分别为0.4,蒸发浓缩,控制浓缩体积比为2.5,冷却至10 ℃结晶,过滤后用少量去离子水清洗杯壁,得到滤液为1.2 L。电解液净化前后化学成分如表3所示,放大实验产物XRD结果如图6所示,结晶产物XRF分析结果如表4所示。
由表3实验结果计算可知:铜电解液中As和Sb价态调整后,蒸发浓缩结晶,其中Cu,As,Sb和Bi脱除率可分别达到82%,62%,55%和85%。
表3 铜电解液净化前后的化学组成Table 3 Compositions of copper electrolyte before and after purification g/L
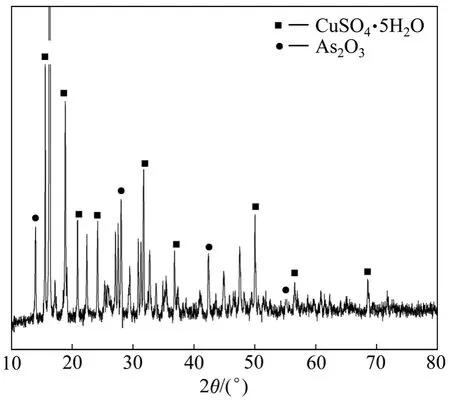
图6 结晶产物的XRD谱Fig.6 XRD pattern of crystal product
表4 结晶产物的化学成分(质量分数)Table 4 Compositions of crystal product %
由图 6可知:还原后蒸发浓缩结晶产物中含有CuSO4·5H2O 和 As2O3。
由表4可知:还原后蒸发浓缩结晶产物成分含Cu为29%,As为5%,Sb为0.37%,Bi为0.2%。
3 结论
(1) 采用 SO2还原铜电解液,经蒸发浓缩,冷却结晶,铜电解液中As,Sb和Bi脱除率随浓缩体积比增加而增加;浓缩体积比一定时,As脱除率随铜电解液中As(T)质量浓度增加而增加,总砷质量浓度对Sb和Bi脱除率影响不大。
(2) 当铜电解液中As(T),Sb(T)质量浓度一定时,调节电解液中 n(As(Ⅴ))/n(As(T))和 n(Sb(Ⅴ))/n(Sb(T)),As脱除率随n(As(Ⅴ))/n(As(T))增加而降低,Sb脱除率随n(As(Ⅴ))/n(As(T))增加而增加;n(As(Ⅴ))/n(As(T))一定时,Sb脱除率随 n(Sb(Ⅴ))/n(Sb(T))增加而降低;适宜的n(As(Ⅴ))/n(As(T))和n(Sb(Ⅴ))/n(Sb(T))分别为0.4。
(3) 当铜电解液体积为3 L,H2SO4的质量浓度为208 g/L,Cu的质量浓度为32 g/L,总As的质量浓度为9.36 g/L,总Sb的质量浓度为0.65 g/L,Bi的质量浓度 0.21 g/L,电解液中 n(As(Ⅴ))/n(As(T))和n(Sb(Ⅴ))/n(Sb(T))分别为0.4时,蒸发浓缩使浓缩体积比为2.5,然后冷却至10 ℃结晶、过滤,Cu,As,Sb和Bi脱除率分别达到82%,62%,55%和85%。
(4) 蒸发浓缩结晶产物为CuSO4·5H2O和As2O3,结晶产物中Cu为29%,As为5%,Sb为0.37%,Bi为0.2%。
[1] Panda B, Das S C. Electrowinning of copper from sulfate electrolyte in presence of sulfurous acid[J]. Hydrometallurgy,2001, 59(1): 55-67.
[2] 仇勇海, 陈白珍, 梅显芝, 等. 控制阴极电势电积法新工艺及其应用[J]. 中南工业大学学报: 自然科学版, 1999, 30(5):501-504.QIU Yong-hai, CHEN Bai-zhen, MEI Xian-zhi, et al. Study and application of new technology of controlling cathodic potential electrowinning[J]. Journal of Central South University of Technology: Natural Science, 1999, 30(5): 501-504.
[3] 仇勇海, 唐仁衡, 陈白珍. 砷化氢析出电势探讨[J]. 中国有色金属学报, 2002, 10(1): 101-104.QIU Yon-hai, TANG Ren-heng, CHEN Bai-zhen. Evolution potential of arsine[J]. The Chinese Journal of Nonferrous Metals,2002, 10(1): 101-104.
[4] Iberhan L, Wiśniewski M. Extraction of arsenic(Ⅲ ) and arsenic(Ⅴ) with Cyanex 925, Cyanex 301 and their mixtures[J].Hydrometallurgy, 2002, 63(1): 23-30.
[5] Raghavan R, Bhatt C V. Comparative study of certain ion-exchange resins for application in copper-bearing process solutions[J]. Hydrometallurgy, 1998, 50(2): 169-183.
[6] 王学文, 肖炳瑞, 张帆. 铜电解液碳酸钡脱铋新工艺[J]. 中国有色金属学报, 2006, 16(7): 1295-1299.WANG Xue-wen, XIAO Bing-rui, ZHANG Fan. New process of bismuth removal from copper electrolyte with barium carbonate[J]. The Chinese Journal of Nonferrous Metals, 2006,16(7): 1295-1299.
[7] Navarro P, Alguacil F J. Adsorption of antimony and arsenic from a copper electrorefining solution onto activated carbon[J].Hydrometallurgy, 2002, 66(1/2/3): 101-105.
[8] XIAO Fa-xin, ZHENG Ya-jie, WANG Yong, et al. Purification mechanism of copper electrolyte by As(Ⅲ)[J]. Transaction of Nonferrous Metals Society of China, 2008, 18(5): 1275-1279.
[9] XIAO Fa-xin, ZHENG Ya-jie, WANG Yong, et al. Novel technology of purification of copper electrolyte[J]. Transaction of Nonferrous Metals Society of China, 2007, 17(5): 1069-1074.
[10] 郑雅杰, 赵攀峰, 王勇, 等. 高电流密度电解对阴极铜质量的影响[J]. 中南大学学报: 自然科学版, 2009, 40(2): 311-316.ZHENG Ya-jie, ZHAO Pan-feng, WANG Yong, et al. Effect of electrorefining with high current density on cathode copper[J].Journal of Central South University: Science and Technology,2009, 40(2): 311-316.
[11] 郑雅杰, 彭映林, 周文科. 价态调控净化铜电解液的方法: CN,102181882A[P]. 2011-04-09.ZHENG Ya-jie, PENG Ying-lin, ZHOU Wen-ke. Method of purifying copper electrolyte by valence state-controllable means:CN, 102181882A[P]. 2011-04-09.
[12] 朱祖泽, 贺家齐. 现代铜冶金学[M]. 北京: 科学出版社, 2003:500-506.ZHU Zu-ze, HE Jia-qi. Modern metallurgy of copper[M].Beijing: Science Press, 2003: 500-506.
[13] 迪安 J A. 兰氏化学手册[M]. 北京: 科学出版社, 1991:300-544.Dean J A. Lange’s handbook of chemistry[M]. Beijing: Science Press, 1991: 300-544.
[14] 郑雅杰, 罗园, 王勇. 采用含砷废水沉淀还原法制备三氧化二砷[J]. 中南大学学报: 自然科学版, 2009, 40(1): 48-54.ZHENG Ya-jie, LUO Yuan, WANG Yong. Arsenic trioxide made by precipitation-reduction method from As-containing waste water[J]. Journal of Central South University: Science and Technology, 2009, 40(1): 48-54.
[15] 张传福, 谭鹏夫. 第VA族元素物理化学数据手册[M]. 长沙:中南大学出版社, 1995: 151-151.ZHANG Chuan-fu, TAN Peng-fu. Physical chemistry data manual of the VA group element[M]. Changsha: Central South University Press, 1995: 151-151.
[16] 文燕, 张源, 张胜树. 铜电解过程中杂质分配的控制[C]//全国铜镍钴生产技术、装备、材料及市场研讨会. 北京: 中国有色金属学会, 2003: 93-97.WEN Yan, ZHANG Yuan, ZHANG Sheng-shu. Control of impurities in copper electrolysis[C]//Proceedings of Symposium of Production Technology, Equipment, Material and Market of Copper, Nickel and Cobalt in China. Beijing: Chinese Nonferrous Metal Society, 2003: 93-97.
[17] ZHENG Ya-jie, XIAO Fa-xin, WANG Yong, et al. Industrial experiment of copper electrolyte purification by copper arsenite[J]. Journal of Central South University: Science and Technology, 2008, 15(2): 204-208.
[18] WANG Xue-wen, CHEN Qi-yuan, YIN Zhou-lan, et al.Identification of arsenato antimonates in copper anode slimes[J].Hydrometallurgy, 2006, 84(3/4): 211-217.
