大米中砷和硒同时测定的方法研究
2012-11-23邓源喜汪张贵柯春林
邓源喜 许 晖 汪张贵 柯春林 马 龙 李 妍
大米中砷和硒同时测定的方法研究
邓源喜 许 晖 汪张贵 柯春林 马 龙 李 妍
(安徽蚌埠学院生物与食品工程系,蚌埠 233030)
应用氢化物发生-原子荧光光谱法对大米样品中砷、硒2种元素同时进行测定,研究仪器条件,主要包括负高压、灯电流、载气流量、屏蔽气流量等对测定结果的影响,在0~10μg/L范围内砷(As)、硒(Se)的浓度与荧光强度呈线性关系,相关系数为0.999 6和0.999 8,加标回收率分别为96.2%~100.8%和98.1%~107.6%,RSD分别≤7.4%和≤5.5%,并同单独对样品中砷、硒测定进行比较,验证方法的可行性。
砷 硒 原子荧光法
目前,食品中砷(As)和硒(Se)元素含量测定的方法主要有比色法、分光光度法、原子吸收光谱法、原子发射光谱法、质谱法、毛细管电泳法及原子荧光光谱法[1-9]。各种测定方法根据本身性质及仪器检出限度又各不相同。其中氢化物原子荧光光谱法是发展于20世纪60年代的原子荧光法分析技术,具有谱线简单、灵敏度高、检测限低和多元素分析的优点,因此,它成为实验室常用的元素测定方法。近几年,应用原子荧光光谱法测定食品中砷和硒已有报道[7]。但对于砷和硒检测一般都是分别消化样品,分别测定,检测比较烦琐、费时、费力。为节约成本、提高检测效率、适应食品快速检测的需要,本试验研究了大米中砷、硒元素测定仪器的各个参数并优化了反应条件,初步建立了湿法一次性消化样品,双通道原子荧光同时检测大米中砷和硒元素含量的方法。
1 材料与方法
1.1 仪器与试剂
1.1.1 仪器
AFS-930双道原子荧光光度计:北京海光仪器有限公司;砷(As)空心阴极灯、硒(Se)空心阴极灯:北京有色金属研究总院;FA1604电天平:上海天平仪器厂。
1.1.2 试剂
As标准贮备液(GBW(E)080117)、Se标准贮备液(GBW(E)080215)(国家标物中心):100μg/mL;As、Se混合标准中间液:1μg/mL;As、Se混合标准工作液:0.01μg/mL。
HNO3、HClO4、HCl(优级纯):国药集团化学试剂有限公司;混合酸(HNO3∶HClO4=4∶1)(优级纯);硼氢化钠、氢氧化钠、硫脲、抗坏血酸、质量分数为5%HC1溶液;5%硫脲+5%抗坏血酸混合液,临用前现配;质量分数为2%硼氢化钠溶液。试剂中除特殊规定外,所有试剂为分析纯,试验用水为蒸馏水或同等纯度水。
1.2 试验方法
1.2.1 样品前处理
将样品搅匀(固体样品则需要磨碎混匀后备用),直接在已称重的100 mL三角瓶中称取样品0.5~2.0 g,分别加入10.0 mL混合酸及3粒玻璃珠,盖上表面皿,放置过夜。次日,将放有样品的上述三角瓶置于电热板上缓慢升温、消煮,待有机质消解,试样变为清亮无色并产生白色浓烟时,再继续加热至剩余体积2 mL左右,切不可蒸干。冷却,再加6 mol/L的盐酸5 mL,重复上述消解加热操作以完全将六价硒还原为四价硒。冷却,转移定容至100 mL容量瓶中。同时做空白试验。吸取10 mL试样消化液于15 mL离心管中,加浓盐酸2.5 mL,5%硫脲+5%抗坏血酸混合液2.5 mL,混匀放置1 h后待测[7]。
1.2.2 样品测定[1,7]
调整仪器的光源及各种测试条件后,输入试样编号、试样质量、稀释体积及测定结果浓度单位等相关参数,启动点火键,预热20 min左右后对As、Se混合标准工作液进行测定,并自动绘制标准曲线。接着转入试样空白测定和试样的依次测定。仪器测量条件如表1所示。

表1 砷和硒的仪器测量条件
1.2.3 试样测定数据处理[1]
取5份不同厂家的大米样品(消化前先将样品干燥粉碎过筛),按照1.2.2的步骤要求测得试样中的砷和硒含量。试样测定数据采用公式进行换算:
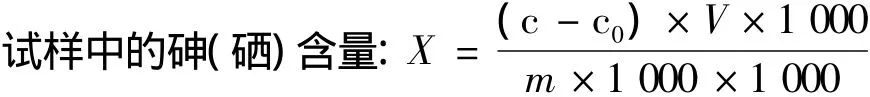
式中:X为试样中砷(硒)的含量/mg/kg;c、c0分别为试样和试样空白消化液的测定浓度/ng/mL(即μg/L);V为试样消化液定容体积/mL(本次测定中V为100.00 mL);m为试样质量/g。
2 结果与讨论
2.1 样品预处理(消化体系)的选择
对比试验了HNO3,HNO3/H2SO4,HNO3/HClO4和HNO3/H2SO4/HClO4溶液消解样品的结果,发现HNO3/HClO4消化体系消解效果好,测定干扰小,结果重现性好。以同一个米样为试验对象,试验了不同配比的HNO3/HClO4消解样品的效果,每一种配比各称5个样,测定米样中砷含量,结果如表2所示,4∶1的HNO3/HClO4消化效果和精密度都较好。试验选用HNO3/HClO4(4∶1)消解样品。
消化过程中加入的硫酸是强氧化剂,由于沸点高,很难驱除,能保持消化液中一定的酸度,但它的强氧化性与抗坏血酸、硫脲还原剂反应而影响五价砷的还原,从而影响砷元素的测定,可能会造成测定结果偏低。盐酸是非氧化性酸,在溶解过程中它表现出弱的还原性。测定过程中加入一定量的盐酸,增加了氢化物发生反应过程中的还原作用,从而提高了荧光强度,使结果准确性得到提高[10]。
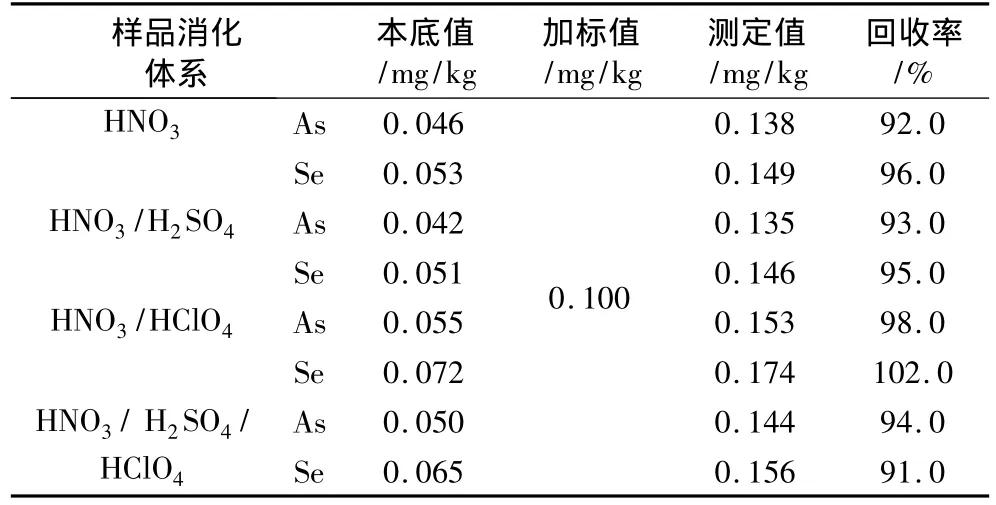
表2 不同消化体系的加标回收率比较
2.2 仪器工作条件的确定
2.2.1 灯电流的确定
灯电流的大小,代表了激发光源的强弱。灯电流大,激发强度大,灵敏度则高。但灯电流过大会缩短灯的寿命,信号水平及噪声同时提高,有时还会造成工作曲线的弯曲。当满足要求时,宜选用较低的灯电流[11]。由试验结果可知(图1),选择砷、硒灯电流为60~80 mA,可以得到较好的线性关系,荧光强度相对稳定,灵敏度高。

图1 灯电流对10μg/L As和Se荧光强度的影响
2.2.2 负高压的选择
尽管光电倍增管负高压增加时,仪器的灵敏度也增大,但过高的负高压会产生较大的噪音,即信号及噪声水平同时提高。当满足要求时,宜选用较低的光电倍增管负高压[11]。由图2试验结果可知,280~300 V负高压可得到较好的线性关系,荧光强度相对稳定,灵敏度高,能够满足分析要求。

图2 负高压对10μg/L As和Se荧光强度的影响
2.2.3 载气、屏蔽气流量的确定
硼氢化钾反应产生的新生态氢与样品反应后生成的硒化氢是由载气运送至原子化器的,载气流量与荧光强度有一定的关系,而屏蔽气可以防止周围大气的渗入,以保证测定时荧光值的稳定。但过低的载气量难以迅速将氢化物带入石英炉,过高的载气量又会冲稀原子的浓度[12]。由图3、图4可知,载气流量在400~500 mL/min、屏蔽气流量在800~900 mL/min时,荧光强度处于较高的稳定平台。测定中选择载气流量为400 mL/min,屏蔽气流量为800 mL/min可以得到稳定的荧光值,即能达到分析要求。

2.2.4 还原剂浓度的选择
试验表明,Se(Ⅵ)必须在盐酸体系中被还原为Se(Ⅳ),才能与硼氢化钠反应,形成SeH4,As(Ⅴ)和As(Ⅲ)均与硼氢化钠反应,但反应速度不同,As(Ⅲ)比As(Ⅴ)快1.5~2倍。因而,尽管As(Ⅴ)的工作曲线线性同样良好,但工作曲线斜率,即灵敏度比As(Ⅲ)约低一倍[12]。本试验用硫脲一抗坏血酸将As(Ⅴ)还原为As(Ⅲ)测定,由试验结果可知(图5),还原剂(NaBH4)浓度过低,则不利于砷和硒转化为气态氢化物,反之,NaBH4浓度过高,则产生大量氢气,稀释氢化物浓度,以上两种情况均使结果降低,因此为保证测定结果的准确性并考虑仪器噪音的因素,将硼氢化钠溶液的浓度确定为2%。

图5 硼氢化钠浓度对10μg/LAs和Se荧光强度的影响
2.2.5 酸浓度的确定
样品和载流要求具有一定的酸度,通过对盐酸、硝酸、硫酸、高氯酸作为反应介质时进行比较,发现盐酸介质的灵敏度较高[12]。本文选择盐酸作为反应介质,按照优化好的测定条件对用不同酸度溶液定容的同一浓度(10μg/mL)As和Se标准工作液进行测定,由图6可知,通过比较发现当盐酸浓度高于5%时,荧光强度相对趋于稳定。为使流路中酸度尽量低以避免流路长时间遭受腐蚀,试验选择5%盐酸介质。

图6 酸度对10μg/LAs和Se荧光强度的影响
2.2.6 共存离子的干扰问题
在研究对砷、硒同时测定的干扰时,发现铜、铅、锑、铋等元素会对它们产生不同程度的干扰,试验表明,加入硫脲-抗坏血酸溶液时,这些离子的干扰被掩蔽,若单独测定硒时,也可以提高酸度来消除,且食品中这些离子的浓度都较低。因而硫脲-抗坏血酸溶液既是还原剂又作为掩蔽剂可掩蔽一些离子的干扰。在选定的工作条件下,对于10μg/L的砷、硒测定,以下浓度离子(mg/L)不干扰测定:Ca2+、Mg2+、Zn2+、Fe3+、Al3+、Mn2+、Cr6+(100)、Bi3+、Hg+、Sb5+(0.5)、Pb2+、Cd2+(0.3),在食品溶液中共存离子未超出此量。砷和硒为100倍也互不影响测定,可不必考虑干扰问题[1,7,12]。
2.3 试样测定与结果分析
2.3.1 砷、硒标准曲线[7,13-14]
如图7所示,由于AFS-930双道原子荧光光度计具有自动进样稀释功能,以砷、硒的浓度(C)为横坐标,以荧光强度(I)为纵坐标进行线性回归,得到砷的曲线方程:I=15.961 2c-4.292 4,其相关系数0.999 6;得到硒的曲线方程:I=33.371 5×c-3.828 6,其相关系数:0.999 8。与此同时,在同样的仪器工作条件下,对空白样品进行了11次平行测定,计算得砷、硒测定结果的标准偏差为0.75%和0.86%。以3倍的标准偏差除以斜率,求得砷、硒的检出限分别为0.14μg/L和0.08μg/L。

图7 砷、硒标准曲线
2.3.2 试样测定结果
由测定结果表3可知,5份大米样品中砷、硒含量均符合国家标准GB 2762—2005《食品中污染物限量》中对砷和硒含量的要求:无机砷≤0.15 mg/kg,硒≤0.3 mg/kg[15]。这表明,就砷和硒含量这一检验项目而言,这次所抽取的不同正规厂家的产品质量安全状况良好。

表3 大米试样中的砷、硒含量
2.3.3 精密度和准确度
对2.3.2中的5份不同的大米样品经消解后的样液,进行6次平行测定,测定结果列于表4。由表4可知,本方法测定结果中,砷、硒的相对标准偏差分别≤7.4%和≤5.5%,表明本法的精密度较高。对上述的样液对应加入1.000、2.000、3.000、4.000、5.000μg/L等5个不同浓度的砷和硒标准溶液进行加标回收试验,计算回收率,结果列于表5。由表5可知,砷和硒加标回收率分别为96.2%~100.8%和98.1%~107.6%,表明本方法的准确度较高。

表4 砷、硒的精密度试验结果

1 1.072 100.2 2 As 0.048 As 0.052 Se 0.070 1.000 1.049 99.7 Se 0.06 2.000 2.016 98.4 2.022 98.1 3 As 0.039 Se 0.079 .000 2.926 96.2 3.68 107.6 4 As 0.035 Se 0.065 4.000 4.005 99.2 4.26 99.0 5 As 0.050 Se 0.051 .000 5.089 100.8 5.15 102.7
3 结论
通过对大米样品进行分类测试、精密度、加标回收等一系列试验,优化了氢化物-原子荧光光谱法同时测定大米中砷、硒含量的条件。与单独对大米中砷、硒含量进行测定相比,该测定方法精密度和准确度均较好,砷、硒的相对标准偏差分别≤7.4%和≤5.5%,砷和硒加标回收率分别为96.2%~100.8%和98.1%~107.6%,所得标准曲线线性的线性相关系数一般都能达到3个9以上,检出限也都在0.01 mg/kg以下;同时操作过程中自动化程度较高,受人为因素的影响少,结果准确可靠;另外,减少了检验过程中的各种误差,缩短了检验周期,大大提高了检验效率,这对检验行业的快速发展提供了很好的技术支持。
[1]沈锋.氢化物原子荧光光谱法同时测定食品中砷和硒[J].中国实用医药,2009,4(15):242-244
[2]易江,许月英,青华.氢化物发生原子吸收分光光度计测定蔬菜中的微量砷[J].光谱学与光谱分析,1987,8(2):67-70
[3]徐芳,邱德仁,胡克季,等.硒的化学与生物化学形态分析综述[J].光谱学与光谱分析.2002,22(2):332-340
[4]张妮娅,郑强,赵建明,等.氢化物发生原子荧光光谱法测定饲料中硒含量的研究[J].中国粮油学报,2008,23(4):205-209
[5]杨惠芬,梁春穗,董仕林,等.食品中无机砷限量卫生标准的研究[J].中国食品卫生杂志,2003,15(1):27-31
[6]Zheng F,Hu B.Dual-column capillary microextraction(CME)combined with electrothermal vaporization inductively coupled plasma mass spectrometry(ETV-ICP-MS)for the speciation of arsenic in human hair extracts[J].JMass Spectrom,2010,45:205-214
[7]曾宇崇.原子荧光光谱法同时测定食品中砷和硒[J].理化检验:化学分册,2005,41(7):475-476
[8]Liu W,Zhao F.A brief review of arsenic uptake and metabolism in plants[J].Environmental Chemistry,2011,30:56-62
[9]无机化学丛书编写组.无机化学丛书[M].北京:科学出版社,1984
[10]高丽娜,边疆.氢化物发生-原子荧光光谱法同时测定保健食品中砷和锑[J].中国卫生检验杂志,2006,16(11):1333-1334
[11]王美全,王海霞.双道氢化物发生原子荧光光谱法同时测定罐头食品中砷和锡[J].中国卫生检验杂志,2003,13(1):60-62
[12]徐风云.应用氢化物发生-原子荧光光谱法联合测定大米中砷和汞[J].生命科学仪器,2007,5(10):48-50
[13]刘忠秋.大米中砷的微波消解-原子荧光光谱测定法[J].辽宁医学院学报,2009,30(1):72-73
[14]邹勇平,束琴霞,刘和蓓.氢化物一原子荧光光谱法测定高邮咸鸭蛋中的硒[J].化学分析计量,2007,16(2):70-71
[15]GB 2762—2005.食品中污染物限量[S].北京:中国标准出版社,2005.
Disquisition in Measuring Arsenic and Selenium Simultaneously in Rice
Deng Yuanxi Xu Hui Wang Zhanggui Ke Chunlin Ma Long Li Yan
(Department of Bioengineering and Food,Bengbu College,Bengbu 233030)
The application for the determination of the arsenic and selenium content simultaneously using hydride generation-atomic fluorescence spectrometry was studied.Taking the measurement of As and Se in rice as an example,the conditions of the instrument,mainly including minus high voltage,current of light,flux of carrier gas,flux of shielding airflow,were studied.The working curve was linear in the range of 0~10μg/L and the correlation coefficient was 0.999 6 and 0.999 8.The recoveries were 96.2%~100.8%and 98.1%~107.6%,respectively,and the RSD were no more than 7.4%and 5.5%.It was available for analyzing the arsenic and selenium contents simultaneously compared with measuring their contents separately.
arsenic,selenium,atomic fluorescence spectrometer
O567.31
A
1003-0174(2012)05-0097-05
省级质量工程建设项目(20101091),高校省级优秀青年人才基金项目(2012SQRL214),蚌埠学院自然科学研究(2011ZR18)
2011-09-08
邓源喜,男,1977年出生,助教,硕士,食品质量与安全
