甲硝唑自然光降解研究
2012-11-22吴波张婷李金霞陈怀侠
吴波,张婷,李金霞,陈怀侠
(湖北大学化学化工学院,湖北 武汉 430062)
药品与个人护理品(pharmaceuticals and personal care products, PPCPs)是2000年以来备受关注的环境新型微污染物.PPCPs包括各种处方药、非处方药、兽药和各种护理用品,如抗生素、类固醇、消炎药、镇静剂、抗癫痫药、显影剂、止痛药、降压药、避孕药、催眠药、减肥药、香料、化妆品、遮光剂、染发剂、发胶、香皂和洗发水等[1-2].PPCPs能够引起生物畸形和微生物的抗药性等[3],因此,开展环境水样中PPCPs检测、转化和归趋研究十分重要.
芬兰、美国、丹麦、英国和巴西等国家已经广泛报道了地表水体(主要是河流)中存在PPCPs的问题.如Vieno等指出,芬兰的污水处理厂出水中普遍存在布洛芬(ibuprofen)、奈普生(naproxen)、酮洛芬(ketoprofen)、双氯芬酸(diclofenac)和苯扎贝特(bezafibrate)5种药品[3];Ternes在2001年报道德国地表水样中氯贝酸的浓度为0.049 μg/L[4];Jolanta等在2001年报道美国地表水中所含双氯芬酸的浓度为10 μg/L[5].目前,对PPCPs的关注主要集中在本体上,而对其在自然环境中的迁移转化研究较少[6].
光化学降解是表层水体中各类污染物的主要消减方式[7].关于PPCPs的光化学行为研究,国内外已开展了一些探索性的工作[8],但多集中于减量化技术研究,而对其在自然光下的降解研究较少.本文中以自然光为光源,以甲硝唑为研究对象,研究了其自然光下的光化学行为,考察了其在纯水、淡水和模拟海水中的光解动力学差异,为该污染物在自然环境中的归趋研究提供了重要的理论数据.
1 实验部分
1.1仪器与试剂仪器:Dionex ultimate 3000 HPLC仪(美国Dionex公司);Aquaplus微量无机型超纯水机(艾科浦公司);紫外分光光度计(UV2300,上海天美公司).
试剂:甲硝唑(metronidazole,99%)购于中国生物药品制品检验所;长江水取自武汉长江二桥下;模拟海水的配制[9]:0.5 mol/L NaCl,0.06 mol/L MgCl2,0.028 mol/L Na2SO4(纯度均为分析纯),溶剂为超纯水.水样的处理:过0.45 μm滤膜后在-20 ℃下冷冻保存备用.储备液的配制:分别在去离子水,过膜淡水及模拟海水中配制400 mg/L甲硝唑溶液,4 ℃冷藏储存,用磷酸盐来调节溶液的pH值.
1.2水解试验将相同浓度的纯水、长江水和模拟海水的甲硝唑溶液(初始浓度C0=10 mg/L)于暗室条件下,温度为25±1 ℃时进行水解实验.分别在第0、5、10、20和50 d取样,由HPLC定量分析甲硝唑的浓度.
1.3光解实验日光光照实验在湖北大学化院楼顶(114°E,31°N,20 m)进行,时间为2010年8-9月晴天的9:00-17:00.反应溶液置于具塞石英试管和普通玻璃管中,垂直日光照射,总照射时间为20 h以上.紫外光实验采用UV光源(UV-B,280~315 nm,30 W),在距离石英试管15 cm处,于暗室中恒温照射.反应溶液中的光照强度(200~420 nm)为7.37 mW/cm2.
以草酸铁钾为化学露光计[10],测定纯水中甲硝唑光解的平均光量子产率.
以上光解实验和量子产率测定过程中,每组实验重复3次,同时设置暗对照.暗对照中,除反应试管用铝箔包裹外,其他条件均与光照实验相同.文中所列降解数据均为扣除暗对照后的数据.
1.4分析检测光解实验中,间隔一定时间取样,以Dionex ultimate 3000 HPLC定量分析甲硝唑的浓度.HPLC分析条件,色谱柱为美国Sepax C18柱(5 μm,4.6 mm×250 mm),配有相同材料的预柱(Agilent公司);流动相为甲醇-水(35∶65,V/V);柱温为35 ℃;检测波长为320 nm.由紫外-可见吸收分光光度计绘制甲硝唑的紫外吸收光谱.
1.5数据处理结合实验数据和文献,本文中选取准一级反应动力学模型处理光降解数据,得到光解速率常数(线性相关系数r2>0.95)和光解半减期t1/2:
C=C0e-kt
(1)
(2)
其中:C0:初始浓度;C:t时刻的浓度;t:时间;k:反应速率常数.
2 结果与讨论
2.1色谱实验条件的优化以甲硝唑峰形和保留时间为评价指标,优化色谱条件.流动相为甲醇-水(35∶65,V/V);柱温为35 ℃;检测波长为320 nm时,甲硝唑的峰形良好,且在7 min内出峰.
2.2水解实验和量子产率的测定室温下,甲硝唑的不同水体溶液被置于暗处保存10 d,结果显示,在纯水、长江水和模拟海水中,甲硝唑分别减少1.8%,2.9% 和 3.2%.说明甲硝唑在纯水、江水和海水中的水解和生物降解可以忽略,后续光降解实验中甲硝唑的减少可认为均来自于光化学作用.参考文献[10],以草酸铁钾为化学露光计,纯水中甲硝唑在自然光下的平均(250~350 nm)光量子产率为0.122±0.001.
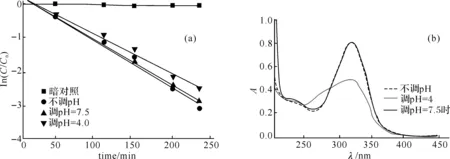
图1 暗对照和不同pH介质中甲硝唑的光降解(a)及其吸收曲线(b)(C=10 mg/L, 15 ℃)
2.3甲硝唑的直接光化学本文中考察不同pH值时甲硝唑在自然光下的直接光降解.如图1(a)所示,甲硝唑在不同pH值溶液中均能很快发生直接光化学反应,且光解符合准一级动力学规律(r2> 0.95),全文对甲硝唑的光降解均按照准一级动力学模型处理.在pH为4.0、5.2(不调pH)和7.5时,光解半衰期分别为60.2,51.6和52.5 min.即酸度升高,降解减慢.图1(b)是相同浓度的甲硝唑在酸性介质中的吸收曲线,显然,酸度增加,吸收曲线形状发生变化,而且吸光系数均减小,故而光降解速度减小.
2.4甲硝唑的间接光化学自然水体中含有各种典型溶解性物质(如NO3-1, HCO3-1,Fe3+),这些物质都可能影响有机物的光化学行为[9].本实验考察太阳光下,纯水、长江水和模拟海水中甲硝唑的光解,研究甲硝唑的间接光化学行为.由图2可知,长江水中的降解速率比纯水中的慢,半衰期分别为63.0 min和51.6 min,这可能是长江水中不溶性杂质的屏蔽效应产生的影响[11];模拟海水中,甲硝唑的降解速率与纯水的降解速率相比明显加快,半衰期为42.2 min,这应该归因于在各种溶解性无机离子的作用下,甲硝唑了发生间接光降解.为进一步了解各种溶解物对甲硝唑光降解的影响,本文中选取了铁离子(Ⅲ),碳酸氢根离子,硝酸根离子为添加物进行了光降解实验,结果见表1.铁离子(Ⅲ)的存在显著减慢甲硝唑的光降解速率,光解速率常数从纯水中的1.369×102降至0.730×102min-1;碳酸氢根离子的存在,使甲硝唑的光解速率常数降到1.140×10-2min-1;而硝酸根离子对甲硝唑光降解的影响不大.即几种离子对甲硝唑光降解影响的顺序为:铁离子(ш)>碳酸氢根离子>硝酸根离子.
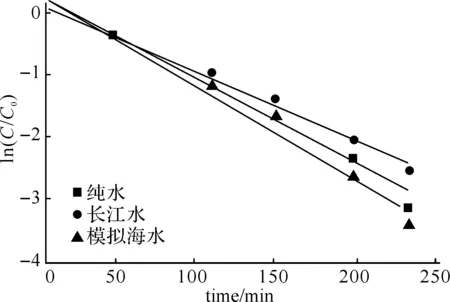
图2 太阳光下不同水体中甲硝唑的降解速率初始浓度C0=10.0 mg/L,温度:25 ℃

表1 太阳光下添加离子后甲硝唑的动力学参数
注:初始浓度C0=10.0 mg/L,温度:25 ℃.
2.5初始浓度对甲硝唑的光降解的影响太阳光照射下,考察不同浓度甲硝唑的光解动力学.实验结果见图3.可见,不同初始浓度的甲硝唑的光降解具有不同的速率,甲硝唑的光解k随C0减小而增加且k和C0表现出良好的线性相关(r2>0.95).对于许多药物和内分泌干扰物质,均观察到其光解k随C0减小而增大的现象,如氯贝酸和卡马西平[12],邻苯二甲酸二丁酯[13].甲硝唑的初始浓度对光解速率常数k的影响,可能是因为光降解过程中有自敏化光解反应的参与[9].
2.6光源对照为探讨光源强度和波长对甲硝唑光降解的影响,本文中选择不同的光源进行光降解实验.图4是甲硝唑的吸收光谱和太阳光的发射光谱图.
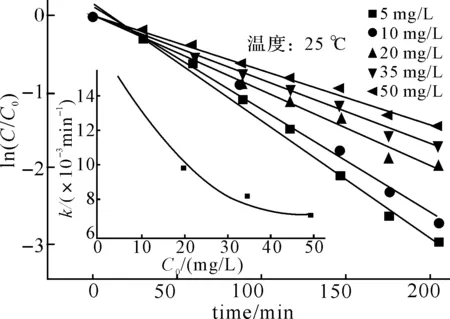
图3 纯水中不同浓度甲硝唑自然光下的光降解

图4 甲硝唑的吸收光谱和太阳光的发射光谱图
由图可知,到达地表的太阳光波长大于290 nm.一般忽略石英材料对紫外可见光的吸收,而玻璃材料通常会吸收300 nm以下的紫外光,而且会对300~400 nm光有明显的折射和散射,造成透射效果欠佳[14-15].在实验中,利用了不同的光源和试管进行光照实验,得到不同波段的光源,分别是A:太阳光+石英试管(大于290 nm),B:太阳光+玻璃试管(玻璃光对300~400 nm的太阳光部分透过),C:紫外光源UV-B (280~315 nm,30 W).图5是甲硝唑在不同光源下的降解情况.通过实验获得ln(C/C0)-t的线性关系,甲硝唑的光降解符合准一级反应动力学(r2> 0.96).甲硝唑在A,B,C3种光源中的降解速率差别明显,由大到小依次是,A>B>C.上述结果的产生原因可能是甲硝唑的最大吸收波长为319 nm,而玻璃试管吸收了290~300 nm的太阳光,且对300~400 nm的太阳光部分透过,导致在玻璃试管的溶液降解相对变慢;紫外灯的降解速度最慢是因为实验用紫外灯强度较小(30 W).由此可见,当光源发射波长接近于甲硝唑的最大吸收波长时,甲硝唑的光降解速率较快;光强越大,甲硝唑光降解越快.
2.6降解产物及毒性甲硝唑分子中含一个芳香性较差的咪唑环,甲硝唑的光降解可能发生在咪唑环的开环破裂.熊振湖等[16]以普通小球藻为测试对象,检测了降解前后甲硝唑水溶液的毒性,发现甲硝唑的降解前后的水溶液都有生物毒性,在反应开始的30 min内水溶液的生物毒性没有降低反而有所增大,但随降解过程的进行,水溶液的生物毒性逐渐减小.原因可能是反应初期产生了数量与浓度相对较大而又具有毒性的降解产物,导致水溶液的生物毒性比未降解的母体化合物还高.Gómez[17]关于有机污染物降解反应的也有类似的研究结果.本文在实验过程中也发现有一中间产物浓度先增大,后减小的现象,与上述结果一致.
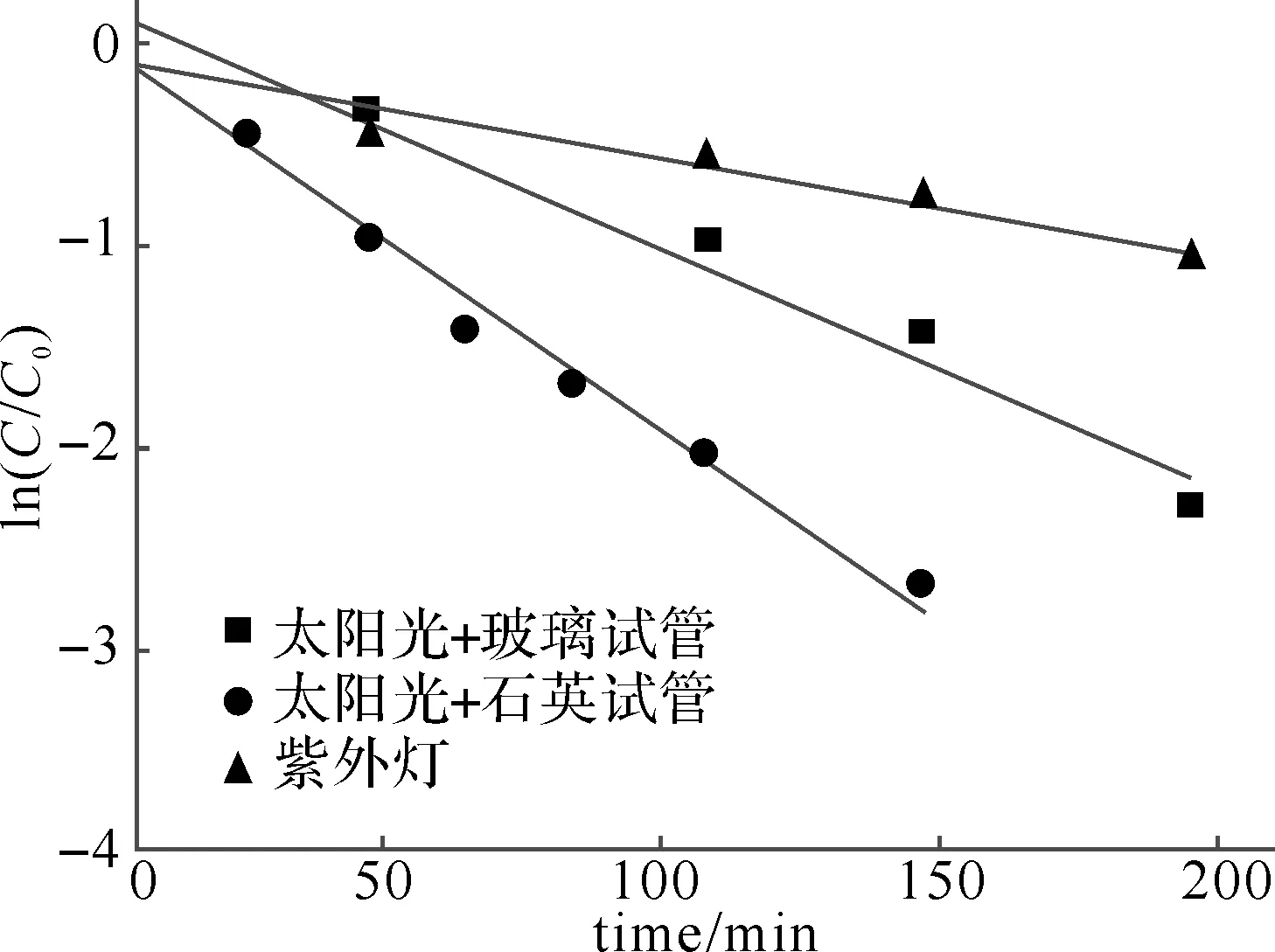
图5 纯水中不同光源下甲硝唑的光降解
3 结论
本文中研究了甲硝唑的自然光降解及其影响因素.结果发现,甲硝唑在自然光下可以很快的发生直接光降解,光解较好的符合一级动力学模型,且在酸性介质下的降解稍慢于中性介质,在模拟海水中的降解快于超纯水中,三价铁离子会明显减慢甲硝唑降解;当光源的强度越大,波长越接近于甲硝唑的最大吸收波长时,其降解越快;甲硝唑的降解速率随初始浓度的增加而减小.由于甲硝唑的光解产物同样具有毒性,因此其环境影响值得关注.
[1] Daughton C G, Ternes T A. Pharmaceuticals and personal care products in the environment:agents of subtle change[J]. Environ Health Persp, 1999, 107 (suppl. 6):907-938.
[2] Martac F O, Juan M L, et al. Behavior of pharmaceuticals, cosmetics and hormones in a sewage treatment plant[J]. Water Research, 2004, 38:2918-2926.
[3] Vieno N M, Tuhkanen T, Kronberg L. Seasonal variation in the occurrence of pharmaceuticals in effluents from a sewage treatment plant and in the recipient water[J].Environ Sci Technol. 2005, 39 (21):8220-8226.
[4] Thomas H. Occurrence, fate and removal of pharmaceutical residues in the aquatic environment:a review of recent research data[J].Toxicology Letters, 2002, 131:5-17.
[5] Jolanta D, Agata Kot-Wasik. Fate and analysis of pharmaceutical residues in the aquatic environment[J].Critical Reviews in Analytical Chemistry, 2004, 34:51-67.
[6] 贾瑷,胡建英,孙建仙,等.环境中的医药品与个人护理品[J]. 化学进展,2001, 21(2/3):390-398.
[7] Robinson P F, Liu Q T, Riddle A M, et al. Modeling the impact of direct phototransformation on predicted environmental concentrations (PECs) of propranolol hydrochloride in UK and US rivers[J]. Chemosphere,2007, 66(4):757-766.
[8] 葛林科, 张思玉, 谢晴, 等. 抗生素在水环境中的光化学行为[J]. 中国科学:化学, 2010, 40(2):124-135.
[9] 葛林科. 水中溶解性物质对氯霉素类和氟喹诺酮类抗生素光降解的影响[D]. 大连:大连理工大学,2009:67-69.
[10] 毕刚, 田世忠, 冯子刚,等.农药光解平均波长量子产率的测定[J]. 分析科学学报, 1995, 11(4):15-19.
[11] Cox L, Hermosín M C, Comejo J, et al. Photolysis of metamitron in water in the presence of soils and soil components[J]. Chemosphere,1996, 33(10) 2057-2064.
[12] Doll T E, Frimmel F H. Fate of pharmaceuticals-photodegradation by simulated solar UV-light[J]. Chemosphere, 2003, 52 (10):1757-1769.
[13] Lau T K, Chu W, Graham N. The degradation of endocrine disruptor di-n-butyl phthalate by UV irradiation:a photolysis and product study[J]. Chemosphere, 2005, 60 (8):1045-1053.
[14] Comber S D W.Abiotic persistence of atrazine and simazine in water[J]. Pestie Sci, 1999, 55(5):696-702.
[15] 李丹, 何愿华, 柳清菊.TiO2薄膜光学性质的研究[J]. 大学物理, 2005,(7):36-39.
[16] 熊振湖, 于万禄, 胡品. 日光辐照草酸铁盐体系降解水中低浓度混合药物及产物的生物毒性评价[J]. 环境科学, 2010, 31(10):2336-2343.
[17] Gómez M J, Sirtori C, Mezcua M, et al. Photodegradation study of three dipyrone metabolites in various water systems:Identification and toxicity of their photodegradation products[J]. Water Research, 2008,42 (10-11):2698-2706.
