利奈唑胺治疗脑出血术后MRSA肺炎疗效分析
2012-11-16凌聪胡细玲陈川蔡梅钦
凌聪 胡细玲 陈川 蔡梅钦
利奈唑胺治疗脑出血术后MRSA肺炎疗效分析
凌聪①胡细玲①陈川①蔡梅钦①
目的:比较利奈唑胺与万古霉素对脑出血术后耐甲氧西林金黄色葡萄球菌(MRSA)肺炎的疗效差异,评估利奈唑胺的临床疗效和安全性。方法:收集2009年1月-2011年10月确诊的48例脑出血术后MRSA肺炎病例的临床资料,分为治疗组和对照组,分别给予利奈唑胺和万古霉素治疗。按卫生部颁发的抗菌药物临床研究指导原则判定疗效,比较和分析两组的疗效和安全性。结果:利奈唑胺治疗组平均退热时间(4.8±1.5)d,治愈率41.67%,有效率91.67%,MRSA清除率75.0%,均优于万古霉素组退热时间(6.7±1.8)d,治愈率25.0%,有效率66.67%,MRSA清除率54.2%;利奈唑胺引起血小板减少4例,万古霉素致肾功能损害3例。结论:利奈唑胺对医院内MRSA肺炎的临床疗效显著,安全性较高。
利奈唑胺; 万古霉素; MRSA; 脑出血术后; 肺炎
医院内肺部感染是脑出血患者常见的并发症,也是脑出血患者主要死因之一。提高脑出血患者肺部感染的治愈率对改善脑出血患者的治疗效果,延长脑出血患者的寿命有重要的意义。随着广谱抗生素的应用,耐甲氧西林金黄色葡萄球菌(MRSA)在医院获得性肺部感染中越来越常见,治疗效果却并不尽如人意。本文将48例脑出血术后发生耐甲氧西林金黄色葡萄球菌(MRSA)感染的患者分成两组,分别应用利奈唑胺(Linezolid)及万古霉素(Vancomycin)治疗,探讨利奈唑胺治疗脑出血术后医院获得性MRSA肺炎的效果及安全性。
1 资料与方法
1.1 一般资料 收集笔者所在科2009年1月-2011年10月收治的48例脑出血术后MRSA肺炎患者资料,其中利奈唑胺治疗组患者24例,男13例,女11例,年龄49~86岁,平均(68.2±9.8)岁。万古霉素对照组治疗24例,男12例,女12例,年龄52~82岁,平均(69.5±8.2)岁。所有患者治疗前血小板计数及肌酐均正常。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 (1)体温>38 ℃,白细胞计数≥10×109/L。(2) X线片提示新的浸润阴影,伴有肺部啰音增多。(3)深部痰培养检出MRSA。
1.3 给药方案 治疗组采用利奈唑胺针剂(商品名:斯沃,美国辉瑞公司,批准文号:国药准字H20060289)。600 mg/次,静脉滴注,q 12 h,疗程14 d。对照组采用万古霉素(商品名:稳可信,美国礼来公司,批准文号:国药准字J20050069)。1 g/次,静脉滴注,q 12 h,疗程14 d。
1.4 观察指标 (1)每日观察并记录患者的症状及体征变化。(2)病原学检查及药物敏感试验,治疗前及治疗结束后行痰液细菌学培养鉴定及药物敏感试验,采用吸痰器留取痰液标本。(3)用药初期和用药后行胸部CT扫描或胸部X线检查。(4)用药初期的血、尿、大便常规,肝肾功能,血气分析等检查,用药后7 d以及治疗结束时复查的各项指标。(5)详细记录治疗期间发生的不良反应,包括发生时间、表现、程度、处理及转归。
1.5 疗效判定标准 根据卫生部颁布的《抗菌药物临床研究指导原则》的规定,临床疗效判断标准分痊愈、显效、进步、无效4级,痊愈和显效两组合计为临床有效,据此计算有效率。
1.6 细菌学疗效评价 细菌清除:治疗结束时病原菌消失,且无新的病原菌出现。部分清除:治疗结束时原培养2种以上病原菌中至少有1种未清除。未清除:治疗结束时病原菌无变化。菌群交替:治疗结束后出现新的病原菌而原发病原菌消失,再度感染其他菌,需再治疗。
1.7 不良反应评价 抗菌药物的不良反应按肯定有关、很可能有关、可能有关、可能无关和无关5级进行评定。以前三者统计药物不良反应。血小板减少判定标准为用药后血小板计数小于基线值(开始治疗前血小板检测值)的75%[1]。肾功能损害的判定标准为肌酐高于正常值上限。
1.8 统计学处理 应用统计学软件SPSS 13.0进行统计分析,计量资料以(±s)表示,采用t检验,计数资料采用 字2检验,P<0.05为差异有统计学意义。
2 结果
2.1 体温 24例利奈唑胺治疗患者,有18例发热,平均退热时间(4.8±1.5)d;24例选择万古霉素治疗患者,有20例肺部感染伴有发热,平均退热时间(6.7±1.8)d。利奈唑胺组退热时间较万古霉素组更快,比较差异有统计学意义(P<0.01)。
2.2 利奈唑胺组与万古霉素组外周血白细胞计数治疗前分别为(16.38±2.69)×109/L、(16.63±2.34)×109/L,差异无统计学意义(P=0.74),治疗后分别为(7.49±1.20)×109/L、(9.65±1.27)×109/L,差异有统计学意义(P<0.01)。
2.3 临床疗效 利奈唑胺组痊愈10例,显效12例,进步2例,无一例无效,治愈率为41.67%,临床有效率为91.67%,万古霉素组治愈6例,显效10例,进步5例,无效3例,治愈率为25.0%,临床有效率为66.67%。两组有效率比较差异有统计学意义(P<0.01)。
2.4 两组清除率比较差异有统计学意义(P<0.01)。见表1。
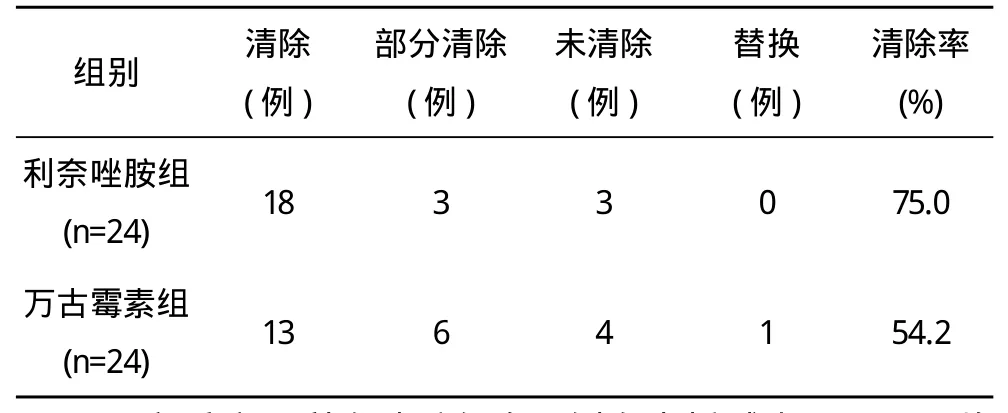
表1 两组MRSA清除率比较
2.5 不良反应 利奈唑胺组有4例血小板减少(16.7%),均可耐受,无需终止治疗,治疗期间未发现因血小板减少引起皮肤出血点、淤斑和内脏出血,停药后血小板逐渐恢复正常。万古霉素组治疗前肌酐正常,治疗过程中有3例肌酐高于正常值上限(12.5%),但不需要停药,耐受性良好。
3 讨论
肺部感染是高血压脑出血患者常见的并发症,也是致死的重要原因之一。尤其是需要外科治疗的脑出血患者,其病情更重,肺部感染的发生率更高,治疗时间更长,费用更高。肺部感染的治疗效果直接影响脑出血患者的预后。耐甲氧西林金黄色葡萄球菌(MRSA)已成为医院内获得感染的重要致病菌。几乎所有的MRSA都是多重耐药菌。糖肽类抗生素万古霉素是长期以来治疗严重MRSA感染的首选药物。近年来国外已逐渐报道对万古霉素敏感性下降甚至耐药的葡萄球菌。尽管国内报道耐万古霉素的菌株不多,但临床治疗显示,尽管万古霉素体外药敏对绝大部分MRSA均敏感,但临床治疗的有效率并不理想,可能与MRSA对万古霉素异质性耐药,以及在严重肺部感染时并发低血压休克,导致肺灌注不足,使得万古霉素难以达到有效的肺组织浓度有关[2]。利奈唑胺是首个获得美国FDA批准用来治疗革兰阳性球菌特别是MRSA的噁唑烷酮类抗菌药物[3]。利奈唑胺对万古霉素敏感性下降的MRSA以及VRE均有效,具有较好的肺组织浓度,其作用机制独特,与其他药物无交叉耐药性,有口服剂型且口服生物利用度近100%。这些特性显示了利奈唑胺有可能成为治疗肺部MRSA感染的又一重要药物。
本研究全部病例分离的菌株均对万古霉素敏感,但万古霉素组临床有效率仅为66.67%,而利奈唑胺组临床有效率达到91.67%。利奈唑胺治疗的患者,平均退热时间为(4.8±1.5)d,明显短于万古霉素组(6.7±1.8)d。除了体温下降更快之外,利奈唑胺组患者治疗后外周血白细胞下降较万古霉素组更明显,同时细菌清除率更高(75.0%)。在治愈率和有效率方面,利奈唑胺组分别为41.67%和91.67%,优于万古霉素组25.0%和66.67%。
在安全性方面,利奈唑胺的不良反应主要是血小板减少,其发生机制与免疫介导有关[4]。本研究中有4例患者出现血小板下降,但并不影响治疗,停药后很快恢复。王秀丽等[5]报道,即使对于基础血小板计数很低的血液病患者,在有血小板支持的情况下,利奈唑胺还是比较安全的。
利奈唑胺在我国应用的时间不长,尚未有耐药性的报道。美国2004年开始,连续4年监测利奈唑胺的耐药情况,已分离出现耐药菌株,尽管只有0.44%[6],但仍值得警惕。随着利奈唑胺在我国应用时间的延长,应用范围的扩大,也必将出现新的耐药菌株。因此,必须严格掌握利奈唑胺的应用指征。
[1] 王博雅,闫素英.利奈唑胺致血小板减少及其防治[J].药物不良反应杂志,2011,13(2):99-102.
[2] Ellis M W.Effect of linezolid in ventilator-associated pneumonia caused by MRSA[J].Expert Rev Antiinfect Ther,2009,7(2):183-188.
[3] Herrmann D J,Peppard W J,Ledeboer N A,et al.Linezolid for the treatment of drug-resistant infections[J].Expert Rev Antiinfect Ther,2008,6(6):825-848.
[4] Bernstein W B,Trotta R F,Rector J T,et al.Mechanisms for linezolid-induced anemia and thrombocytopenia[J].Ann Pharmacother,2003,37(4):517-520.
[5] 王秀丽,徐明珠,吴德沛.利奈唑胺治疗中性粒细胞减少血液病革兰阳性球菌感染76例临床分析[J].中国实用内科杂志,2011,31(1):76-78.
[6] Jones R N,Ross J E,Castanheira M,et al.United States resistance surveillance results for linezolid (LEADER Program for 2007)[J]. Diagn Microbiol Infect Dis,2008,62(4):416-426.
10.3969/j.issn.1674-4985.2012.24.048
①中山大学附属第三医院 广东 广州 510630
蔡梅钦
2012-06-15) (本文编辑:李静)
