复方阿莫西林乳房注入剂无菌检查方法的确立
2012-11-14郝利华杨秀玉
郝利华,杨秀玉,宋 洋
(1.中国兽医药品监察所,北京 100081;2.青岛农业大学,山东青岛 266000)
复方阿莫西林乳房注入剂是“十一五”国家科技支撑计划项目研制的新制剂。由阿莫西林、舒巴坦、泼尼松龙与矿物油制成的供乳房灌注用灭菌混悬油溶液,用于奶牛乳房炎的治疗。阿莫西林通过抑制细菌细胞壁的合成而起抗菌作用[1],兽医临床上常用于金黄色葡萄球菌、链球菌等革兰阳性菌和大肠杆菌、巴氏杆菌等革兰阴性菌引起的感染。舒巴坦是青霉烷砜类β-内酰胺酶抑制剂,与β-内酰胺类抗生素联合应用后可产生明显的增效作用,提高后者的抗菌活性,又扩大了抗菌谱[2-3]。处方中添加糖皮质激素类药物泼尼松龙,以增加机体对炎症的耐受性以及降低炎症的血管反应与细胞反应,减少炎症后遗症。为了保证药品的质量和用药安全,必须进行无菌控制。本文根据《中国兽药典》2010 年版一部附录[4]、检验操作规程[5]对复方阿莫西林乳房注入剂的无菌检查进行了实验研究,建立了可靠的无菌检查方法并进行了验证。
1 材料与试药
1.1 供试品 复方阿莫西林乳房注入剂(规格:12 g/支,含阿莫西林三水合物 0.8 g,批号 20090401、20090402、20090403,生产厂家:成都中牧生物药业有限公司)。
1.2 青霉素酶 来源:中国药品生物制品检定所(批号20100105;规格:每1 mL大于300万单位)。
1.3 培养基及冲洗液 培养基:硫乙醇酸盐液体培养基、改良马丁培养基、营养肉汤培养基、营养琼脂培养基。冲洗液:0.1%聚乙二醇或1%吐温-80的0.1%中性酪蛋白胨灭菌溶液(酪蛋白胨1 g,加蒸馏水1000 mL,加热溶解,调pH值为7.6,过滤,分装灭菌)。以上培养基均由中国兽医药品监察所提供,培养基均经过无菌性检查和灵敏度检查合格。
1.4 验证实验用菌种(第三代) (1)金黄色葡萄球菌(Staphylococcus)[CMCC(B)26003];(2)铜绿假单孢菌(Pseudomonas aeruginosa)[CMCC(B)10104];(3)枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501];(4)生孢梭菌(Clostridium sporogenes)[CMCC(B)64941];(5)白色念珠菌(Candida albicans)[CMCC(F)98001](均为中国兽医药品监察所保存)。
1.5 仪器 杭州高得泰林HTY-2000A无菌检查仪(杭州高得泰林生物设备有限公司),北京牛牛基因有限公司全封闭式无菌滤器。
2 方法
2.1 菌液制备[4](1)分别取金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌的新鲜培养物至营养肉汤,于35℃培养18~24 h,用无菌0.9%氯化钠溶液制成每1 mL含菌数小于100 CFU的菌悬液备用。(2)取生孢梭菌的新鲜培养物至硫乙醇酸盐培养基中,于35℃培养18~24 h,用无菌0.9%氯化钠溶液制成每1 mL含菌数小于100 CFU备用。(3)取白色念珠菌的新鲜培养物至改良马丁培养基中,于25℃培养24~48 h,用无菌0.9%氯化钠溶液制成每1 mL含菌数小于100 CFU备用。
2.2 菌液计数 取上述5种菌液,金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌、生孢梭菌各1 mL用营养琼脂培养基35℃培养24~48 h;白色念珠菌1 mL用改良马丁琼脂培养基25℃培养48~72 h,每种菌液接种2个平皿。计数,取平均值。活菌计数结果见表1。
2.3 培养基的灵敏度和无菌检查 取装量12 mL的硫乙醇酸盐流体培养基10管,分别接种金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单孢菌、生孢梭菌各2管,每管接菌量为1 mL(含10~100 CFU/mL),余下2管作为空白对照。取装量9 mL的改良马丁培养基4管,接种白色念珠菌2管,每管接菌量为1 mL(含10~100CFU/mL),余下2管做空白对照,置规定的温度培养5 d,逐日记录培养结果。
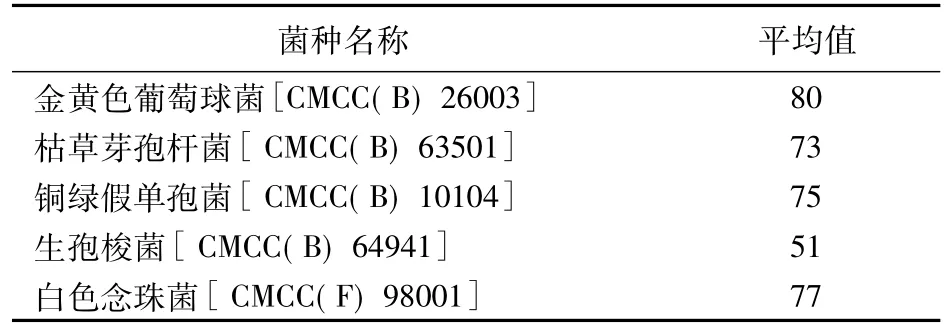
表1 活菌计数结果表 CFU/mL
2.4 薄膜过滤法[4]取本品10支,倾倒出全部内容物,混匀,取10 g,加入300 mL含0.1%聚乙二醇或1%吐温-80的0.1%中性酪蛋白胨灭菌溶液,振摇使充分混匀,置无菌滤器内,抽干,用上述灭菌溶液冲洗滤膜3次,每次100 mL,在最后一次的冲洗液中加入小于100 CFU/mL的金黄色葡萄球菌,照薄膜过滤法[4]检查。
2.5 直接加入法[4]
2.5.1 青霉素酶灭活剂量确定 取供试品10支,挤出内容物于无菌容器中,混匀,取供试品10 g,加稀释液200 mL,充分振摇使分散。取上述溶液20 mL于5支灭菌试管中,分别以每1 mg阿莫西林加36000单位、18000单位、9000单位、6000单位和3000单位的青霉素酶,于37℃放置30 min,作为供试液。取上述供试液各3 mL于45 mL硫乙醇酸盐液体培养基中,加小于100 CFU的金黄色葡萄球菌,于30~35℃培养24 h。
2.5.2 青霉素酶作用时间确定 青霉素酶灭活时间分别为20、30、45 min,其余步骤同2.5.1 项。
2.5.3 所用稀释液的量 方法同2.5.1项,稀释液用量分别为 300、200、100 mL。
2.5.4 培养基用量确定 按2.5.1项处理后的样品分别加入15、45、100、300 mL硫乙醇酸盐液体培养基中,加入规定量的金黄色葡萄球菌,按规定培养。
2.5.5 无菌验证[4-6]取本品10支,倾倒出全部内容物,混匀,取10 g,加入200 mL含0.1%聚乙二醇或1%吐温-80的0.1%中性酪蛋白胨灭菌溶液,充分振摇使分散均匀,加青霉素酶600万单位(每1 mg阿莫西林加青霉素酶9000单位),37℃孵育30 min。取8支45 mL的硫乙醇酸盐液体培养基,分别接种小于100 CFU的金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌、生孢梭菌各2支,一支加入酶作用后的供试液3 mL,另一支作为阳性对照;2支45 mL改良马丁液体培养基,分别接种小于100 CFU的白色念珠菌,其中一支加入酶作用后的供试液3 mL,另一支为阳性对照。另取同批号的硫乙醇酸盐液体培养基及改良马丁液体培养基,作为阴性对照组,置规定的温度培养3~5 d。重复无菌验证试验2次。
2.6 供试品无菌检查 取三批供试品,按照验证过的无菌检验方法进行检查。
3 结果
3.1 培养基灵敏度及无菌检查 结果如表2所示。

表2 培养基的灵敏度和无菌检查
3.2 薄膜过滤法 采用杭州高得泰林有限公司的无菌集菌器,供试液不能全部通过滤膜;更换冲洗液,效果未改变。采用北京牛牛基因有限公司滤器过滤,能够使药物和冲洗液通过滤器,但过滤时间长,试验中有崩膜现象发生。
3.3 直接加入法
3.3.1 青霉素酶灭活剂量的确定 以阿莫西林量计算,每1 mg阿莫西林加6000单位及以上青霉素酶,可将供试品灭活,结合无菌验证最终选用每1 mg阿莫西林加9000单位青霉素酶灭活。
3.3.2 青霉素酶作用时间 青霉素酶作用20、30、45 min均可将供试品灭活,为保证作用时间,又不会使试验时间太长,青霉素酶作用时间选用30 min。
3.3.3 所用稀释液的量 以三个剂量的稀释液稀释样品,发现供试品加入100 mL稀释液中,油滴挂壁严重,影响试验菌生长观察,为使供试品充分分散,故选用200 mL剂量进行稀释。
3.3.4 培养基用量 培养基用量为15 mL时,培养24 h后供试液组生孢梭菌与枯草芽孢杆菌管较对照管菌液生长缓慢,而45 mL以上时,各菌两管生长无差别。
3.3.5 无菌验证 结果见表3。上述验证菌株在此实验条件下均能生长,证明了方法的有效性。具体实验中可选择金黄色葡萄球菌作为阳性菌株。
3.4 供试品无菌检查 供试品阳性对照管24 h后观察菌液生长良好,供试品管和阴性对照管14 d内均无菌生长。
4 讨论
4.1 分别按《中国兽药典》规定的两种无菌检查法对复方阿莫西林乳房注入剂进行了无菌方法研究。由于乳房注入剂剂型及工艺特点,供试品较黏稠,采用薄膜过滤法时不能使滤液完全通过滤膜,操作无法进行;对不同厂家无菌集菌器进行比较,发现过滤困难并有崩膜现象发生,故无法采用薄膜过滤法。试验最终选用直接加入法,并确定了青霉素酶的灭活剂量,建立了直接加入的无菌检查方法,并进行了方法学验证,本文确立的无菌检查方法可用于该药物的无菌检查。
4.2 具有抑菌活性的供试品无菌检查,可根据《中国兽药典》二〇一〇年版一部附录加入中和剂或灭活剂消除供试品的抑菌活性。本研究采用青霉素酶消除供试品的抑菌成分,并通过增加培养基用量消除了供试品对敏感菌的抑菌活性。
4.3 考虑到本实验室无生物安全柜,而黑曲霉对试验环境影响较大,且黑曲霉非本品的敏感菌,认为不做黑曲霉的无菌验证对试验结果无影响,故未进行黑曲霉的无菌验证试验。
[1]沈建忠,谢联金.兽医药理学[M].北京:中国农业大学出版社,2000.
[2]Williams J D.β -Lactamases and β -Lactamase inhibitors[J].International journal of antimicrobial agents,1999,12(suppl 1):S3-S7.
[3]丁宏斌,李建成,刘金凤,等.半合成青霉素与β-内酰胺酶抑制剂对奶牛乳房炎致病菌体外联合药敏的研究[J].中国兽医杂志,2009,45(8):87-89.
[4]中国兽药典委员会.中华人民共和国兽药典二〇一〇年版一部[M].北京:中国农业出版社,2011:附录137.
[5]中国药品生物制品检定所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2005:313-323.
[6]苏德模.微生物学检验手册[M].北京:科学出版社,2000:197.
