芒果皮提取物的体外清除自由基作用研究*
2012-11-14周荣光杨兆祥何凌宇普俊学
周荣光,杨兆祥,王 金,何凌宇,普俊学
(1.昆明制药集团股份有限公司药物研究院,云南 昆明650100;2.昆明理工大学生命科学与技术学院,云南 昆明650224;3.云南中医学院中药学院,云南 昆明650500)
芒果系漆树科芒果属植物芒果(Mangif er a indical L.)的成熟果实,主产于热带、亚热带,是世界第二大热带水果,被誉为“热带水果之王”。在我国,芒果主要分布在云南(东南部)、贵州(南部)和广西(南部)三省,多为家养栽培,为当地的重要经济作物。研究表明,芒果果皮含有大量的黄酮[1]、山酮[1]、多糖[2]以及种类众多的小分子多酚类物质[3],具有止咳化痰[4]、抗炎[4]、抑 菌[5]、抗 氧 化[6]等 作 用。目 前,芒 果 除 鲜 食外,主要被加工成饮料、罐头、果冻等,加工过程中产生的约占鲜果重量5%~10%的芒果皮则被抛弃,不仅浪费资源,而且污染环境。因此,如何利用废弃的芒果皮资源,进行开发利用,变废为宝,具有十分重要的意义。本文对芒果皮的水提取物、乙醇提取物和石油醚提取物的清除自由基活性进行研究,为芒果皮的科学开发利用提供理论依据。
1 实验材料
1.1 试剂与仪器 AB204-N型电子天平(瑞士 Mettler公司);Shi madzu UV2401PC紫外可见分光光度仪(日本岛津公司);HH-4数显恒温水浴锅(天津市恒温水浴锅厂);LD-500刀片式粉碎机(长沙市岳麓区常宏制药机械设备厂);PGX-330 A-12 H光照箱(宁波莱福科技有限公司)。核黄素(VB2)、氯化硝基四氮唑兰(NBT),番红花红(Safranine T),蛋氨酸,2,2-二苯基-1-苦肼基(DPPH)购自Sig ma-Aldrich公司。乙醇、石油醚、二甲基亚砜(DMSO)为化学纯,购自昆明汕滇精细化学品有限公司;其它试剂均为分析纯,实验用水为二次蒸馏水。
1.2 药材 芒果,购自昆明水果市场。
2 实验方法
2.1 芒果皮提取物的制备 取新鲜成熟芒果,自来水洗净,晾干,用水果刀均匀削取果皮,果皮厚度约1~5 mm。果皮置阳光下晒干,用刀片式粉碎机粉碎至20 mm以下。称取粉碎后的芒果皮3份,50 g/份,分别加入水、95%乙醇和石油醚500 mL,加热回流提取2 h,重复提取3次,提取液趁热过滤,过滤液合并,减压浓缩为浸膏,冷冻干燥,分别得到水提取物(EW)9.5 g,95%乙醇提取物(EEt)7.3 g和石油醚提取物(EP)3.8 g。取上述芒果皮的水提取物、95%乙醇提取物和石油醚提取物适量,以二甲基亚砜(DMSO)为溶剂,配制不同浓度的待测溶液,备用。
从“有计划的商品经济”到“社会主义市场经济”,从“民主法制”到“依法治国”,从“精神文明”到“文化强国”,从调整社会关系到构建“和谐社会”,从植树造林到“生态文明”,从“一国两制”到香港、澳门回归,从“革命与战争”到“和平与发展”,神州大地处处涌动着改革的大潮,开放的窗口迎接着八面来风。
产生的羟自由基(·OH)与指示剂发生反应,当体系中存在自由基清除剂时,清除剂与羟自由基作用,使羟自由基对指示剂的作用降低,通过检测指示剂的变化情况,即可获得清除剂对羟自由基的清除能力。根据所用指示剂,通常采用的方法有邻二氮菲法和亚甲基蓝(MB)法等。但这些方法多适用于测定单纯的有机物的活性,不适用于组分复杂的提取物的羟自由基活性的测定。本文采用Fenton反应产生羟自由基使番红花红褪色的方法来测定芒果皮提取物清除羟自由基的活性,该方法具有抗干扰能力强,重现性好,稳定可靠的特点。
说明低磷环境抑制了苦荞根系生长,不耐低磷苦荞受影响更严重。同时,各苦荞幼苗茎叶干重的变化大于根系干重,这是根冠比值上升的主要原因。与正常供磷浓度(P1)相比,P2浓度下,除‘KQ10-11’外,其它基因型苦荞根冠比均有升高;P3浓度下,各基因型苦荞根冠比显著升高,而‘KQ10-11’的根冠比却显著降低。说明不耐低磷苦荞品种‘KQ10-11’的根系对低磷胁迫更敏感,受低磷胁迫影响程度更大。
芒果皮的95%乙醇提取物(EEt)和水提取物(EW)对超氧阴离子自由基的清除作用显著强于石油醚提取物(EP)。3种提取物对超氧阴离子的清除作用与样品浓度呈一定的线性关系,EP线性方程为y=0.416 8x+5.164 3,R2=0.943 5,IC50=107.57μg/mL;EW 线性方程为y=0.7855x+5.267 9,R2=0.956 4,IC50=56.95μg/mL;EEt在0~80μg/mL范围内呈现良好的线性,y=1.099 5x+3.64,R2=0.987 3,IC50=42.16μg/mL,当样品浓度≥80μg/mL,清除率随浓度的变化趋缓。见图2。
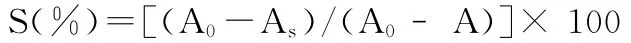
3 实验结果与讨论
3.1 对DPPH自由基的清除作用 DPPH在有机溶剂中是一种稳定的自由基,其乙醇溶液显深紫色,在517 n m处有强吸收。当与抗自由基活性物质作用时,其孤对电子被配对,因而吸收消失或减弱,通过测定吸收减弱的程度,可评价自由基清除剂的活性。
2.3 超氧阴离子自由基清除能力测定 采用光照核黄素方法[8]。用p H 7.4的PSB缓冲液为溶剂,配制1.67×10~5 mol·L-1核黄素,0.01 mol·L-1蛋氨酸,4.6×10~5 mol·L-1氯化硝基四氮唑兰(NBT)。分别取上述3种溶液各2.0 mL,加入1.2.1中不同浓度的待测试样溶液1.0 mL,置光照箱中于4 500 lx下光照30 min,用紫外-可见分光光度计于560 nm处测定吸光度值As;同法,以1.0 mL DMSO代替样品溶液,测定吸光度值A0。用p H 7.4的PSB缓冲溶液6.0 mL+DMSO 1.0 mL作参比溶液。取3次测试平均值,按下式计算清除率:
借鉴欧盟水框架分类分项建立标准的方法,建立北京山区河溪生态评价体系(表2)。基于北京地区的研究水平和对实际生产实践的指导需求,本体系生物要素中的要素项暂时不包含鱼类,各要素项生态质量均分为4级;对水文地貌和物理化学两大要素类不分要素项,生态质量均分为5级。根据该分级体系和标准,针对各要素类或要素项分别评定生态质量等级。
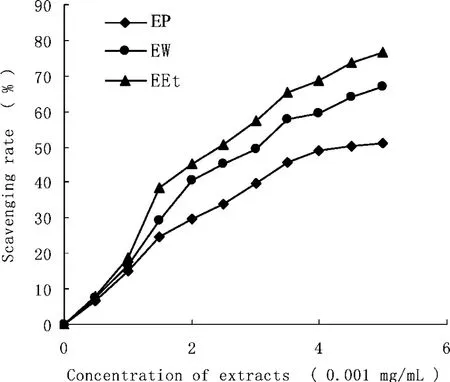
图1 不同浓度下提取物对DPPH自由基的清除率
3.3 对羟自由基的清除作用 石油醚提取物(EP)线性方程y=17.1x+1.689 3,R2=0.966 2,IC50=2.83 mg/mL;水提取物(EW)在0~1.25 mg/mL范围内呈现良好的线性,y=51.669x+4.490 5,R2=0.981 6,IC50=0.88 mg/mL,当样品浓度≥1.25 mg/mL,清除率随浓度的变化趋缓;95%乙醇提取物(EEt)在 0~1.00 mg/mL 范围内线性方程为 y=84.52x+9.08,R2=0.935 5,IC50=0.484 mg/mL,当样品浓度≥1.00 mg/mL,清除率随浓度的变化明显趋缓。对羟自由基的清除能力大小为EEt>EW>EP。见图3。
2.4 羟自由基清除能力测定 采用Fenton反应产生羟自由基使番红花红褪色的方法[9]。取p H 7.4的PSB缓冲溶液1.0mL,40μg/mL番红花红1.0 mL,0.945 mmol·L-1EDTA-Fe(Ⅱ)(新鲜配制)1.0 mL,加入2.1中不同浓度的待测试样溶液0.5 mL,3%H2O2溶液1.0 mL(新鲜配制),混合后在37℃水浴中反应30 min,用紫外-可见分光光度计在520 nm处测定吸光度As;同法,以0.5 mL DMSO代替样品溶液,测定吸光度A0;以0.5 mL DMSO代替样品溶液,以1.0 mL蒸馏水代替3%H2O2溶液,测定吸光度A。用3.5 mL蒸馏水+PSB缓冲溶液1.0 mL作参比溶液。取3次测试平均值,按下式计算清除率:

图2 不同浓度下提取物对超氧阴离子自由基的清除率
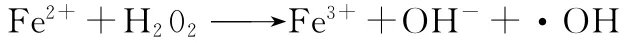
2.2 DPPH自由基清除能力测定[7]DPPH用70%的乙醇配制成5×10~5 mol/L的溶液。取上述5×10~5 mol/L的DPPH溶液3.0 mL,加入2.1中不同浓度的待测试样溶液1.0 mL,于25℃反应15 min,用紫外-可见分光光度计于517 n m处测定吸光度值As;取5×10~5 mol/L的DPPH 3.0 mL,加入DMSO 1.0 mL,同法测定吸光度值A0。用70%乙醇3.0 mL+DMSO 1.0 mL作参比溶液。取3次测试平均值,按下式计算清除率:
3.2 对超氧阴离子自由基的清除作用 用光照核黄素的方法产生超氧阴离子自由基,可使氯化硝基四氮唑兰产生蓝色物质,该物质在560 n m处有最大吸收峰。随着反应的进行,蓝色物质的生成就越多,加入芒果皮提取物样品溶液可使超氧阴离子自由基的产生受到抑制,进而蓝色物质的生成也受到抑制。测定该波长下的吸光度值的变化,可反映芒果皮提取物对超氧阴离子自由基的清除能力。
芒果皮的水提取物(EW)、95%乙醇提取物(EEt)和石油醚提取物(EP)对DPPH自由基均有良好的清除作用,浓度越高,清除能力越强。通过回归分析,得EP的DPPH自由基清除率线性方程为y=10.6x+4.954 5,R2=0.954,IC50=4.25 μg/mL;EW 线性方程为y=13.707x+5.477 3,R2=0.954 5,IC50=3.25μg/mL;EEt线性方程为y=15.658x+6.572 7,R2=0.948 5,IC50=2.77μg/mL。IC50越小,抗自由基活性越强。依据IC50值,3种提取物对DPPH自由基的清除能力大小为EEt>EW>EP。见图1。
羟自由基非常活泼,在含氧自由基中其氧化活性最强,但存在时间短,一般难于直接测定。本文采用间接法测定,其原理是利用Fenton反应产生羟自由基:作用,其在药品和保健品方面的应用开发具有巨大潜力,前景广阔。本研究结果为芒果皮的深入开发利用提供了科学依据。

图3 不同浓度下提取物对羟自由基的清除率
4 结论
本文研究表明,芒果皮的3种溶剂提取物对DPPH自由基、超氧阴离子自由基和羟自由基均有很好的清除作用,并且清除率与样品浓度呈一定的线性关系,浓度越高,清除作用越强;采用不同的提取溶剂,所得到的提取物清除自由基的能力存在显著差异,对DPPH自由基、超氧阴离子自由基和羟自由基的清除能力为乙醇提取物>水提取物>石油醚提取物。因此,提取芒果皮的溶剂以选择乙醇为宜。
采用SPSS 16.0软件进行资料统计分析,符合正态分布的定性资料采用χ2检验,定量资料采用方差分析或重复测量设计方差,非正态分布资料采用非参数Kruskal-Wallis(校正)检验。
依据《导基》课程内容、考试大纲及导游人员岗位能力培养要求,进行总结和归纳,收集素材,分教学阶段构建教学的内容项目和任务体系(如表1)。
现代医学研究证明,自由基会引起人体蛋白质变性、酶失活、DNA链断裂、生物膜结构损伤、细胞解体乃至机体病变和死亡,自由基及其诱导的氧化反应是导致生物衰老和某些疾病如癌症、糖尿病、风湿性关节炎、心脑血管疾病等的重要因素。本文研究表明,芒果皮提取物对不同的自由基均有良好的清除
[1]Schieber A,Berardini N,Carle R.Identification of flavonol and xanthone glycosides from mango(Mangifera indica L.Cv.“Tommy Atkins”)peels by high-perfor mance liquid chromatography-electrospray ionization mass spectrometry[J].Agric.and Food Chem,2003,51(17):5006~5011.
[2]王维民,汪敏 .芒果皮粗多糖提取的影响因素及工艺的研究[J].农产品加工(学刊),2005,9~131.
[3]Ajila C M,Bhat S G,Prasada R.Valuable components of raw and ripe peels from t wo Indian mango varieties[J].Food Chemistry,2007,102(4):1006~1011.
[4]黄敏琪,林忠文,曾宪彪,等 .芒果皮提取物止咳化痰和抗炎作用研究[J].中草药,2007,38(8):1233~1234.
[5]覃丽俭,吴长兴,吴莉宇 .杧果皮不同萃取物的抑茵活性初探[J].热带农业科学,2007,27(2):21~25.
[6]李琳,姜新发,张志斌,等 .枇杷皮和芒果皮粗提液抗氧化活性研究[J].电子科技大学学报,2003,32(6):755~759.
[7]L R Fukumoto,G Mazza.Assessing antioxidant and prooxidant activities of phenolic compounds[J].J Agric Food Chem,2000,48(8):3597~3604.
[8]刘杰超,王思新,焦中高,等 .苹果多酚提取物抗氧化活性的体外试验[J].果树学报,2005,22(2):106~110.
[9]张建胜,王雪梅,高云涛,等 .伸筋草提取物体外清除活性氧自由基及抗氧化作用研究[J].云南中医中药杂志,2008,29(3):38~39.
