石墨烯和铂/石墨烯的合成及其表征
2012-11-09田建华单忠强
陈 宽 田建华*, 崔 兰 林 娜 单忠强
(1天津大学化工学院,2天津大学分析测试中心,天津 300072)
石墨烯和铂/石墨烯的合成及其表征
陈 宽1田建华*,1崔 兰2林 娜1单忠强1
(1天津大学化工学院,2天津大学分析测试中心,天津 300072)
以天然鳞状石墨为原料,采用化学氧化法合成氧化石墨,在此基础上采用低温热解膨胀结合微波加热乙二醇还原法合成石墨烯(Gr)以及铂/石墨烯(Pt/Gr)复合材料。SEM和TEM显示所制备的石墨烯为层状结构的半透明薄膜。采用X射线光电子能谱(XPS)和傅立叶转换红外光谱(FTIR)分别确定氧化石墨、膨胀石墨及石墨烯表面含氧官能团的数量和性质。以所制备的碳氧原子比5.94的石墨烯作为载体制备出可用于质子交换膜燃料电池的高负载量的Pt/Gr催化剂,在铂载量高达60%时,表面铂粒子依然具有高分散性,平均粒径为3.8 nm。
石墨烯;热膨胀;乙二醇还原;铂/石墨烯
石墨烯具有独特的单原子层二维晶体结构,其理论比表面积高达2 630 m2·g-1,具有突出的不受温度影响的高速电子迁移率(15 000 cm2·V-1·s-1)和低密度、高的热导率和强度等[1]。从2004年英国曼彻斯特大学的Geim教授等在Science上发表了关于“微机械剥离法”获取石墨烯的首篇文章至今,对石墨烯的研究逐渐升温并不断获得新的研究成果[2,3]。作为重要的纳米材料,石墨烯奇特的结构与性能不仅体现出在基础科学研究方面的重要价值,也预示着良好的应用前景和经济利益[4]。
单层石墨烯本身是一种严格意义上的二维结构的材料,由于热力学不稳定性而难以独立稳定存在。但是研究表明,各种方法合成的石墨烯均不是一个完美且光洁平整的二维薄膜,其自身能够稳定存在源于其表面存在大量的微观褶皱[5,6]。目前制备石墨烯的主要方法包括微机械分离法、化学气相沉积法、外延生长法和氧化石墨还原法等[7,8]。其中,氧化石墨还原法由于合成工艺简单而备受推崇。
在采用热膨胀剥离技术的氧化石墨还原法中,氧化石墨表面的含氧基团在高温无氧环境下分解为CO2和水蒸汽。当气体的生成速率大于扩散速率时,产生的层间压力有可能超过石墨烯片层间的范德华力,从而使氧化石墨产生膨胀剥离[9]。传统的高温热膨胀(800~1 000℃)不可避免地会有碳的损失以及表面组成的变化,改进的方法是低温(300~400℃)热膨胀或者采用化学还原[10,11]。化学还原利于调控膨胀石墨表面含氧基团数量同时获得剥离程度较高的石墨烯,但相关工艺尚需探讨。加入添加剂以阻止石墨烯片层的堆叠的研究工作也有报道[12],但这种石墨烯表面可能被包覆剂所覆盖。
本实验采用热解膨胀结合乙二醇还原法制备石墨烯材料。作为石墨烯材料的应用,本文合成了铂/石墨烯复合材料。碳载Pt催化剂在能源和化工领域有广泛应用,而且一直是新一代质子交换膜燃料电池 (PEMFC)的首选高活性和高稳定性催化剂[13-15]。为使Pt粒子尽可能地分布在质子交换膜附近的高效反应区以获得高的催化剂利用率,PEMFC催化剂的Pt载量高达20wt%~60wt%,Pt粒子尺寸在3~4 nm,且在载体表面高度分散。石墨烯独特的表面特性使其在合成高载量催化剂方面优势明显。
1 实验部分
1.1 膨胀石墨的制备
采用改进的Hummer法合成氧化石墨 (GO)[16]。将浓硫酸(天津市化学试剂五厂)和浓磷酸以8∶1体积比混合后浸入冰水浴冷却。然后将天然鳞状石墨(天津市大茂化学试剂厂)和高锰酸钾以1∶3重量比混合均匀后倒入混酸中,搅拌反应2 h后撤除冰浴,45℃水浴反应30 min。之后再次移入冰浴,搅拌下滴加与浓硫酸等体积的去离子水,滴加完毕后恒温45℃水浴搅拌反应4 h。反应结束后,加入3%的过氧化氢溶液,直至液体由棕褐色变为淡黄色并且不再产生气体为止。再经过离心、除去上层清液、加入同等体积的去离子水后超声分散,透析(透析袋为美国联合碳化产品),70℃烘箱内干燥,得到片状氧化石墨。(本文试剂未标注来源的均为天津市江天化工技术有限公司产品)。
称取一定量的氧化石墨,研磨后放入石英舟置于管式炉中,在氮气保护下,以10℃·min-1的速率升温至400℃,在该温度下维持4 h之后,缓慢降温至室温,得到不完全剥离的膨胀石墨(EG),将其保存在干燥箱中备用。
1.2 石墨烯及其复合材料的合成
采用微波加热乙二醇法进一步还原膨胀石墨。(1)EG粉末中加入适量乙二醇和水的混合溶液,超声结合磁力搅拌使其分散均匀,过程中用0.5 mol·L-1的NaOH乙二醇溶液调节pH值至11;(2)体系密封后放入微波炉,700 W功率加热2 min,重复三次。(3)搅拌冷却至室温,分别用去离子水和无水乙醇搅拌洗涤,抽滤,80℃鼓风干燥箱干燥,得到石墨烯样品备用。采用相同的方法合成不同铂含量的Pt/Gr材料,不同之处在于步骤(2)之后滴加分别滴加 0.7 mL,4.0 mL 氯铂酸的乙二醇溶液 (7.9 mg·mL-1),经过同样的加热方式和提取方式分别获得质量分数20%和60%的Pt/Gr材料。
1.3 石墨烯的表征
本实验采用场发射电子显微镜 (美国FEI公司Nanosem 430)对碳材料形貌进行表征。使用透射电镜(日本JEOC公司JEM-100CXⅡ)观察样品内部组织形态与结构。X射线衍射分析采用日本理学D/max-2500型X射线衍射仪,采用Cu靶,Kα射线源(λ=0.154 056 nm),管电压 40 kV,管电流 200 mA,扫描速度为 8°·min-1,扫描范围 2θ为 10°~85°。
采用KBr压片法制样,在Avatar 360型红外光谱仪上进行测试,观察材料在400~4 000 cm-1范围内吸收峰的位置来分析样品所含官能团。
采用X射线光电子能谱 (ESCA system的PHI1600型)测定碳材料表面的氧含量,使用Mg Kα线作为X射线源,测试环境真空度为10-8~10-9Pa,参考标准为C1s的电子结合能(284.6 eV)。
2 结果与讨论
2.1 膨胀石墨制备石墨烯的工艺优化
含氧基团的数量在抑制石墨烯片层间堆叠时起到非常重要的作用,也是影响Pt前驱体在石墨烯表面吸附的重要因素。实验采用还原性适中的乙二醇作为还原剂,既可以满足恢复膨胀石墨表面的缺陷,使膨胀石墨中的碳原子由sp3结构还原成sp2结构的要求,又可以调控膨胀石墨表面含氧基团数量达到实验设定的范围。乙二醇也可以兼作溶剂,用乙二醇分散的膨胀石墨要比水分散的膨胀石墨均一、稳定,可以有效防止加热过程中局部温度过高导致的石墨烯的堆叠。

图1 膨胀石墨和石墨烯的高倍SEM图Fig.1 High magnification SEM image of expanded graphite and graphene
实验过程中我们发现,膨胀石墨在碱性环境下分散较好,向乙二醇体系中加入少量的去离子水,调节悬浮液的pH值至11,微波加热还原,最终获得的石墨烯片层剥离度高,表面含氧基团控制在15wt%~20wt%范围之内。
图1是膨胀石墨(a)和石墨烯(b)的SEM图,从图中可以看出,氧化石墨热膨胀之后,片层间并未剥离完全,经过乙二醇进一步还原之后,膨胀石墨片层表面的含氧基团克服层间范德华力将片层撑开,形成剥离度很高的石墨烯。
图2为乙二醇还原膨胀石墨(EG)制得的石墨烯的TEM图。可以看出,乙二醇还原制得的石墨烯几乎是透明的,并且表面纹理呈褶皱状,石墨烯表面残留的含氧基团是导致产生这些褶皱的根本原因,这些褶皱不仅增大了石墨烯的比表面积,而且在一定程度上抑制了片层之间的堆叠,在一定程度上稳定了片层之间的结构[10]。

图2 石墨烯的TEM图Fig.2 TEM image of grapheme
2.2 石墨烯表面官能团的表征
图3为各种碳材料的FTIR谱图。从图中可以看出,氧化石墨表面的极性基团主要是羟基、羧基及环氧基等极性基团,这一点可以从图中吸收峰的位置看出,3 394 cm-1处的峰变宽并延伸至低波数区,为典型的COOH中羟基的伸缩振动峰,而且有基团间缔合。1 724 cm-1处出现的峰应为羰基或羧基中C=O的伸缩振动峰[17],1 622 cm-1处可能是双键的伸缩振动峰,1 152 cm-1,1 113 cm-1位置的峰一般归属为脂肪醚的吸收峰。这些极性基团的嵌入,破坏了石墨的共轭π键,同时也使氧化石墨具备很强的亲水性,特别是表面羟基的存在,很容易和水分子之间形成氢键。经过热膨胀之后,氧化石墨表面的亲水基团大部分被除去,尤其羧基和羰基官能团,吸收峰强度明显下降,有些基团的吸收峰甚至消失。而经过乙二醇化学还原之后得到的石墨烯,膨胀石墨大部分被还原,基本恢复了石墨的sp2杂化结构,各含氧基团的吸收峰进一步被削弱或消失。

图3 碳材料的红外谱图Fig.3 Infrared radiation spectra of carbon materials
2.3 石墨烯的表面组成
XPS测试是对氧化石墨、膨胀石墨和石墨烯表面元素组成的定量分析。表1为3种碳材料表面元素组成的数据,经过高温和化学处理之后,碳表面的含氧量从32.3%逐步递减为18.3%,碳氧原子比从2.48提高到5.94,尤其是高温膨胀这一步,氧含量降低的非常明显,这一结果是和红外测试得到的数据相吻合的,说明高温对于氧化石墨脱氧实现重石墨化[9]起着重要的作用,经过高温热处理,氧化石墨的残碳率明显得到提高,表明大部分氧在氧化石墨的热处理过程中被除去,乙二醇还原进一步降低了最终产品石墨烯表面的氧含量。
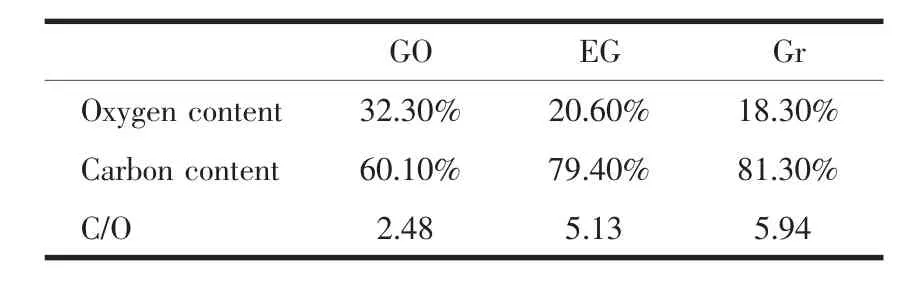
表1 碳材料的表面元素含量Table 1 Element content on the surface of carbon materials
图4是XPS测试获得的氧化石墨、膨胀石墨及石墨烯的C1s电子结合能图。从图中可以看出,三者的结合能分别在284.6 eV处依次增强,峰面积增加,说明最终获得的石墨烯中C=C/C-C结构的增加。氧化石墨中仍含有大量未被氧化的C-C/C=C结构(284.58 eV),比较GO和Gr在结合能为284.6 eV处的数据可以发现,这些结构很稳定,前后差别不大。含氧基团主要是以环氧基(286.6 eV)的结构形式存在,该结构类似于脂肪醚,所以这一结论和红外谱图是一致的。氧化石墨经过高温处理和化学还原后,表面的环氧基团基本不复存在,这是由于环氧基的结构不稳定性导致的,在高温和酸性条件下很容易发生反应生成羟基(286.3 eV)、羰基(287.4 eV)和羧基(289.4 eV)等含氧基团[18]。
表2是C1s结合能对应的基团,以及各成分的含量百分比。对比表中EG和GO的XPS数据,我们可以发现,原来不存在的羟基和羰基含量百分比陡然增加,而且两者百分比之和接近环氧基的含量百分比,这正是环氧基分解后转化的结果。
2.4 Pt/Gr的物化性能表征
相比于颗粒状碳载体,石墨烯片状结构和发达的比表面积能够有效抑制铂粒子的团聚,更适宜作为高铂载量催化剂载体。而且按照实验预设的反应方式,得到的石墨烯表面均匀分布一些功能化含氧基团,这些含氧官能团一方面阻止了层与层之间的搭接,使石墨烯发达的比表面得以保持,另一方面经热膨胀和化学还原后,表面含氧基团基本转化成羟基和羰基,使石墨烯在水相中能够稳定分散,更有利于铂前驱体在石墨烯表面的吸附,即形成更多的结晶中心。
图5是TEM测试结果。图片显示质量分数为20%和60%的Pt/Gr中铂晶体的粒径分别为3.5 nm和3.8 nm,且分散性很好。
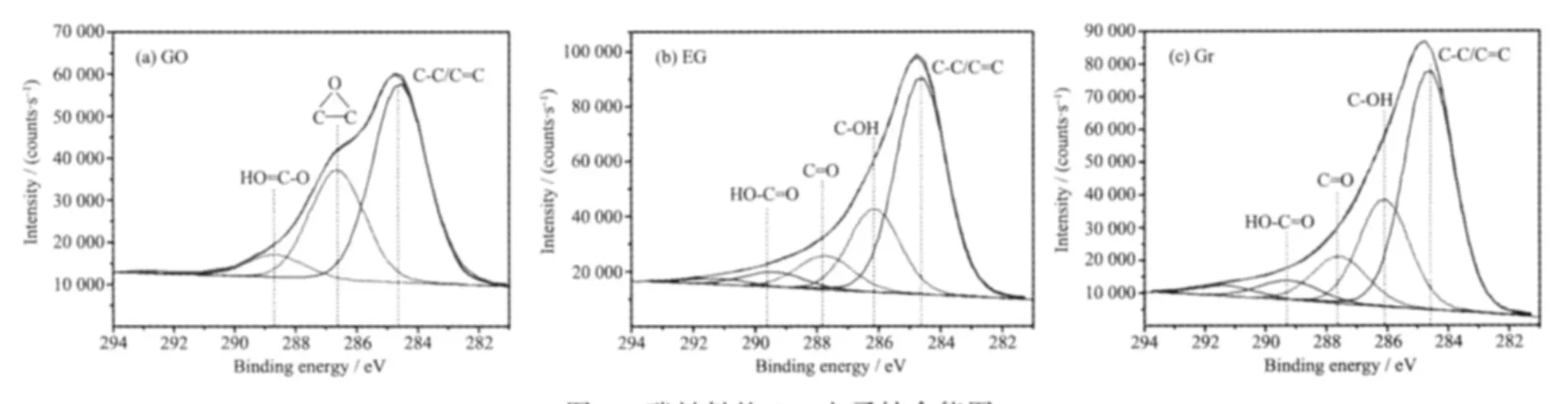
图4 碳材料的C1s电子结合能图Fig.4 Eelectron binding energies of C1s in carbon materials

表2 三种碳材料的C1s电子结合能数据Table 2 XPS data of C1s in Go,E-GO and Gr

图5 不同铂含量的Pt/Gr的高倍TEM图Fig.5 High magnification TEM images of Pt/Graphene with different platinum mass fraction
图6为Pt/Gr的XRD图,从图中可以看出,氧化石墨和石墨2θ角分别位于 10°和26.5°附近的C(002)衍射峰都消失了,说明石墨经氧化,高温膨胀处理、化学还原后,基本上已经形成平面结构的石墨烯[19]。 2θ角为 39°、46°和 67°附近处出现了Pt(111)、Pt(200)和 Pt(220)的晶面衍射峰,说明氯铂酸还原后得到的铂晶体是面心立方结构[20]。

图6 不同铂含量的Pt/Gr的XRD图Fig.6 XRD patterns of Pt/Graphene under different platinum mass fraction
3 结 论
结合低温热解膨胀法和微波加热乙二醇还原法,制备出石墨烯及其铂/石墨烯复合材料。热膨胀温度对于氧化石墨转变为热膨胀石墨起着重要的作用,经过400℃热处理,氧化石墨的残碳率明显得到提高,大部分氧在氧化石墨的热处理过程中被除去,乙二醇还原进一步降低了最终产品石墨烯表面的氧含量。实验合成的石墨烯呈半透明薄膜层状结构,XPS和FT-IR分析表明其表面含有羟基和羰基等含氧基团,碳氧原子比约为5.94。以其作为质子交换膜燃料电池催化剂的载体,合成的铂载量为20%和60%的Pt/Gr材料中,铂颗粒的粒径分别约为3.5 nm和3.8 nm,且分散性良好。
[1]Allen M J,Tung V C,Kaner R B.Chem.Rev.,2010,110(1):132-145
[2]Novoselov K S,Geim A K,Morozov S V,et al.Science,2004,306(5696):666-669
[3]Geim A K.Science,2009,324:1530-1534
[4]Patchkovskii S,Tse J S,Yurchenko S N,et al.Proc.Natl.Acad.Sci.,2005,102(30):10439-10440
[5]Meyer J C,Geim A K,Katsnelson I M,et al.Solid State Commun.,2007,143(1-2):101-109
[6]Geim A K,Nonoselov K S.Nat.Mater.,2007,6(3):183-191
[7]Berger C,Song Z M,Li X B,et al.Science,2006,312:1191-1196
[8]Li X S,Cai W W,An J H,et al.Science,2009,324(5932):1312-1314
[9]YANG Yong-Gang(杨永岗),CHEN Cheng-Meng(陈成猛),WEN Yue-Fang(温月芳),et al.New Carbon Mater.(Xinxing Tan Cailiao),2008,23(3):193-200
[10]Schniepp H C,Li J L,McAllister M J,et al.J.Phys.Chem.B,2006,110(17):8535-8539
[11]Park S,Ruoff R S.Nat.Nanotechnol.,2009,4:219-224
[12]Stankovich S,Piner R D,Chen Xin Q,et al.J.Mater.Chem,2006,16:155-158
[13]Kou R,Shao Y Y,Wang D H,et al.Electrochem.Commun.,2009,11(5):954-957
[14]Uhma S H,Joob J Y,Bongc S Y,et al.ECS.Trans.,2010,33(1):1725-1732
[15]CHEN Wei-Xiang(陈卫祥),YU Gui-Yan(俞贵艳),ZHAO Jie(赵杰),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2004,20(12):1467-1470
[16]Marcano D C,Kosynkin D V,Berlin J M,et al.ACS.Nano,2010,4(8):4806-4814
[17]LIU Xiu-Ying(刘秀影),SONG Ying(宋英),LI Cun-Mei(李存梅),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(11):2128-2132
[18]CHEN Cao(陈操),ZHAI Wen-Tao(翟文涛),ZHENG Wen-Ge(郑文革),et al.J.Inorg.Mater.(Wuji Cailiao Xuebao),2011,26(7):707-710
[19]WEN Zhu-Liang(温祝亮),YANG Su-Dong(杨苏东),SONG Qi-Jun(宋启军),et al.Acta.Phys-Chim.Sin.(Wuli Huaxue Xuebao),2010,26(6):1570-1574
[20]ZHONG Qi-Ling(钟启玲),ZHANG Bing(张兵),DING Yue-Min(丁月敏),et al.Acta.Phys-Chim.Sin.(Wuli Huaxue Xuebao),2007,23(3):429-432
Preparation and Characterization of Graphene and Platinum/Graphene
CHEN Kuan1TIAN Jian-Hua*,1CUI Lan2LIN Na1SHAN Zhong-Qiang1
(1School of Chemical Engineering and Technology,2Analysis Center,Tianjin University,Tianjin 300072,China)
Graphite oxide was prepared from natural flake graphite by chemical oxidation method and subsequently thermal expansion method was applied to produce the expanded graphite(EG).On the basis of this,we employed the microwave-heating ethylene glycol method to synthesize graphene and platinum/graphene(Pt/Gr)composite.The SEM and TEM images revealed that the graphene we produced by our method was subtransparent thin film with layer structures.FT-IR and XPS were used to characterize the amount and property of carbon materials.We found that grapheme (nC/nO=5.94)can be used as the carrier of high platinum loading PEMFC catalyst.When the mass fraction of platinum increased to 60%,the platinum particles can still uniformly scattered on the surface of graphene without aggregation seriously.The particle size of platinum was 3.8 nm on average.
graphene;thermal expansion;ethylene glycol reduction;platinum/graphene
TQ127.1
A
1001-4861(2012)08-1541-06
2011-12-07。收修改稿日期:2012-04-06。
国家973计划(No.2009CB220105)资助项目。
*通讯联系人。 E-mail:jhtian@tju.edu.cn
