胰腺癌组织Skp2与C-myc的表达及意义
2012-11-07李居剑刘建生王艳
李居剑 刘建生 王艳
·短篇论著·
胰腺癌组织Skp2与C-myc的表达及意义
李居剑 刘建生 王艳
细胞周期调节失控是肿瘤发生、发展的重要分子事件。S期激酶相关蛋白2(S-phase kinase associated protein 2,Skp2)是在细胞周期研究中发现的一种F-box蛋白,它通过调节泛素-蛋白酶途径,参与细胞周期的调控[1]。而C-myc是一种原癌基因,是细胞从G0/G1期进入S期的“开关”,参与调控细胞增殖、分化及凋亡等[2]。有研究表明[3],Skp2可活化C-myc靶基因,引起S期转换,而C-myc也可通过激活cullin基因,导致Skp2基因表达增高,二者协同作用参与肿瘤的发生与发展。本研究检测Skp2、C-myc蛋白在胰腺癌组织中的表达,探讨其与临床病理特征的关系。
一、资料与方法
1.病例资料:收集山西医科大学第一医院2003年1月至2010年12月间行手术切除并经病理证实的胰腺癌标本48例。患者术前均未行放化疗治疗,其中男26例,女22例,年龄31~77岁,平均(59±11)岁。取20例同期手术切除的癌旁胰腺组织作为对照。
2.免疫组化染色:鼠抗人Skp2单抗、鼠抗人C-myc蛋白单抗及二抗PV-6002均购自北京中杉金桥生物技术有限公司。应用Envision免疫组化二步法检测Skp2和C-myc蛋白表达。以PBS液代替一抗作阴性对照。
Skp2阳性染色主要位于胞核,C-myc阳性染色则位于胞质或胞核,阳性着色均为出现棕黄色颗粒。随机观察10个高倍镜视野,参照Takeuchi等[4]方法,以阳性细胞百分数和染色强度评分。阳性细胞<10%为0分,10%~29%为1分,30%~59%为2分,60%~74%为3分,≥75%为4分。无染色为0分,淡黄色为1分,棕黄色为2分,深棕黄色为3分。两分值相乘,>1为阳性,≤1为阴性。
3.统计学处理:应用SPSS17.0统计软件进行分析。显著性差异采用χ2检验,相关性分析采用Spearman等级相关分析。P<0.05为差异具有统计学意义。
二、结果
1.Skp2和C-myc蛋白在胰腺癌和癌旁胰腺组织中的表达:48例胰腺癌组织中Skp2的阳性表达率为79.2%(38/48),显著高于癌旁胰腺组织的20.0%(4/20)(χ2=20.927,P<0.01)。48例胰腺癌组织中C-myc的阳性表达率为77.1%(37/48),显著高于癌旁胰腺组织中的15.0%(3/20)(χ2=22.465,P<0.01,图1)。

图1Skp2(a)、C-myc(b)在胰腺癌组织中的表达(免疫组化 ×400)
2.Skp2和C-myc蛋白表达与胰腺癌临床病理特征的关系:胰腺癌Skp2和C-myc表达均与性别、年龄、肿瘤大小及部位无关(P值均>0.05),而与癌组织的分化程度、淋巴结转移及临床分期有关(P值均<0.05,表1)。
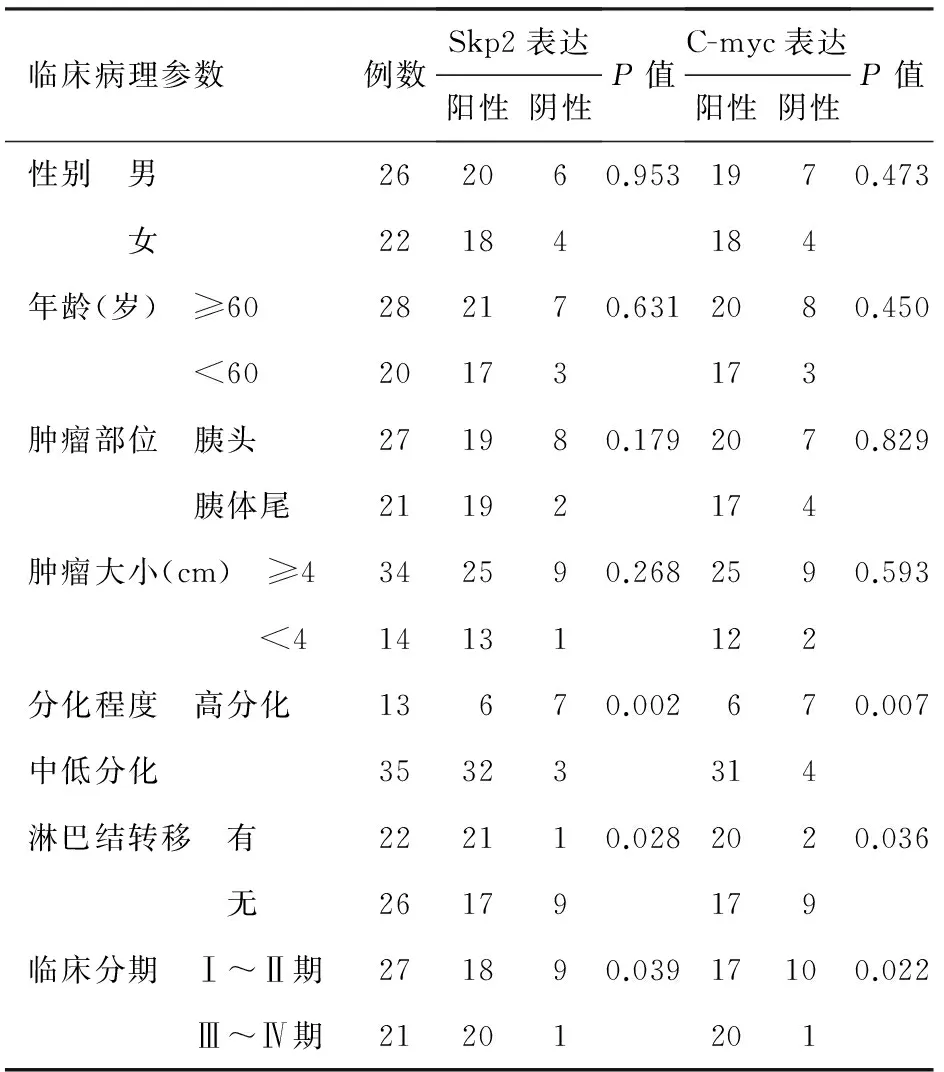
表1 Skp2、C-myc的表达与胰腺癌临床病理特征的关系
3.胰腺癌Skp2和C-myc蛋白表达的相关性:38例Skp2表达阳性的胰腺癌组织中,33例C-myc阳性表达;10例Skp2阴性表达的胰腺癌组织中,6例C-myc表达阴性,Skp2与C-myc的表达呈显著正相关(r=0.453,P<0.01)。
讨论Skp2是泛素连接酶复合物(Skp1-Cullin-F-box,SCF)中的一种F-box蛋白,其作为SCF的底物识别亚基,特异性识别底物并诱导其泛素化降解来调控细胞周期。p27kip1蛋白是其主要的靶物质,对细胞G1~S期转换具有抑制作用,p27kip1的降解可导致细胞恶性增殖[5]。Skp2蛋白在许多恶性肿瘤中均有异常升高,包括口腔鳞状细胞癌、非小细胞肺癌、胃癌和肝癌等,且Skp2高表达患者较低表达者预后更差[6-8]。本实验研究发现,Skp2在胰腺癌组织显著高表达,且Skp2的表达与肿瘤分化程度、淋巴结转移及临床分期有关。提示Skp2与胰腺癌的侵袭、转移能力具有一定的相关性。
C-myc是一种与细胞周期关系密切的原癌基因,其表达可使细胞获能进入S期。C-myc对细胞具有双重作用,既可刺激细胞增殖,也可促进细胞凋亡,同时C-myc的高表达还抑制细胞的分化,从而参与肿瘤的形成[9-10]。本实验研究结果显示,胰腺癌组织C-myc蛋白高表达,其表达与肿瘤分化程度、淋巴结转移及临床分期相关,提示C-myc与胰腺癌的发生发展亦有密切关系。
本研究结果还显示,Skp2与C-myc在胰腺癌组织中的表达呈正相关性,提示二者的协同作用参与了胰腺癌的发生与发展,与Kim等11的结果一致。
[1] Ganoth D, Bornstein G, Ko TK, et al. The cell-cycle regulatory protein Cks1 is required for SCF(Skp2)-mediated ubiquitinylation of p27. Nat Cell Biol, 2001,3:321-324.
[2] Morrish F, Isern N, Sadilek M, et al. c-Myc activates multiple metabolic networks to generate substrates for cell cycle entry. Oncogene, 2009,28:2485-2491.
[3] O′Hagan RC, Ohh M, David G, et al. Myc-enhanced expression of Cul1 promotes ubiquitin-dependent proteolysis and cell cycle progression. Genes Dev, 2000,14:2185-2191.
[4] Takeuchi H, Fujimoto A, Tanaka M, et al. CCL21 chemokine regulates chemokine receptor CCR7 bearing malignant melanoma cells. Clin Cancer Res, 2004,10:2351-2358.
[5] 高海燕,钟立厚,胡克.Skp2蛋白在非小细胞肺癌中的表达及其与C-myc蛋白表达的关系.中国肺癌杂志,2004,7:493-496.
[6] Reichert M, Saur D, Hamacher R, et al. Phosphoinositide-3-kinase signaling controls S-phase kinase-associated protein 2 transcription via E2F1 in pancreatic ductal adenocarcinoma cells. Cancer Res, 2007,67:4149-4156.
[7] Osoegawa A, Yoshino I, Tanaka S, et al. Regulation of p27kip1 by S-phase kinase-associated protein 2 is associated with aggressiveness in non-small-cell lung cancer. J Clin Oncol, 2004,22: 4165-4173.
[8] 胡少辉,张志伟,陈孝平,等.Skp2,C-myc在肝细胞肝癌中的表达及其意义.中国普通外科杂志,2006,1:45-48.
[9] 邓景岳,毕明刚. 影响原癌基因C-myc作用因素的研究进展.肿瘤, 2009,29:1176-1179.
[10] Morrish F, Isern N, Sadilek M, et al.c-Myc activates multiple metabolic networks to generate substrates for cell cycle entry. Oncogene, 2009,28:2485-2491.
[11] Kim S, Herbst A, Tworkowski K, et al. Skp2 regulates Myc protein stability and activity. Mol Cell, 2003,11:1177-1188.
10.3760/cma.j.issn.1674-1935.2012.05.018
030001 山西省太原市,山西医科大学第一医院普外科
刘建生,Email:syyyljs@126.com
2011-11-04)
(本文编辑:吕芳萍)
